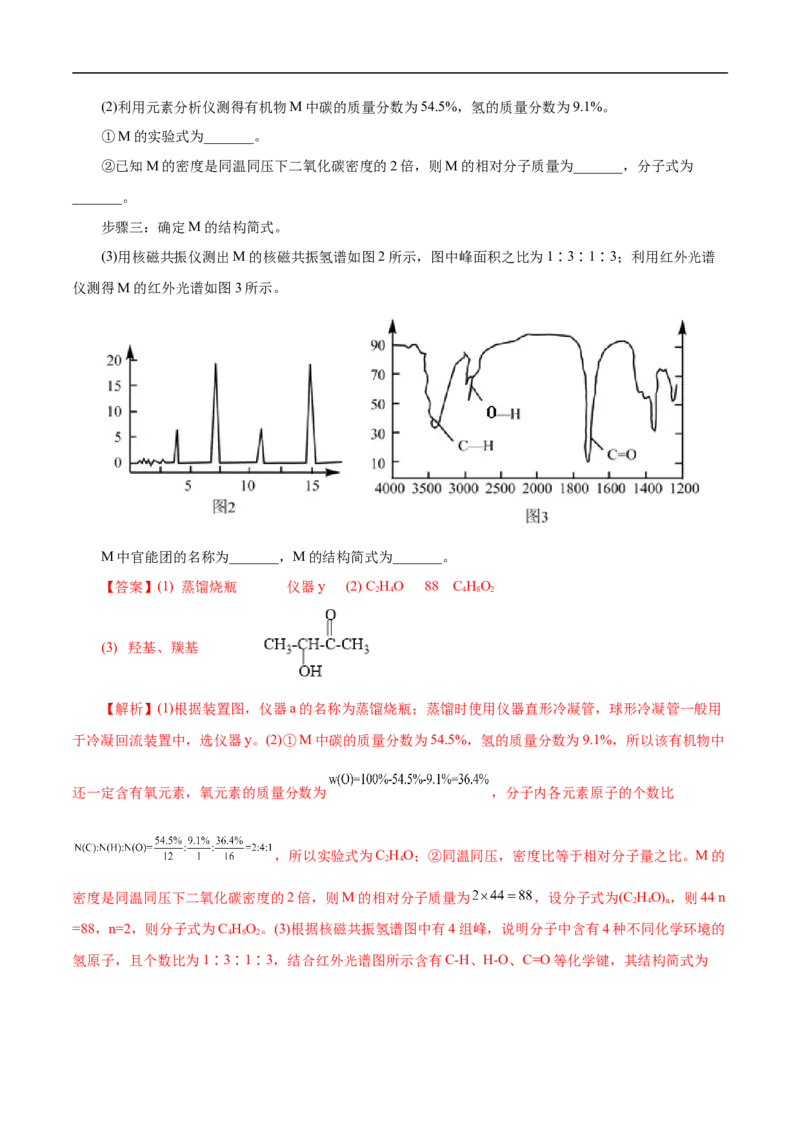
文档内容
考点 31 研究有机物的一般方法
研究有机物的一般方法是研究有机物的基础,是高考的重要考点之一,高考中常见的考点如下:了解
分离提纯的常见方法,掌握蒸馏、重结晶和萃取实验的基本技能;了解测定有机化合物元素含量、相对分
子质量的一般方法,并能根据其确定有机化合物的分子式;了解燃烧法测定有机物的元素组成,了解质谱
法、红外光谱、核磁共振氢谱等先进的分析方法
预计2023年的高考仍然在非选择题中出现,尤其是在有机合成与推断题、有机综合实验题中。
一、分离、提纯有机物的常见方法
二、有机化合物分子式的确定
分离、提纯有机物的常见方法
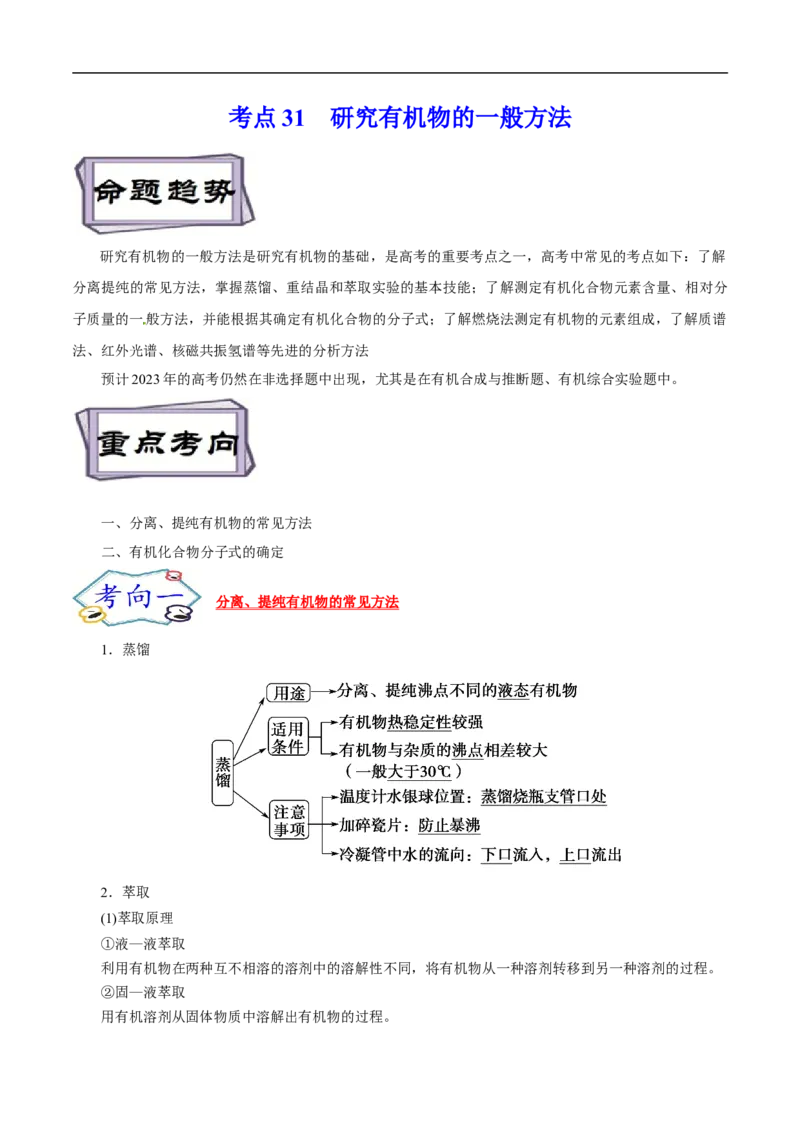
1.蒸馏
2.萃取
(1)萃取原理
①液—液萃取
利用有机物在两种互不相溶的溶剂中的溶解性不同,将有机物从一种溶剂转移到另一种溶剂的过程。
②固—液萃取
用有机溶剂从固体物质中溶解出有机物的过程。(2)仪器:分液漏斗、铁架台、烧杯。
(3)操作要求
加萃取剂后充分振荡,静置分层后,打开分液漏斗活塞,从下口将下层液体放出,并及时关闭活塞,
上层液体从上口倒出。
3.重结晶
(1)适用条件
①重结晶是提纯固态有机物的常用方法。
②杂质在所选溶剂中溶解度很大或很小,易于除去。
③被提纯的有机物在所选溶剂中的溶解度受温度的影响较大;该有机物在热溶液中的溶解度较大,冷
溶液中的溶解度较小,冷却后易于结晶析出。
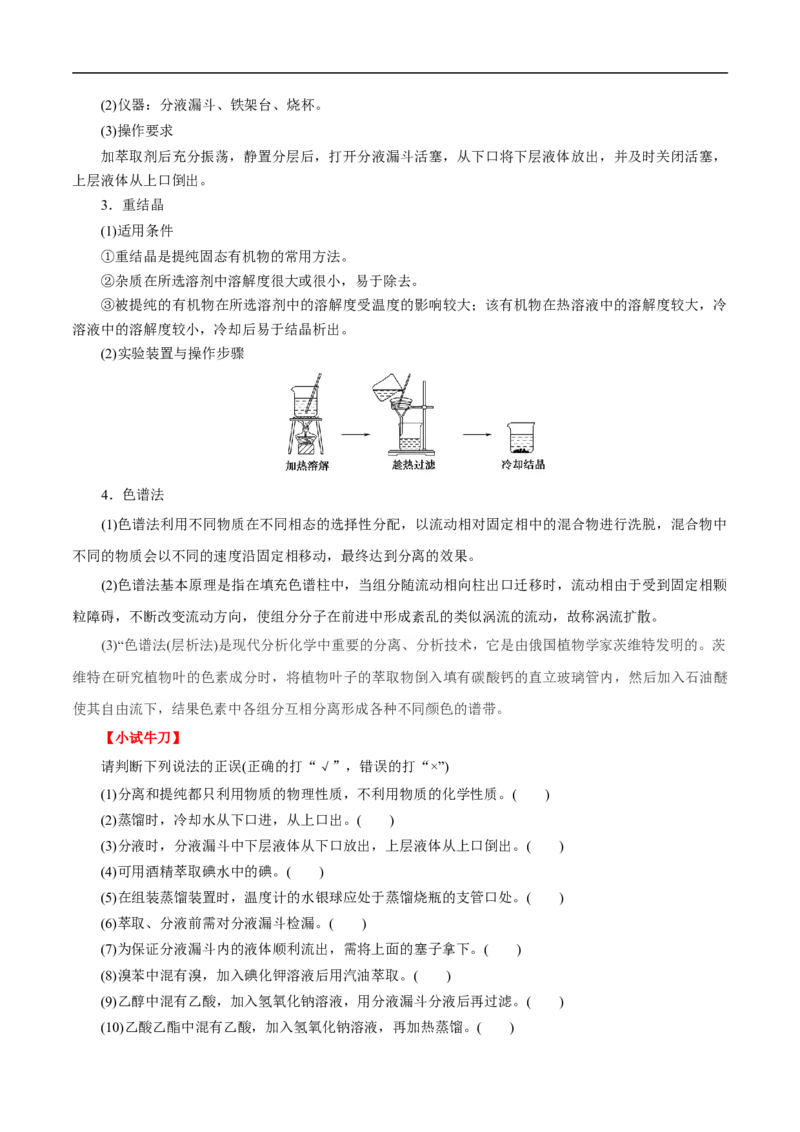
(2)实验装置与操作步骤
4.色谱法
(1)色谱法利用不同物质在不同相态的选择性分配,以流动相对固定相中的混合物进行洗脱,混合物中
不同的物质会以不同的速度沿固定相移动,最终达到分离的效果。
(2)色谱法基本原理是指在填充色谱柱中,当组分随流动相向柱出口迁移时,流动相由于受到固定相颗
粒障碍,不断改变流动方向,使组分分子在前进中形成紊乱的类似涡流的流动,故称涡流扩散。
(3)“色谱法(层析法)是现代分析化学中重要的分离、分析技术,它是由俄国植物学家茨维特发明的。茨
维特在研究植物叶的色素成分时,将植物叶子的萃取物倒入填有碳酸钙的直立玻璃管内,然后加入石油醚
使其自由流下,结果色素中各组分互相分离形成各种不同颜色的谱带。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)分离和提纯都只利用物质的物理性质,不利用物质的化学性质。( )
(2)蒸馏时,冷却水从下口进,从上口出。( )
(3)分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。( )
(4)可用酒精萃取碘水中的碘。( )
(5)在组装蒸馏装置时,温度计的水银球应处于蒸馏烧瓶的支管口处。( )
(6)萃取、分液前需对分液漏斗检漏。( )
(7)为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下。( )
(8)溴苯中混有溴,加入碘化钾溶液后用汽油萃取。( )
(9)乙醇中混有乙酸,加入氢氧化钠溶液,用分液漏斗分液后再过滤。( )
(10)乙酸乙酯中混有乙酸,加入氢氧化钠溶液,再加热蒸馏。( )(11)苯中混有乙酸,加入氢氧化钠溶液,再用分液漏斗分液。( )
(12)用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏。( )
(13)用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液。( )
(14)在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失。( )
(15)作为重结晶实验的溶剂,杂质在此溶剂中的溶解度受温度影响应该很大。( )
(16)提纯粗苯甲酸的方法可以用重结晶法。( )
(17)在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到室温才过滤。( )
(18)在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加入少量蒸馏水,然后趁热过滤。( )
答案:(1) × (2)√ (3) √ (4)× (5) √ (6)√ (7)√ (8)× (9)× (10)× (11)√ (12)√ (13)×
(14)√ (15) × (16) √ (17) × (18)√
【典例】
例1 分离下列混合物,应选用蒸馏操作的是( )
A.汽油和柴油 B.溴水 C.硝酸钾和氯化钠的混合物 D.四氯化碳和水
【答案】A
【解析】A项,汽油和柴油互溶,但二者沸点不同,故用蒸馏操作分离;B项,用萃取、分液、蒸馏
操作分离;C项,用结晶操作分离;D项,四氯化碳和水互不相溶,用分液操作分离。
例2 下列关于物质的分离、提纯实验中的一些操作或做法,正确的是( )
A.在组装蒸馏装置时,温度计的水银球应伸入液面下
B.用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏
C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量NaOH溶液
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤
【答案】B
【解析】A项,蒸馏时,温度计的水银球应置于蒸馏烧瓶的支管口处,A错误;B项,用生石灰吸水,
利用乙醇沸点低加热蒸出,B正确;C项,苯甲酸会与NaOH溶液反应,C错误;D项,要趁热过滤,D
错误。
【对点提升】
对点1 下列各组混合物中,可以用分液漏斗进行分离的是 ( )
A.乙醛和乙醇 B.苯和水 C.酒精和水 D.乙醛和水
【答案】B
【解析】A项,乙醛和乙醇互溶,不能用分液漏斗进行分离,A错误;B项,苯和水不溶,能用分液
漏斗进行分离,B正确; C项,酒精和水互溶,不能用分液漏斗进行分离,C错误;D项,乙醛和水互溶,
不能用分液漏斗进行分离,D错误。故选B。
对点2 下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 目的 分离方法 原理A 分离溶于水的碘 乙醇萃取 碘在乙醇中的溶解度较大
B 分离乙酸乙酯和乙醇 分液 乙酸乙酯和乙醇的密度不同
C 除去KNO 固体中混杂的NaCl 重结晶 NaCl在水中的溶解度很大
3
D 除去丁醇中的乙醚 蒸馏 丁醇与乙醚的沸点相差较大
【答案】D
【解析】乙醇与水互溶,不能用作萃取剂,A错误;乙醇和乙酸乙酯互溶,不能用分液法分离,B错
误;除去KNO 中的NaCl杂质,可利用二者在不同温度下溶解度变化差别大,使用重结晶法分离,C错误;
3
分离两种沸点差别较大的互溶液体,一般使用蒸馏法,D正确。
【巧学妙记】
1.研究有机化合物一般要经过的几个基本步骤:
2.常见有机物的分离、提纯
方法 目的 主要仪器 实例
分离、提纯沸点相差很大 蒸馏烧瓶、
蒸馏 分离乙酸和乙醇
的液态混合物 冷凝管
将有机物从一种溶剂转移 用四氯化碳将碘水中的碘
萃取 分液漏斗
到另一种溶剂 提取出来
分离互不相溶的液态混合
分液 分液漏斗 分离汽油和水
物
利用温度对溶解度的影响 烧杯、酒精灯、蒸发皿、
重结晶 提纯苯甲酸
提纯有机物 漏斗
洗气 分离提纯气体混合物 洗气瓶 除去甲烷中的乙烯
有机化合物分子式的确定
1.元素分析
(1)定性分析:确定有机物分子的元素组成。
用化学方法鉴定有机物分子的元素组成。如燃烧后,一般C生成CO 、H生成HO、N生成N 、S生
2 2 2
成SO 、Cl生成HCl。
2
(2)定量分析法(李比希法)2.相对分子质量的测定——质谱法
(1)原理。用高能电子流等轰击样品分子,使该分子失去电子变成带正电荷的分子离子和碎片离子。分
子离子、碎片离子各自具有不同的相对质量,它们在磁场的作用下到达检测器的时间将因质量的不同而先
后有别,其结果被记录为质谱图。
(2)质荷比。指分子离子、碎片离子的相对质量与其电荷的比值。质谱图中,质荷比的最大值就表示了
样品分子的相对分子质量。例如,由图可知,样品分子的相对分子质量为46。
(3)质谱法的优点:快速、微量、精确。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)李比希法是定量研究有机物中元素组成的方法( )
(2)元素分析仪可用于分析有机物中的元素组成( )
(3)利用李比希法可以确定有机物分子的最简式( )
(4)元素分析可以确定未知物的分子式( )
(5)验证有机物属于烃时只需测定产物中的CO 和HO的物质的量之比( )
2 2
(6)有机物燃烧后只生成CO 和HO的物质不一定只含有碳氢两种元素( )
2 2
(7)有机物的实验式、分子式一定不同( )
(8)燃烧后只产生CO 和HO的物质不一定只含有碳、氢两种元素( )
2 2
答案:(1) √ (2)√ (3) √ (4)× (5) × (6)√ (7) × (8) √
【典例】例1 为验证某有机物(只含C、H、O三种元素中的两种或三种)属于烃的含氧衍生物,下列方法正确
的是( )
A.验证其完全燃烧后的产物只有HO和CO
2 2
B.测定其燃烧产物中HO和CO 的物质的量之比
2 2
C.测定其完全燃烧时消耗有机物的物质的量与生成的HO和CO 的物质的量之比
2 2
D.测定该试样的质量及试样完全燃烧后生成的HO和CO 的质量
2 2
【答案】D
【解析】A项,烃的含氧衍生物或烃燃烧都生成HO和CO ,不能确定是否含有氧元素,错误;B项,
2 2
测定其燃烧产物中HO和CO 的物质的量之比只能确定该有机物分子中碳原子、氢原子的个数比,不能确
2 2
定是否含有氧元素,错误;C项,测定其完全燃烧时消耗有机物的物质的量与生成的HO和CO 的物质的
2 2
量之比,只能确定该有机物分子中碳原子和氢原子的个数,不能确定是否含有氧元素,错误;D项,测定
该试样的质量及试样完全燃烧后生成的HO和CO 的质量,可以确定一定质量的有机物中含有碳、氢元素
2 2
的质量,根据质量守恒可确定是否含有氧元素,正确。
【对点提升】
对点1 燃烧0.1 mol某有机物得0.2 mol CO 和0.3 mol HO,由此得出的结论不正确的是( )
2 2
A.该有机物分子的结构简式为CH—CH
3 3
B.该有机物中碳、氢元素原子数目之比为1∶3
C.该有机物分子中不可能含有 双键
D.该有机物分子中可能含有氧原子
【答案】A
【解析】A项,根据元素守恒和原子守恒,推出0.1mol有机物中含有0.2molC和0.6molH,即1mol该
有机物中有2molC和6molH,因为题中无法确认有机物的质量或相对分子质量,因此无法确认有机物中是
否含氧元素,即无法确认有机物结构简式,故A错误;B项,根据A选项分析,该有机物中碳、氢元素原
子数目之比为2:6=1:3,B正确;C项,1mol该有机物中含有2molC和6molH,该有机物分子式
C HO,不饱和度为0,即不含碳碳双键,故C正确;D项,根据A选项分析,该有机物中可能存在氧元
2 6 x
素,也可能不存在氧元素,故D正确。
对点2 某化合物6.4g在氧气中充分燃烧,只生成8.8gCO 和7.2gH O,下列关于该有机物的说法中
2 2
不正确的是( )
A.属于醇类 B.碳、氢原子个数比为
C.相对分子质量为32 D.无法确定分子式【答案】D
【解析】该有机物中, , ,
, , ,则该有机物中含有O元素,其物
质的量为 , ,则该有机物的实验式为
CHO,由于H原子已经达到饱和,则其最简式即为其分子式,即分子式为CHO。A项,该物质的分子式
4 4
为CHO,结构简式可以为CHOH,属于醇类,故A正确;B项,该物质中碳、氢原子个数比为1:4,故
4 3
B正确;C项,该有机物的分子式为CHO,相对分子质量为32,故C正确;D项,该有机物的分子式为
4
CHO,故D错误;故选D。
4
【巧学妙记】
1.确定有机物分子式的基本方法
2.确定有机物分子式的其他方法
(1)通式法
类别 通式 相对分子质量
烷烃 C H M=14n+2(n≥1)
n 2n+2 r
M=14n(烯烃,n≥2),
r
烯烃、环烷烃 C H
n 2n
M=14n(环烷烃,n≥3)
r
M=14n-2(炔烃,n≥2;
r
炔烃、二烯烃 C H
n 2n-2
二烯烃,n≥4)
苯及其同系物 C H M=14n-6(n≥6)
n 2n-6 r
饱和一元醇 C H O M=14n+2+16
n 2n+2 r饱和一元醛 C H O M=14n+16
n 2n r
饱和一元酸及酯 C H O M=14n+32
n 2n 2 r
(2)商余法
用烃(CH)的相对分子质量除以14,看商数和余数。
x y
①=m……2,该烃分子式为C H 。
n 2n+2
②=m……0,该烃分子式为C H 。
n 2n
③=m……12,该烃分子式为C H 。
n 2n-2
④=m……8,该烃分子式为C H 。
n 2n-6
(M:相对分子质量 n:分子式中碳原子的数目)
r
(3)化学方程式法
利用有机反应中反应物、生成物之间“量”的关系求分子式的方法。
利用燃烧反应的化学方程式,由题给条件并依据下列燃烧通式所得CO 和HO的量求解x、y、z。
2 2
CH+(x+)O ――→xCO+HO、CHO+(x+-)O ――→xCO+HO。
x y 2 2 2 x y z 2 2 2
有机化合物结构式的确定
1.红外光谱
(1)作用:初步判断某有机物中含有何种化学键或官能团。
(2)原理:不同的化学键或官能团吸收频率不同,在红外光谱图上将处于不同的位置。
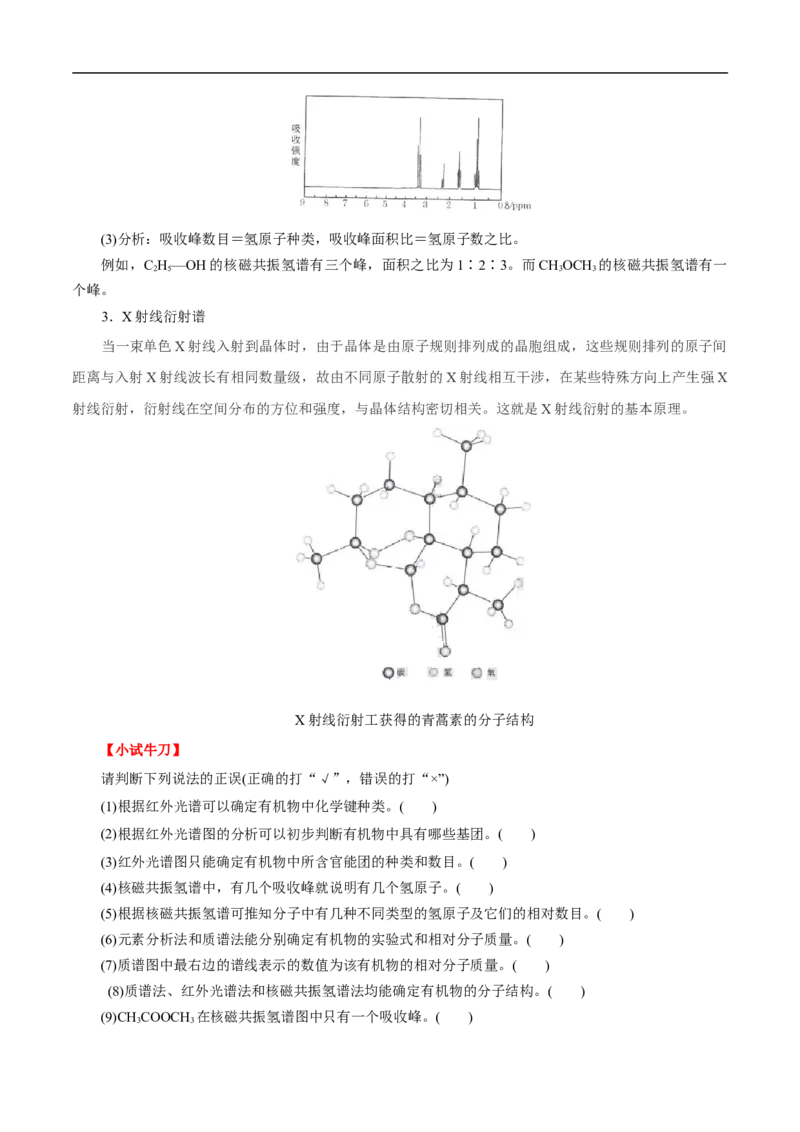
例如:分子式为C HO的红外光谱上发现有O—H键,C—H键和C—O键,可推知该分子的结构简式
2 6
为C H—OH。
2 5
乙醇红外光谱图
2.核磁共振氢谱
(1)作用:测定有机物分子中氢原子的种类和数目。
(2)原理:处在不同化学环境中的氢原子因产生共振时吸收电磁波的频率不同,在谱图上出现的位置也
不同,而且吸收峰的面积与氢原子数成正比。
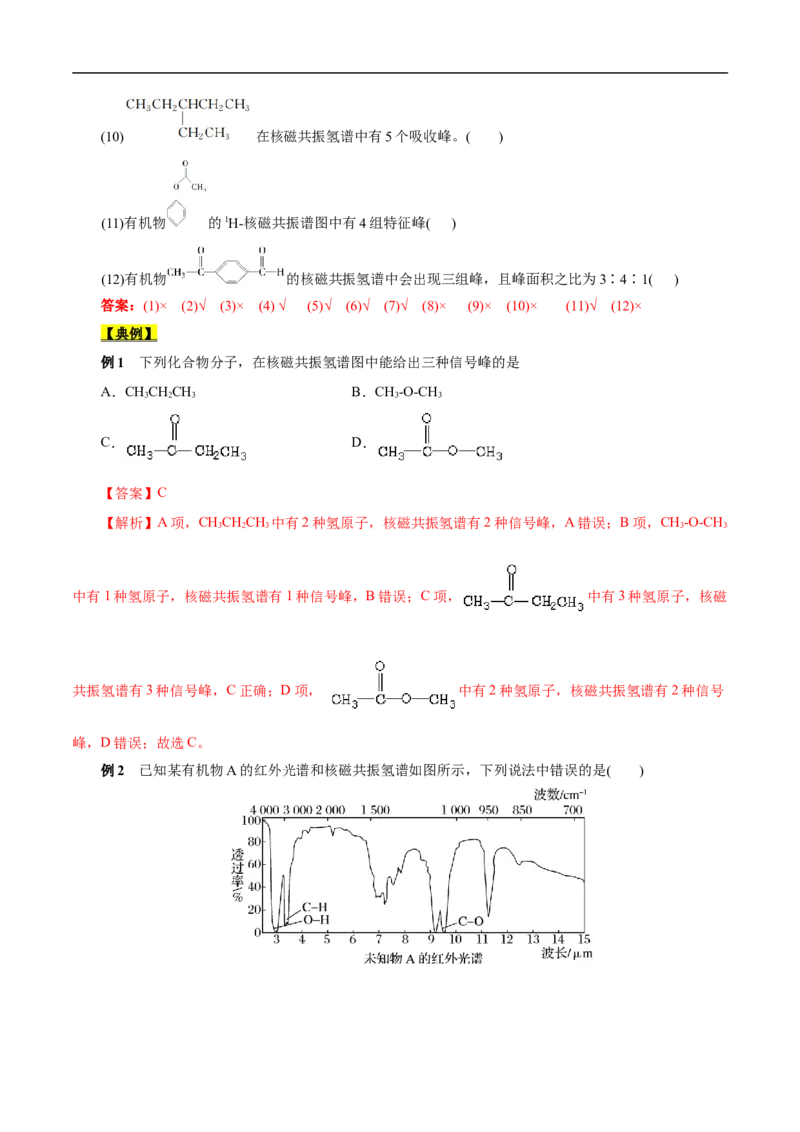
(CH)CHCH 的核磁共振氢谱如下图:
3 2 3(3)分析:吸收峰数目=氢原子种类,吸收峰面积比=氢原子数之比。
例如,C H—OH的核磁共振氢谱有三个峰,面积之比为1∶2∶3。而CHOCH 的核磁共振氢谱有一
2 5 3 3
个峰。
3.X射线衍射谱
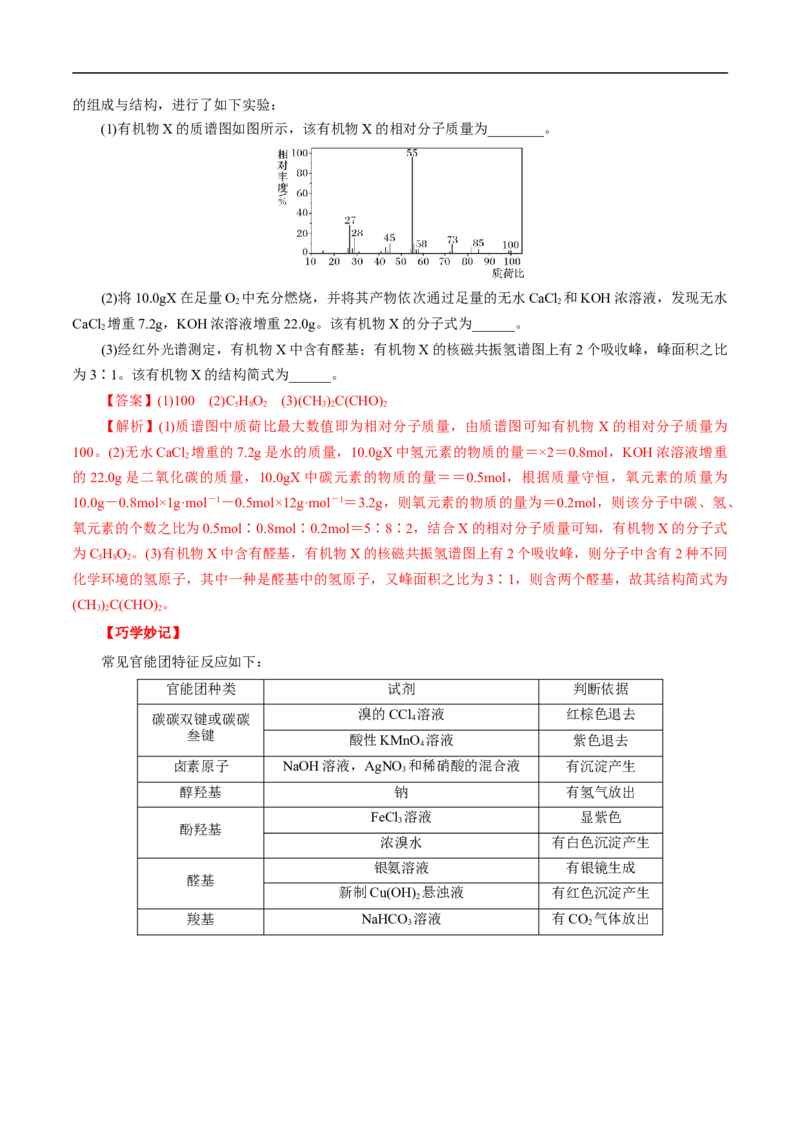
当一束单色X射线入射到晶体时,由于晶体是由原子规则排列成的晶胞组成,这些规则排列的原子间
距离与入射X射线波长有相同数量级,故由不同原子散射的X射线相互干涉,在某些特殊方向上产生强X
射线衍射,衍射线在空间分布的方位和强度,与晶体结构密切相关。这就是X射线衍射的基本原理。
X射线衍射工获得的青蒿素的分子结构
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)根据红外光谱可以确定有机物中化学键种类。( )
(2)根据红外光谱图的分析可以初步判断有机物中具有哪些基团。( )
(3)红外光谱图只能确定有机物中所含官能团的种类和数目。( )
(4)核磁共振氢谱中,有几个吸收峰就说明有几个氢原子。( )
(5)根据核磁共振氢谱可推知分子中有几种不同类型的氢原子及它们的相对数目。( )
(6)元素分析法和质谱法能分别确定有机物的实验式和相对分子质量。( )
(7)质谱图中最右边的谱线表示的数值为该有机物的相对分子质量。( )
(8)质谱法、红外光谱法和核磁共振氢谱法均能确定有机物的分子结构。( )
(9)CH COOCH 在核磁共振氢谱图中只有一个吸收峰。( )
3 3(10) 在核磁共振氢谱中有5个吸收峰。( )
(11)有机物 的1H-核磁共振谱图中有4组特征峰( )
(12)有机物 的核磁共振氢谱中会出现三组峰,且峰面积之比为3∶4∶1( )
答案:(1)× (2)√ (3)× (4) √ (5)√ (6)√ (7)√ (8)× (9)× (10)× (11)√ (12)×
【典例】
例1 下列化合物分子,在核磁共振氢谱图中能给出三种信号峰的是
A.CHCHCH B.CH-O-CH
3 2 3 3 3
C. D.
【答案】C
【解析】A项,CHCHCH 中有2种氢原子,核磁共振氢谱有2种信号峰,A错误;B项,CH-O-CH
3 2 3 3 3
中有1种氢原子,核磁共振氢谱有1种信号峰,B错误;C项, 中有3种氢原子,核磁
共振氢谱有3种信号峰,C正确;D项, 中有2种氢原子,核磁共振氢谱有2种信号
峰,D错误;故选C。
例2 已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C.仅由A的核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的化学式为C HO,则其结构简式为CH—O—CH
2 6 3 3
【答案】D
【解析】红外光谱图中给出的化学键有C—H键、O—H键和C—O键三种,A项正确;核磁共振氢谱
图中峰的个数即代表氢的种类,故B项正确;核磁共振氢谱峰的面积表示氢的数目比,在没有明确化学式
的情况下,无法得知氢原子总数,C项正确;若A为CH—O—CH ,则无O—H键,与所给红外光谱图不
3 3
符,且其核磁共振氢谱图应只有1个峰,与核磁共振氢谱图不符,故D项不正确。
【对点提升】
对点1 下列说法不正确的是( )
A.通过红外光谱分析可以区分丁醛和乙酸乙酯
B.可利用原子光谱上的特征谱线来鉴定元素
C. 的核磁共振氢谱中有5组峰
D.对乙醇和二甲醚进行质谱分析,质谱图完全相同
【答案】D
【解析】A项,红外光谱仪可确定有机物中官能团及化学键,丁醛含醛基,乙酸乙酯含酯基,则红外
光谱仪可以区分丁醛和乙酸乙酯,故A正确;B项,不同元素原子的吸收光谱或发射光谱不同,常利用原
子光谱上的特征谱线来鉴定元素,故B正确;C项, 有5种H原子,则核磁共振氢
谱中有5组峰,故C正确;D项,乙醇和二甲醚结构不同,最大荷比相同,则质谱图不完全相同,故D错
误;故选D。
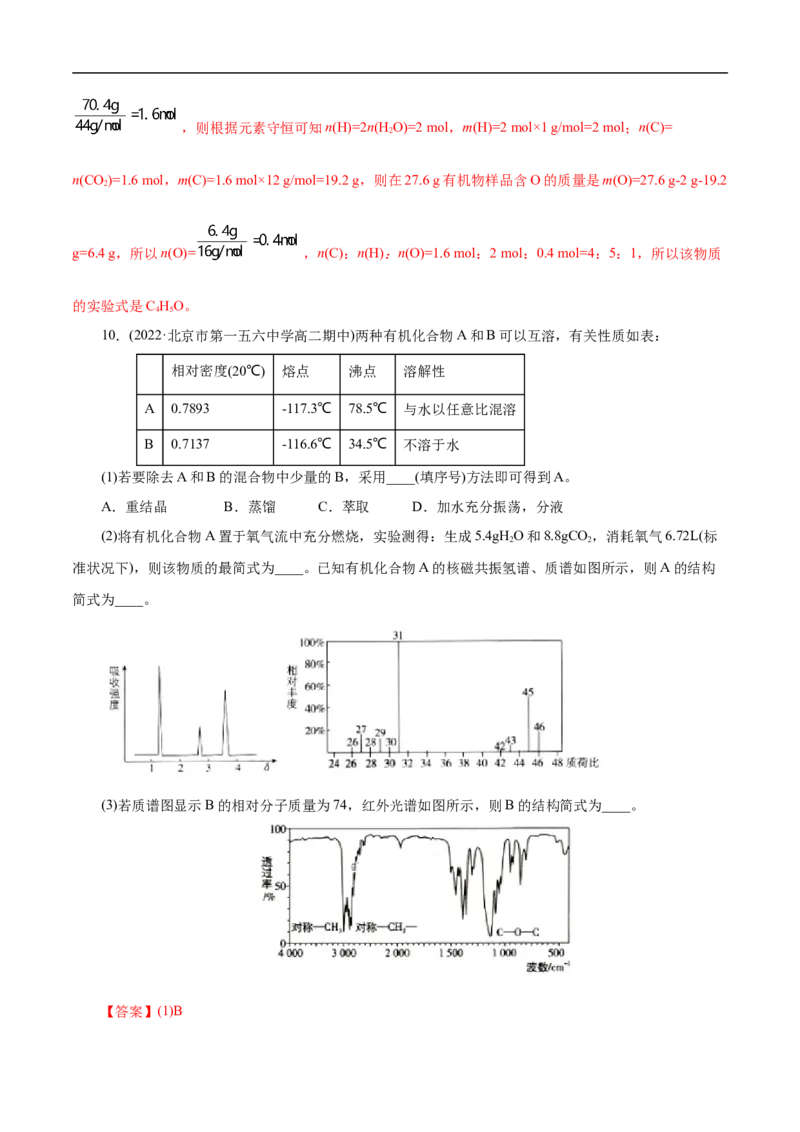
对点2 有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行了如下实验:
(1)有机物X的质谱图如图所示,该有机物X的相对分子质量为________。
(2)将10.0gX在足量O 中充分燃烧,并将其产物依次通过足量的无水CaCl 和KOH浓溶液,发现无水
2 2
CaCl 增重7.2g,KOH浓溶液增重22.0g。该有机物X的分子式为______。
2
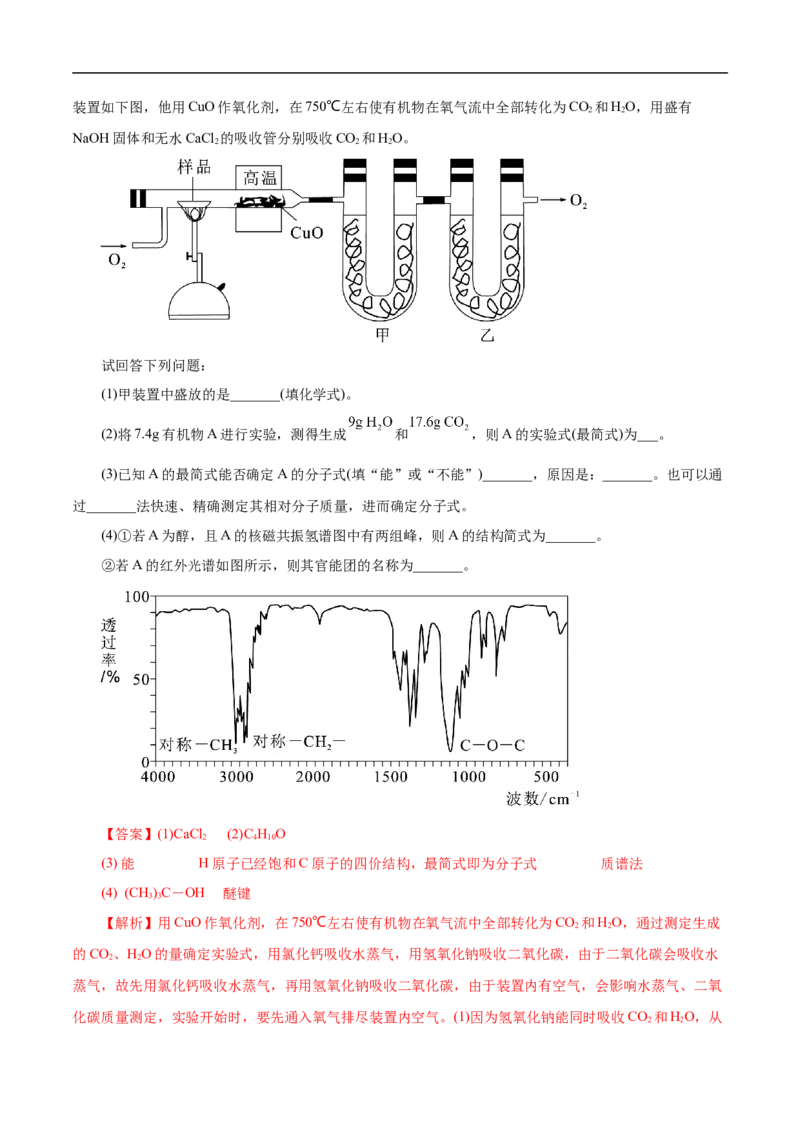
(3)经红外光谱测定,有机物X中含有醛基;有机物X的核磁共振氢谱图上有2个吸收峰,峰面积之比
为3∶1。该有机物X的结构简式为______。
【答案】(1)100 (2)C HO (3)(CH )C(CHO)
5 8 2 3 2 2
【解析】(1)质谱图中质荷比最大数值即为相对分子质量,由质谱图可知有机物 X的相对分子质量为
100。(2)无水CaCl 增重的7.2g是水的质量,10.0gX中氢元素的物质的量=×2=0.8mol,KOH浓溶液增重
2
的22.0g是二氧化碳的质量,10.0gX中碳元素的物质的量==0.5mol,根据质量守恒,氧元素的质量为
10.0g-0.8mol×1g·mol-1-0.5mol×12g·mol-1=3.2g,则氧元素的物质的量为=0.2mol,则该分子中碳、氢、
氧元素的个数之比为0.5mol∶0.8mol∶0.2mol=5∶8∶2,结合X的相对分子质量可知,有机物X的分子式
为C HO。(3)有机物X中含有醛基,有机物X的核磁共振氢谱图上有2个吸收峰,则分子中含有2种不同
5 8 2
化学环境的氢原子,其中一种是醛基中的氢原子,又峰面积之比为3∶1,则含两个醛基,故其结构简式为
(CH)C(CHO) 。
3 2 2
【巧学妙记】
常见官能团特征反应如下:
官能团种类 试剂 判断依据
溴的CCl 溶液 红棕色退去
碳碳双键或碳碳 4
叁键
酸性KMnO 溶液 紫色退去
4
卤素原子 NaOH溶液,AgNO 和稀硝酸的混合液 有沉淀产生
3
醇羟基 钠 有氢气放出
FeCl 溶液 显紫色
3
酚羟基
浓溴水 有白色沉淀产生
银氨溶液 有银镜生成
醛基
新制Cu(OH) 悬浊液 有红色沉淀产生
2
羧基 NaHCO 溶液 有CO 气体放出
3 21.能够快速、微量、精确的测定出有机物的相对分子质量的物理方法是( )
A.质谱法 B.红外光谱法 C.紫外光谱法 D.核磁共振氢谱法
【答案】A
【解析】A项,质谱仪其实是把有机物打成很多小块,会有很多不同的分子出现,其中最大的那个相
对分子质量就是该有机物的相对分子质量,A正确;B项,红外光谱是用于鉴定有机物中所含的各种官能
团,双键,三键,羟基,羧基、羰基等,B错误;C项,紫外光谱是为了了解未知物的初步的化学结构,
从光谱信息中得到该物质的基团或者化学键产生的吸收情况,初步判断该物质的结构信息,C错误;D项,
核磁共振是检验不同环境的H的数量.有多少种不同的H,就有多少个峰,各个峰的高度大致上能显示各
种H的数量比例,D错误。故选A。
2.根据以下信息判断,分离乙醇、乙二醇混合物的最佳方法是( )
熔点/℃ 沸点/℃ 密度/g·cm-3 溶解性
乙醇 -114 78 0.79 与水以任意比例互溶
乙二醇 -13 197 1.11 与水以任意比例互溶
A.分液 B.用水萃取 C.蒸馏 D.重结晶
【答案】C
【解析】由图表可知,常温下乙醇、乙二醇为互溶的液体,沸点相差比较大,所以可以用蒸馏的办法
进行分离,故选C。
3.为提纯下列物质(括号内的为杂质),所选用的除杂试剂和分离方法都正确的是( )
选项 A B C D被提纯物质 乙醇(水) 乙醇(乙酸) 乙烷(乙烯) 溴苯(溴)
除杂试剂 生石灰 氢氧化钠溶液 酸性高锰酸钾溶液 KI溶液
分离方法 蒸馏 分液 洗气 分液
【答案】A
【解析】A项,生石灰与水反应,消耗了乙醇中混有的水,蒸馏可得到乙醇;A项正确;B项,乙醇
易溶于水,利用分液的方法不能将乙醇与盐溶液分离开;B项错误;C项,酸性高锰酸钾溶液可将乙烯氧
化为二氧化碳,引入了新的杂质;C项错误;D项,溴可将KI氧化为碘单质,而碘易溶于溴苯,引入了新
的杂质,D项错误;故选A。
4.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式。
以下用于研究有机物的方法正确的是( )
A.通常用过滤来分离、提纯液态有机混合物
B.质谱仪可以用于确定有机物中氢原子的种类
C.核磁共振氢谱可以用于确定有机物的相对分子质量
D.红外光谱可以用于确定有机物分子中的基团
【答案】D
【解析】分离、提纯液态有机混合物,常根据有机物的沸点不同,用蒸馏的方法分离,而重结晶、萃
取、蒸发不能达到分离的目的,A错误;核磁共振仪用于测定有机物分子中氢原子的种类和数目,质谱仪
用于测定有机物的相对分子质量,B错误;核磁共振氢谱可以用于测定有机物分子中氢原子的种类和数目,
C错误;红外光谱可以用于确定有机物分子中的基团,D正确。
2.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是( )
A.在组装蒸馏装置时,温度计的水银球应伸入液面下
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水
C.用苯萃取溴水时有机层应从下口放出
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤
【答案】B
【解析】A项,蒸馏时,温度计的水银球应在支管口处,故A错误;B项,减少过滤时苯甲酸的损失,
防止过饱和提前析出结晶,故B正确;C项,苯的密度小于水,分液时上层液体从上口倒出,故C错误;
D项,应趁热过滤,故D错误。
3.下列说法中不正确的是( )
A.蒸馏是分离提纯相互互溶的液态有机物的常用方法B.石油分馏可获得乙烯、丙烯和丁二烯
C.通过煤的直接或间接液化,可以获得燃料油及多种化工原料
D.重结晶法提纯苯甲酸时,杂质的溶解度很小或很大均易于除去
【答案】B
【解析】A项,蒸馏是利用互溶物质沸点的不同,分离提纯液态有机物的常用方法,A项正确;B项,
石油经过裂解可获得乙烯、丙烯和丁二烯,B项错误;C项,通过煤的直接或间接液化,可以获得燃料油
及多种化工原料,C项正确;D项,杂质的溶解度很小或很大,都可以根据溶解度的差异进行分离,可用
重结晶的方法提纯苯甲酸,D项正确;故选B。
7.已知青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于有机溶剂,如丙酮、氯仿,可溶于乙醇、
乙醚等,在水中几乎不溶,熔点为156~157 ℃,热稳定性差。乙醚的沸点为35 ℃。如图是从黄花青蒿中提
取青蒿素的工艺流程,下列有关实验操作的说法正确的是 ( )
A.研碎时应该将黄花青蒿置于烧杯中
B.操作Ⅰ是萃取,所用的玻璃仪器有烧杯、分液漏斗
C.操作Ⅱ是蒸馏,所用的玻璃仪器主要有蒸馏烧瓶、酒精灯、冷凝管、温度计、锥形瓶
D.操作Ⅲ是用酒精灯加热,然后加水溶解、过滤
【答案】C
【解析】根据题给流程可知,对黄花青蒿进行干燥、研碎,可以增大黄花青蒿与乙醚的接触面积,提
高青蒿素的浸取率;用乙醚对固体粉末进行浸取后,过滤,可得提取液和残渣;提取液经过蒸馏后可得青
蒿素的粗品;向粗品中加入乙醇,浓缩、结晶、过滤可得精品,据此解答。研碎时应该将黄花青蒿置于研
钵中进行,选项A错误;由上述分析可知,操作Ⅰ是将固体和液体分离的操作,是过滤,选项B错误;操
作Ⅱ是将提取液中的乙醚分离出去的操作,是蒸馏,蒸馏用到的玻璃仪器主要有蒸馏烧瓶、酒精灯、冷凝
管、温度计、锥形瓶,选项C正确;酒精灯加热温度较高,青蒿素热稳定性差,由粗品得精品时不能用酒
精灯加热,选项D错误。
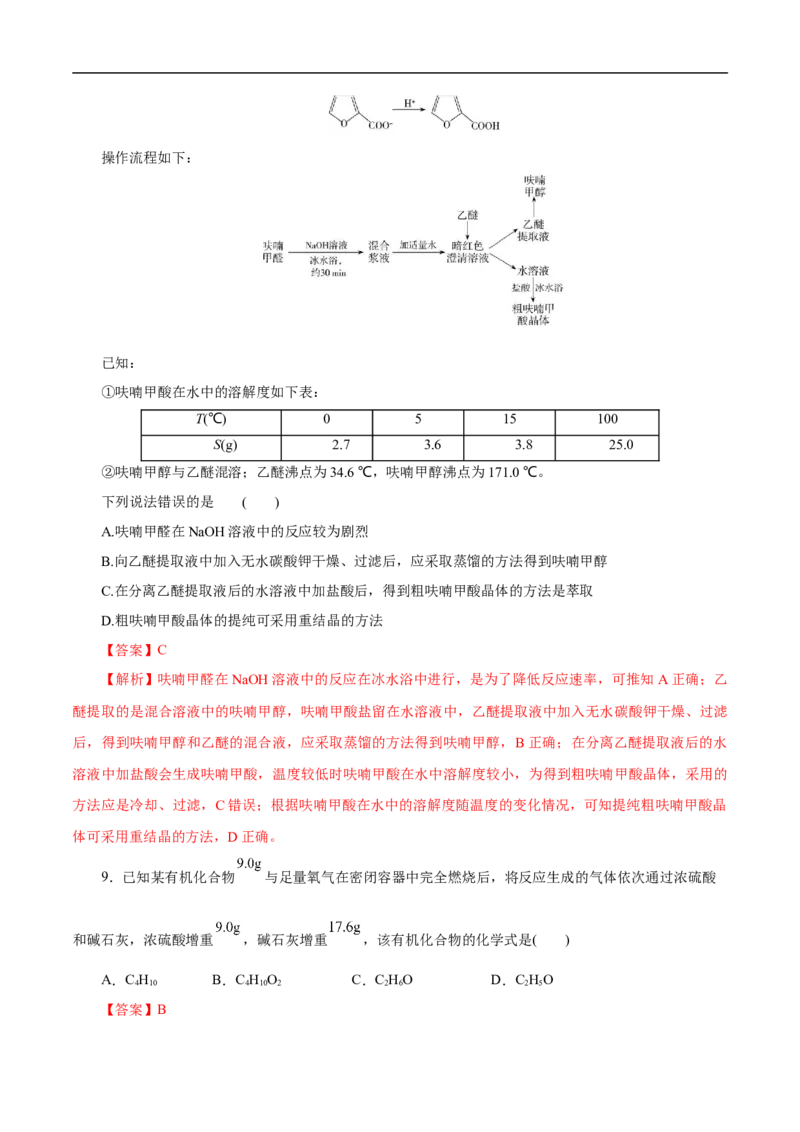
8.实验室可利用呋喃甲醛( )在碱性环境下发生交叉的Cannizzaro反应,生成呋喃甲酸(
)和呋喃甲醇( ),反应过程如下:
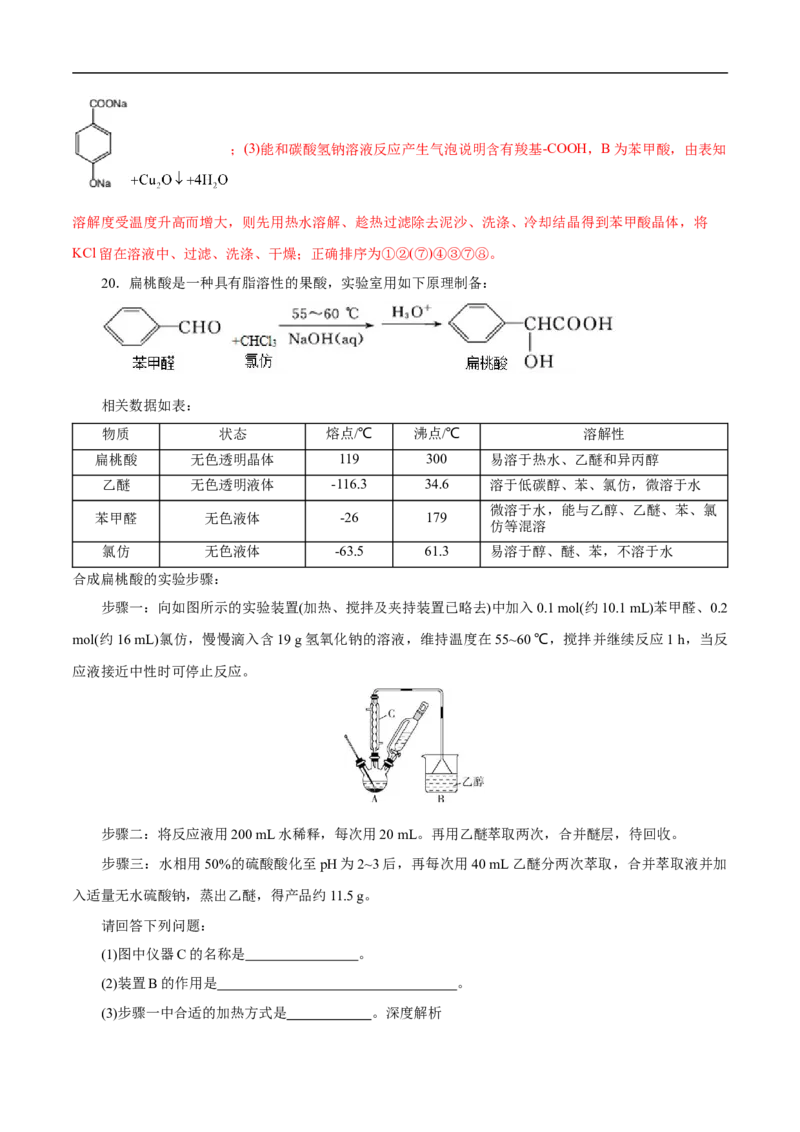
2操作流程如下:
已知:
①呋喃甲酸在水中的溶解度如下表:
T(℃) 0 5 15 100
S(g) 2.7 3.6 3.8 25.0
②呋喃甲醇与乙醚混溶;乙醚沸点为34.6 ℃,呋喃甲醇沸点为171.0 ℃。
下列说法错误的是 ( )
A.呋喃甲醛在NaOH溶液中的反应较为剧烈
B.向乙醚提取液中加入无水碳酸钾干燥、过滤后,应采取蒸馏的方法得到呋喃甲醇
C.在分离乙醚提取液后的水溶液中加盐酸后,得到粗呋喃甲酸晶体的方法是萃取
D.粗呋喃甲酸晶体的提纯可采用重结晶的方法
【答案】C
【解析】呋喃甲醛在NaOH溶液中的反应在冰水浴中进行,是为了降低反应速率,可推知A正确;乙
醚提取的是混合溶液中的呋喃甲醇,呋喃甲酸盐留在水溶液中,乙醚提取液中加入无水碳酸钾干燥、过滤
后,得到呋喃甲醇和乙醚的混合液,应采取蒸馏的方法得到呋喃甲醇,B正确;在分离乙醚提取液后的水
溶液中加盐酸会生成呋喃甲酸,温度较低时呋喃甲酸在水中溶解度较小,为得到粗呋喃甲酸晶体,采用的
方法应是冷却、过滤,C错误;根据呋喃甲酸在水中的溶解度随温度的变化情况,可知提纯粗呋喃甲酸晶
体可采用重结晶的方法,D正确。
9.已知某有机化合物 与足量氧气在密闭容器中完全燃烧后,将反应生成的气体依次通过浓硫酸
和碱石灰,浓硫酸增重 ,碱石灰增重 ,该有机化合物的化学式是( )
A.C H B.C H O C.C HO D.C HO
4 10 4 10 2 2 6 2 5
【答案】B【解析】将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重9.0g为水的质量,碱石灰增重
17.6g为二氧化碳的质量,生成水的物质的量为: ,9.0g该有机物分子中含有H原子的物
质的量为:5.6mol×2=1.0mol,生成二氧化碳的物质的量为: ,9.0g该有机物分子中含有
C原子的物质的量为0.4mol,9.0g该有机物分子中含有氧原子的物质的量为:
,该有机物分子中含有C、H、O原子的物质的量之比为:
0.4mol:1.0mol:0.2mol=2:5:1,该有机物的最简式为C HO,由于H原子没有饱和,该有机物分子式
2 5
为C H O,故选B。
4 10 2
10.某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO 和7.2 g H O。下列说法正确的是( )
2 2
A.该化合物仅含碳、氢两种元素
B.该化合物中碳、氢原子个数比为1∶8
C.无法确定该化合物是否含有氧元素
D.该化合物中一定含有氧元素
【答案】D
【解析】经计算,n(CO)==0.2 mol,n(H O)==0.4 mol,即6.4 g的化合物中,含0.2 mol C,0.8
2 2
mol H,即2.4 g C,0.8 g H,则该化合物含有(6.4-2.4-0.8)g O,即3.2 g O,则氧元素的物质的量为=0.2
mol,所以6.4 g的化合物含0.2 mol C,0.8 mol H,0.2 mol O,则经分析,6.4 g的化合物含0.2 mol C,0.8
mol H,0.2 mol O,A错误;碳、氢原子的个数比等于其元素的物质的量之比,即 0.2 mol∶0.8 mol=
1∶4,B错误;经分析,6.4 g的化合物中含有0.2 mol O,C错误;经分析,该化合物中含有氧元素,D正
确。
11.将有机物完全燃烧,生成CO 和HO。将12 g该有机物的完全燃烧产物通过浓HSO ,浓HSO
2 2 2 4 2 4
增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。则该有机物的分子式为( )
A.C H B.C HO C.C HO D.C HO
4 10 2 6 3 8 2 4 2
【答案】C
【解析】n(H O)==0.8 mol,n(CO)==0.6 mol,该有机物中m(H)=2×0.8 mol×1 g/mol=1.6 g,m(C)
2 2
=0.6 mol×12 g/mol=7.2 g,因m(H)+m(C)<12 g,所以该有机物中含有氧元素,则有机物中氧元素的物质
的量为:n(O)==0.2 mol。则n(C)∶n(H)∶n(O)=0.6∶(0.8×2)∶0.2=3∶8∶1,因此看出氢原子已饱和,故有机物的分子式为C HO。
3 8
12.某有机化合物只含碳、氢、氧元素,其中w(C)=60%,w(H)=13.33%,0.2 mol 该有机物的质量
为12 g,则它的分子式为( )
A.CH B.C HO C.C HO D.CHO
4 3 8 2 4 2 2
【答案】B
【解析】方法一 先求12 g有机物中含C、H的质量,进而确定含O的质量,再求实验式和相对分子
质量,最后求分子式。N(C)∶N(H)∶N(O)=[w(C)/12]∶[w(H)/1]∶[w(O)/16]=(60%/12)∶(13.33%/
1)∶(26.67%/16)≈3∶8∶1。设其分子式为(C HO) ,则n=60/60=1。所以其分子式为C HO。方法二 先
3 8 n 3 8
求相对分子质量,再求1 mol该有机物中分别含C、H、O三种元素的物质的量,进而确定分子式。
13.某有机化合物3.2g,在O 中完全燃烧生成4.4gCO 和3.6gH O,下列说法正确的是( )
2 2 2
A.该有机物一定是烃 B.该有机物的分子式为CHO
4
C.该有机物中可能含有氧元素 D.该有机物一定不能与钠反应
【答案】B
【解析】化合物3.2g燃烧生成4.4gCO 和3.6gH O,根据元素守恒则一定含有C、H元素,4.4g二氧化
2 2
碳的物质的量为 =0.1mol,n(C)=n(CO )=0.1mol,m(C)=0.1mol×12g/mol=1.2g,3.6g水的物质的量
2
为 =0.2mol,n(H)=2n(H O)=0.4mol,m(H)=0.4g,由于m(C)+m(H)=1.2g+0.4g=1.6g<3.2g,所以该
2
化合物中一定含有氧元素,该化合物为烃的含氧衍生物,氧元素的物质的量为 =0.1mol,故化合
物中n(C):n(H):n(O)=0.1mol∶0.4mol∶0.1mol=1∶4∶1,此有机物的分子式为CHO。A项,该有机物分
4
子中含有C、H、O三种元素,属于烃的含氧衍生物,A错误;B项,由分析,该有机物的分子式为
CHO,B正确;C项,根据分析可知,该有机物中一定含有氧元素,C错误;D项,分子式为CHO的物
4 4
质可能为CHOH,能与Na发生反应生成CHONa和H,D错误;故选B。
3 3 2
14.0.2mol某烃X在O 中充分燃烧,将燃烧后的产物依次通入浓硫酸,碱石灰中,浓硫酸增重
2
14.4g,碱石灰增重26.4g,则烃X的分子式为( )
A.C H B.C H C.C H D.C H
2 4 3 6 3 8 4 8
【答案】C【解析】烃X在O 中充分燃烧,浓硫酸增重14.4g,为水的质量,水的物质的量为 =0.8mol,
2
氢原子的物质的量为1.6mol,碱石灰增重26.4g,为二氧化碳的质量,二氧化碳的物质的量为
=0.6mol,碳原子的物质的量为0.6mol,则烃X中C原子的个数为 =3,H原子的个数为 =8,
烃X的分子式为:C H,故选C。
3 8
15.4.4g某有机化合物(M)在足量氧气中完全燃烧,只生成11gCO 和5.4gH O。则下列分析正确的是(
2 2
)
A.M中不含氧元素
B.M能与H 发生加成反应
2
C.M分子中含有的官能团只可能为羟基
D.M的同分异构体(不考总立体异构)的数目大于8
【答案】D
【解析】4.4g某有机化合物燃烧生成11gCO 和5.4gH O,根据元素守恒则一定含有C、H元素,11g
2 2
二氧化碳的物质的量为 ,n(C)=n(CO )=0.25mol,m(C)=nM=0.25mol×12g/
2
mol=3g,5.4g水的物质的量为: ,n(H)=2n(H O)=0.6mol,m(H)=0.6g,由于m(C)
2
+m(H)=3g+0.6g=3.6g<4.4g,所以该化合物中一定含有氧元素,且n(O)= ,该有机
物分子中含有的故化合物中N(C):N(H):N(O)=0.25mol:0.6mol:0.05mol=5:12:1,其最简式为
C H O。A项,由分析可知,M一定含有氧元素,故A错误;B项,结合分析可知,该有机物最简式为
5 12
C H O,为饱和结构,只含有单键,不能与氢气发生加成反应,故B错误;C项,M分子为C H O,可能
5 12 5 12
结构为CHCHCHCHCHOH,官能团是羟基,可能是CHCH CHOCH CH,官能团是醚键,故C错误;
3 2 2 2 2 3 2 2 2 3D项,M分子为C H O,结构为 、 、 、
5 12
等,还含有醚类,同分异构体超过8种,故D正确;故选D。
16.有机物X完全燃烧的产物只有二氧化碳和水,元素组成分析发现,该物质中碳元素的质量分数为
64.86%,氢元素的质量分数为13.51%,它的核磁共振氢谱有5组明显的吸收峰,且只含有两个甲基。下列
关 于有机物X的说法正确的是( )
A.分子式为C HO
3 8
B.X催化氧化能生成醛
C.X消去可以生成两种结构的烯烃(考虑顺反异构)
D.与X互为官能团异构的同分异构体有3种
【答案】D
【解析】由题意可知,有机物X中碳元素和氢元素的质量分数之和小于100%,完全燃烧的产物只有
二氧化碳和水,则有机物中含有氧元素,氧元素的质量分数为(1—64.86%—13.51%)=21.63%,有机物中碳、
氢、氧的个数比为 =4:10:1,有机物的实验式为C H O,由碳原
4 10
子和氢原子的个数比可知,有机物实验式就是分子式,由核磁共振氢谱有5组明显的吸收峰,且只含有两
个甲基可知,该有机物为 。A项,有机物的分子式为C H O,故A错误;B项,X
4 10
为 发生催化氧化反应生成 ,不能得到醛类,故B错误;C项,X在一定条件下,发生消去反应生成 、 、 ,故
C错误;D项,与 含有相同官能团的同分异构体有1—丁醇、2—甲基—1—丙醇、2—
甲基—2—丙醇,共3种,故D正确;故选D。
17.某物质的分子式为C HO,取该物质ag在足量的O 中充分燃烧后,将产物全部通入过量的
x y z 2
NaO 中,若NaO 固体的质量增加了bg,且a