文档内容
选择题标准练
选择题标准练(一)
1.化学与生产、生活密切相关。下列说法错误的是( )
A.“神舟十三号”载人飞船中使用的碳纤维是一种新型有机高分子材料
B.将餐厨垃圾中的油脂分离出来,可以制造肥皂和生物柴油
C.二氧化硫可用作葡萄酒的食品添加剂,用来杀菌和防止色素被氧化
D.冬奥会颁奖花束用的编制材料是以羊毛为原料的绒线,其主要成分是蛋白质
答案 A
解析 碳纤维是新型无机非金属材料,故 A错误;油脂经过皂化反应制肥皂,油脂与甲醇
在催化剂条件下发生酯交换制造生物柴油,故 B正确;羊毛的主要成分是蛋白质,故D正
确。
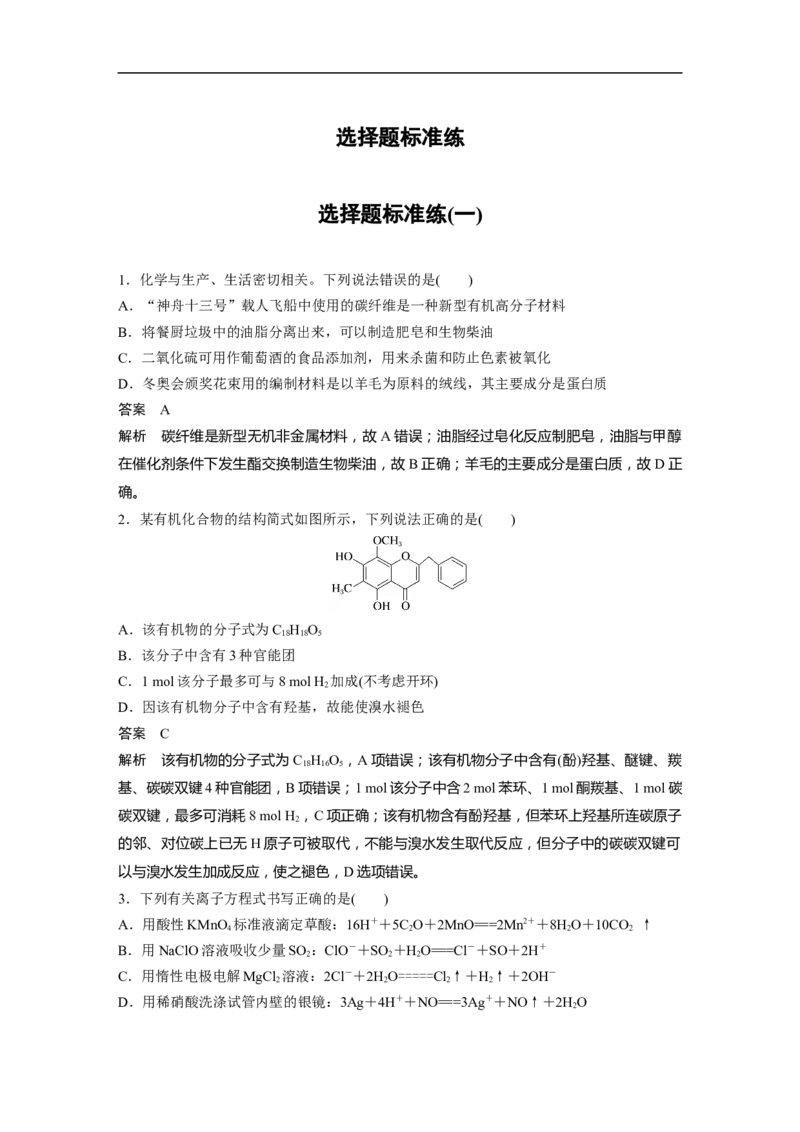
2.某有机化合物的结构简式如图所示,下列说法正确的是( )
A.该有机物的分子式为C H O
18 18 5
B.该分子中含有3种官能团
C.1 mol该分子最多可与8 mol H 加成(不考虑开环)
2
D.因该有机物分子中含有羟基,故能使溴水褪色
答案 C
解析 该有机物的分子式为C H O ,A项错误;该有机物分子中含有(酚)羟基、醚键、羰
18 16 5
基、碳碳双键4种官能团,B项错误;1 mol该分子中含2 mol苯环、1 mol酮羰基、1 mol碳
碳双键,最多可消耗8 mol H ,C项正确;该有机物含有酚羟基,但苯环上羟基所连碳原子
2
的邻、对位碳上已无H原子可被取代,不能与溴水发生取代反应,但分子中的碳碳双键可
以与溴水发生加成反应,使之褪色,D选项错误。
3.下列有关离子方程式书写正确的是( )
A.用酸性KMnO 标准液滴定草酸:16H++5C O+2MnO===2Mn2++8HO+10CO ↑
4 2 2 2
B.用NaClO溶液吸收少量SO :ClO-+SO +HO===Cl-+SO+2H+
2 2 2
C.用惰性电极电解MgCl 溶液:2Cl-+2HO=====Cl↑+H↑+2OH-
2 2 2 2
D.用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO===3Ag++NO↑+2HO
2答案 D
解析 草酸属于弱酸,不能拆写为离子,A不正确;用次氯酸钠溶液吸收少量二氧化硫有次
氯酸生成:3ClO-+SO +HO===2HClO+SO+Cl-,B不正确;溶液中含有镁离子,根据
2 2
离子反应条件判断,生成氢氧化镁沉淀,C不正确;稀硝酸和银反应生成硝酸银、一氧化氮
和水,D正确。
4.以锂硫电池(电池的总反应为2Li+xS===LiS)为电源,电解含(NH )SO 的废水制备硫酸
2 x 4 2 4
和化肥的原理如图(不考虑其他杂质离子的反应)。下列说法正确的是( )
A.a为锂硫电池的负极
B.电解池中膜1和膜2都是阳离子交换膜
C.锂硫电池每消耗2.8 g锂,理论上M室产生2.24 L气体(标准状况)
D.电解一段时间后,原料室中溶液的pH会下降
答案 C
解析 以锂硫电池为电源,通过电解含(NH )SO 的废水制备硫酸和化肥,M室得到硫酸说
4 2 4
明是氢氧根离子放电,电极反应式为2HO-4e-===4H++O↑,则a为正极,b为负极,故
2 2
A错误;电解池中阴离子移向阳极,SO通过膜1由原料室移向M室,则膜1为阴离子交换
膜,故 B 错误;由锂硫电池总反应 2Li+xS===LiS 可得负极反应式为 2Li+S-2e-
2 x
===LiS ,消耗2.8 g锂即物质的量为=0.4 mol,转移0.4 mol e-,M室的电极反应式为
2 x
2HO-4e-===4H++O↑,生成0.1 mol氧气,标准状况下气体体积为0.1 mol×22.4 L·mol-
2 2
1=
2.24 L,故C正确;N室的电极反应是溶液中氢离子放电生成氢气,NH通过膜2由原料室
移向N室,c(NH)减小,使NH+HONH ·H O+H+向左移动,c(H+)减小,原料室中溶
2 3 2
液的pH增大,故D错误。
5.N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol NO与0.5 mol O 充分反应后,混合气体分子中氮原子数目为N
2 A
B.常温下,100 mL 0.1 mol·L-1 Na CO 溶液中阴离子总数目为0.01N
2 3 A
C.常温下,5.6 g Fe与足量浓硝酸完全反应,转移电子数目为0.3N
A
D.等物质的量的乙烷(C H) 与乙醛(C HO)分子中含共用电子对数目均为7N
2 6 2 4 A
答案 A解析 1 mol NO与0.5 mol O 充分反应后,混合气体分子中氮原子的物质的量为1 mol,数
2
目为N ,故A正确;常温下,100 mL 0.1 mol·L-1 Na CO 溶液中,碳酸根离子水解生成氢
A 2 3
氧根离子和碳酸氢根离子,阴离子总数大于0.01N ,故B错误;常温下,Fe在浓硝酸中发
A
生钝化,5.6 g Fe与足量浓硝酸不能完全反应,转移电子数目小于0.3N ,故C错误;1个乙
A
烷分子中含7个共用电子对,1个乙醛分子中含7个共用电子对,等物质的量的乙烷(C H)
2 6
与乙醛(C HO)分子中含共用电子对数目不能确定,故D错误。
2 4
6.短周期元素X、Y、Z的原子序数依次减小,三者组成的化合物M(组成中阴、阳离子个
数比为1∶3,其中阴离子的结构如图)常用作冶炼铝的助熔剂,X是地壳中含量最多的金属
元素,Z无正价。下列说法正确的是( )
A.简单离子半径:X>Z>Y
B.化合物YZ中只含共价键
C.Y和Z的单质都能与水反应产生气体
D.X、Y的单质分别与氧气化合均只得到一种产物
答案 C
解析 由题干信息推知X是Al元素;Z无正价,Z是F元素,M是NaAlF ,Y是Na元素。
3 6
电子层结构相同,核电荷数越多离子半径越小,简单离子半径:F->Na+>Al3+,故A错误;
NaF是离子化合物,只含离子键,故B错误;Na和水反应生成氢氧化钠和氢气,F 和水反
2
应生成HF和氧气,故C正确;Na和氧气反应可以生成NaO、NaO,故D错误。
2 2 2
7.下列有关实验的方案设计、现象和结论都正确的是( )
选项 目的 方案设计 现象和结论
检验某溶液中是 向该溶液中滴加几滴新制氯水,振荡, 溶液变为红色,则该
A
否含有Fe2+ 再加入少量KSCN溶液 溶液中含有Fe2+
在试管中加入0.5 g淀粉和4 mL 2 mol·
判断淀粉是否完 溶液显蓝色,则说明
B L-1 HSO 溶液,加热,冷却后,取少量
2 4
全水解 淀粉未水解
水解后的溶液于试管中,加入碘酒
向两支试管中各加入2 mL 10% H O 溶 滴加 CuCl 溶液的试
2 2 2
探究Cu2+、Mn2+
C 液,再分别加入2滴1 mol·L-1 CuCl 溶 管出现气泡快,说明
2
的催化效果
液、2滴1 mol·L-1 MnSO 溶液 Cu2+的催化效果好
4
装有FeS固体的试管
向两支试管中加入等物质的量的CuS和 产生气泡,装有CuS
比较 CuS 和 FeS
D FeS固体,然后分别加入等体积2 mol·L- 固体的试管无明显现
的K 大小
sp
1的HCl溶液 象,则证明 K (FeS)
sp
>K (CuS)
sp答案 D
解析 Fe2+能被新制氯水氧化成Fe3+,应先加KSCN溶液无现象,后加新制氯水溶液变红色,
证明溶液中含有Fe2+,故A错误;溶液显蓝色,说明淀粉未完全水解或未水解,故B错误;
CuCl 溶液和MnSO 溶液的阴离子不同,不能排除阴离子的干扰,故C错误。
2 4