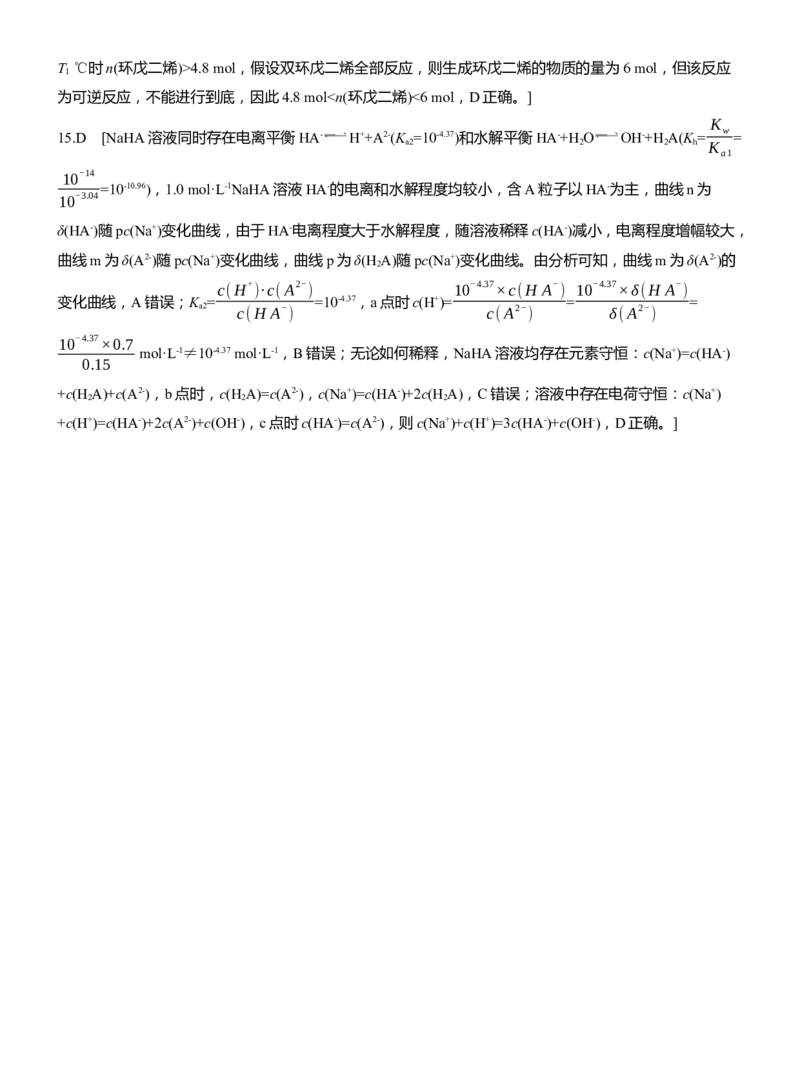文档内容
选择题标准练(二)
(选择题1~10题,每小题3分,11~15题,每小题4分,共50分)
1.生产食盐的主要来源之一为内陆井矿盐。下列说法正确的是( )
A.钻井用的铁制设备被腐蚀的过程涉及原电池原理
B.卤水净化所用的助沉剂聚丙烯酰胺属于无机非金属材料
C.蒸发制盐利用的原理是NaCl的溶解度随温度变化明显
D.食盐中添加I ,可以帮助人们避免碘缺乏
2
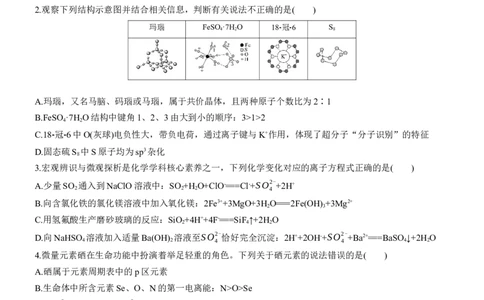
2.观察下列结构示意图并结合相关信息,判断有关说法不正确的是( )
玛瑙 FeSO
4
·7H
2
O 18⁃冠⁃6 S
8
A.玛瑙,又名马脑、码瑙或马瑙,属于共价晶体,且两种原子个数比为2∶1
B.FeSO ·7H O结构中键角1、2、3由大到小的顺序:3>1>2
4 2
C.18⁃ 冠 ⁃6中O(灰球)电负性大,带负电荷,通过离子键与K+作用,体现了超分子“分子识别”的特征
D.固态硫S 中S原子均为sp3杂化
8
3.宏观辨识与微观探析是化学学科核心素养之一,下列化学变化对应的离子方程式正确的是( )
A.少量SO 通入到NaClO溶液中:SO +H O+ClO-===Cl-+SO2- +2H+
2 2 2 4
B.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe3++3MgO+3H O===2Fe(OH) +3Mg2+
2 3
C.用氢氟酸生产磨砂玻璃的反应:SiO +4H++4F-===SiF ↑+2H O
2 4 2
D.向NaHSO 溶液加入适量Ba(OH) 溶液至SO2-恰好完全沉淀:2H++2OH-+SO2- +Ba2+===BaSO ↓+2H O
4 2 4 4 4 2
4.微量元素硒在生命功能中扮演着举足轻重的角色。下列关于硒元素的说法错误的是( )
A.硒属于元素周期表中的p区元素
B.生命体中所含元素Se、O、N的第一电离能:N>O>Se
C.SeO2-能被氧化成SeO2-
3 4
D.硒与机体内氨基酸能通过离子键形成硒蛋白
5.异甘草素具有抗肿瘤、抗病毒等药物功效。合成中间体Z的部分路线如图:下列有关化合物X、Y和Z的说法正确的是( )
A.1 mol Z中含有6 mol碳氧σ键
B.X分子中的所有原子一定共平面
C.Y能发生加成、氧化和消去反应
D.Z与足量的氢气加成后的产物分子中含有3个手性碳原子
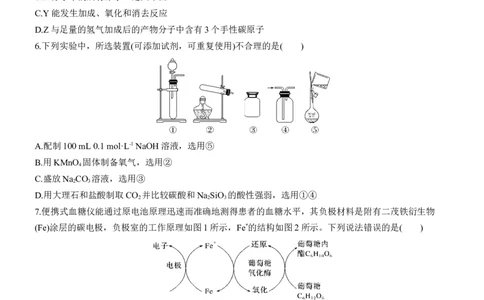
6.下列实验中,所选装置(可添加试剂,可重复使用)不合理的是( )
A.配制100 mL 0.1 mol·L-1 NaOH溶液,选用⑤
B.用KMnO 固体制备氧气,选用②
4
C.盛放Na CO 溶液,选用③
2 3
D.用大理石和盐酸制取CO 并比较碳酸和Na SiO 的酸性强弱,选用①④
2 2 3
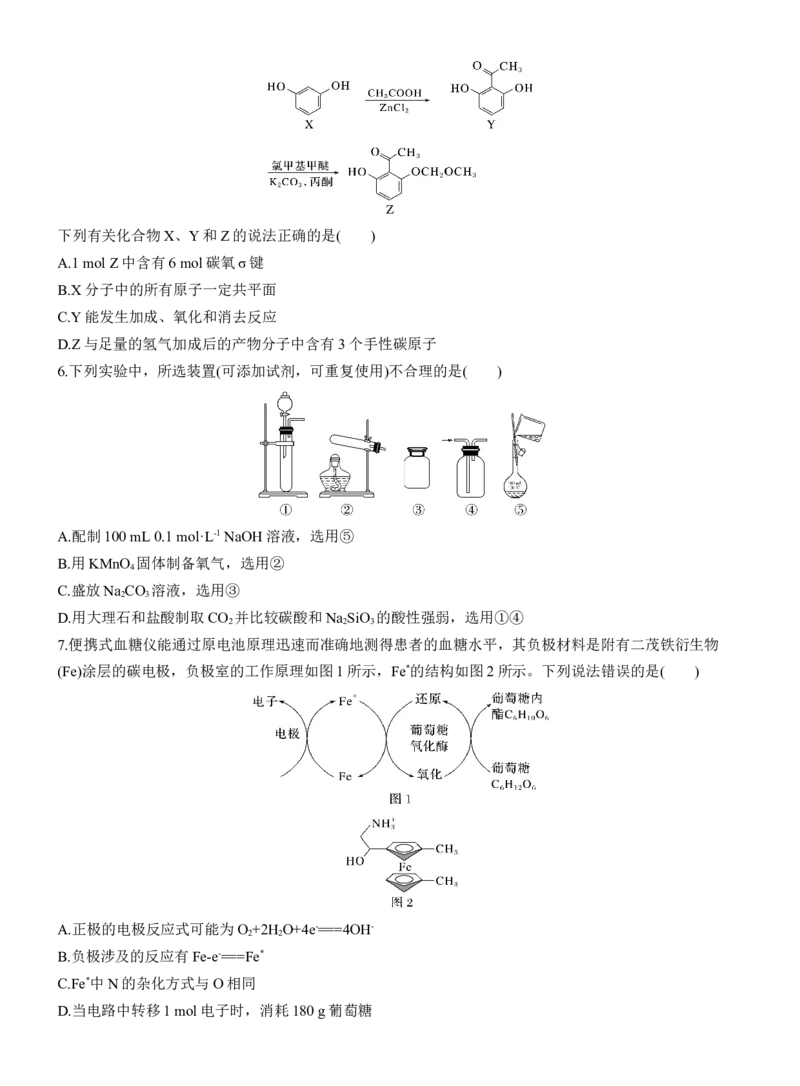
7.便携式血糖仪能通过原电池原理迅速而准确地测得患者的血糖水平,其负极材料是附有二茂铁衍生物
(Fe)涂层的碳电极,负极室的工作原理如图1所示,Fe*的结构如图2所示。下列说法错误的是( )
A.正极的电极反应式可能为O +2H O+4e-===4OH-
2 2
B.负极涉及的反应有Fe-e-===Fe*
C.Fe*中N的杂化方式与O相同
D.当电路中转移1 mol电子时,消耗180 g葡萄糖8.实验室用粉煤灰(主要含Al O ,SiO 等)制备碱式硫酸铝[Al (SO ) (OH) ]溶液,并用于烟气脱硫研究,
2 3 2 2 4 x 6-2x
其转化流程如图所示。下列说法错误的是( )
A.滤渣Ⅰ的主要成分为SiO
2
B.制备碱式硫酸铝[Al (SO ) (OH) ]溶液不涉及氧化还原反应
2 4 x 6-2x
C.调节pH低于3.6会导致溶液中铝元素的含量降低
D.碱式硫酸铝[Al (SO ) (OH) ]溶液多次循环使用后c(SO2- )增大的原因是部分的硫元素被氧化
2 4 x 6-2x 4
9.X、Y、Z、Q、R是分别占据5个主族和前四周期的五种元素,原子序数依次增大。基态Y原子的5个轨
道上都有电子,基态Z原子核外有3个未成对电子,Q的单质(常温下为气态)和NaOH溶液在常温下发生
歧化反应生成两种盐,R的L和M层电子数相同。下列说法正确的是( )
A.Y和R形成的化合物只含有离子键
B.X和Q基态原子的未成对电子数不同
C.元素电负性:Z>Q>R
D.Z和Q形成的分子可能是极性分子
10.工业上使用多种方式解决CO 、SO 、NO 所带来的环境问题。如SNCR技术以尿素作为还原剂实现脱
2 2 2
硝,CH CH(OH)COONa(乳酸钠)、Ca(ClO) 和离子液体(指在室温或接近室温时呈液态的盐类物质,由阴、
3 2
阳离子组成)等溶液可用于气体吸收。已知:25 ℃时,几种酸的电离常数:H SO K =1.3×10-2,
2 3 a1
K =6.2×10-5;CH CH(OH)COOH(乳酸) K=1.4×10-4。下列有关说法正确的是( )
a2 3 a
A.CO 、SO 、NO 均属于大气污染物
2 2 2
B.SNCR脱硝技术存在反应:2CO(N H ) +6NO===5N +2CO +4H O
2 2 2 2 2
C.工业上可利用碱溶液对NO直接进行化学吸收
D.CH CH(OH)COONa(乳酸钠)溶液吸收SO 的离子方程式为2CH CH(OH)COO-
3 2 3
+SO +H O===2CH
CH(OH)COOH+SO2-
2 2 3 3
11.离子液体1⁃ 丁基 ⁃3⁃ 甲基咪唑四氟硼酸盐[Bmim][BF
4
]对许多物质都具有良好的溶解性,其结构如图所示。
下列说法错误的是( )
A.[Bmim][BF ]室温下能导电
4
B.F—B—F键角:BF
>BF-
3 4C.BF-的空间结构为平面正四边形
4
D.[Bmim][BF ]中N的杂化方式只有一种
4
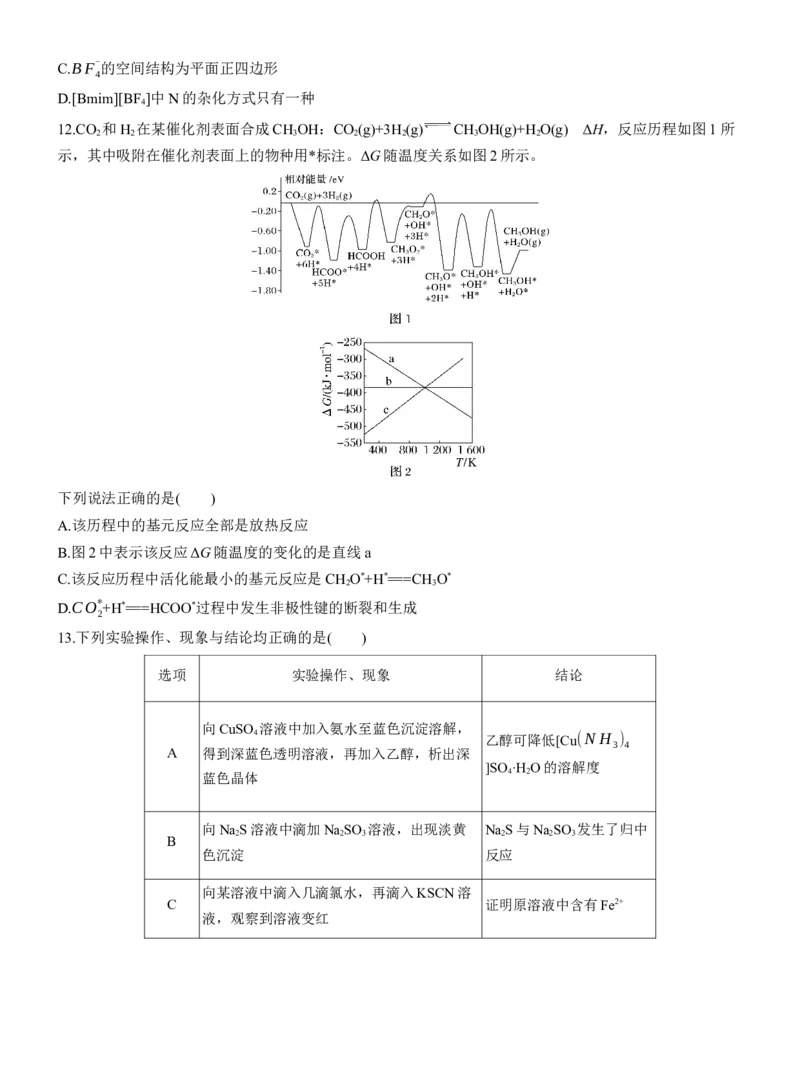
12.CO 和H 在某催化剂表面合成CH OH:CO (g)+3H (g) CH OH(g)+H O(g) ΔH,反应历程如图1所
2 2 3 2 2 3 2
示,其中吸附在催化剂表面上的物种用*标注。ΔG随温度关系如图2所示。
下列说法正确的是( )
A.该历程中的基元反应全部是放热反应
B.图2中表示该反应ΔG随温度的变化的是直线a
C.该反应历程中活化能最小的基元反应是CH O*+H*===CH O*
2 3
D.CO* +H*===HCOO*过程中发生非极性键的断裂和生成
2
13.下列实验操作、现象与结论均正确的是( )
选项 实验操作、现象 结论
向CuSO 溶液中加入氨水至蓝色沉淀溶解,
4 乙醇可降低[Cu(N H )
3 4
A 得到深蓝色透明溶液,再加入乙醇,析出深
]SO ·H O的溶解度
蓝色晶体 4 2
向NaS溶液中滴加NaSO 溶液,出现淡黄 NaS与NaSO 发生了归中
2 2 3 2 2 3
B
色沉淀 反应
向某溶液中滴入几滴氯水,再滴入KSCN溶
C 证明原溶液中含有Fe2+
液,观察到溶液变红先向一支试管中加入1 mL 10%蔗糖溶液和5
D 滴10%H SO 溶液,加热煮沸,再加入新制 蔗糖未发生水解
2 4
的Cu(OH) ,加热,无砖红色沉淀产生
2
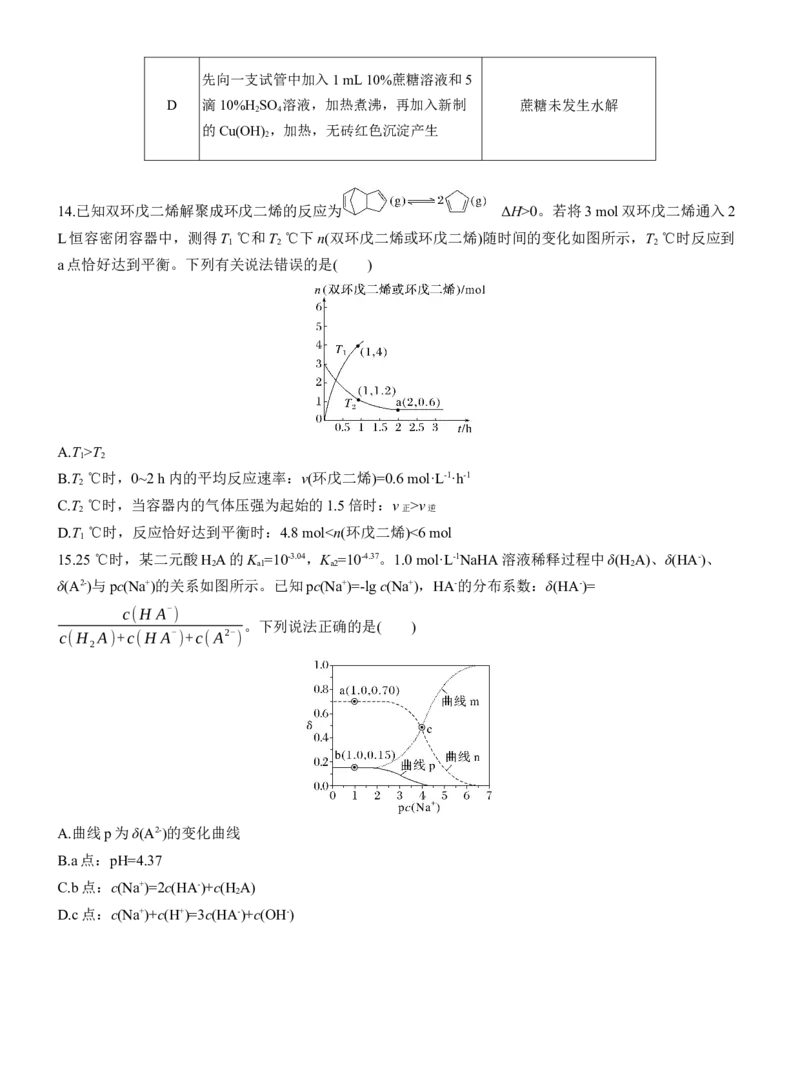
14.已知双环戊二烯解聚成环戊二烯的反应为 ΔH>0。若将3 mol双环戊二烯通入2
L恒容密闭容器中,测得T ℃和T ℃下n(双环戊二烯或环戊二烯)随时间的变化如图所示,T ℃时反应到
1 2 2
a点恰好达到平衡。下列有关说法错误的是( )
A.T >T
1 2
B.T ℃时,0~2 h内的平均反应速率:v(环戊二烯)=0.6 mol·L-1·h-1
2
C.T ℃时,当容器内的气体压强为起始的1.5倍时:v >v
2 正 逆
D.T ℃时,反应恰好达到平衡时:4.8 mol1>2,故B正确;18⁃冠⁃6中O与K+之间并非离子键,而是
通过配位键结合,故C错误;固态硫S 中S原子形成了2个共价键,还有2个孤电子对,故采用sp3杂化,
8
故D正确。]
3.B [二氧化硫具有比较强的还原性、次氯酸根具有比较强的氧化性,少量SO 通入到NaClO溶液中,发
2
生氧化还原反应,由于次氯酸根过量,生成的氢离子会和次氯酸根结合生成次氯酸,其离子方程式为
SO +H
O+3ClO-===Cl-+SO2-
+2HClO,故A错误;氯化铁和氯化镁为强酸弱碱盐,其溶液呈酸性,所以向
2 2 4
含氯化铁的氯化镁溶液中加入氧化镁,氧化镁和氯化铁溶液反应生成氢氧化铁和氯化镁,其反应的离子方
程式为2Fe3++3MgO+3H O===2Fe(OH) +3Mg2+,故B正确;磨砂玻璃中的二氧化硅能和氢氟酸反应,生成
2 3
SiF 和H O,由于氢氟酸为弱酸,不能拆开写,故C错误;向NaHSO 溶液加入适量Ba(OH)
溶液至SO2-
4 2 4 2 4
恰好完全沉淀,反应的离子方程式为H++OH-+SO2-
+Ba2+===BaSO ↓+H O,故D错误。]
4 4 2
4.D
[基态硒的价层电子排布式为4s24p4,属于p区元素,A项正确;根据氧化还原的性质,SeO2-
中硒为
3
+4价,能被氧化成+6价的SeO2-
,C项正确;Se与氨基酸通过共价键结合,D项错误。]
4
5.A [根据单键都是σ键,双键是1个σ键1个π键,1 mol Z中含有6 mol碳氧σ键,A正确;因为—OH
中的氧是sp3杂化,再加上单键可以旋转,X分子中的所有原子不一定共平面,B错误;Y中官能团有酮羰
基、酚羟基,能发生加成、氧化反应,因苯环结构稳定,酚羟基不能发生消去反应,C错误;Z与足量的
氢气加成后的产物分子为 其中含有4个手性碳原子(标*),D错误。]
6.C [配制100 mL 0.1 mol·L-1NaOH溶液需选用100 mL容量瓶,移液时需通过玻璃棒引流,A正确;因为
碳酸钠水解显碱性,能和玻璃中的SiO 反应,实验室盛放Na CO 溶液的试剂瓶不能用磨口玻璃塞,C错
2 2 3
误;用大理石和盐酸制取CO 并比较碳酸和Na SiO 的酸性强弱,选用①可以制得CO ,但由于HCl具有
2 2 3 2
挥发性,故需先经过④(盛有饱和NaHCO 溶液)洗气后再通入④(盛有Na SiO 溶液),D正确。]
3 2 3
7.D [若在有氧条件下,正极的电极反应式可能为O +2H O+4e-===4OH-,A项正确;由图可知,负极涉及
2 2
的反应有Fe-e-===Fe*,B项正确;Fe*中N和O都是sp3杂化,C项正确;1 mol葡萄糖的质量为180 g,转
化为1 mol葡萄糖内酯转移2 mol电子,D项错误。]8.C [酸浸时发生反应的离子方程式为Al O +6H+===2Al3++3H O,而SiO 不溶于酸,滤渣Ⅰ的主要成分为
2 3 2 2
SiO ,A正确;制备过程没有发生元素化合价变化,B正确;调节pH低于3.6会导致溶液中H+较多,会使
2
碱式硫酸铝[Al (SO ) (OH) ]的生成量减少,但溶液中铝元素的含量不会降低,C错误;碱式硫酸铝溶液
2 4 x 6-2x
循环吸收SO ,溶于水的SO 与水反应生成H SO ,加热时,部分被氧化为H SO
,使溶液中c(SO2-
)增大,
2 2 2 3 2 4 4
D正确。]
9.D [X为H;Y的5个轨道上都有电子,Y可能为第二周期的N、O、F;Z有3个未成对电子,Z可能为
第二周期的N或第三周期的P,故Y是O或F,Z是P;Q的单质和NaOH发生歧化反应生成两种盐,Q为
第三周期的Cl,确定Y是O,不是与Cl同主族的F;R的L和M层的电子数相同,3d轨道未排电子,在
第四周期又不位于第ⅠA族,所以R是Ca。综上,X为H,Y是O,Z是P,Q为Cl,R是Ca。Y和R形
成的化合物过氧化钙中含有非极性共价键和离子键,故A项错误;X和Q,即H和Cl,基态原子的未成对
电子数均为1,故B项错误;同周期元素电负性从左到右依次增大,同主族元素电负性从上到下依次减小,
所以元素电负性:Cl>P>Ca,故C项错误;Z和Q形成的PCl 分子是极性分子,故D项正确。]
3
10.B [CO 不属于大气污染物,A项错误;NO不能单独被碱液吸收,C项错误;CH CH(OH)COONa(乳酸
2 3
钠)溶液吸收SO 的离子方程式为CH CH(OH)COO-+SO +H
O===HSO-
+CH CH(OH)COOH,D项错误。]
2 3 2 2 3 3
11.C [离子液体指在室温或接近室温时呈液态的盐类物质,由阴、阳离子组成,故室温下能导电,A项正
确;BF
中B是sp2杂化,而BF-
中B是sp3杂化,故F—B—F键角:BF
>BF-
,B项正确;根据VSEPR
3 4 3 4
3+1-4×1
模型可知,BF-
中B的价层电子对数为4+ =4,空间结构为正四面体形,C项错误;[Bmim]
4 2
[BF ]中形成大π键,N的杂化方式只有一种,D项正确。]
4
12.C [该反应历程中有的基元反应中,反应物的总能量小于生成物的总能量,是吸热反应,A项错误;由
图可知,该反应的ΔH<0,ΔS<0,由ΔG=ΔH-TΔS可知,直线方程的斜率是正值,则为直线c,B项错误;
从图中可以看出,活化能最小的反应是CH O*+H*===CH
O*,C项正确;CO*
+H*===HCOO*过程中断裂碳
2 3 2
氧键,形成碳氢键,则发生极性键的断裂和生成,D项错误。]
13.A [Na SO
溶液呈碱性,S2-和SO2-
在碱性溶液中能共存,向Na S溶液中滴加Na SO 溶液,不会出现
2 3 3 2 2 3
淡黄色沉淀,B项错误;向某溶液中滴入几滴氯水,再滴入KSCN溶液,观察到溶液变红,可能原溶液中
只有Fe3+无Fe2+,C项错误;加入新制的Cu(OH) 之前应该先加NaOH溶液调至碱性,D项错误。]
2
14.B [由图可知,T ℃时,双环戊二烯前1 h减少1.8 mol,相当于环戊二烯增加3.6 mol,T ℃时,环戊二
2 1
烯前1 h增加4 mol>3.6 mol,所以T >T ,A正确;T ℃时,0~2 h内的平均反应速率:v(环戊二烯)=
1 2 2
2×(3mol-0.6mol)
=1.2 mol·L-1·h-1,B错误;由a点可知,T ℃时,平衡时气体总物质的量为2×(3
2 L×2 h 2
mol-0.6 mol)+0.6 mol=5.4 mol,是初始3 mol的1.8倍,气体的压强为起始时的1.5倍时,反应正向进行,v
>v ,C正确;在T ℃时,反应达到平衡,消耗双环戊二烯的物质的量为(3-0.6)mol=2.4 mol,此时生成
正 逆 2
环戊二烯的物质的量为2.4×2 mol=4.8 mol,因为T >T ,该反应为吸热反应,升高温度,平衡正向移动,则
1 2T ℃时n(环戊二烯)>4.8 mol,假设双环戊二烯全部反应,则生成环戊二烯的物质的量为6 mol,但该反应
1
为可逆反应,不能进行到底,因此4.8 mol