文档内容
选择题标准练(四)
1.近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识判断错
误的是( )
A.我国科学家实现了二氧化碳加氢制汽油,汽油是烃的混合物
B.北斗三号卫星搭载了精密计时的铷原子钟,铷的金属性强于钾
C.万米深海潜水器“奋斗者”号外壳所用的钛合金属于金属材料
D.“天和核心舱”用到氮化硼陶瓷,石墨型、金刚石型氮化硼互为同素异形体
答案 D
解析 汽油是烃的混合物,A正确;铷是第五周期碱金属元素,金属性强于相同主族第四周
期的钾,B正确;金属材料包括纯金属和它们的合金,钛合金属于金属材料,C正确;石墨
型氮化硼和金刚石型氮化硼都是化合物,不互为同素异形体,D错误。
2.奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物,也
是国家的战略储备药。其结构如图所示,下列关于奥司他韦的说法正确的是( )
A.该物质能使酸性高锰酸钾溶液褪色
B.属于芳香化合物
C.1 mol该物质最多可与3 mol Br 发生加成反应
2
D.分子中官能团种类有4种
答案 A
解析 由结构简式可知,奥司他韦分子中含有的碳碳双键能被酸性高锰酸钾溶液氧化,使高
锰酸钾溶液褪色,故A正确;由结构简式可知,奥司他韦分子中不含有苯环,不属于芳香
化合物,故B错误;由结构简式可知,奥司他韦分子中含有的碳碳双键能与溴水发生加成
反应,1 mol奥司他韦分子只能与1 mol Br 发生加成反应,故C错误;由结构简式可知,奥
2
司他韦分子中含有的官能团为碳碳双键、醚键、酰胺基、氨基、酯基,共5种,故D错误。
3.下列离子方程式书写正确的是( )
A.足量碳酸氢钙溶液与少量澄清石灰水反应:HCO+Ca2++OH-===CaCO ↓+HO
3 2
B.纯碱与足量醋酸溶液反应:CO+2H+===CO↑+HO
2 2
C.氢氧化镁与稀硫酸反应:H++OH-===HO
2
D.足量CO 通入澄清石灰水中:CO+Ca2++2OH-===CaCO ↓+HO
2 2 3 2
答案 A
解析 足量 Ca(HCO ) 溶液与少量 Ca(OH) 反应的离子方程式为 Ca2++OH-+
3 2 2HCO===CaCO ↓+HO,A正确;CHCOOH为弱电解质,离子方程式中不可拆,离子方程
3 2 3
式应写为2CHCOOH+CO===2CHCOO-+HO+CO↑,B错误;Mg(OH) 为沉淀,离子
3 3 2 2 2
方程式中不可拆,离子方程式应写为Mg(OH) +2H+===Mg2++2HO,C错误;足量CO 通
2 2 2
入澄清石灰水中,反应生成Ca(HCO ),离子方程式应写为CO+OH-===HCO,D错误。
3 2 2
4.我国科学家设计了一种能将苯酚(C HO)氧化为CO 和HO的原电池—电解池组合装置
6 6 2 2
(如图所示,其中·OH是具有强氧化性的羟基自由基),实现发电、环保二位一体。下列说法
正确的是( )
A.电极的电势比较:c>b>a>d
B.c电极区有氢气生成,溶液质量减小
C.d电极区发生反应: HO-e-===·OH+H+,28·OH+C HO===6CO↑+17HO
2 6 6 2 2
D.工作时,Ⅱ 室中Na+、Cl-数目都减小,则M、N分别为阴、阳离子交换膜
答案 C
解析 a极发生还原反应:Cr O+6e-+7HO===2Cr(OH) +8OH-,该电极为原电池正极,b
2 2 3
极苯酚失电子被氧化为CO ,电极反应式为C HOH-28e-+11HO===6CO↑+28H+,该
2 6 5 2 2
电极为原电池负极,c极为电解池阴极,电极反应为2H++2e-===H↑,d极为电解池阳极,
2
电极反应为 HO-e-===H++·OH,·OH 可进一步氧化苯酚,化学方程式为 C HOH+
2 6 5
28·OH===6CO↑+17HO,据此答题。电极的电势比较:a(正极)>d(阳极)>c(阴极)>b(负极),
2 2
A错误;c电极区消耗2 mol H+生成氢气,则有2 mol H+由右室进入左室,所以溶液质量不
变,B错误;由分析可知,a为正极,原电池中阳离子向正极移动,阴离子向负极移动,Ⅱ
室中Na+透过M膜进入a极区,Cl-透过N膜进入b极区,所以M为阳离子交换膜,N为阴
离子交换膜,D错误。
5.N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1 mol月球表面的氦-3(3He)含有的质子数为3N
A
B.1 mol N 和3 mol H 反应生成NH 的分子数为2N
2 2 3 A
C.1 L 0.1 mol·L-1 NH Cl溶液中,NH的数目为0.1N
4 A
D.26 g C H 与C H 混合物中含C—H的数目为2N
2 2 6 6 A
答案 D
解析 He的质子数为2,1 mol氦-3(3He)含有的质子数为2N ,故A错误;合成氨的反应为可
A
逆反应,不能进行彻底,故NH 的分子数小于2N ,故B错误;1 L 0.1 mol·L-1 NH Cl 溶液
3 A 4
中NH Cl的物质的量为0.1 mol,NH是弱碱阳离子,在水溶液中会水解,故NH的数目小于
40.1N ,故C错误;C H 与C H 具有相同的最简式CH,26 g C H 与C H 混合物中含C—H的
A 2 2 6 6 2 2 6 6
数目为×N mol-1=2N ,故D正确。
A A
6.W、X、Y、Z、R为原子序数依次增大(小于20),且分属不同主族的元素,由它们组成
的物质RWXY Z 是激光器的核心材料,其中R、W、X的化合价与主族序数相同,R的主
2 3 2
族序数是其周期序数的。Y是地壳中含量最高的元素,Z单质为18电子分子。下列说法正
确的是( )
A.X的最高价氧化物对应的水化物为弱酸
B.R的单质与冷水反应缓慢
C.原子半径:R>W>Z>Y
D.非金属性:Y>Z
答案 A
解析 据题给信息分析知R为K,Y为O,Z为F,因为W、X、Y(O)、Z(F)的原子序数依
次增大,所以W、X位于第二周期,设其化合价依次为a、b,则1+2a+b-3×2-2=0,
2a+b=7,仅当a=2、b=3时合理,所以W为Be,X为B,该物质是KBe BOF 。硼的非
2 3 2
金属性较弱,其最高价氧化物对应的水化物HBO 为弱酸,A项正确;K的单质与冷水反应
3 3
剧烈,B项错误;原子半径:K>Be>O>F,C项错误;非金属性:O<F,D项错误。
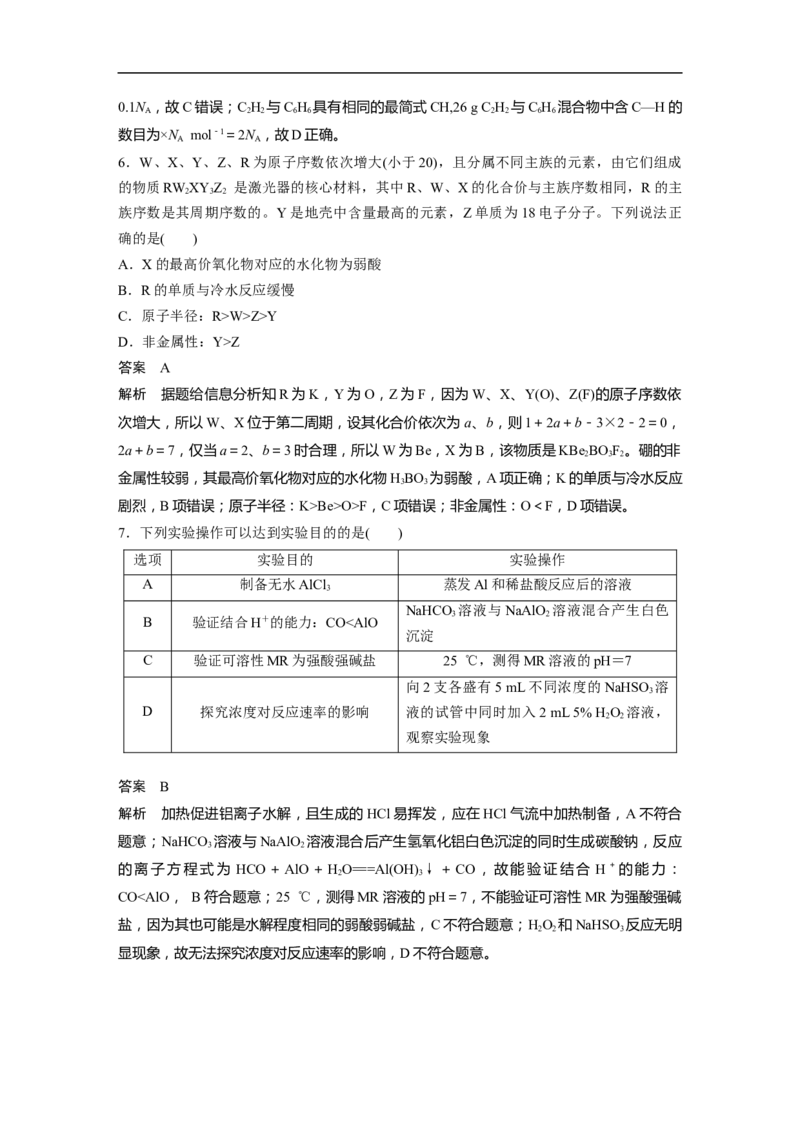
7.下列实验操作可以达到实验目的的是( )
选项 实验目的 实验操作
A 制备无水AlCl 蒸发Al和稀盐酸反应后的溶液
3
NaHCO 溶液与NaAlO 溶液混合产生白色
3 2
B 验证结合H+的能力:CO