文档内容
通关 02 化学用语 方程式的书写
【高考预测】预测考向,总结常考点及应对的策略
【误区点拨】点拨常见的易错点
【抢分通关】分析命题热点,把握解题技巧,精选名校模拟题
概率预测 ☆ ☆ ☆ ☆ ☆
题型预测 选择题、填空题☆ ☆ ☆ ☆ ☆
①化学用语的综合考查
考向预测
②离子方程式的书写
化学用语属于化学学科重要的基础性知识,随着新高考自主命题省份的增多,以及选择题题目的增多,单
独考查化学用语的题目也随之增多,主要考查考生对不同形式化学用语的识别能力,考查应用化学用语准
确表示物质性质和化学变化的能力。根据试题考查点的不同,可将本专题分为两个考向:一是表示物质组
成化学用语的正误判断;二是表示物质变化化学用语的正误判断。化学用语的考查以对知识的识记、再现
能力为主,题型多为选择题,在近几年高考中单独命题较少;化学用语是化学学科的专有语言,是化学学
科素养的重要组成部分,属于高频考点,主要出现在Ⅱ卷非选择题中,如离子方程式的书写是每年高考命
题的热点,题型为填空题,主要出现在工业流程题和实验题中。
技法1 “电子式”书写的一般程序
(1)一判断:首先要判断是阴离子还是阳离子,是离子化合物还是共价化合物。
(2)二注意:①共价化合物仅有电子对的偏移,没有电子的得失,所以不能用“[ ]”,而离子化合物有电子
的得失,所以阴离子和复杂阳离子应用“[ ]”;②根据原子的成键规则,要注意判断原子的连接顺序及共
用电子对的数目。
技法2 非氧化还原反应陌生化学(离子)方程式的书写
新情境下非氧化还原类化学(离子)方程式的书写,因没有涉及元素化合物的变化,故组成物质的各元素
在发生反应时复分解重组,生成常见物质,一般用观察法即可配平。
1、书写非氧化还原反应化学(离子)方程式的步骤:
①根据实验事实写出反应物和生成物的化学式。
②配平化学方程式。
③注明化学方程式发生的条件并注明“↑ ”、“↓”。2、书写技巧
(1)运用“证据→推理→符号”思路书写新情况化学(离子)方程式的基本过程如下:“读”取题目中
的有效信息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即
可轻松写出规范的方程式。
(2)根据“中和”原理或“强酸制弱酸”原理书写化学(离子)方程式,如酸(酸式盐)与碱可发生中和反
应、强酸与弱酸盐可以反应。
(3)根据“广义”的水解书写化学(离子)方程式:广义的水解观认为,无论是盐的水解还是非盐的水
解,其最终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质。
(4)根据对热稳定性的理解书写化学(离子)方程式,如铵盐、弱酸酸式盐、难溶氢氧化物、难溶碳酸
盐受热易分解。
(5)多元弱酸盐与其多元弱酸反应生成其酸式盐。
技法3 氧化还原反应陌生化学(离子)方程式的书写
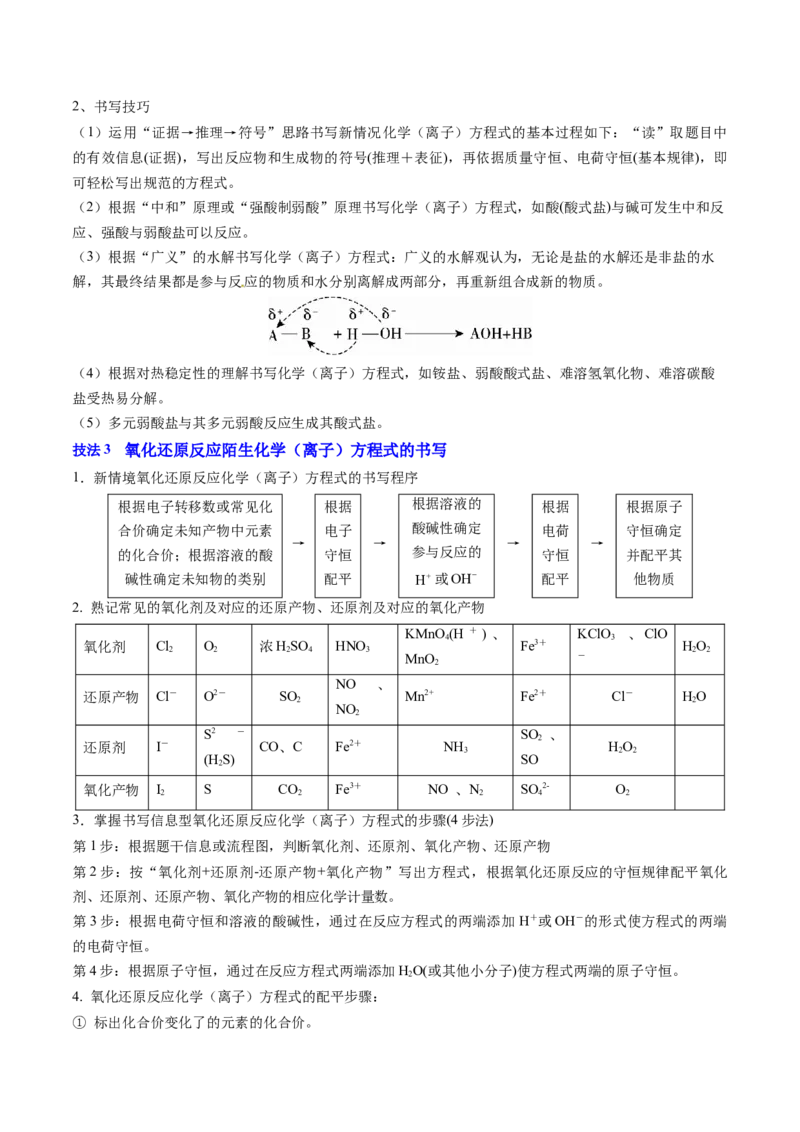
1.新情境氧化还原反应化学(离子)方程式的书写程序
根据电子转移数或常见化 根据 根据溶液的 根据 根据原子
合价确定未知产物中元素 电子 酸碱性确定 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 参与反应的 守恒 并配平其
碱性确定未知物的类别 配平 H或OH 配平 他物质
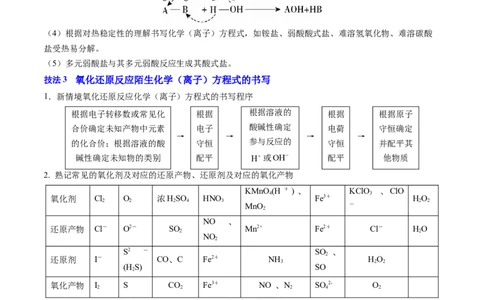
2. 熟记常见的氧化剂及对应的还原产物、还原剂及对应的氧化产物
KMnO (H + ) 、 KClO 、ClO
4 3
氧化剂 Cl O 浓HSO HNO Fe3+ HO
2 2 2 4 3 2 2
MnO -
2
NO 、
还原产物 Cl- O2- SO Mn2+ Fe2+ Cl- HO
2 2
NO
2
S2 - SO 、
2
还原剂 I- CO、C Fe2+ NH HO
3 2 2
(H S) SO
2
氧化产物 I S CO Fe3+ NO 、N SO 2- O
2 2 2 4 2
3.掌握书写信息型氧化还原反应化学(离子)方程式的步骤(4步法)
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧化
剂、还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的两端
的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
4. 氧化还原反应化学(离子)方程式的配平步骤:
① 标出化合价变化了的元素的化合价。② 列变化:分别标出化合价升高数和化合价降低数
③ 根据化合价升降总数相等确定发生氧化还原反应的物质的化学计量数。
④ 利用元素守恒,观察配平其他物质
5. “补缺”的技巧——缺项化学(离子)方程式的配平:
配平化学(离子)方程式时,有时要用H+、OH-、HO来使化学方程式两边电荷及原子守恒,总的原则是
2
酸性溶液中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:
酸性环境 碱性环境
反应物中少氧 左边加HO,右边加H+ 左边加OH-,右边加HO
2 2
反应物中多氧 左边加H+,右边加HO 左边加HO,右边加OH-
2 2
【易错提醒】绝不可能出现的情况:H+→OH- 或者OH-→H+。
技法4 离子方程式的正误判断
第一步:判断是否符合客观事实
(1)只有实际发生的离子反应才能书写。
(2)方程式中的化学式、各种符号及反应产物必须符合客观事实。
第二步:化学式拆分的准确性
同时满足易溶、易电离两个条件的物质才能改写为离子形式,否则以化学式表示。
第三步:判断产物的正确性
(1)分析变价元素产物的合理性。
(2)反应物的量不同,产物不同。
(3)滴加顺序不同,产物不同。
第四步:判断守恒性
(1)原子是否守恒。离子方程式两边同种元素的原子个数相等。
(2)电荷是否守恒。离子方程式两边的电荷总数相等。
(3)氧化还原反应中电子得失是否守恒。
技法5 化学用语试题题型特点
1.本类试题主要分为两种形式:一是无主题的四个无关联选项正误的判斯,可简称为“0十4”型;二是有
主题的四个无关联选项正误的判断,可简称为“1十4”型;
2.四个选项的考查点各不相同,常见有核素、电子式,结构简式、球棍模型、空间填充模型、电子排布
式、轨道表示式、化学健、化合价等;
3.每个选项均由两部分组成:一是需要表示的对象以及化学用语类型:二是化学用语。
技法6 化学用语的解题模型
1.元素符号和化学式的书写:
方法:熟记元素符号和名称,正确书写化学式。
注意:化合物中各元素正负化合价的代数和为零。
2.离子符号的书写:
方法:先写出物质的化学式,然后在元素符号的右上角标出离子所带电荷数,先写数字后写正负号,数字
为1时省略。注意:离子符号前的数字表示离子的个数。
3.化学方程式的书写:
方法:根据反应事实和质量守恒定律书写化学方程式。
注意:化学方程式必须配平;反应条件、沉淀和气体的符号等要正确书写。
4.质量守恒定律的应用:
方法:根据化字反应前后元素种类不变、原子种类和数目不变解题。
注意:适用于解释化学反应的现像和预测新物质的组成。
5.根据化学式计算:
方法:根据化学式计值物质的相对分子质量:组成元素的质量比.某元素的质量分数等。
注意:计时数值要准确,单位要正确。
6.化合价的应用:
方法:根据化合物中各元素正负化合价的代数和为零的原则,计算出未知元素的化合价。
注意:化合价标在元素符号的正上方,且正负号在前、数字在后。
一、化学用语使用要注意“四个误区”:
(1)书写电子式时要注意:①明确是离子化合物还是共价化合物;②切勿漏掉未成键电子对;③理清原子的
排列顺序,如 ;④离子(或根)带电荷,基团不显电性,如 OH-为 ,—OH 为
。
(2)结构简式需保留官能团,如CH==CH ,不能写成CHCH ,还要注意有机物中原子的连接情况,如—
2 2 2 2
NO ,不能写成—ON。
2 2
(3)各“式”切勿张冠李戴:是名称还是化学式,是分子式还是实验式,是结构式还是结构简式,是原子结
构示意图还是离子结构示意图,是化学方程式还是离子方程式等。
(4)化学方程式或离子方程式要遵守质量守恒,化学计量数要最简,注明反应条件并注意“↑”“↓”“
”“===”“―→”符号的使用。
二、有机物结构表示方法中的“四个误区”:
误区一 把简单有机物的分子式与结构简式等同起来,如C HOH是乙醇的结构简式而非分子式,乙醇的
2 5
分子式是C HO。
2 6
误区二 把不饱和烃结构中的碳碳双键或三键省略,如乙烯的结构简式误写为CHCH ,乙炔的结构简式
2 2
误写为CHCH等。
误区三 比例模型与球棍模型辨别不清,从而产生错误,原因是未能理解它们的特点及二者的区别。
误区四 把电子式和结构式混写在同一个分子结构中,出现错误的式子。
三、书写电子式、结构式和结构简式时易出现的误区
1.“·”或“×”使用混乱如HO 的电子式应为 ,易误写成 。
2 2
2.错误使用括号
(1)如HO 的电子式应为 ,易误写成 。
2 2
(2)如 的电子式应为 ,易误写成 。
(3)如HCl的电子式为 ,易误写成 。
3.共用电子对数目写错
(1)如CO 的电子式应为 ,易误写成 。
2
(2) 的电子式应为 ,易误写成 。
4.复杂离子与简单离子混淆不清
(1)如 的电子式应为 ,易误写成 。
(2)如Cl-的电子式应为 ,易误写成Cl-。
5.原子结合顺序写错
如HClO的电子式应为 ,易误写成 。
6.混淆电子式与化学式的书写
(1)如NaO 的电子式应为 ,易误写成 。
2 2
(2)如NaS的电子式为应为 ,易误写成 。
2
7.“→”与“ ”表示意义不清
(1)如 ,易误写成 。
(2)如HCl的形成过程: ,易误写成 。
8.漏写孤电子对
(1)如N 的电子式应为 ,易误写成 。
2
(2)如NH 的电子式应为 ,易误写成 。
3
9.根、基电子式混淆不清
如OH−的电子式应为 ,易误写成 。10.误将电荷数标成化合价
如NaO 的电子式应为 ,易误写成 。
2 2
11.离子符号与离子电子式混淆不清
的电子式应为 易写成 。
12.书写结构式时易出现的错误
(1)如次氯酸的结构式应为H—O—Cl,易误写成H—Cl—O。
(2)如聚丙烯的结构简式应为: ,易误写成 。
(3)如二氧化碳的结构式为:O=C=O,易误写成O—C—O。
(4)如 的结构式为: ,易误写成 。
13.书写结构简式时易出现的错误
(1)如乙烯的结构简式为:CH=CH ,易误写成 。
2 2
(2)如聚丙烯的结构简式为: ,易误写成
(3)如反式聚异戊二烯的结构简式为: ,易误写成 。
四、化学(离子)方程式的书写常见错误分析
化学方程式是重要的化学用语,也是学习化学的重要工具。正确书写化学(离子)方程式,是学好它的前
提和保证。下面就书写化学(离子)方程式的常见错误分析如下,希望同学们知错而改,以免犯同样的错
误。
1、违背客观事实,随意臆造反应。
只有明确知道一个化学反应真实发生,才能相应地书写出反应的化学(离子)方程式。不能不顾客观事实,
随意臆造实际不存在或不发生的反应。
2、违背质量守恒定律,未配平原子个数。
任何一个化学反应都必须遵循质量守恒定律,也就是说在化学反应前后,各种原子个数保持不变
如果没有配平化学方程式,就违背了该定律,将导致化学方程式出错。这是最常见的错误,希望引起
同学们的注意。
3、错写物质的化学式,导致错误的化学方程式
正确书写物质的化学式,是正确书写化学(离子)方程式的保证。书写化学式必项满足各元素化合价的代数
和为零,如果物质的化学式写错,就必然导致化学方程式出错。4、任意改变条件,不注或乱注条件
有的化学反应需要在一定条件下进行,如点然、加热、高温等,此时需注明反应的条件。如果反
应是在常温下进行,则可省略反应条件。改变了反应条件,可能使反应停止或生成物改变。
5、错把催化剂当反应物或生成物。
有些化学反应需要用到催化剂,以改变反应速率。催化剂的质量和化学性质在反应前后不变,属
于反应的条件,但不属于反应物或生成物。
6、气体(沉淀)符号使用不当。
有些化学反应生成了气体或固体,需要用符号来表示,但并不是所有生成气体或固体的反应都
必须标出。若反应物中有气体(或固体)参与,生成了气体或固体),则不需标明。
7、化学计量数之比不是最简整数比。
在化学(离子)方程式中,各化学式前的系数称为化学计量数。化学计量数表示参与反应的各物质的分子个
数比,应为最简比。
8、短线未改等号,导致前功尽弃。
书写化学(离子)方程式的最后一步是将化学方程式中的短线改成等号,这标志一个化学方程式书写结束
了,在实际学习过程中,同学们最容易忽略这一点。
【热点一】表示物质组成化学用语的正误判断
1.(2024·广东·一模)下列化学用语表达正确的是
A. 的结构式:Cl-S-S-Cl
B.基态Mn原子价层电子轨道表示式:
C.四氯化碳分子的空间填充模型:
D. 的原子结构示意图:
2.(2024·湖南岳阳·二模)下列有关化学用语表示正确的是
A. 的电子式:
B.填充模型 可以表示甲烷分子,也可以表示四氯化碳分子C.能体现环己烷 稳定空间构型的键线式:
D.甲醛中π键的电子云轮廓图:
3.(2024·广西柳州·三模)下列化学用语或图示表达正确的是
A.HCl的电子式: B.基态碳原子的轨道表示式:
C.中子数为7的氮原子: D. 的VSEPR模型:
4.(2024·天津南开·一模)下列有关化学用语表示不正确的是
A.反-2-丁烯的结构简式:
B. 的电子式:
C.金刚石中碳原子杂化轨道类型:
D. 的VSEPR模型:
5.(2024·河北·一模)下列化学用语或图示不正确的是
B.4-乙基-1,4-辛二烯 C.三氯化磷
A.氯化铯晶胞 D. 电子式
结构简式 结构式
【热点二】表示物质变化化学用语的正误判断
1.(2024·湖北·二模)化学用语可以表达化学过程。下列化学用语的表达错误的是
A.用离子方程式表示铜在氨水中被腐蚀:
B.用电子式表示水分子的形成过程:
C.牙膏中添加氟化物能预防龋齿的原因:D.用化学方程式表示钢铁表面进行“烤蓝”处理:
2.(2023·河北邢台·模拟预测)化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示 的形成过程:
B.用离子方程式表示泡沫灭火器的原理:
C.用电子云轮廓图表示H-H键的形成示意图:
D.用化学方程式表示甲醛与苯酚生成酚醛树脂的反应:n +nHCHO
+(n-1)HO
2
3.(2024·四川绵阳·模拟预测)下列离子方程式书写正确的是
A.KClO碱性溶液与 反应制备高铁酸钾:
B.用白醋浸泡过的淀粉—KI试纸检验加碘盐中的 :
C.向NaClO溶液中通入少量 气体:
D. 溶液与足量的NaOH溶液反应:
4.(23-24高三上·安徽六安·阶段练习)下列说法正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.葡萄糖的燃烧热为 ,则
C.已知冰的熔化热为 ,冰中氢键键能为 。假设每摩尔冰中有 氢键,且熔化热完
全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
D.在一定条件下,将 和 置于密闭容器中充分反应生成 ,放出热量
,则该反应的热化学方程式
5.(2024·浙江省浙南名校联盟高三第一次联考)下列反应的离子方程式正确的是( )
A.HO中投入Na18O 固体:4HO+4Na 18O=8Na++2OH-+618OH-+18O↑+O ↑
2 2 2 2 2 2 2 2
B.邻羟基苯甲醛中加入足量浓溴水: +2Br → ↓+2H++2Br-
2C.二元弱酸亚磷酸(H PO )溶液中滴加少量的NaOH溶液:HPO +2OH-=HPO 2-+2H O
3 3 3 3 3 2
D.NH Al(SO ) 溶液中滴加足量Ba(OH) 溶液:NH ++Al3++2SO2-+2Ba2++5OH-=2BaSO ↓+Al(OH) -
4 4 2 2 4 4 4 4
+NH•H O
3 2
【热点三】化学用语的综合考查
1.(2024·河北邢台·模拟预测)下列过程用离子方程式表示正确的是
A.铅蓄电池充电时阴极的电极反应式:
B.以铁为电极电解 溶液的阳极的电极反应式:
C.把铜粉加入含双氧水的氨水中,溶液变蓝:
D.在 溶液中滴加少量 溶液:
2.(2024·辽宁·一模)下列化学用语或表述正确的是
A.基态氧原子的轨道表示式:
B.甲醛分子的空间填充模型:
C.用电子式表示 HCl的形成过程:
D.钢铁发生吸氧腐蚀时的负极反应式:O + 2H O + 4e-= 4OH-
2 2
3.(2024·河南信阳·二模)我国科学家在氢气的制备和应用等方面都取得了重大成果。如水煤气法制氢反
应中, 与足量 反应生成 和 吸收 的热量。 在金属冶炼、新能源
开发、碳中和等方面具有重要应用,如 在催化剂作用下与 反应可得到 。下列化学反应表
示错误的是
A.水煤气法制氢:
B. 催化加氢生成 的反应:
C.电解水制氢的阳极反应:
D. 与水反应:
4.(2024·安徽黄山·一模) 磷酸铁锂电池充电时锂离子由 电极迁移至石墨电极形成 ,
的前体 可由 、 、 在 的条件下反应制得,下列化学反应表示正
确的是
A.锂燃烧的热化学方程式:
B.锂-空气电池充电的阳极反应:
C. 的水解“释氨”过程:D.制备 的离子方程式:
5.(2024·江苏南京·一模)氧元素是地球上存在最广泛的元素,也是与生命活动息息相关的主要元素,其
单质及化合物在多方面具有重要应用。工业上用分离液态空气、光催化分解水等方法制取 。氢氧燃料电
池是最早实用化的燃料电池,具有结构简单、能量转化效率高等优点;25℃和 下, 的燃烧热为
。过氧化物如 、 等可以作为优秀的氧化剂。下列化学反应表示正确的是
A. 燃烧的热化学方程式:
B. 吸收 :
C.Fe和 反应化学方程式:
D.碱性氢氧燃料电池正极反应: