文档内容
高考解密06 化学反应与能量变化
考点热度 ★★★★★
考点1、反应热及其表示方法
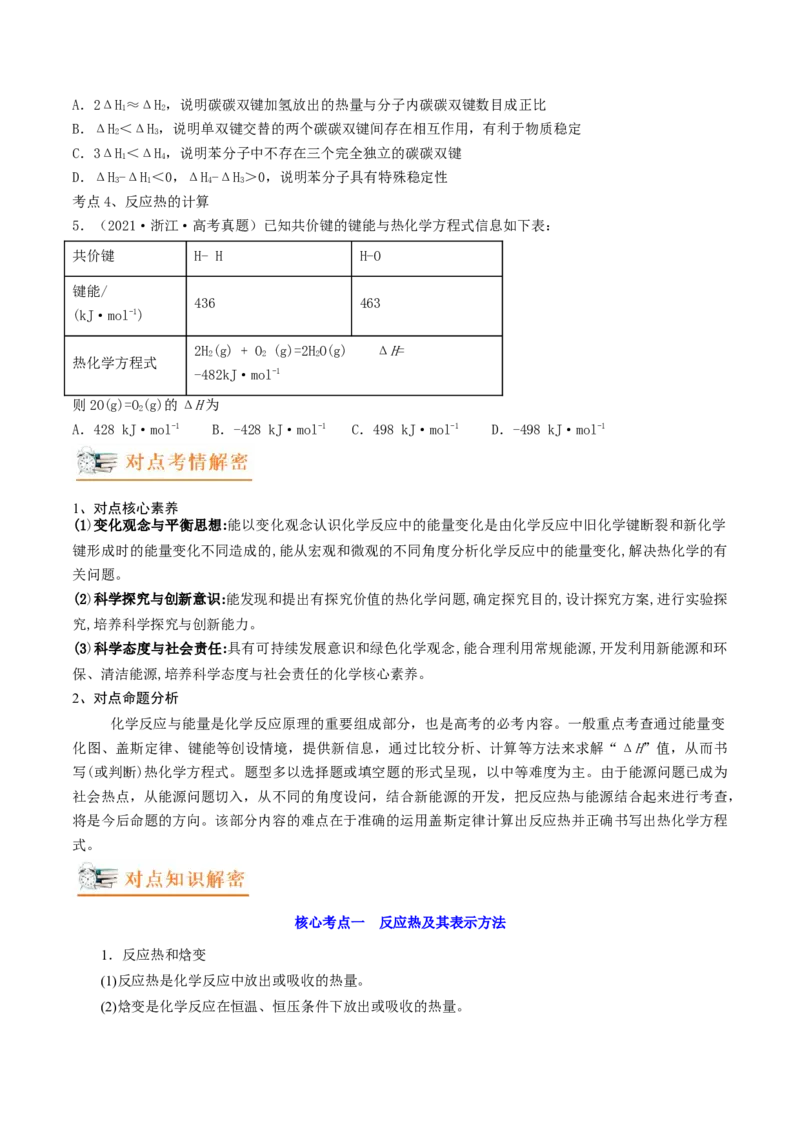
1.(2022·浙江·高考真题)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO
能量/
249 218 39 10 0 0
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
考点2、热化学方程式的正误判断
2.(2016·浙江·高考真题)已知:CH(g)的燃烧热为-890.31kJ•mol-1,则下列热化学方程式正确的是
4
A.CH(g)+2O(g)=CO(g)+2HO(l) △H=+890.31kJ•mol-1
4 2 2 2
B.CH(g)+2O(g)=CO+2HO(g) △H=-890.31kJ•mol-1
4 2 2 2
C.CH(g)+O(g)=CO(g)+2HO(l) △H=-890.31kJ•mol-1
4 2 2
D.CH(g)+2O(g)=CO(g)+2HO(l) △H=-890.31kJ•mol-1
4 2 2 2
考点3、反应热的大小比较
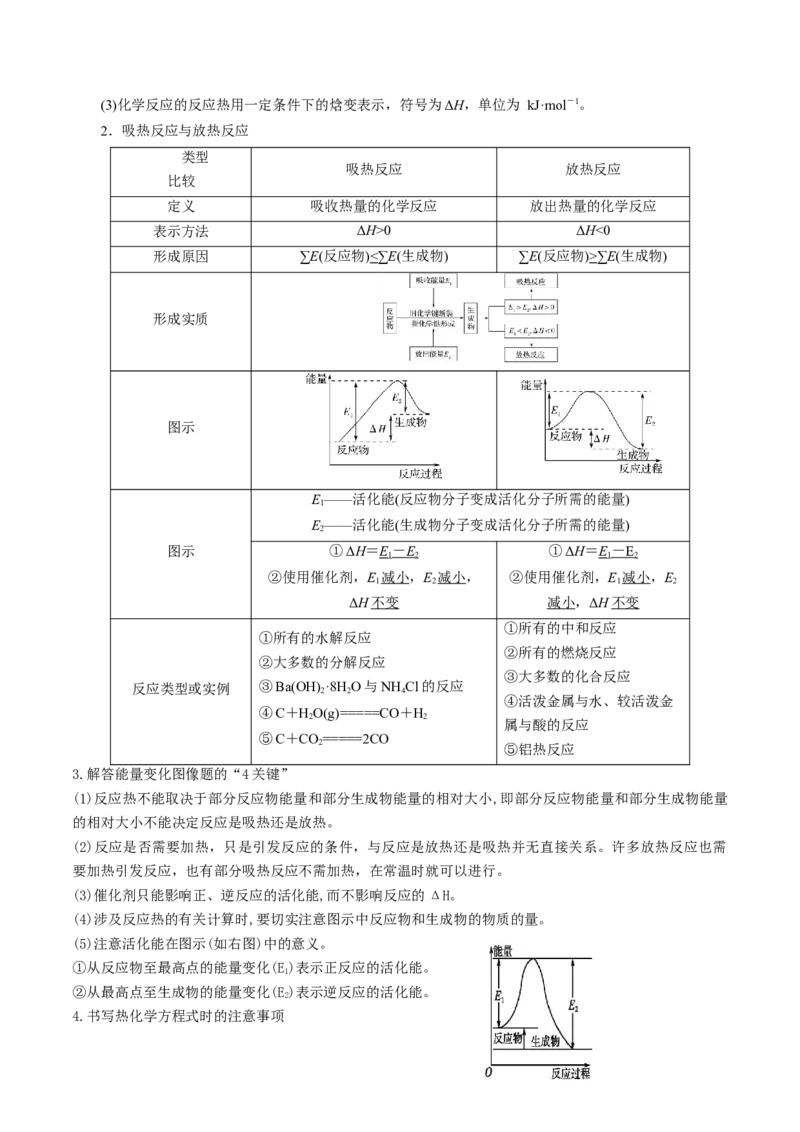
3.(2022·浙江·高考真题)相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图
所示:
下列推理不正确的是A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH<0,ΔH-ΔH>0,说明苯分子具有特殊稳定性
3 1 4 3
考点4、反应热的计算
5.(2021·浙江·高考真题)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/
436 463
(kJ·mol-1)
2H(g) + O (g)=2HO(g) ΔH=
2 2 2
热化学方程式
-482kJ·mol-1
则2O(g)=O(g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
1、对点核心素养
(1)变化观念与平衡思想:能以变化观念认识化学反应中的能量变化是由化学反应中旧化学键断裂和新化学
键形成时的能量变化不同造成的,能从宏观和微观的不同角度分析化学反应中的能量变化,解决热化学的有
关问题。
(2)科学探究与创新意识:能发现和提出有探究价值的热化学问题,确定探究目的,设计探究方案,进行实验探
究,培养科学探究与创新能力。
(3)科学态度与社会责任:具有可持续发展意识和绿色化学观念,能合理利用常规能源,开发利用新能源和环
保、清洁能源,培养科学态度与社会责任的化学核心素养。
2、对点命题分析
化学反应与能量是化学反应原理的重要组成部分,也是高考的必考内容。一般重点考查通过能量变
化图、盖斯定律、键能等创设情境,提供新信息,通过比较分析、计算等方法来求解“ΔH”值,从而书
写(或判断)热化学方程式。题型多以选择题或填空题的形式呈现,以中等难度为主。由于能源问题已成为
社会热点,从能源问题切入,从不同的角度设问,结合新能源的开发,把反应热与能源结合起来进行考查,
将是今后命题的方向。该部分内容的难点在于准确的运用盖斯定律计算出反应热并正确书写出热化学方程
式。
核心考点一 反应热及其表示方法
1.反应热和焓变
(1)反应热是化学反应中放出或吸收的热量。
(2)焓变是化学反应在恒温、恒压条件下放出或吸收的热量。(3)化学反应的反应热用一定条件下的焓变表示,符号为ΔH,单位为 kJ·mol-1。
2.吸热反应与放热反应
类型
吸热反应 放热反应
比较
定义 吸收热量的化学反应 放出热量的化学反应
表示方法 ΔH>0 ΔH<0
形成原因 ∑E(反应物)<∑E(生成物) ∑E(反应物)>∑E(生成物)
形成实质
图示
E——活化能(反应物分子变成活化分子所需的能量)
1
E——活化能(生成物分子变成活化分子所需的能量)
2
图示 ①ΔH=E - E ①ΔH=E - E
1 2 1 2
②使用催化剂,E 减小,E 减小, ②使用催化剂,E 减小,E
1 2 1 2
ΔH不变 减小,ΔH不变
①所有的中和反应
①所有的水解反应
②所有的燃烧反应
②大多数的分解反应
③大多数的化合反应
反应类型或实例 ③Ba(OH) ·8H O与NH Cl的反应
2 2 4
④活泼金属与水、较活泼金
④C+HO(g)=====CO+H
2 2
属与酸的反应
⑤C+CO=====2CO
2 ⑤铝热反应
3.解答能量变化图像题的“4关键”
(1)反应热不能取决于部分反应物能量和部分生成物能量的相对大小,即部分反应物能量和部分生成物能量
的相对大小不能决定反应是吸热还是放热。
(2)反应是否需要加热,只是引发反应的条件,与反应是放热还是吸热并无直接关系。许多放热反应也需
要加热引发反应,也有部分吸热反应不需加热,在常温时就可以进行。
(3)催化剂只能影响正、逆反应的活化能,而不影响反应的ΔH。
(4)涉及反应热的有关计算时,要切实注意图示中反应物和生成物的物质的量。
(5)注意活化能在图示(如右图)中的意义。
①从反应物至最高点的能量变化(E)表示正反应的活化能。
1
②从最高点至生成物的能量变化(E)表示逆反应的活化能。
2
4.书写热化学方程式时的注意事项(1)注明反应条件:反应热与测定条件(温度、压强等)有关,特定条件下要注明反应时的温度和压强。绝大
多数反应是在25 ℃、101 kPa下进行测定的,可不注明。
(2)注明物质状态:常用s、l、g、aq分别表示固体、液体、气体、溶液。
(3)注意符号单位:ΔH应包括“+”或“-”、数字和单位( kJ·mol-1)。
(4)注意守恒关系:①原子守恒和得失电子守恒;②能量守恒(ΔH与化学计量数相对应)。
(5)区别于普通方程式:不需要标注“↑”“↓”“点燃”“加热”等。
(6)注意热化学方程式的化学计量数。
(7)对于具有同素异形体的物质,除了要注明聚集状态之外,还要注明物质的名称。
热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,可以是整数,也可以是分数。且
化学计量数必须与ΔH相对应,如果化学计量数加倍,则ΔH也要加倍。
5.燃烧热和中和热应用中的注意事项
(1)燃烧热是指101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时放出的热量,并不是1 mol可燃物燃
烧时放出的热量就是燃烧热。必须是1 mol纯物质完全燃烧生成稳定的氧化物,如C燃烧应生成CO 而不
2
是CO,H 燃烧应生成液态水而不是气态水。
2
(2)中和热不是指1 mol酸与1 mol碱中和时的热效应,而是指强酸和强碱在稀溶液中发生中和反应生成1
mol H2O(l)的热效应。弱酸与强碱,强酸与弱碱或弱酸与弱碱反应时,因电离吸热,放出的热量减少。若用
浓硫酸(或NaOH固体),因溶解放热会使放出的热量增多。
6.利用键能计算反应热,要熟记公式:ΔH=反应物总键能-生成物总键能,其关键是弄清物质中化学键的
数目。在中学阶段要掌握常见单质、化合物中所含共价键的数目。原子晶体:1 mol金刚石中含2 mol C—
C键,1 mol硅中含2 mol Si—Si键,1 mol SiO 晶体中含4 mol Si—O键;分子晶体:1 mol P 中含有6 mol
2 4
P—P键,1 mol P O (即五氧化二磷)中,含有12 mol P—O键、4 mol P===O键,1 mol C H 中含有6 mol C
4 10 2 6
—H键和1 mol C—C键。
核心考点二 盖斯定律 反应热的计算
1.盖斯定律
(1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的反应
热只与反应体系的始态和终态有关,而与反应的途径无关。
(2)根据盖斯定律计算ΔH的步骤和方法
①计算步骤
②计算方法(3)盖斯定律应用
1)当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH
也同样要进行加减运算,且要带“+”“-”符号。
2)将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
3)同一物质的三态变化(固、液、气),状态由固→ 液→气变化时,会吸热;反之会放热。
4)利用状态,迅速比较反应热的大小(若反应为放热反应)
①当反应物状态相同,生成物状态不同时,生成固体放热最多,生成气体放热最少。
②当反应物状态不同,生成物状态相同时,固体反应放热最少,气体反应放热最多。
③在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。
2.反应热计算的四种方法
(1)根据燃烧热数据,求算反应放出的热量。
利用公式:Q=燃烧热×n(可燃物的物质的量)
如已知H 的燃烧热ΔH=-285.8 kJ·mol-1,若H2的物质的量为 2 mol,则2 mol H 燃烧放出的热量为 2
2 2
mol×285.8 kJ·mol-1=571.6 kJ。
(2)依据反应物与生成物的总能量计算。
ΔH=E生成物-E反应物。
(3)根据键能数据(E)计算。
ΔH=反应物键能总和-生成物键能总和
(4)根据盖斯定律计算反应热。
若一个热化学方程式可由另外几个热化学方程式相加减而得到,则该反应的反应热也可通过这几个化学反
应的反应热相加减而得到。
3.比较反应热大小的四个注意要点
(1)反应物和生成物的状态:
物质的气、液、固三态的变化与反应热的关系。
(2)ΔH的符号:比较反应热的大小时,不要只比较ΔH数值的大小,还要考虑其符号。
(3)参加反应物质的量:当反应物和生成物的状态相同时,参加反应物质的量越多,放热反应的 ΔH越小,
吸热反应的ΔH越大。(4)反应的程度:参加反应物质的量和状态相同时,反应的程度越大,热量变化越大。
4.反应热计算的常见失误点
(1)根据已知的热化学方程式进行计算时,要清楚已知热化学方程式的化学计量数表示的物质的量与已知物
质的量之间的比例关系,然后进行计算。
(2)根据化学键断裂和形成过程中的能量变化计算反应热时,要注意断键和成键的总数,计算时必须是断键
和成键时吸收和放出的总能量。
(3)运用盖斯定律进行计算,在调整方程式时,要注意ΔH的值也要随之调整。
(4)物理变化也会有热效应:在物理变化过程中,也会有能量变化,虽然不属于吸热反应或放热反应,但
在进行相关反应热计算时,必须要考虑发生物理变化时的热效应,如物质的三态变化或物质的溶解过程中
的能量变化等。
(5)不可忽视化学键的物质的量:根据键能计算反应热时,要注意弄清各种化学键的物质的量,既要考虑
热化学方程式中物质的化学计量数,又要考虑物质中各种化学键的个数,再进行计算。反应热(ΔH)等于
反应物中的键能总和减去生成物中的键能总和,即ΔH=ΣE -ΣE (E表示键能)。如反应3H(g)+
反 生 2
N(g)2NH(g) ΔH=3E(H—H)+E(N≡N)-6E(N—H)。
2 3
(6)严格保证热化学方程式与ΔH变化的一致性
a.热化学方程式乘以某一个数时,反应热数值也必须乘上该数。
b.热化学方程式相加减时,相同状态的同种物质之间可相加减,反应热也随之相加减。
c.将一个热化学方程式颠倒时,ΔH的“+”“-”号必须随之改变。
考点1、反应热及其表示方法
【高考解密】本考点主要考查反应过程能量变化中概念理解、能量之间的相互转化、能量变化图的分析与
应用,通常结合化学反应速率和化学平衡命题,以选择题的形式出现,正确理解概念,将概念应用到图象
进行分析,就能得出正确的答案。
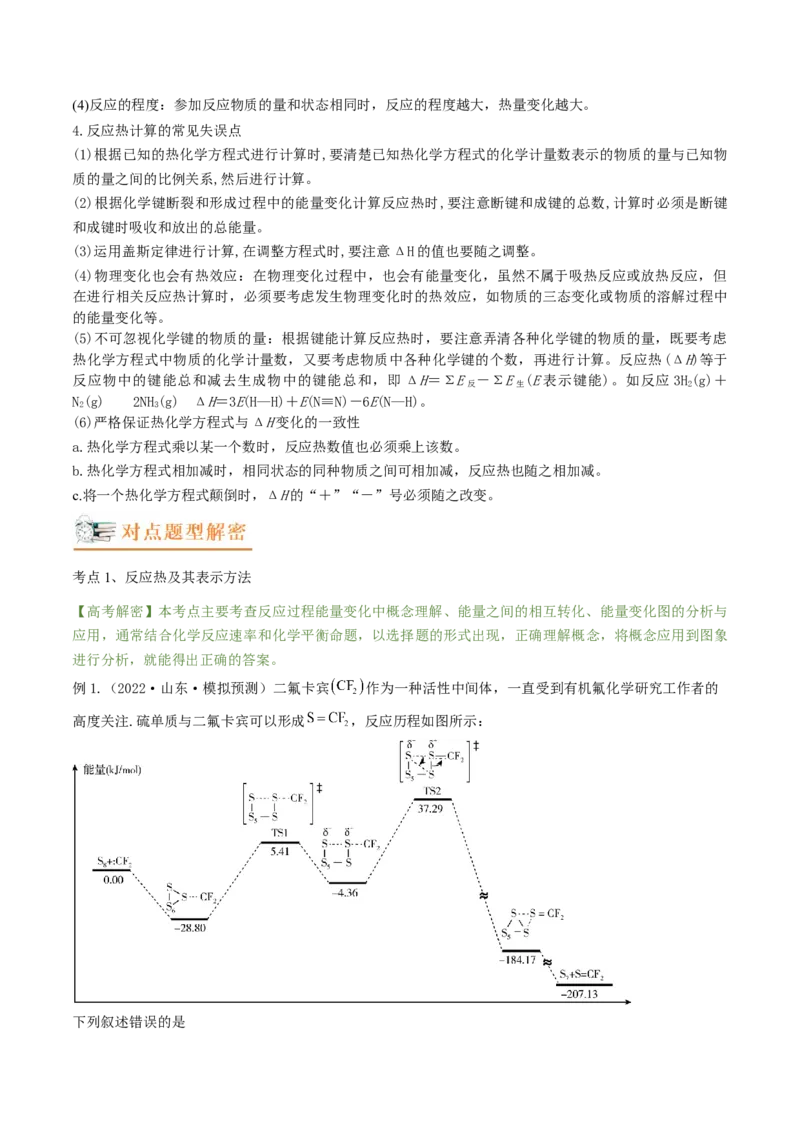
例1.(2022·山东·模拟预测)二氟卡宾 作为一种活性中间体,一直受到有机氟化学研究工作者的
高度关注.硫单质与二氟卡宾可以形成 ,反应历程如图所示:
下列叙述错误的是A. 和 生成 反应的
B.由 生成 的活化能为
C.上述反应历程中存在 键的断裂和生成
D.决定反应速率的基元反应的活化能为
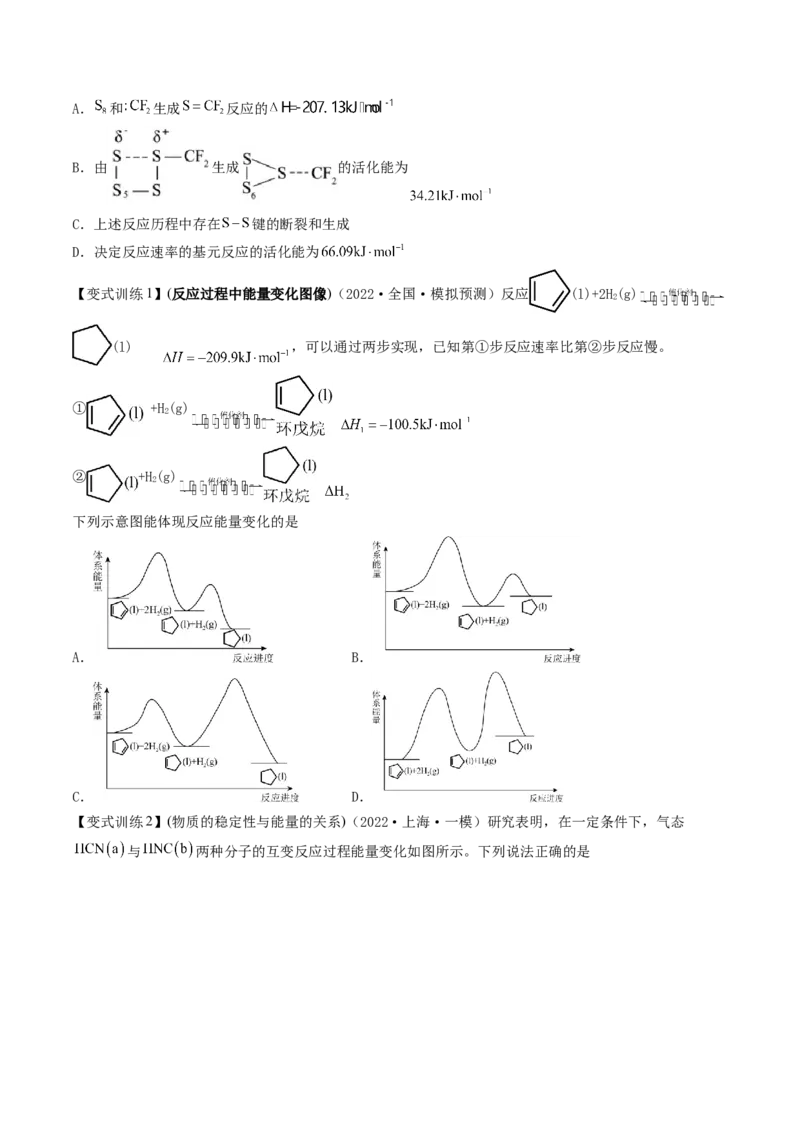
【变式训练1】(反应过程中能量变化图像)(2022·全国·模拟预测)反应 (l)+2H(g)
2
(l) ,可以通过两步实现,已知第①步反应速率比第②步反应慢。
① +H(g)
2
② +H(g)
2
下列示意图能体现反应能量变化的是
A. B.
C. D.
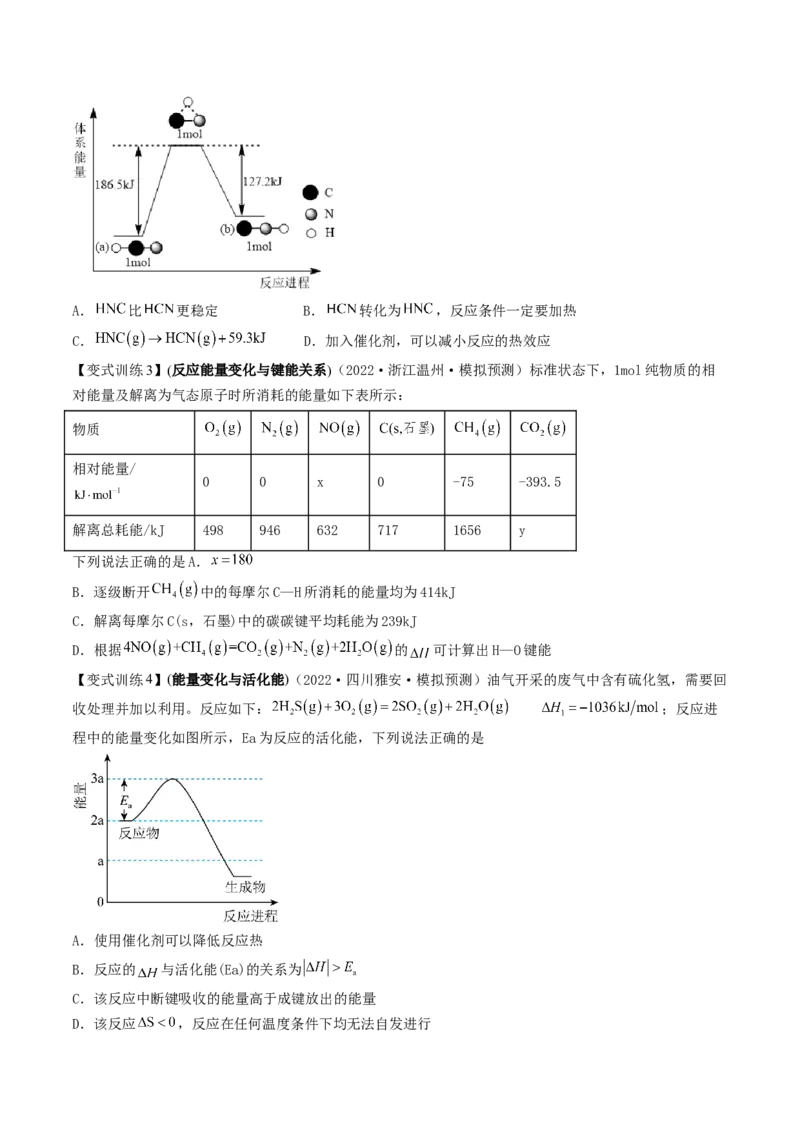
【变式训练2】(物质的稳定性与能量的关系)(2022·上海·一模)研究表明,在一定条件下,气态
与 两种分子的互变反应过程能量变化如图所示。下列说法正确的是A. 比 更稳定 B. 转化为 ,反应条件一定要加热
C. D.加入催化剂,可以减小反应的热效应
【变式训练3】(反应能量变化与键能关系)(2022·浙江温州·模拟预测)标准状态下,1mol纯物质的相
对能量及解离为气态原子时所消耗的能量如下表所示:
物质
相对能量/
0 0 x 0 -75 -393.5
解离总耗能/kJ 498 946 632 717 1656 y
下列说法正确的是A.
B.逐级断开 中的每摩尔C—H所消耗的能量均为414kJ
C.解离每摩尔C(s,石墨)中的碳碳键平均耗能为239kJ
D.根据 的 可计算出H—O键能
【变式训练4】(能量变化与活化能)(2022·四川雅安·模拟预测)油气开采的废气中含有硫化氢,需要回
收处理并加以利用。反应如下: ;反应进
程中的能量变化如图所示,Ea为反应的活化能,下列说法正确的是
A.使用催化剂可以降低反应热
B.反应的 与活化能(Ea)的关系为
C.该反应中断键吸收的能量高于成键放出的能量
D.该反应 ,反应在任何温度条件下均无法自发进行【变式训练5】(反应历程与能量变化)(2022·湖南·邵阳市第二中学模拟预测)我国科学家实现了在铜催
化剂条件下将DMF[(CH)NCHO]转化为三甲胺[N(CH)]。计算机模拟单个DMF分子在铜催化剂表面的反应历
3 2 3 3
程如图所示,下列说法正确的是
A.该历程中最小能垒的化学方程式为 (CH)NCHOH*=(CH)NCH+OH*
3 2 2 3 2 2
B.该历程中最大能垒(活化能)为2.16eV
C.该反应热化学方程式为(CH)NCHO(g)+2H(g)=N(CH)(g)+HO(g) ΔH=-1.02ev•mol-1
3 2 2 3 3 2
D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率
考点2、考查热化学方程式的书写与正误判断
【高考解密】本考点主要考查热化学方程式的书写及热化学方程式的正误判断,以选择题和主观题的形式
出现,正确理解热化学方程式的概念及书写步骤、应用盖斯定律计算反应热,根据热化学方程式书写的注
意事项来判断热化学方程式的正误。
例2.(2021·浙江·模拟预测)下列有关热化学方程式的评价不合理的是
选
实验事实 热化学方程式 评价
项
与足量水完全反应生成
A 正确
,放出热量260.6kJ
B 热值为 正确
已知 不正确;因为同
C 时还生成了硫酸
,将稀硫酸与稀氢氧化
钡沉淀
钡溶液混合
不正确;明确的
已知25℃、101kPa下,120g石墨完全燃 同素异形体要注
D
烧放出热量3935.1kJ 名称:C(s,石
墨)
A.A B.B C.C D.D
【变式训练1】(热化学方程式的书写) (2021•河北选择性考试节选)当今,世界多国相继规划了碳达峰、碳
中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据
如表:
物质 H(g) C(石墨,s) C H(l)
2 6 6
燃烧热△H(kJ•mol-1) -285.8 -393.5 -3267.5
(1)则25℃时H(g)和C(石墨,s)生成C H(l)的热化学方程式为________。
2 6 6
【变式训练2】(热化学方程式的理解)(2022·天津市第四十七中学高三期中)下列有关热化学方程式的叙
述正确的是
A.已知 ,则金刚石比石墨稳定
B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
C.甲烷的燃烧热为 ,则甲烷燃烧的热化学方程式可表示为
D.已知 ,则含 的稀溶液与稀醋酸完全
中和,放出小于 的热量
【变式训练3】(热化学方程式的正误判断)(2022·重庆市永川北山中学校高三期中)下列热化学方程式正
确的是
A.31g白磷比31g红磷能量多bkJ,
B.1mol 、0.5mol 完全反应后,放出热量98.3kJ
C.
D. 的燃烧热为
考点3、考查反应热的大小比较
【高考解密】本考点主要考查反应热的大小比较,主要以选择题的形式出现,比较时要注意是比较数值大
小还是比较ΔH,同时要注意反应热与反应中各物质的物质的量及状态相对应,可以应用多种方法进行比
较。
例3.(2022·天津·模拟预测)已知几种离子反应的热化学方程式如下
①
②
③
④
下列有关判断正确的是
A. , B.C. D.
【变式训练】(2022·浙江·模拟预测)已知NaHCO 溶液与盐酸,反应生成CO 吸热,NaCO 溶液与盐酸反
3 2 2 3
应生成CO 放热。关于下列△H的判断正确的是
2
A. B.
C. D.
考点4、考查反应热的计算
【高考解密】本考点主要考查反应热的计算,主要以选择题和主观题的形式出现,可以应用键能、物质本
身的能量、热化学方程式、燃烧热、中和热、盖斯定律等计算反应热。
例4.(2022·重庆市育才中学模拟预测)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世
瞩目的成就。碳酰肼类化合物 是种优良的含能材料,可作为火箭推进剂的组分,其相关
反应的能量变化如图所示,已知 ,则 为
A. B. C. D.
【变式训练1】(通过燃烧热计算反应热)(2022·北京·模拟预测)已知:C(s,石墨)+O(g)=CO(g)
2 2
ΔH=-393.5kJ/mol
1
CO(g)+ O(g)=CO(g) ΔH=-283kJ/mol
2 2 2
理论上2mol石墨不充分燃烧,生成等物质的量的CO(g)和CO(g)放出的热量是
2
A.676.5kJ B.504kJ C.283kJ D.110.5kJ
【变式训练2】(通过键能计算反应热)(2022·安徽铜陵·二模)已知:
其他数据如下表:
化学键 C=O O=O C-H O-H C=C
键能/( x
798 413 463 615
)下列说法正确的是A.乙烯的燃烧热为
B.
C.
D.当生成4molO-H键时,该反应放出热量一定为akJ
【变式训练3】(通过盖斯定律计算反应热)(2022·浙江·温州中学模拟预测)已知 固体
溶于水放热,有关过程能量变化如图
下列说法正确的是
A.反应① , B.
C. D.