文档内容
化学反应与能量
第 1 讲 化学反应的热效应
课 程 标 准 知 识 建 构
1.能辨识化学反应中的能量转化形式,能解释化学反应
中能量变化的本质。
2.能进行反应焓变的简单计算,能用热化学方程式表
示反应中的能量变化,能运用反应焓变合理选择和利
用化学反应。
3.能举例说明化学在解决能源危机中的重要作用,能
分析能源的利用对自然环境和社会发展的影响。
4.能综合考虑化学变化中的物质变化和能量变化来分
析、解决实际问题,如煤炭的综合利用等。
一、焓变 热化学方程式
1.化学反应的实质与特征
2.焓与焓变3.反应热
(1)概念:反应热是一定条件下化学反应释放或吸收的热量。
(2)反应热和焓变的关系:恒压条件下进行的化学反应的焓变等于反应热,因
此常用 Δ H 表示反应热。
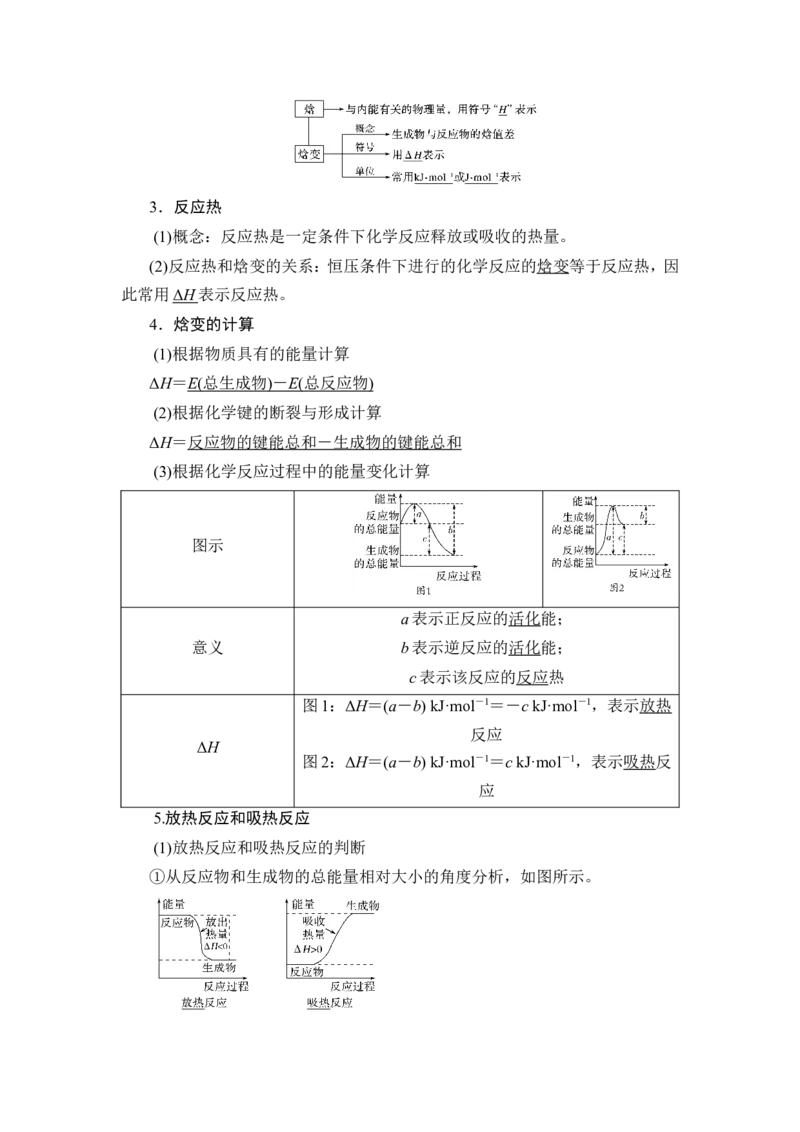
4.焓变的计算
(1)根据物质具有的能量计算
ΔH= E ( 总生成物 ) - E ( 总反应物 )
(2)根据化学键的断裂与形成计算
ΔH=反应物的键能总和-生成物的键能总和
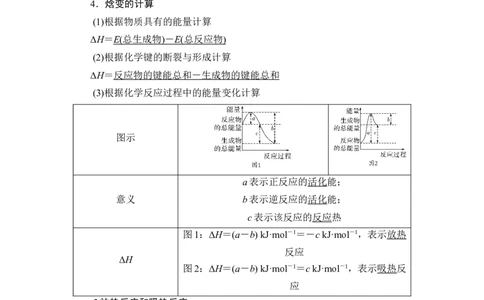
(3)根据化学反应过程中的能量变化计算
图示
a表示正反应的活化能;
意义 b表示逆反应的活化能;
c表示该反应的反应热
图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热
反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反
应
5.放热反应和吸热反应
(1)放热反应和吸热反应的判断
①从反应物和生成物的总能量相对大小的角度分析,如图所示。②从反应热的量化参数——键能的角度分析
(2)常见的放热反应
①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反
应;⑤物质的缓慢氧化等。
(3)常见的吸热反应:①大多数分解反应;②盐类的水解;③Ba(OH) ·8H O与
2 2
NH Cl反应;④碳和水蒸气、C和CO 的反应等。
4 2
【特别提醒】
(1)过程(包括物理过程、化学过程)与化学反应的区别,有能量变化的过程不
一定是放热反应或吸热反应。如水结成冰放热,但不属于放热反应。
(2)化学反应是放热还是吸热与反应发生的条件没有必然联系。如吸热反应
NH Cl与Ba(OH) ·8H O在常温常压下即可进行。
4 2 2
6.热化学方程式
(1)概念:表示参加反应物质的量和反应热的关系的化学方程式。
(2)意义:表明了化学反应中的物质变化和能量变化。
如 2H (g)+O (g)===2H O(l) ΔH=-571.6 kJ·mol-1表示: 2_mol 氢气和
2 2 2
1_mol 氧气反应生成 2_mol 液态水时放出 571.6_kJ 的热量 。
(3)热化学方程式的书写要求及步骤
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)所有的放热反应不需要加热就能进行反应 ( )
(2)物质发生化学变化一定伴有能量的变化( )
(3)浓H SO 稀释是放热反应( )
2 4
(4)活化能越大,表明反应断裂旧化学键需要克服的能量越高( )(5)吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放
出的总能量( )
(6)同温同压下,反应H (g)+Cl (g)===2HCl(g)在光照和点燃条件下的ΔH不
2 2
同( )
(7)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
答案 (1)× (2)√ (3)× (4)√ (5)√ (6)× (7)√
二、燃烧热、中和热和能源
1.燃烧热和中和热的比较
燃烧热 中和热
101 kPa时,1_mol 纯物质 在稀溶液里,酸与碱发生
概念 完全燃烧生成指定产物时 中和反应生成 1_mol 水 时
所放出的热量 所放出的热量
能量变化 放热
相同点
ΔH及其单位 ΔH<0,单位均为kJ·mol-1
反应物的量 1_mol 不一定为1 mol
生成物的量 不确定 生成的水为1_mol
不同点 强酸与强碱反应的中和热
燃烧热ΔH=
表示方法 ΔH=
-a kJ·mol-1(a>0)
- 57.3_kJ·mo l - 1
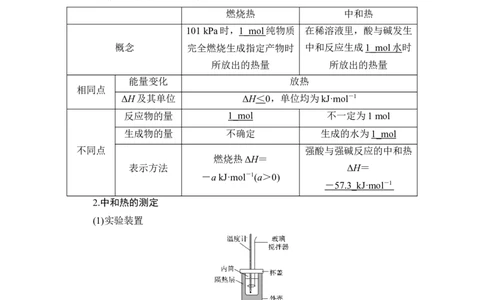
2.中和热的测定
(1)实验装置
(2)测定原理
ΔH=-
c=4.18 J·g-1·℃-1=4.18×10-3 kJ·g-1·℃-1;
n为生成H O的物质的量。
2
(3)实验步骤(4)注意事项
①泡沫塑料板和碎泡沫塑料(或纸条)的作用是保温。
②为保证酸完全中和,采取的措施是若采用的酸、碱浓度相等,可采用碱体积
稍过量。
3.能源
(1)能源的分类
(2)解决能源问题的措施
①提高能源的利用效率:a.改善开采、运输、加工等各个环节;b.科学控制燃烧
反应,使燃料充分燃烧。
②开发新能源:开发资源丰富、可以再生、没有污染或污染很小的新能源。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)燃料电池中将甲醇蒸气转化为氢气的热化学方程式是 CH OH(g)+
3
O (g)===CO (g)+2H (g) ΔH=-192.9 kJ·mol-1,则CH OH(g)的燃烧热为192.9
2 2 2 3
kJ·mol-1( )
(2)已知稀溶液中,H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则稀
2
醋酸与稀氢氧化钠溶液反应生成1 mol水时放出57.3 kJ的热量( )
(3)已知 H+(aq)+OH-(aq)===H O(l) ΔH=-57.3 kJ·mol-1,则 H SO 和
2 2 4
Ba(OH) 反应的反应热ΔH=2×(-57.3) kJ·mol-1( )
2
(4)H (g)的燃烧热是285.8 kJ·mol-1,则2H O(g)===2H (g)+O (g) ΔH=+
2 2 2 2
571.6 kJ·mol-1( )
答案 (1)× (2)× (3)× (4)×
三、盖斯定律与反应热的比较1.盖斯定律
(1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是
相同的。即:化学反应的反应热只与反应体系的始态和终态有关,而与反应的途
径无关。
(2)意义:间接计算某些反应的反应热。
2.反应热大小的比较
(1)看物质状态。物质的气、液、固三态转化时的能量变化如下:
(2)看ΔH的符号。比较反应热大小时不要只比较ΔH数值的大小,还要考虑其
符号。
(3)看化学计量数。当反应物与生成物的状态相同时,化学计量数越大,放热
反应的ΔH越小,吸热反应的ΔH越大。
(4)看反应的程度。对于可逆反应,参加反应的物质的量和状态相同时,反应
的程度越大,热量变化越大。
【诊断3】 试比较下列各组ΔH的大小。
(1)同一反应,生成物状态不同时
A(g)+B(g)===C(g) ΔH <0
1
A(g)+B(g)===C(l) ΔH <0
2
则ΔH ________(填“>”“<”或“=”,下同)ΔH 。
1 2
(2)同一反应,反应物状态不同时
S(g)+O (g)===SO (g) ΔH <0
2 2 1
S(s)+O (g)===SO (g) ΔH <0
2 2 2
则ΔH ________ΔH 。
1 2
答案 (1)> (2)<
解析 (1)因为C(g)===C(l) ΔH <0
3
则ΔH =ΔH -ΔH ,ΔH <ΔH 。
3 2 1 2 1
(2)
ΔH +ΔH =ΔH ,则ΔH =ΔH -ΔH ,又ΔH <0,所以ΔH <ΔH 。
2 3 1 3 1 2 3 1 2考点一 化学反应过程热效应的分析
【典例1】 (2020·福建福州市高三期末)已知几种物质之间的能量关系如图所
示, 下列说法中不正确的是( )
A.使用合适催化剂,不能减小反应的焓变
B. ΔH=+28.7 kJ/mol
C. (g)中,热能转化为产物内部的能量
D. (g),反应物的总能量高于生成物的总能量
答案 C
解析 A.使用合适催化剂可降低反应的活化能,但不能减小反应的焓变,故
A正确;B. (g)+H (g)=== (g) ΔH=237.1 kJ/mol-208.4 kJ/mol=+
2
28.7 kJ/mol,故 B 正确;C. (g)+H (g)=== (g) ΔH=119.6 kJ/mol-
2
237.1 kJ/mol=-117.5 kJ/mol,产物内部的能量转化为热能,故C错误;D.
(g)+H (g)=== (g) ΔH=-119.6 kJ/mol,反应为放热反应,反应物的总能量
2
高于生成物的总能量,故D正确。
【对点练 1】 (化学反应过程中能量变化分析)已知化学反应 A (g)+
2
B (g)===2AB(g) ΔH=+100 kJ·mol-1的能量变化如图所示,判断下列叙述中正
2
确的是( )
A.加入催化剂,该反应的反应热ΔH将减小
B.每形成2 mol A—B键,将吸收b kJ能量
C.每生成2分子AB吸收(a-b) kJ热量D.该反应正反应的活化能大于100 kJ·mol-1
答案 D
解析 催化剂不能改变反应热的大小,A错误;形成化学键,释放能量,B错
误;热化学方程式中,化学计量数代表物质的量,C错误。
【对点练2】 (依据键能或能量变化计算焓变)(2021·湖南汨罗市高三检测)如
图是金属镁和卤素单质(X )反应的能量变化示意图。下列说法正确的是( )
2
A.热稳定性:MgF 0 D.ΔH >ΔH
3 4 3 4答案 B
解析 形成化学键要放出热量,ΔH <0,第二个反应是盐类的水解反应,是吸
1
热反应,ΔH >0,A项错误;ΔH 是负值,ΔH 是正值,ΔH <ΔH ,B项正确;酸碱中
2 1 2 1 2
和反应是放热反应,ΔH <0,ΔH <0,C项错误;第四个反应(醋酸是弱酸,电离吸
3 4
热)放出的热量小于第三个反应,但ΔH 和ΔH 都是负值,则ΔH <ΔH ,D项错误。
3 4 3 4
4.(2020·天津学业水平等级考试,10)理论研究表明,在101 kPa和298 K下,
HCN(g)HNC(g)异构化反应过程的能量变化如图所示。下列说法错误的是(
)
A.HCN比HNC稳定
B.该异构化反应的ΔH=+59.3 kJ·mol-1
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
答案 D
解析 HNC的能量比HCN高,则稳定性较好的是HCN,A项正确;该异构化
反应的ΔH=+59.3 kJ·mol-1,为吸热反应,则正反应的活化能大于逆反应的活化
能,B、C项正确;使用催化剂只能改变反应的历程,但是不影响反应的反应热,D
项错误。
5.(高考组合题)
(1)(2020· 课 标 全 国 Ⅱ , 28) 乙 烷 在 一 定 条 件 可 发 生 如 下 反 应 :
C H (g)===C H (g)+H (g) ΔH ,相关物质的燃烧热数据如表所示:
2 6 2 4 2 1
物质 C H (g) C H (g) H (g)
2 6 2 4 2
燃烧热ΔH/(kJ·mol-1) -1 560 -1 411 -286
则ΔH =________ kJ·mol-1。
1
(2)(2020·山东学业水平等级考试,18)探究CH OH合成反应化学平衡的影响
3
因素,有利于提高CH OH的产率。以CO 、H 为原料合成CH OH涉及的主要反
3 2 2 3
应如下:
Ⅰ.CO (g)+3H (g)CH OH(g)+H O(g) ΔH =-49.5 kJ·mol-1
2 2 3 2 1
Ⅱ.CO(g)+2H (g)CH OH(g)
2 3ΔH =-90.4 kJ·mol-1
2
Ⅲ.CO (g)+H (g)CO(g)+H O(g) ΔH
2 2 2 3
回答下列问题:
ΔH =________ kJ·mol-1。
3
答案 (1)+137 (2)+40.9
解析 (1)根据题表中数据信息可写出热化学方程式(ⅰ)C H (g)+
2 6
O (g)===2CO (g) + 3H O(l) ΔH = - 1 560 kJ·mol - 1 、 (ⅱ)C H (g) +
2 2 2 2 4
3O (g)===2CO (g)+2H O(l) ΔH=-1 411 kJ·mol-1、(ⅲ)H (g)+O (g)===H O(l)
2 2 2 2 2 2
ΔH=-286 kJ·mol-1,根据盖斯定律,由(ⅰ)-(ⅱ)-(ⅲ)得C H (g)===C H (g)+
2 6 2 4
H (g) ΔH =+137 kJ·mol-1。
2 1
(2)分析三个热化学方程式,可应用盖斯定律计算,ΔH =ΔH -ΔH =-49.5
3 1 2
kJ·mol-1-(-90.4 kJ·mol-1)=+40.9 kJ·mol-1。
6.(2019·课标全国Ⅰ,28)水煤气变换[CO(g)+H O(g)===CO (g)+H (g)]是重
2 2 2
要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列
问题:
我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换
的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”)。该历程
中最大能垒(活化能)E =________eV,写出该步骤的化学方程式___________。
正
答 案 小 于 2.02 COOH* + H* + H O*===COOH* + 2H* + OH*( 或
2
H O*===H*+OH*)
2
解析 观察起始态物质的相对能量与终态物质的相对能量知,终态物质相对
能量低于始态物质相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相
对能量与起始态物质相对能量相差越大,活化能越大,由题图知,最大活化能E
正
=1.86 eV-(-0.16 eV)=2.02 eV,该步起始物质为COOH*+H*+H O*,产物为
2
COOH*+2H*+OH*。一、选择题(每小题只有一个选项符合题意)
1.(2020·河南省驻马店市高三期末)“太阳能燃料”国际会议于2019年10
月在我国武汉举行,旨在交流和探讨太阳能光催化分解水制氢、太阳能光催化二
氧化碳转化为燃料等问题。下列说法错误的是( )
A.太阳能燃料属于一次能源
B.直接电催化CO 制取燃料时,燃料是阴极产物
2
C.用光催化分解水产生的H 是理想的绿色能源
2
D.研发和利用太阳能燃料,有利于经济的可持续发展
答案 A
解析 太阳能燃料属于二次能源,故A错误;直接电催化CO 制取燃料时,化
2
合价降低,在阴极反应,因此燃料是阴极产物,故B正确;用光催化分解水产生的
H ,氢气燃烧放出热量多,无污染,是理想的绿色能源,故C正确;研发和利用太
2
阳能燃料,消耗能量较低,有利于经济的可持续发展,故D正确。
2.下列反应中符合图示能量变化的是( )
A.电解Al O 得到Al和O
2 3 2
B.Ba(OH) ·8H O与NH Cl反应
2 2 4
C.铝热反应
D.灼热的炭与CO 反应
2
答案 C
解析 根据图示可知反应物的总能量高于生成物的总能量,反应发生时会释
放能量,故反应是放热反应。电解Al O 得到Al和O 的反应是吸热反应,与图像
2 3 2
不符,故A错误;Ba(OH) ·8H O与NH Cl的反应是吸热反应,与图像不符,故B
2 2 4
错误;铝热反应是放热反应,反应物的总能量高于生成物的总能量,与图像相符,
故C正确;灼热的炭与CO 反应产生CO,该反应是吸热反应,与图像不符,故D
2
错误。
3.分别向1 L 0.5 mol·L-1的Ba(OH) 溶液中加入①浓硫酸;②稀硫酸;③稀硝
2
酸,恰好完全反应时的热效应分别为ΔH 、ΔH 、ΔH ,下列关系中正确的是( )
1 2 3A.ΔH >ΔH >ΔH B.ΔH <ΔH <ΔH
1 2 3 1 2 3
C.ΔH >ΔH =ΔH D.ΔH =ΔH <ΔH
1 2 3 1 2 3
答案 B
解析 混合时浓硫酸在被稀释的过程中放热;浓、稀硫酸在与Ba(OH) 反应
2
时还会形成BaSO 沉淀,Ba2+、SO之间形成化学键的过程中也会放出热量。因放
4
热反应的ΔH取负值,故ΔH <ΔH <ΔH 。
1 2 3
4.(2019·九江高三模拟)25 ℃、101 kPa时,强酸与强碱的稀溶液发生中和反
应的中和热为57.3 kJ·mol-1,辛烷的燃烧热为5 518 kJ·mol-1。下列热化学方程式
书写正确的是( )
A.2H+(aq)+SO(aq)+Ba2+(aq)+2OH-(aq)===BaSO (s)+2H O(l) ΔH=-
4 2
57.3 kJ·mol-1
B.KOH(aq)+H SO (aq)===K SO (aq)+H O(l) ΔH=-57.3 kJ·mol-1
2 4 2 4 2
C.C H (l)+O (g)===8CO (g)+9H O(g) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
D.2C H (g)+25O (g)===16CO (g)+18H O(l) ΔH=-5 518 kJ·mol-1
8 18 2 2 2
答案 B
解析 A项,所列热化学方程式中有两个错误,一是中和热是指反应生成 1
mol H O(l)时的反应热,二是当有BaSO 沉淀生成时,反应放出的热量会增加,生
2 4
成1 mol H O(l)时放出的热量大于57.3 kJ,错误;C项,燃烧热是指1 mol纯物质
2
完全燃烧生成指定产物时所产生的热量,产物中的水应为液态,错误;D项,当2
mol辛烷完全燃烧时,产生的热量为11 036 kJ,且辛烷应为液态,错误。
5.(2020·海南海口市一中高三三模)下列关于热化学反应的描述中正确的是(
)
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H SO 和Ca(OH) 完全
2 4 2
反应的中和热为-114.6 kJ/mol
B.CO(g)的燃烧热是 283.0 kJ/mol,则表示 CO 燃烧热的热化学方程式为
2CO(g)+O (g)===2CO (g) ΔH=-283.0 kJ/mol
2 2
C.一个化学反应的热效应,只与反应的始态与终态有关,与反应的过程无关
D.需要加热才能发生的反应一定是吸热反应
答案 C
解析 H SO 和Ca(OH) 反应生成水和硫酸钙沉淀,放出更多的热量,则
2 4 2
H SO 和Ca(OH) 反应的中和热ΔH<-57.3 kJ/mol,故A错误;表示CO燃烧热
2 4 2
的热化学方程式为 CO(g)+O (g)===CO (g)反应的ΔH=-283.0 kJ·mol-1,故B
2 2错误;物质能量一定,对于确定的反应,化学反应的反应热只与体系始态和终态
有关,与变化途径无关,故C正确;某些放热反应也需要加热条件才能发生反应;
需要加热才能发生的反应不一定是吸热反应,故D错误。
6.(2021·湖南汨罗市高三检测)已知:
①CO(g)+H O(g)===CO (g)+H (g) ΔH
2 2 2 1
②CH (g)+H O(g)===CO(g)+3H (g) ΔH
4 2 2 2
下列推断正确的是( )
A.若CO的燃烧热为ΔH ,则H 的燃烧热为ΔH -ΔH
3 2 3 1
B.反应CH (g)+CO (g)===2CO(g)+2H (g)的ΔH=ΔH -ΔH
4 2 2 1 2
C.若反应②的反应物总能量低于生成物总能量,则ΔH <0
2
D.若等物质的量的CO和H 完全燃烧生成气态产物时后者放热更多,则ΔH
2 1
>0
答案 D
解析 A.若CO的燃烧热为ΔH ,则③CO(g)+O (g)===CO (g) ΔH ,③-
3 2 2 3
①,整理可得H (g)+O (g)===H O(g) ΔH=ΔH -ΔH ,由于H O的稳定状态是
2 2 2 3 1 2
液态,因此该反应热不能表示氢气的燃烧热,A错误;B.①-②,整理可得CH (g)
4
+CO (g)===2CO(g)+2H (g)的ΔH=ΔH -ΔH ,B错误;C.若反应②的反应物总
2 2 2 1
能量低于生成物总能量,则该反应是吸热反应,ΔH >0,C错误; D.③CO(g)+
2
O (g)===CO (g) ΔH ,④H (g)+O (g)===H O(g) ΔH ,若等物质的量的CO和
2 2 3 2 2 2 4
H 完全燃烧生成气态产物时后者放热更多,则 ΔH >ΔH ,③-④,整理可得
2 3 4
CO(g)+H O(g)===CO (g)+H (g) ΔH =ΔH -ΔH >0,D正确。
2 2 2 1 3 4
7.(2020·长沙市第一中学高三测试)在25 ℃、101 kPa 时,C(s)、H (g)、
2
CH COOH(l)的燃烧热分别为393.5 kJ·mol-1、285.8 kJ·mol-1、870.3 kJ·mol-1,则
3
2C(s)+2H (g)+O (g)===CH COOH(l)的反应热为( )
2 2 3
A.-488.3 kJ·mol-1 B.+488.3 kJ·mol-1
C.-191 kJ·mol-1 D.+191 kJ·mol-1
答案 A
解析 由题知表示各物质燃烧热的热化学方程式分别为① C(s)+
O (g)===CO (g) ΔH=-393.5 kJ·mol-1;② H (g)+O (g)===H O(l) ΔH=-
2 2 2 2 2
285.8 kJ·mol-1;③ CH COOH(l)+2O (g)===2CO (g)+2H O(l) ΔH=-870.3
3 2 2 2
kJ·mol-1。则2C(s)+2H (g)+O (g)===CH COOH(l)可由反应①×2+②×2-③得
2 2 3
出,则反应热为(-393.5 kJ·mol-1)×2+(-285.8 kJ·mol-1)×2-(-870.3 kJ·mol-1)=-488.3 kJ·mol-1。
8.NF 是一种温室气体,其存储能量的能力是CO 的12 000~20 000倍,在
3 2
大气中的寿命可长达740年,如表所示是几种化学键的键能:
化学键 N≡N F—F N—F
键能/(kJ·mol-1) 946 154.8 283.0
下列说法中正确的是( )
A.过程N (g)―→2N(g)放出能量
2
B.过程N(g)+3F(g)―→NF (g)放出能量
3
C.反应N (g)+3F (g)===2NF (g)的ΔH>0
2 2 3
D.NF 吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
3
答案 B
解析 A.N (g)→2N(g)为化学键的断裂过程,应吸收能量,故A错误;B.N(g)
2
+3F(g)→NF (g)为形成化学键的过程,放出能量,故 B 正确;C.反应 N (g)+
3 2
3F (g)===2NF (g) ΔH=(946+3×154.8-283.0×6) kJ·mol-1=-287.6 kJ·mol-
2 3
1,ΔH<0,为放热反应,故C错误;D.NF 吸收能量后如果没有化学键的断裂与生
3
成,无化学变化的发生,故D错误。
9.(2020·广东广州、深圳学调联盟高三调研)用H O 和H SO 的混合溶液可
2 2 2 4
溶出废旧印刷电路板上的铜。已知:
Cu(s)+2H+(aq)===Cu2+(aq)+H (g)
2
ΔH=+64.39 kJ/mol
2H O (l)===2H O(l)+O (g)
2 2 2 2
ΔH=-196.46 kJ/mol
H (g)+O (g)===H O(l) ΔH=-285.84 kJ/mol
2 2 2
在H SO 溶液中,Cu与H O 反应生成Cu2+(aq)和H O(l)的反应热ΔH等于(
2 4 2 2 2
)
A.-319.68 kJ/mol B.-417.91 kJ/mol
C.-448.46 kJ/mol D.+546.69 kJ/mol
答案 A
解析 ①Cu(s)+2H+(aq)===Cu2+(aq)+H (g)
2
ΔH=+64.39 kJ/mol
②2H O (l)===2H O(l)+O (g)
2 2 2 2
ΔH=-196.46 kJ/mol③H (g)+O (g)===H O(l)
2 2 2
ΔH=-285.84 kJ/mol
根据盖斯定律,将①+×②+③,整理可得:Cu(s)+H O (l)+2H+(aq)===Cu2
2 2
+(aq)+2H O(l) ΔH=-319.68 kJ/mol,故合理选项是A。
2
10.下列有关热化学方程式的叙述正确的是( )
A.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋
酸 和 稀 NaOH 溶 液 反 应 的 热 化 学 方 程 式 为 : NaOH(aq) +
CH COOH(aq)===CH COONa(aq)+H O(l) ΔH=-57.4 kJ·mol-1
3 3 2
B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C.已知反应2H (g)+O (g)===2H O(l) ΔH=-571.6 kJ·mol-1,则H 的燃烧
2 2 2 2
热为571.6 kJ·mol-1
D.已知2C(s)+2O (g)===2CO (g) ΔH 2C(s)+O (g)===2CO(g) ΔH ,则
2 2 1, 2 2
ΔH >ΔH
1 2
答案 B
解析 醋酸是弱酸,电离需要吸收热量,所以稀醋酸和稀NaOH溶液反应,产
生1 mol水时放出的热量小于57.4 kJ,A项错误;物质所含有的能量越低越稳定,
金刚石的能量高于石墨,则石墨比金刚石稳定,B项正确;2 mol H 完全燃烧产生
2
2 mol液态水,放出的热量是571.6 kJ,所以1 mol H 完全燃烧生成1 mol液态水,
2
放出的热量是571.6 kJ÷2=285.8 kJ,则氢气的燃烧热为285.8 kJ·mol-1,C项错误;
碳的燃烧反应是放热反应,完全燃烧放出的热量多于不完全燃烧放出的热量,但
焓变是负数,所以ΔH <ΔH ,D项错误。
1 2
11.(2020·河南省驻马店市高三期末)1 mol常见金属M和卤素反应的焓变
ΔH(单位:kJ·mol-1)示意图如图,反应物和生成物均为常温时的稳定状态。下列选
项中不正确的是( )
A.MBr 与Cl 反应的ΔH<0
2 2
B.化合物的热稳定性顺序:MI >MBr >MCl >MF
2 2 2 2
C.MBr (s)+F (g)===MF (s)+Br (l),ΔH=-600 kJ·mol-1
2 2 2 2
D.由MCl (s)制得M的反应是吸热反应
2
答案 B解析 ① M(s)+Cl (g)=== MCl (s) ΔH=-641.3 kJ·mol-1 ;② M(s)+
2 2
Br (l)=== MBr (s) ΔH=-524 kJ·mol-1 ;①-②可得 MBr (s)+Cl (g)===
2 2 2 2
MCl (s)+Br (l) ΔH=-117.3 kJ·mol-1,A正确;放出的能量越多,产物的能量越
2 2
低,物质越稳定,所以化合物的热稳定性顺序为MI