文档内容
专题 08 化学反应与能量变化
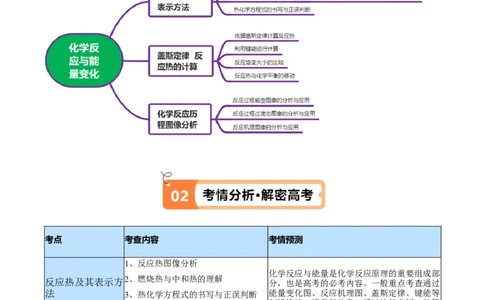
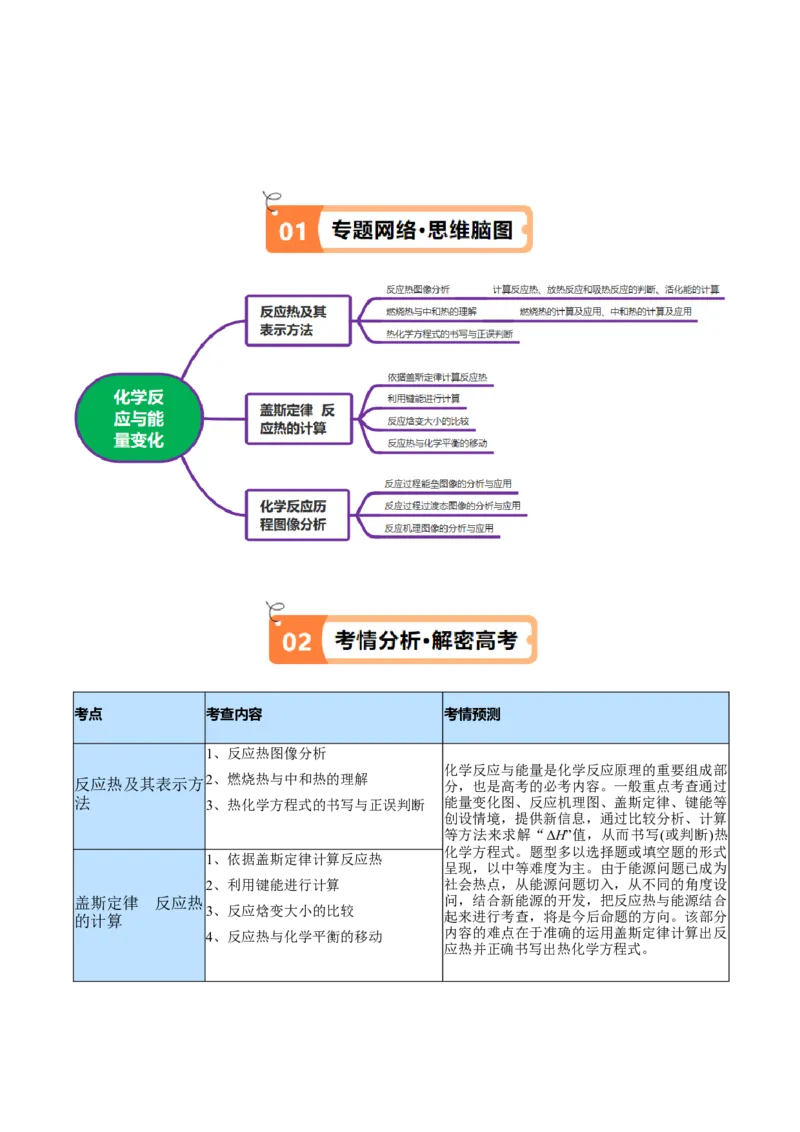
01专题网络·思维脑图
02考情分析·解密高考
03高频考点·以考定法
考点一 反应热及其表示方法 考点二 盖斯定律 反应热的计算
【高考解密】 【高考解密】
命题点01反应热图像分析 命题点01 依据盖斯定律计算反应热
命题点02燃烧热与中和热的理解 命题点02 利用键能进行计算
命题点03热化学方程式的书写与正误判断 命题点03 反应焓变大小的比较
【技巧解密】 命题点04 反应热与化学平衡的移动
【考向预测】 【技巧解密】
【考向预测】
04核心素养·微专题
微专题 化学反应历程图像分析考点 考查内容 考情预测
1、反应热图像分析
化学反应与能量是化学反应原理的重要组成部
反应热及其表示方2、燃烧热与中和热的理解
分,也是高考的必考内容。一般重点考查通过
法 3、热化学方程式的书写与正误判断 能量变化图、反应机理图、盖斯定律、键能等
创设情境,提供新信息,通过比较分析、计算
等方法来求解“ΔH”值,从而书写(或判断)热
化学方程式。题型多以选择题或填空题的形式
1、依据盖斯定律计算反应热
呈现,以中等难度为主。由于能源问题已成为
2、利用键能进行计算 社会热点,从能源问题切入,从不同的角度设
盖斯定律 反应热 问,结合新能源的开发,把反应热与能源结合
3、反应焓变大小的比较
的计算 起来进行考查,将是今后命题的方向。该部分
4、反应热与化学平衡的移动 内容的难点在于准确的运用盖斯定律计算出反
应热并正确书写出热化学方程式。考点一 反应热及其表示方法
命题点01反应热图像分析
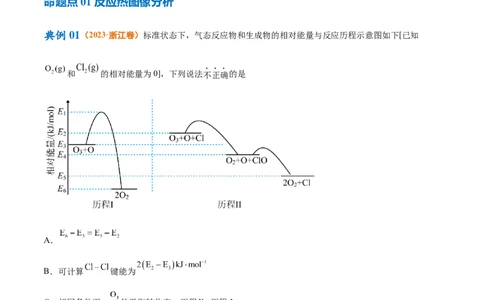
典例01(2023·浙江卷)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知
和 的相对能量为0],下列说法不正确的是
A.
B.可计算 键能为
C.相同条件下, 的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
典例02(2021·浙江卷)在298.15 K、100 kPa条件下,N(g) +3H (g)=2NH (g) ΔH=-92.4 kJ·mol-1,N
2 2 3 2
(g) 、H(g)和NH (g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。一定压强下,1 mol反应中,反应物
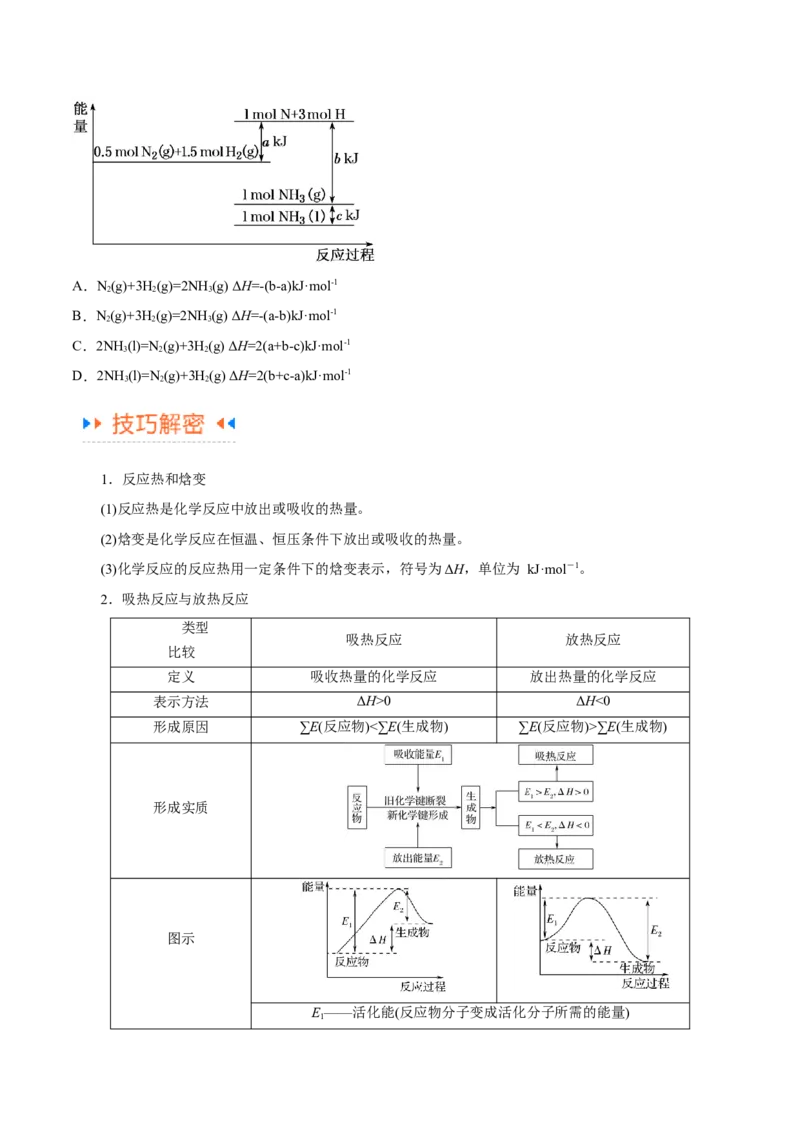
2 3[N (g) +3H (g)]、生成物[2NH (g)]的能量随温度T的变化示意图合理的是
2 2 3
A. B.
C. D.
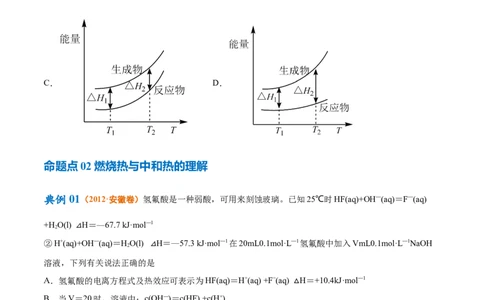
命题点02燃烧热与中和热的理解
典例01(2012·安徽卷)氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时HF(aq)+OH—(aq)=F—(aq)
+H O(l) H=—67.7 kJ·mol—1
2
②H+(a△q)+OH—(aq)=HO(l) H=—57.3 kJ·mol—1在20mL0.1mol·L—1氢氟酸中加入VmL0.1mol·L—1NaOH
2
溶液,下列有关说法正确的△是
A.氢氟酸的电离方程式及热效应可表示为HF(aq)=H+(aq) +F−(aq) H=+10.4kJ·mol—1
B.当V=20时,溶液中:c(OH—)=c(HF) +c(H+) △
C.当V=20时,溶液中:c(F—)<c(Na+)=0.1mol·L—1
D.当V>0时,溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+)
典例02(2012·天津卷)运用有关概念判断下列叙述正确的是
A.1mol H 燃烧放出的热量为H 的燃烧热
2 2
B.NaSO 和HO 的反应为氧化还原反应
2 3 2 2C. 和 互为同系物
D.BaSO 的水溶液不导电,故BaSO 是弱电解质
4 4
命题点03热化学方程式的书写与正误判断
典例01(2023·海南卷)各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
物质
A.
B.
C.
D.
典例02(2023·海南卷)各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
物质
A.
B.
C.
D.
典例03(2016·浙江卷)根据能量变化示意图,下列热化学方程式正确的是A.N(g)+3H(g)=2NH (g) ΔH=-(b-a)kJ·mol-1
2 2 3
B.N(g)+3H(g)=2NH (g) ΔH=-(a-b)kJ·mol-1
2 2 3
C.2NH (l)=N (g)+3H(g) ΔH=2(a+b-c)kJ·mol-1
3 2 2
D.2NH (l)=N (g)+3H(g) ΔH=2(b+c-a)kJ·mol-1
3 2 2
1.反应热和焓变
(1)反应热是化学反应中放出或吸收的热量。
(2)焓变是化学反应在恒温、恒压条件下放出或吸收的热量。
(3)化学反应的反应热用一定条件下的焓变表示,符号为ΔH,单位为 kJ·mol-1。
2.吸热反应与放热反应
类型
吸热反应 放热反应
比较
定义 吸收热量的化学反应 放出热量的化学反应
表示方法 ΔH>0 ΔH<0
形成原因 ∑E(反应物)<∑E(生成物) ∑E(反应物)>∑E(生成物)
形成实质
图示
E——活化能(反应物分子变成活化分子所需的能量)
1E——活化能(生成物分子变成活化分子所需的能量)
2
①ΔH=E-E ①ΔH=E-E
1 2 1 2
②使用催化剂,E 减小,E 减小, ②使用催化剂,E 减小,E
1 2 1 2
ΔH不变 减小,ΔH不变
①所有的中和反应
①所有的水解反应
②所有的燃烧反应
②大多数的分解反应
③大多数的化合反应
反应类型或实例 ③Ba(OH) ·8H O与NH Cl的反应
2 2 4
④活泼金属与水、较活泼金
④C+HO(g)=====CO+H
2 2 属与酸的反应
⑤C+CO=====2CO
2 ⑤铝热反应
3.解答能量变化图像题的“4关键”
(1)反应热不能取决于部分反应物能量和部分生成物能量的相对大小,即部分反应物能量和部分生成物能量的
相对大小不能决定反应是吸热还是放热。
(2)反应是否需要加热,只是引发反应的条件,与反应是放热还是吸热并无直接关系。许多放热反应也需要
加热引发反应,也有部分吸热反应不需加热,在常温时就可以进行。
(3)催化剂只能影响正、逆反应的活化能,而不影响反应的ΔH。
(4)涉及反应热的有关计算时,要切实注意图示中反应物和生成物的物质的量。
(5)注意活化能在图示(如右图)中的意义。
①从反应物至最高点的能量变化(E )表示正反应的活化能。
1
②从最高点至生成物的能量变化(E )表示逆反应的活化能。
2
4.书写热化学方程式时的注意事项
(1)注明反应条件:反应热与测定条件(温度、压强等)有关,特定条件下要注明反
应时的温度和压强。绝大多数反应是在25 ℃、101 kPa下进行测定的,可不注明。
(2)注明物质状态:常用s、l、g、aq分别表示固体、液体、气体、溶液。
(3)注意符号单位:ΔH应包括“+”或“-”、数字和单位( kJ·mol-1)。
(4)注意守恒关系:①原子守恒和得失电子守恒;②能量守恒(ΔH与化学计量数相对应)。
(5)区别于普通方程式:不需要标注“↑”“↓”“点燃”“加热”等。
(6)注意热化学方程式的化学计量数。
(7)对于具有同素异形体的物质,除了要注明聚集状态之外,还要注明物质的名称。
(8)热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,可以是整数,也可以是分数。
且化学计量数必须与ΔH相对应,如果化学计量数加倍,则ΔH也要加倍。
5.燃烧热和中和热应用中的注意事项
(1)燃烧热是指101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时放出的热量,并不是1 mol可燃物燃烧时放出的热量就是燃烧热。必须是1 mol纯物质完全燃烧生成稳定的氧化物,如C燃烧应生成CO 而不是
2
CO,H 燃烧应生成液态水而不是气态水。
2
(2)中和热不是指1 mol酸与1 mol碱中和时的热效应,而是指强酸和强碱在稀溶液中发生中和反应生成1 mol
H2O(l)的热效应。弱酸与强碱,强酸与弱碱或弱酸与弱碱反应时,因电离吸热,放出的热量减少。若用浓硫酸
(或NaOH固体),因溶解放热会使放出的热量增多。
6.利用键能计算反应热,要熟记公式:ΔH=反应物总键能-生成物总键能,其关键是弄清物质中化学键的
数目。在中学阶段要掌握常见单质、化合物中所含共价键的数目。原子晶体:1 mol金刚石中含2 mol C—
C键,1 mol硅中含2 mol Si—Si键,1 mol SiO 晶体中含4 mol Si—O键;分子晶体:1 mol P 中含有6 mol
2 4
P—P键,1 mol P O (即五氧化二磷)中,含有12 mol P—O键、4 mol P===O键,1 mol C H 中含有6 mol C
4 10 2 6
—H键和1 mol C—C键。
6.判断热化学方程式正误的“五看”
一看状态―→看各物质的聚集状态是否正确;
二看符号―→看ΔH的“+”“-”是否正确;
三看单位―→看反应热的单位是否为kJ/mol;
四看数值―→看反应热数值与化学计量数是否相对应;
五看概念―→看燃烧热、中和热的热化学方程式。
考向01 反应热图像分析
1.(2023·浙江·校联考三模)XH和 反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中
加入一定量的XH和 ,t min时测得 ,下列有关说法不正确的是
1
A.t min时容器内的压强比初始状态更大
1
B.C.只改变反应温度,t min时可能出现
1
D.相同条件下,在 ( )时测定,可能出现
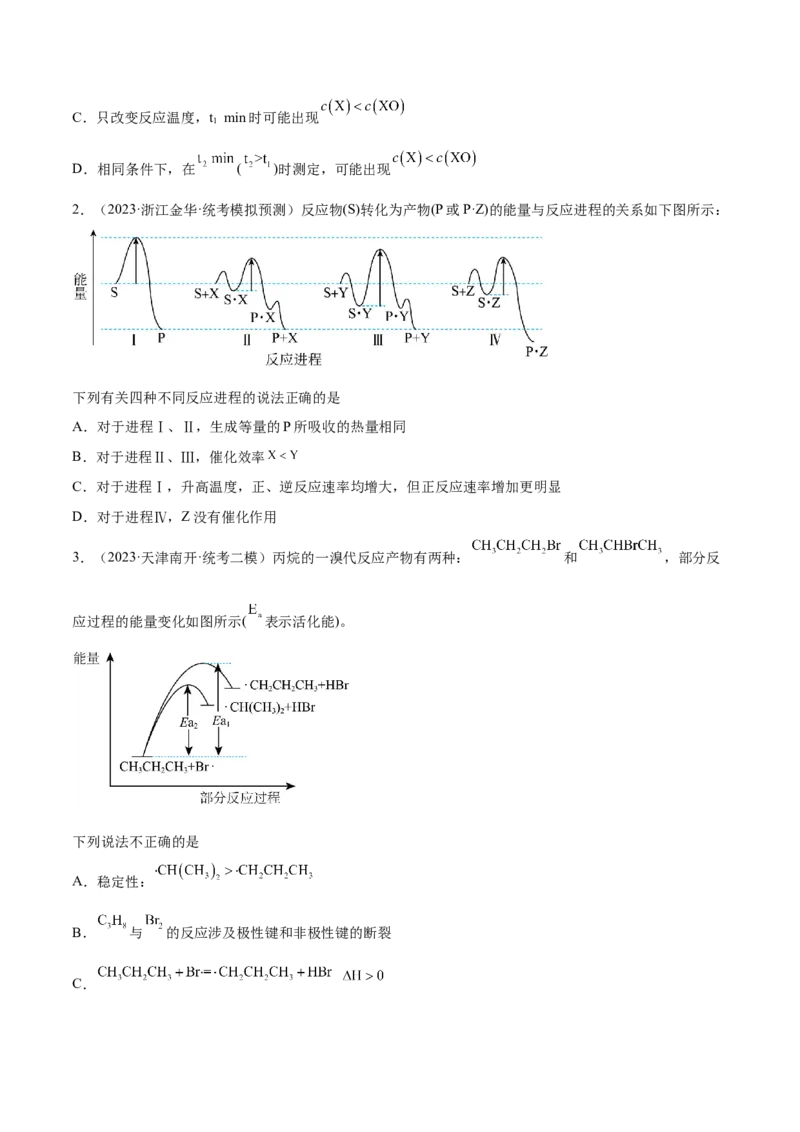
2.(2023·浙江金华·统考模拟预测)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A.对于进程Ⅰ、Ⅱ,生成等量的P所吸收的热量相同
B.对于进程Ⅱ、Ⅲ,催化效率
C.对于进程Ⅰ,升高温度,正、逆反应速率均增大,但正反应速率增加更明显
D.对于进程Ⅳ,Z没有催化作用
3.(2023·天津南开·统考二模)丙烷的一溴代反应产物有两种: 和 ,部分反
应过程的能量变化如图所示( 表示活化能)。
下列说法不正确的是
A.稳定性:
B. 与 的反应涉及极性键和非极性键的断裂
C.D.比较 和 推测生成速率:
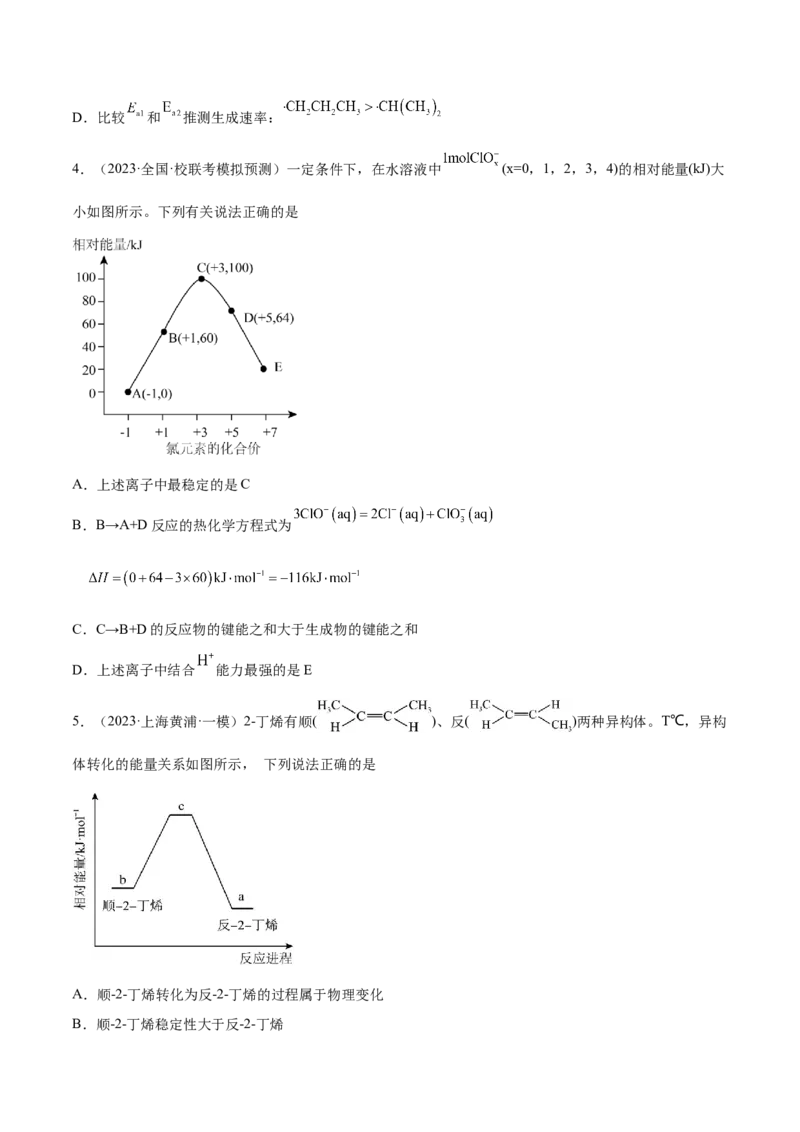
4.(2023·全国·校联考模拟预测)一定条件下,在水溶液中 (x=0,1,2,3,4)的相对能量(kJ)大
小如图所示。下列有关说法正确的是
A.上述离子中最稳定的是C
B.B→A+D反应的热化学方程式为
C.C→B+D的反应物的键能之和大于生成物的键能之和
D.上述离子中结合 能力最强的是E
5.(2023·上海黄浦·一模)2-丁烯有顺( )、反( )两种异构体。T℃,异构
体转化的能量关系如图所示, 下列说法正确的是
A.顺-2-丁烯转化为反-2-丁烯的过程属于物理变化
B.顺-2-丁烯稳定性大于反-2-丁烯C.发生加成反应时,顺−2−丁烯断键吸收的能量低于反−2−丁烯断键吸收的能量
D.T℃,1mol顺−2−丁烯完全转化成反−2−丁烯放出热量(c-b)kJ
考向02燃烧热与中和热的理解
1.(2023·四川雅安·统考模拟预测)已知:
则下列说法正确的是
A.H(g)的燃烧热△H=-571.6 kJ·mol-1
2
B.
C.等质量的H(g)和CHOH(I)完全燃烧生成CO 和液态水,H(g)放出的热量多
2 3 2 2
D.2molH (g)在足量氧气中完全燃烧生成气态水放出的热量大于571.6kJ
2
2.(2023·辽宁·校联考模拟预测)下列有关及应热和热化学方程式的描述不正确的是
A.已知: ,则稀氨水和稀 溶液完全反应生成
时,放出热量少于
B.热化学方程式各物质前的化学计量数既可以是整数也可以是分数,既表示分子数也表示物质的量
C. ,20℃和25℃时, 的燃烧热不同
D.键能数值为平均值,用键能求出的反应热是估算值
3.(2023·广东广州·广州市第二中学校考模拟预测)下列依据热化学方程式得出的结论正确的是
A.若2H(g)+O(g)=2HO(g) ΔH=-483.6kJ·mol-1,则H 的标准燃烧热为-241.8kJ·mol-1
2 2 2 2
B.若C(石墨;s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H O(l) ΔH=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和,
2
放出28.7kJ的热量
D.已知2C(s)+2O(g)=2CO (g) ΔH;2C(s)+O(g)=2CO(g) ΔH,则ΔH>ΔH
2 2 l 2 2 l 2
4.(2023上·河南安阳·高三统考期中)已知:①2H(g)+O(g)=2HO(l) ΔH=-571.6 kJ/mol-1②H+(aq)
2 2 2+OH-(aq)=HO(l) ΔH=-57.3 kJ·mol-1。下列说法中错误的是
2
A.①式表示25 ℃,101 kpa时,2 mol H 和1 mol O 完全燃烧生成2 mol H O(l)放热571.6 kJ
2 2 2
B.2H(g)+O(g)===2HO(g)中ΔH大于-571.6 kJ·mol-1
2 2 2
C.将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量为57.3 kJ
D.将含1 mol NaOH的稀溶液与含1 mol CH COOH的稀溶液混合后放出的热量小于57.3 kJ
3
5.(2023上·河北石家庄·高三石家庄精英中学期中)化学反应在有新物质生成的同时,一定伴随有能量的
变化。下列说法正确的是
A.已知H 的燃烧热为285.8kJ/mol,则表示H 燃烧热的热化学方程式为H(g)+ O(g)=HO(l)
2 2 2 2 2
H=-285.8kJ/mol
△B.已知H+(aq)+OH—(ag)=H
2
O(l) H=—57.3kJ/mol,用含49.0gH
2
SO
4
的浓硫酸与足量稀NaOH溶液反应,
放出57.3kJ热量 △
C.H(g)与O(g)充分反应生成等量的气态水比液态水放出的热量更多
2 2
D.已知I(g)+H(g) 2HI(g) H=-11kJ/mol,现将1molI (g)和1molH (g)充入密闭容器中充分反应后,放
2 2 2 2
出的热量为11kJ △
考向03热化学方程式的书写与正误判断
1.(2023上·陕西西安·高三校考期中)25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表
示该反应的热化学方程式正确的是
A.
B.
C.
D.
2.(2023上·安徽滁州·高三安徽省滁州中学校考期中)已知:各相关物质的燃烧热数据,如下表。
物质 C(s)
燃烧热 /(kJ·mol-1) -393.5 -1366.8 -285.8
下列热化学方程式正确的是A. kJmol-1
⋅
B. kJmol-1
⋅
C. kJmol-1
⋅
D. kJmol-1
⋅
3.(2023上·福建福州·高三福建省福州屏东中学校考期中) 完全燃烧生成 和液态 时,
放出 热量,则下列热化学方程式正确的是
A.
B.
C.
D.
4.(2023上·海南海口·高三海口一中校考期中) 是一种火箭燃料。已知在25℃、101 kPa下,
完全燃烧生成氮气和液态水时放出133.5 kJ热量。则下列热化学方程中正确的是
A.
B.
C.
D.
5.(2023上·四川凉山·高三宁南中学校联考期中)下列有关热化学方程式的描述正确的是
A.一定条件下,表示甲烷( )燃烧热的热化学方程式为:B.氢氧化钾稀溶液和盐酸稀溶液反应,表示中和热的热化学方程式为:
C. 完全燃烧生成 和 时,放出 热量:
D.若 ,则 和 置于密闭容器中充分反
应放出热量为
考点二 盖斯定律 反应热的计算
命题点01依据盖斯定律计算反应热
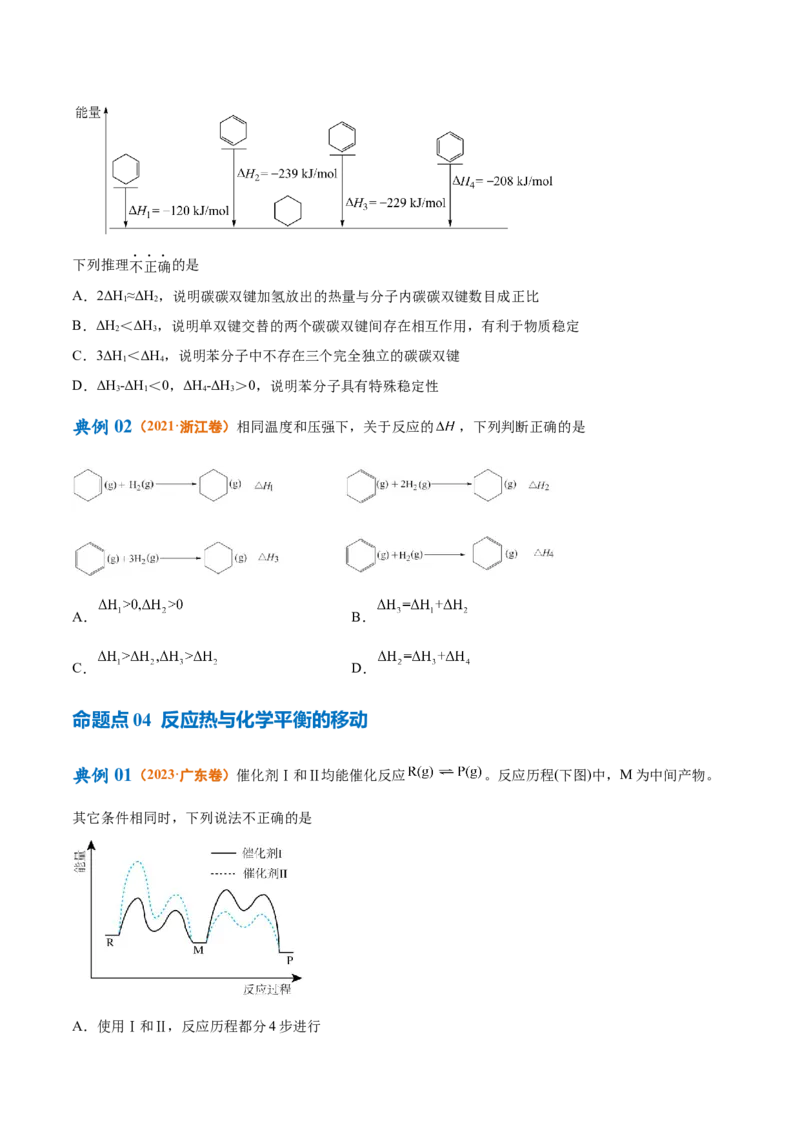
典例01(2022·重庆卷)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH )SO 的离子键
4 2 4
强弱,设计如图所示的循环过程,可得△H/(kJ•mol-1)为
4
A.+533 B.+686 C.+838 D.+1143
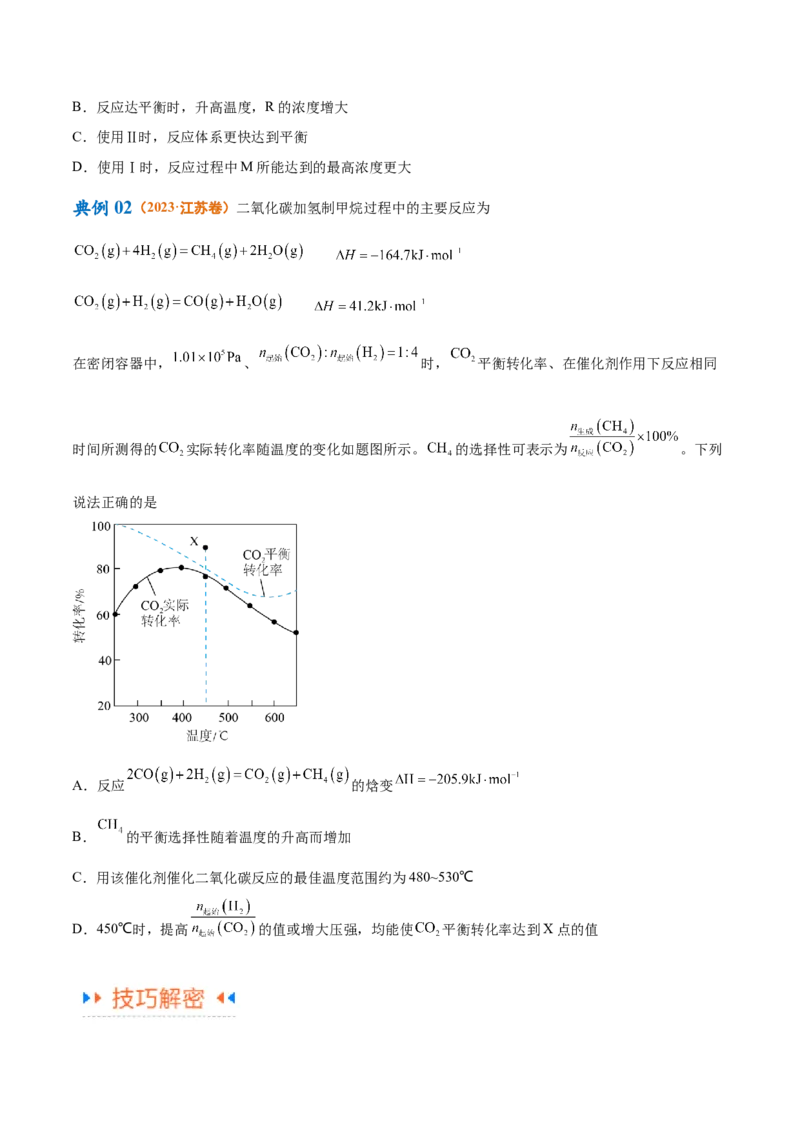
典例02(2020·北京卷)依据图示关系,下列说法不正确的是
A.石墨燃烧是放热反应B.1molC(石墨)和1molCO分别在足量O 中燃烧,全部转化为CO,前者放热多
2 2
C.C(石墨)+CO (g)=2CO(g) ΔH=ΔH-ΔH
2 1 2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
命题点02 利用键能进行计算
典例01(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO
能量/ 249 218 39 10 0 0
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
典例02(2021·浙江卷)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
命题点03 反应焓变大小的比较
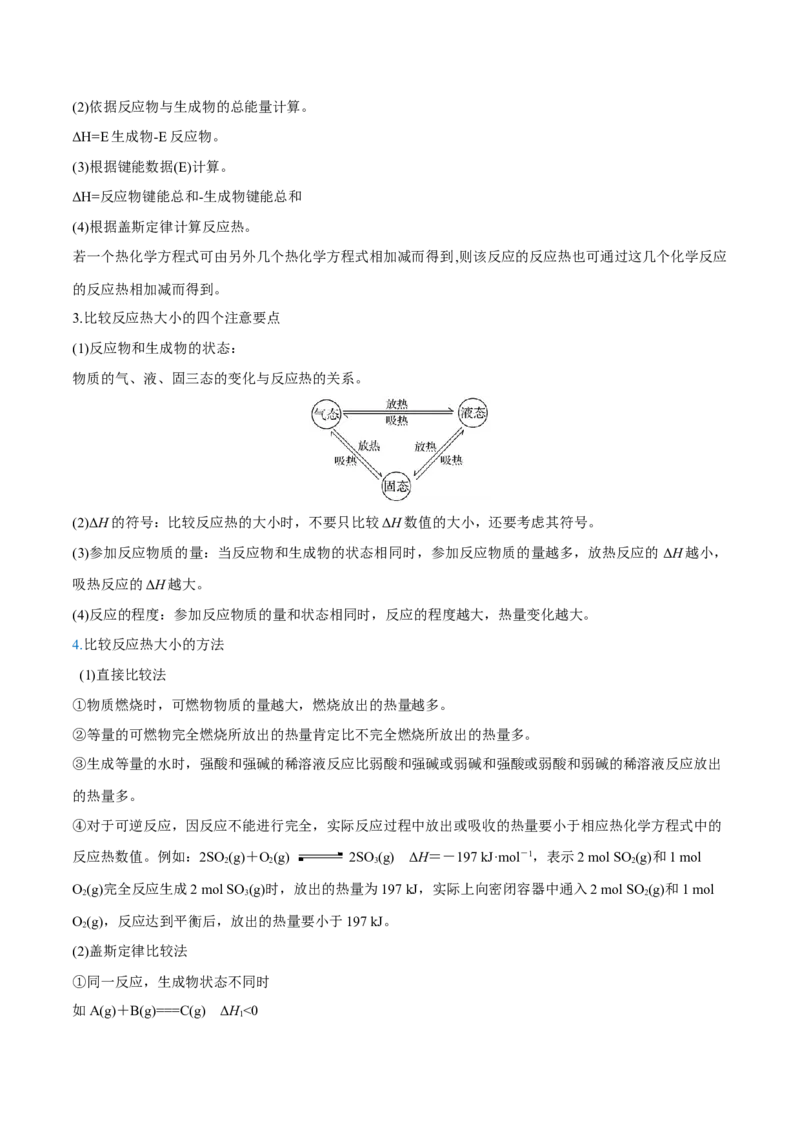
典例01(2022·浙江卷)相关有机物分别与氢气发生加成反应生成1mol环己烷( )的能量变化如图
所示:下列推理不正确的是
A.2ΔH≈ΔH,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
1 2
B.ΔH<ΔH,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
2 3
C.3ΔH<ΔH,说明苯分子中不存在三个完全独立的碳碳双键
1 4
D.ΔH-ΔH <0,ΔH-ΔH >0,说明苯分子具有特殊稳定性
3 1 4 3
典例02(2021·浙江卷)相同温度和压强下,关于反应的 ,下列判断正确的是
A. B.
C. D.
命题点04 反应热与化学平衡的移动
典例01(2023·广东卷)催化剂Ⅰ和Ⅱ均能催化反应 。反应历程(下图)中,M为中间产物。
其它条件相同时,下列说法不正确的是
A.使用Ⅰ和Ⅱ,反应历程都分4步进行B.反应达平衡时,升高温度,R的浓度增大
C.使用Ⅱ时,反应体系更快达到平衡
D.使用Ⅰ时,反应过程中M所能达到的最高浓度更大
典例02(2023·江苏卷)二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是
A.反应 的焓变
B. 的平衡选择性随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值1.盖斯定律
(1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:化学反应的反应
热只与反应体系的始态和终态有关,而与反应的途径无关。
(2)根据盖斯定律计算ΔH的步骤和方法
①计算步骤
②计算方法
(3)盖斯定律应用
1)当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH
也同样要进行加减运算,且要带“+”“-”符号。
2)将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。
3)同一物质的三态变化(固、液、气),状态由固→ 液→气变化时,会吸热;反之会放热。
4)利用状态,迅速比较反应热的大小(若反应为放热反应)
①当反应物状态相同,生成物状态不同时,生成固体放热最多,生成气体放热最少。
②当反应物状态不同,生成物状态相同时,固体反应放热最少,气体反应放热最多。
③在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。
2.反应热计算的四种方法
(1)根据燃烧热数据,求算反应放出的热量。
利用公式:Q=燃烧热×n(可燃物的物质的量)
如已知 H 的燃烧热 ΔH=-285.8 kJ·mol-1,若 H2 的物质的量为 2 mol,则 2 mol H 燃烧放出的热量为 2
2 2
mol×285.8 kJ·mol-1=571.6 kJ。(2)依据反应物与生成物的总能量计算。
ΔH=E生成物-E反应物。
(3)根据键能数据(E)计算。
ΔH=反应物键能总和-生成物键能总和
(4)根据盖斯定律计算反应热。
若一个热化学方程式可由另外几个热化学方程式相加减而得到,则该反应的反应热也可通过这几个化学反应
的反应热相加减而得到。
3.比较反应热大小的四个注意要点
(1)反应物和生成物的状态:
物质的气、液、固三态的变化与反应热的关系。
(2)ΔH的符号:比较反应热的大小时,不要只比较ΔH数值的大小,还要考虑其符号。
(3)参加反应物质的量:当反应物和生成物的状态相同时,参加反应物质的量越多,放热反应的 ΔH越小,
吸热反应的ΔH越大。
(4)反应的程度:参加反应物质的量和状态相同时,反应的程度越大,热量变化越大。
4.比较反应热大小的方法
(1)直接比较法
①物质燃烧时,可燃物物质的量越大,燃烧放出的热量越多。
②等量的可燃物完全燃烧所放出的热量肯定比不完全燃烧所放出的热量多。
③生成等量的水时,强酸和强碱的稀溶液反应比弱酸和强碱或弱碱和强酸或弱酸和弱碱的稀溶液反应放出
的热量多。
④对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的热量要小于相应热化学方程式中的
反应热数值。例如:2SO (g)+O(g ) 2SO (g) ΔH=-197 kJ·mol-1,表示2 mol SO (g)和1 mol
2 2 3 2
O(g)完全反应生成2 mol SO (g)时,放出的热量为197 kJ,实际上向密闭容器中通入2 mol SO (g)和1 mol
2 3 2
O(g),反应达到平衡后,放出的热量要小于197 kJ。
2
(2)盖斯定律比较法
①同一反应,生成物状态不同时
如A(g)+B(g)===C(g) ΔH<0
1A(g)+B(g)===C(l) ΔH<0
2
C(g)===C(l) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
1 3 2 1 2 3
所以ΔH<ΔH。
2 1
②同一反应,反应物状态不同时
如S(g)+O(g)===SO (g) ΔH<0
2 2 1
S(s)+O(g)===SO (g) ΔH<0
2 2 2
S(g)===S(s) ΔH<0
3
ΔH+ΔH=ΔH,ΔH<0,ΔH<0,ΔH<0,
2 3 1 1 2 3
所以ΔH<ΔH。
1 2
5.反应热计算的常见失误点
(1)根据已知的热化学方程式进行计算时,要清楚已知热化学方程式的化学计量数表示的物质的量与已知物质
的量之间的比例关系,然后进行计算。
(2)根据化学键断裂和形成过程中的能量变化计算反应热时,要注意断键和成键的总数,计算时必须是断键和
成键时吸收和放出的总能量。
(3)运用盖斯定律进行计算,在调整方程式时,要注意ΔH的值也要随之调整。
(4)物理变化也会有热效应:在物理变化过程中,也会有能量变化,虽然不属于吸热反应或放热反应,但在
进行相关反应热计算时,必须要考虑发生物理变化时的热效应,如物质的三态变化或物质的溶解过程中的
能量变化等。
(5)不可忽视化学键的物质的量:根据键能计算反应热时,要注意弄清各种化学键的物质的量,既要考虑热
化学方程式中物质的化学计量数,又要考虑物质中各种化学键的个数,再进行计算。反应热(ΔH)等于反应
物中的键能总和减去生成物中的键能总和,即 ΔH=ΣE -ΣE (E 表示键能)。如反应 3H(g)+
反 生 2
N(g)2NH(g) ΔH=3E(H—H)+E(N≡N)-6E(N—H)。
2 3
(6)严格保证热化学方程式与ΔH变化的一致性
a.热化学方程式乘以某一个数时,反应热数值也必须乘上该数。
b.热化学方程式相加减时,相同状态的同种物质之间可相加减,反应热也随之相加减。
c.将一个热化学方程式颠倒时,ΔH的“+”“-”号必须随之改变。考向01 依据盖斯定律计算反应热
1.(2023·山西·统考一模) 和 均为重要的化工原料,都满足 电子稳定结构。
已知:①
②
③断裂 相关化学键所吸收的能量如下表所示:
化学键
能量 a b c
下列说法错误的是
A. 的结构式为
B. 的电子式:
C.
D.
2.(2023上·山西吕梁·高三山西省孝义中学校校考开学考试)已知丙烯( ,气态)的燃烧热
,环丙烷( ,气态)的燃烧热 ,下列热化学方程式或叙述正
确的是
A. (g)+ O(g)=3CO (g)+3HO(g)
2 2 2
B. (g)+3O(g)=3CO(g)+3HO(l)
2 2
C.丙烯比环丙烷稳定D. (g) (g)
3.(2023上·江西新余·高三新余市第一中学校考开学考试)已知下列热化学方程式:
①
②
③
则反应 的焓变为
A.−488.3kJ/mol B.−244.15kJ/mol C.488.3kJ/mol D.244.15kJ/mol
4.(2023上·全国·高三统考开学考试)由金属镁和氧气生成氧化镁的相关反应及其热效应(kJ·mol⁻¹)如下
图所示。由此可判断ΔH 等于
A.725 kJ∙mol−1 B.−725 kJ∙mol−1 C.1929 kJ∙mol−1 D.−1929 kJ∙mol−1
5.(2023·山东菏泽·山东省鄄城县第一中学校考三模)已知 、 、 可作为燃料电池
的燃料,其相关热化学方程式如下。
①
②
③
④
下列说法正确的是
A.B.反应③的
C.反应①中若生成 ,则
D.反应②中的 能表示甲烷的燃烧热
考向02 利用键能进行计算
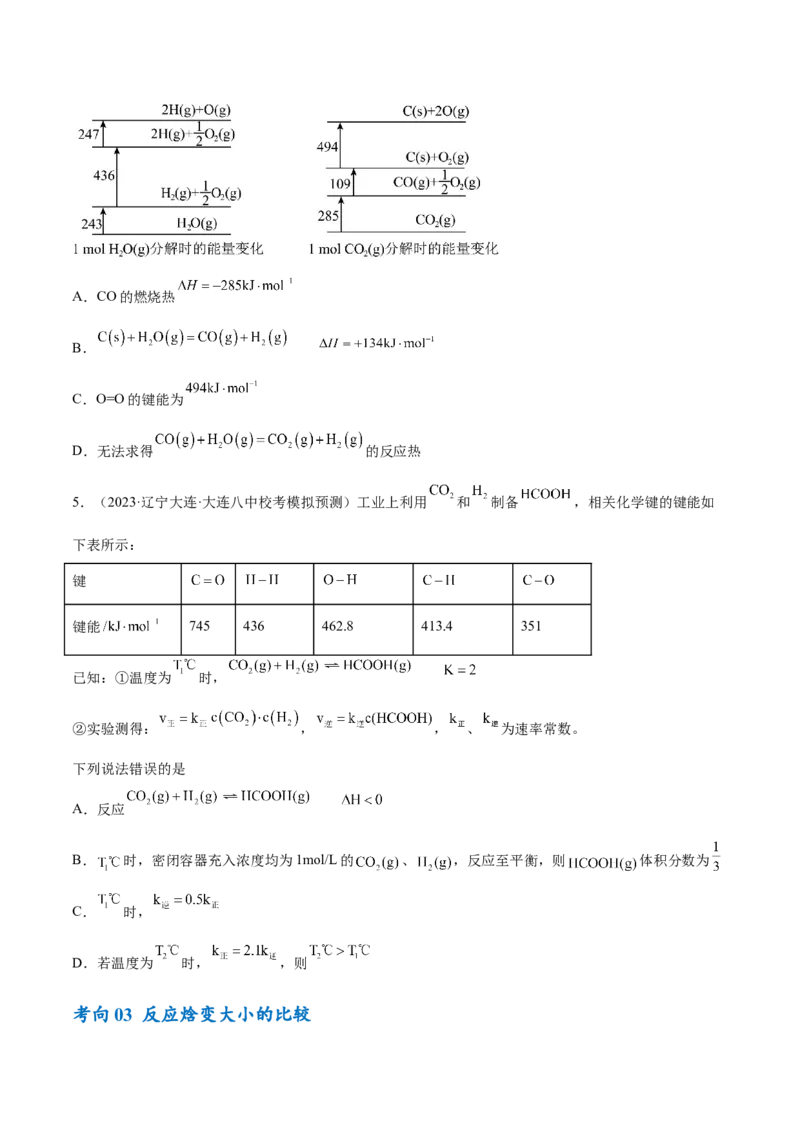
1.(2023·内蒙古赤峰·统考一模)苯和液溴反应进程中的能量变化如图所示。
已知:①断裂化学键所需要的能量(kJ/mol):
C−H C−Br Br−Br(g) H−Br(g)
413 276 194 366
②
③
下列叙述正确的是
A.该反应为放热反应,ΔH=-55 kJ/mol
B.第一步是该反应的决速步骤
C.该反应的原子利用率约为 88%
D.可用NaOH溶液除去溴苯中混有的Br
2
2.(2023·四川资阳·统考一模)我国科学家成功研发了甲烷和二氧化碳的共转化技术,助力“碳中和”目
标。该催化反应历程如图所示:已知部分化学键的键能数据如下:
共价键
键能(kJ/mol) 413 497 462 351 348
下列说法不正确的是
A.该催化反应历程中没有非极性键断裂
B.催化剂的使用降低了该反应的活化能和焓变
C.总反应的原子利用率为100%
D.该反应的热化学方程式为:
3.(2022·浙江·校联考一模)在标准状况下,1mol离子晶体完全分离成气态阳离子、阴离子所吸收的能量
可以用(U)来表示,LiO 是离子晶体,其(U)的实验值可通过玻恩—哈伯热力学循环图计算得到
2
已知 ;
下列说法不正确的是
A.U(LiO)=+2980kJ/mol B.O=O键能为498kJ/mol
2
C.ΔH=703kJ/mol D.Li第一电离能I=1040kJ/mol
2 1
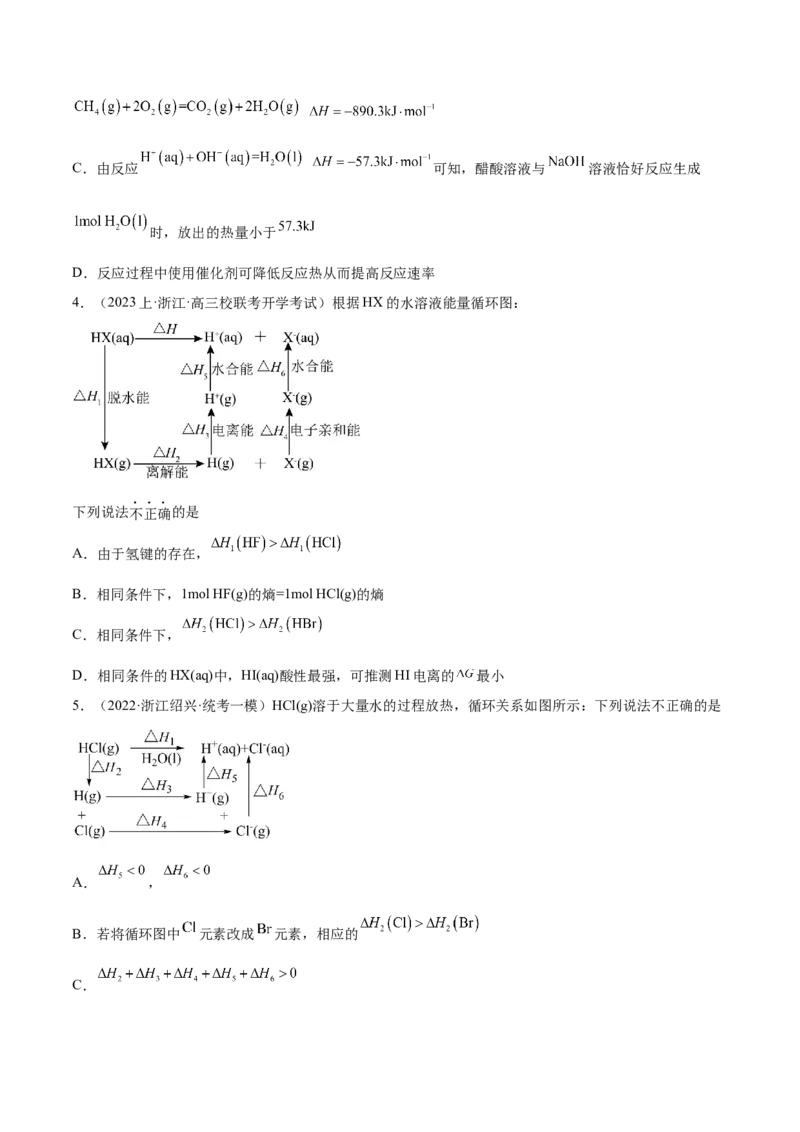
4.(2023·河南·校联考一模)如图1、图2分别表示 和 分解时的能量变化情况(单位:
kJ)。下列说法错误的是A.CO的燃烧热
B.
C.O=O的键能为
D.无法求得 的反应热
5.(2023·辽宁大连·大连八中校考模拟预测)工业上利用 和 制备 ,相关化学键的键能如
下表所示:
键
键能 745 436 462.8 413.4 351
已知:①温度为 时,
②实验测得: , , 、 为速率常数。
下列说法错误的是
A.反应
B. 时,密闭容器充入浓度均为1mol/L的 、 ,反应至平衡,则 体积分数为
C. 时,
D.若温度为 时, ,则
考向03 反应焓变大小的比较1.(2023上·重庆沙坪坝·高三重庆南开中学校考期中)已知2mol金属钾和1mol氯气反应的能量循环如图
所示,下列说法正确的是
A.在相同条件下, ,则
B.在相同条件下, ,则
C. 且该过程形成了分子间作用力
D.
2.(2022上·重庆沙坪坝·高三重庆一中校考阶段练习)几种物质间的转化焓变如图所示,下列说法不正确
的是
A.
B.
C.
D.在相同条件下,若将O元素改为S元素,则 会增大
3.(2023上·四川成都·高三校联考开学考试)下列说法正确的是
A.已知 , ,则
B.甲烷的燃烧热 ,则甲烷燃烧的热化学方程式可表示为:C.由反应 可知,醋酸溶液与 溶液恰好反应生成
时,放出的热量小于
D.反应过程中使用催化剂可降低反应热从而提高反应速率
4.(2023上·浙江·高三校联考开学考试)根据HX的水溶液能量循环图:
下列说法不正确的是
A.由于氢键的存在,
B.相同条件下,1mol HF(g)的熵=1mol HCl(g)的熵
C.相同条件下,
D.相同条件的HX(aq)中,HI(aq)酸性最强,可推测HI电离的 最小
5.(2022·浙江绍兴·统考一模)HCl(g)溶于大量水的过程放热,循环关系如图所示:下列说法不正确的是
A. ,
B.若将循环图中 元素改成 元素,相应的
C.D.
考向04 反应热与化学平衡的移动
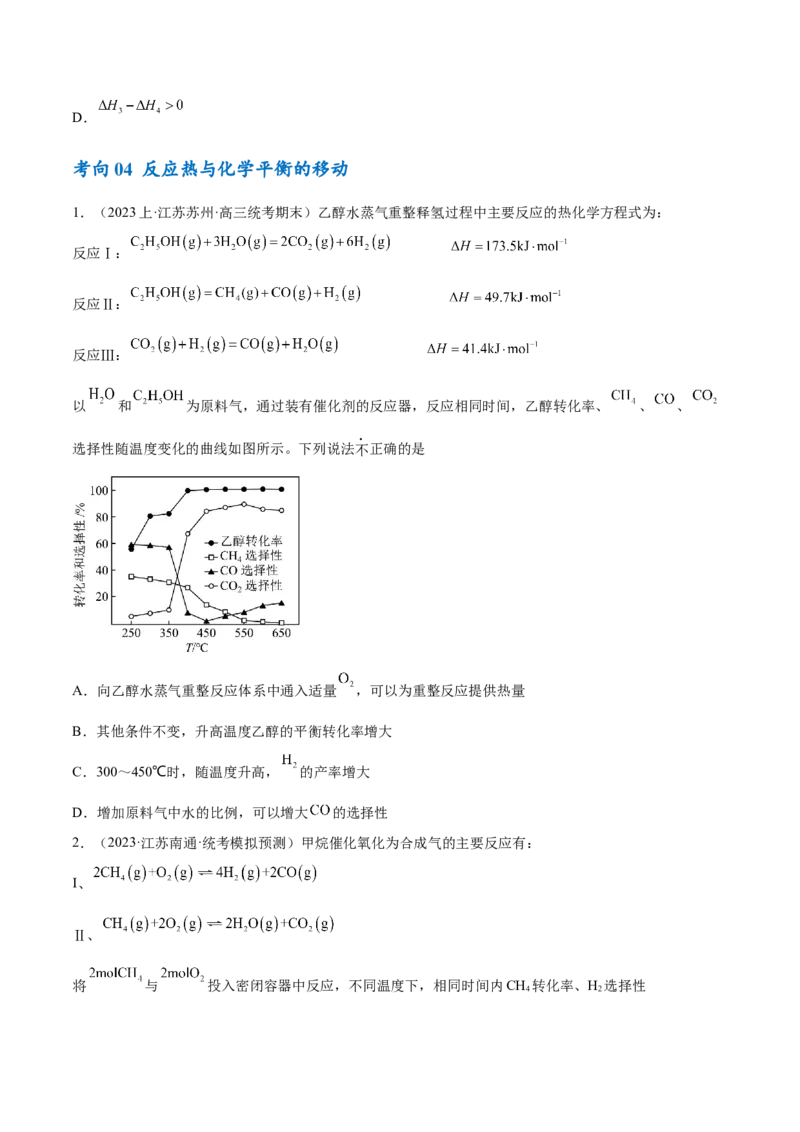
1.(2023上·江苏苏州·高三统考期末)乙醇水蒸气重整释氢过程中主要反应的热化学方程式为:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
以 和 为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率、 、 、
选择性随温度变化的曲线如图所示。下列说法不正确的是
A.向乙醇水蒸气重整反应体系中通入适量 ,可以为重整反应提供热量
B.其他条件不变,升高温度乙醇的平衡转化率增大
C.300~450℃时,随温度升高, 的产率增大
D.增加原料气中水的比例,可以增大 的选择性
2.(2023·江苏南通·统考模拟预测)甲烷催化氧化为合成气的主要反应有:
I、
Ⅱ、
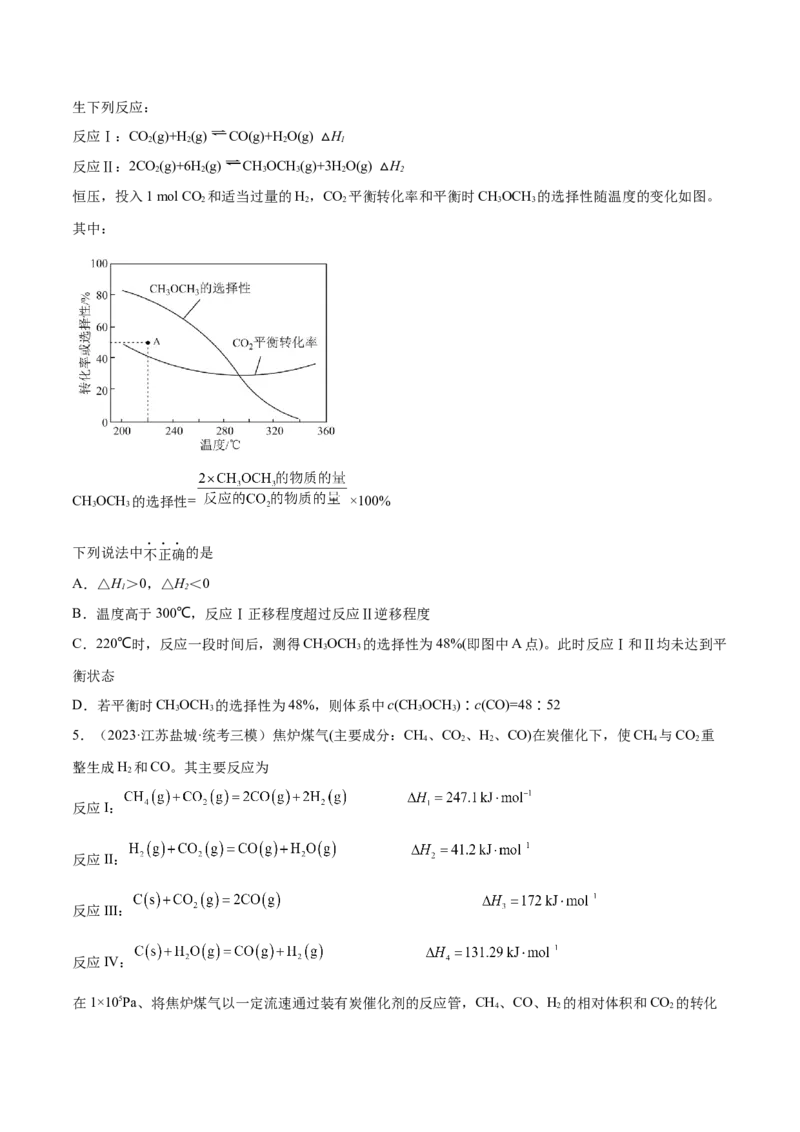
将 与 投入密闭容器中反应,不同温度下,相同时间内CH 转化率、H 选择性
4 2与CO的选择性 随温度的变化如图所示,下列说法正确的是
A.由题可知,反应I为吸热反应
B.在700℃时,容器中生成的CO 的物质的量为1.44mol
2
C.在500℃、600℃、700℃时都可能发生
D.该过程中,低温有利于合成气的生成
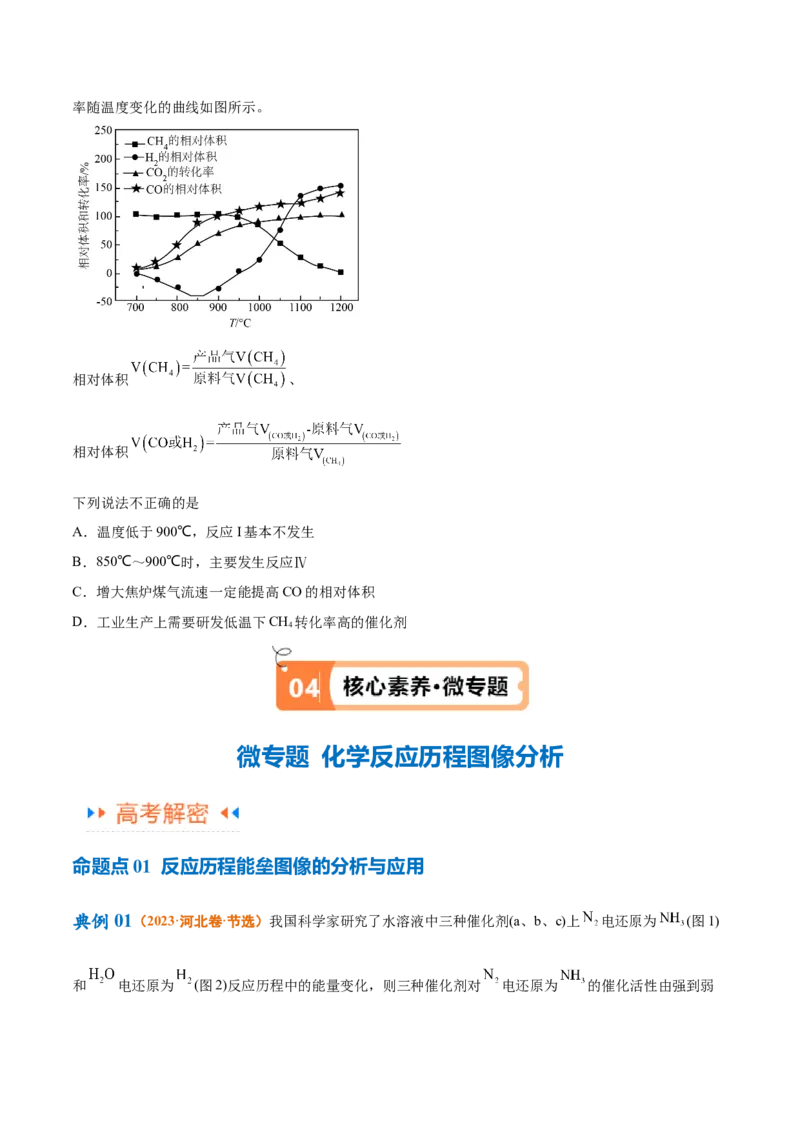
3.(2023·江苏南京·南京师大附中校考模拟预测)在298K、101kPa下,由稳定的单质发生反应生成1mol
化合物的反应热叫该化合物的标准摩尔生成热△Hmθ。氧族元素氢化物a、b、c、d的生成热数据如图。下
f
列判断正确的是
A.沸点:HO>HS>HSe>H Te
2 2 2 2
B.HS(g)+ O(g)=S(s)+HO(1) H=-265 kJ/mol
2 2 2
△
C.HSe(g)=Se(g)+H(g) H=+81 kJ/mol
2 2
D.反应Te(s)+H(g) HT△e(g)达平衡后升温,平衡常数将减小
2 2
4.(2023·北京海淀·101中学校考三模)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发
2 2生下列反应:
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) H
2 2 2 1
反应Ⅱ:2CO(g)+6H(g) CHOCH (g)+△3HO(g) H
2 2 3 3 2 2
恒压,投入1 mol CO 和适当过量的H,CO 平衡转△化率和平衡时CHOCH 的选择性随温度的变化如图。
2 2 2 3 3
其中:
CHOCH 的选择性= ×100%
3 3
下列说法中不正确的是
A.△H>0,△H<0
1 2
B.温度高于300℃,反应Ⅰ正移程度超过反应Ⅱ逆移程度
C.220℃时,反应一段时间后,测得CHOCH 的选择性为48%(即图中A点)。此时反应Ⅰ和Ⅱ均未达到平
3 3
衡状态
D.若平衡时CHOCH 的选择性为48%,则体系中c(CHOCH )∶c(CO)=48∶52
3 3 3 3
5.(2023·江苏盐城·统考三模)焦炉煤气(主要成分:CH、CO、H、CO)在炭催化下,使CH 与CO 重
4 2 2 4 2
整生成H 和CO。其主要反应为
2
反应I:
反应II:
反应III:
反应IV:
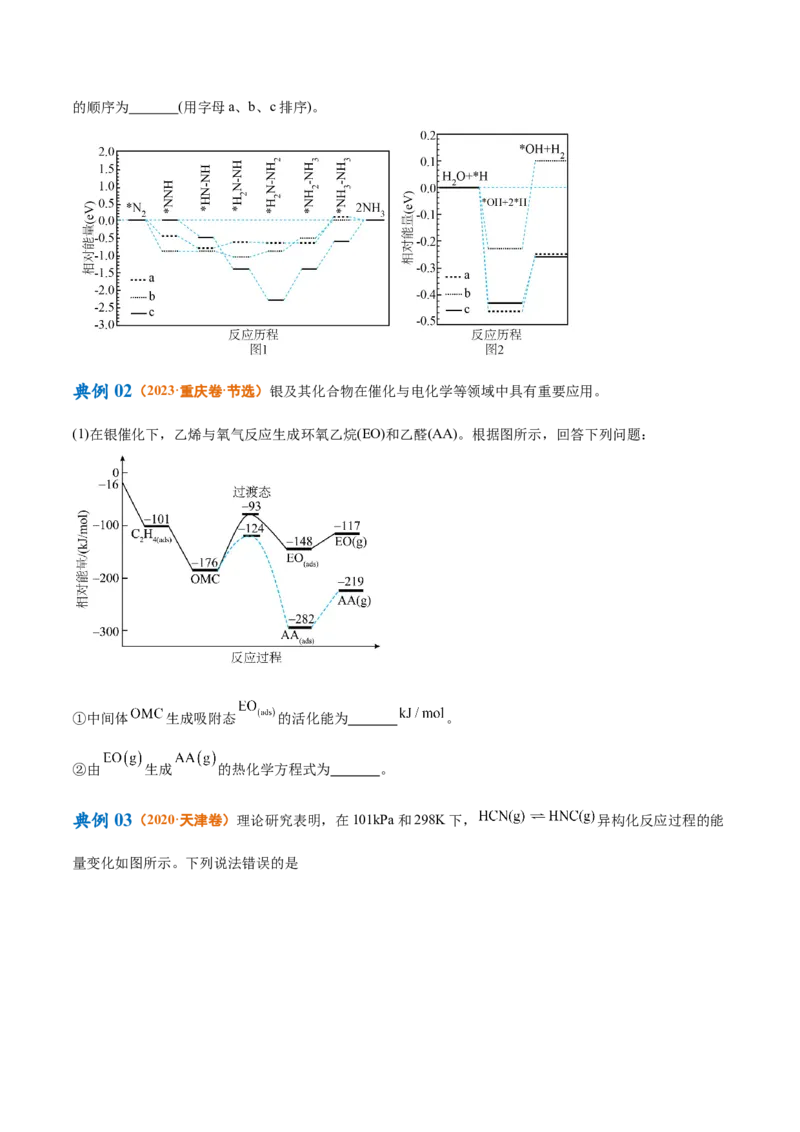
在1×105Pa、将焦炉煤气以一定流速通过装有炭催化剂的反应管,CH、CO、H 的相对体积和CO 的转化
4 2 2率随温度变化的曲线如图所示。
相对体积 、
相对体积
下列说法不正确的是
A.温度低于900℃,反应I基本不发生
B.850℃~900℃时,主要发生反应Ⅳ
C.增大焦炉煤气流速一定能提高CO的相对体积
D.工业生产上需要研发低温下CH 转化率高的催化剂
4
微专题 化学反应历程图像分析
命题点01 反应历程能垒图像的分析与应用
典例01(2023·河北卷·节选)我国科学家研究了水溶液中三种催化剂(a、b、c)上 电还原为 (图1)
和 电还原为 (图2)反应历程中的能量变化,则三种催化剂对 电还原为 的催化活性由强到弱的顺序为 (用字母a、b、c排序)。
典例02(2023·重庆卷·节选)银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:
①中间体 生成吸附态 的活化能为 。
②由 生成 的热化学方程式为 。
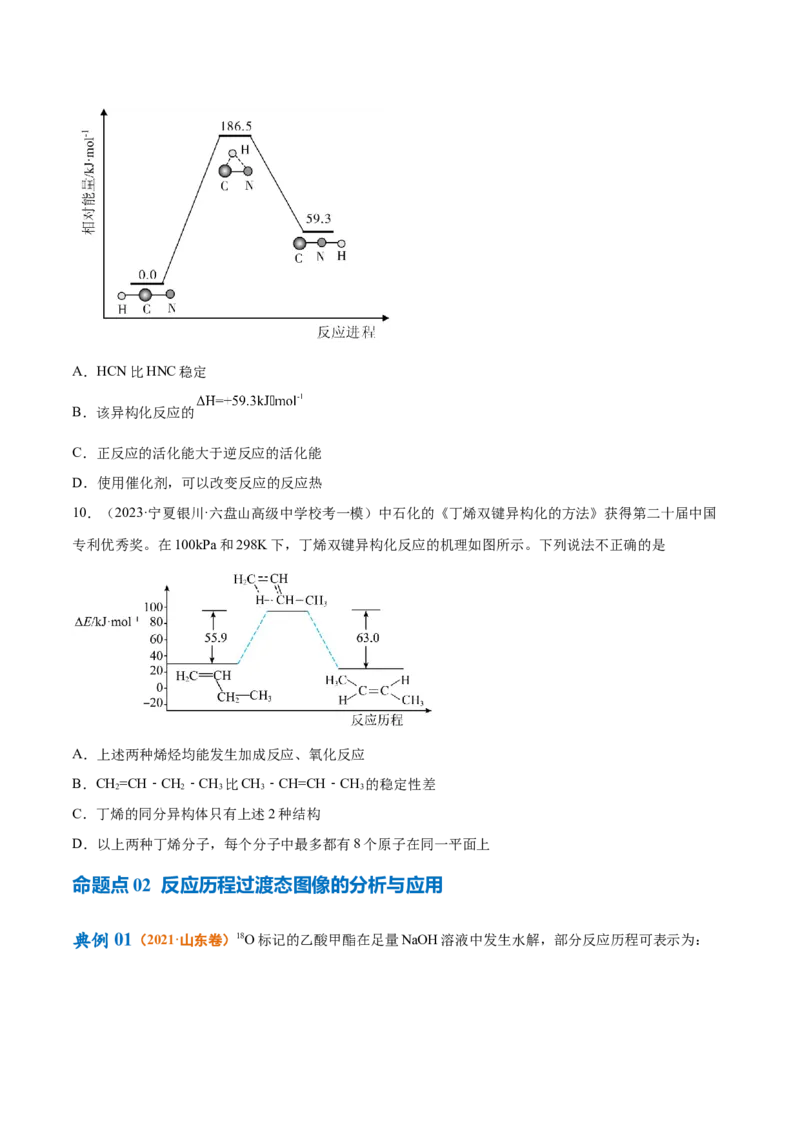
典例03(2020·天津卷)理论研究表明,在101kPa和298K下, 异构化反应过程的能
量变化如图所示。下列说法错误的是A.HCN比HNC稳定
B.该异构化反应的
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
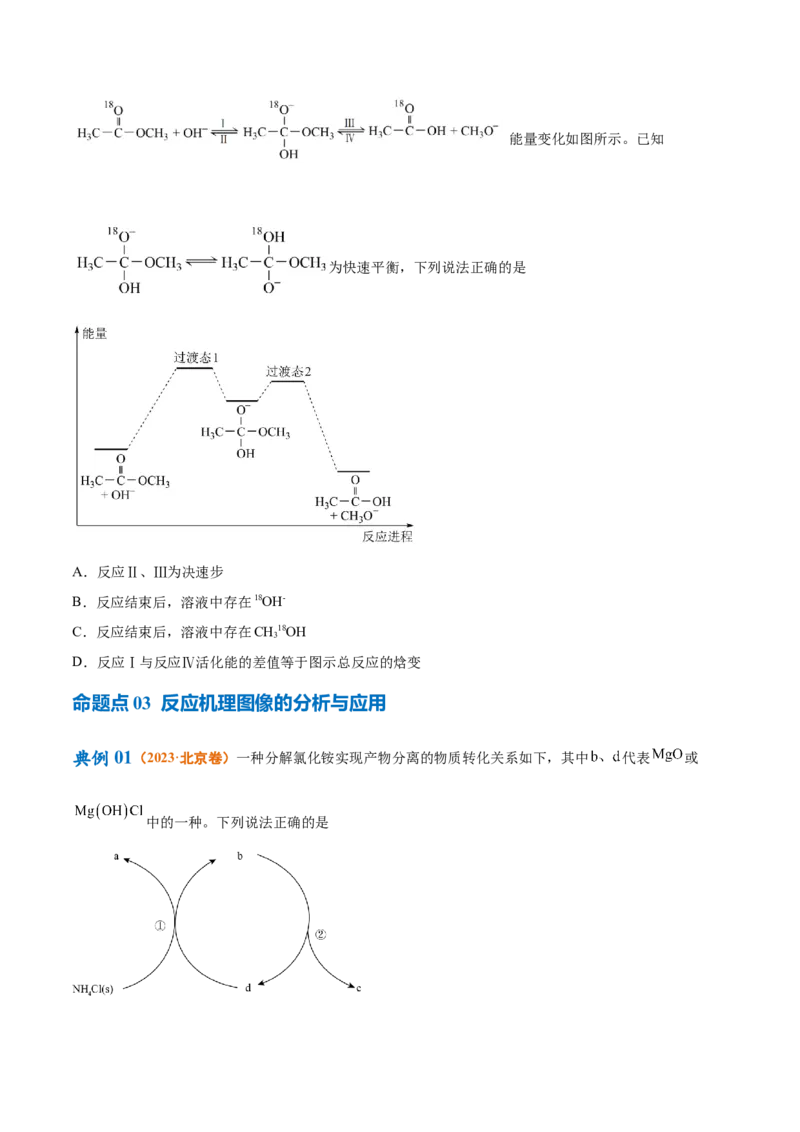
10.(2023·宁夏银川·六盘山高级中学校考一模)中石化的《丁烯双键异构化的方法》获得第二十届中国
专利优秀奖。在100kPa和298K下,丁烯双键异构化反应的机理如图所示。下列说法不正确的是
A.上述两种烯烃均能发生加成反应、氧化反应
B.CH=CH﹣CH﹣CH 比CH﹣CH=CH﹣CH 的稳定性差
2 2 3 3 3
C.丁烯的同分异构体只有上述2种结构
D.以上两种丁烯分子,每个分子中最多都有8个原子在同一平面上
命题点02 反应历程过渡态图像的分析与应用
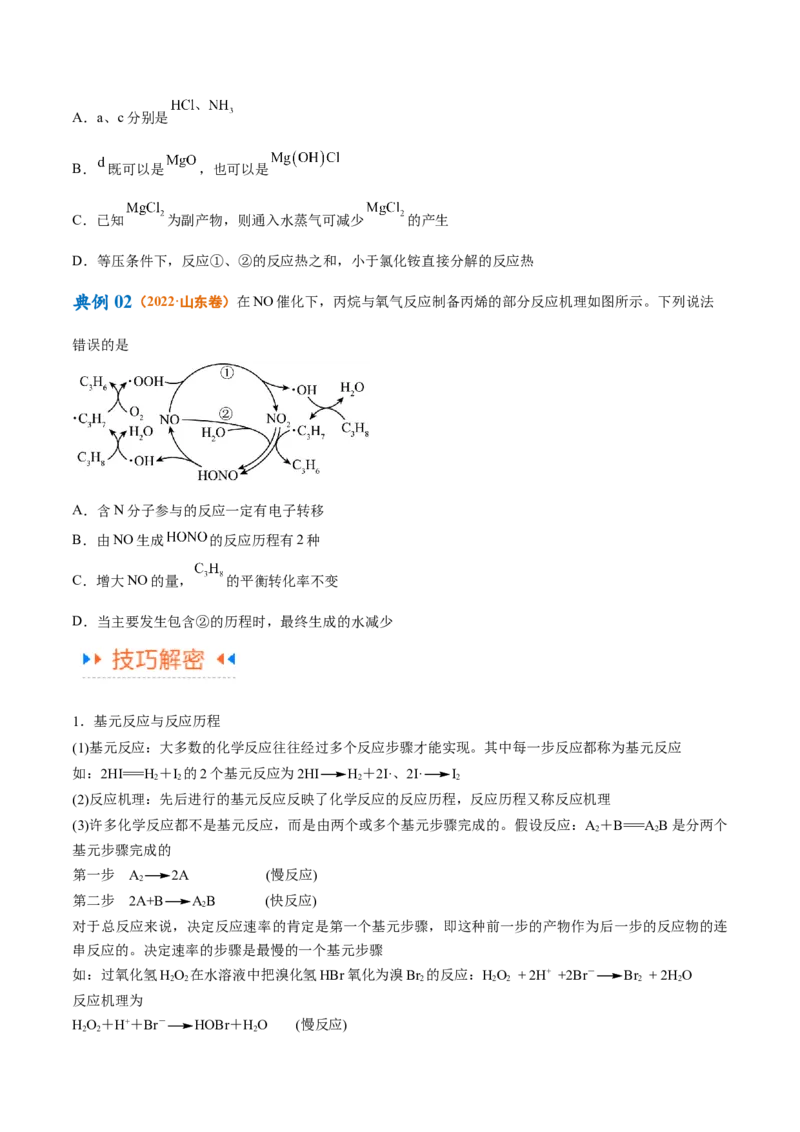
典例01(2021·山东卷)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:能量变化如图所示。已知
为快速平衡,下列说法正确的是
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
命题点03 反应机理图像的分析与应用
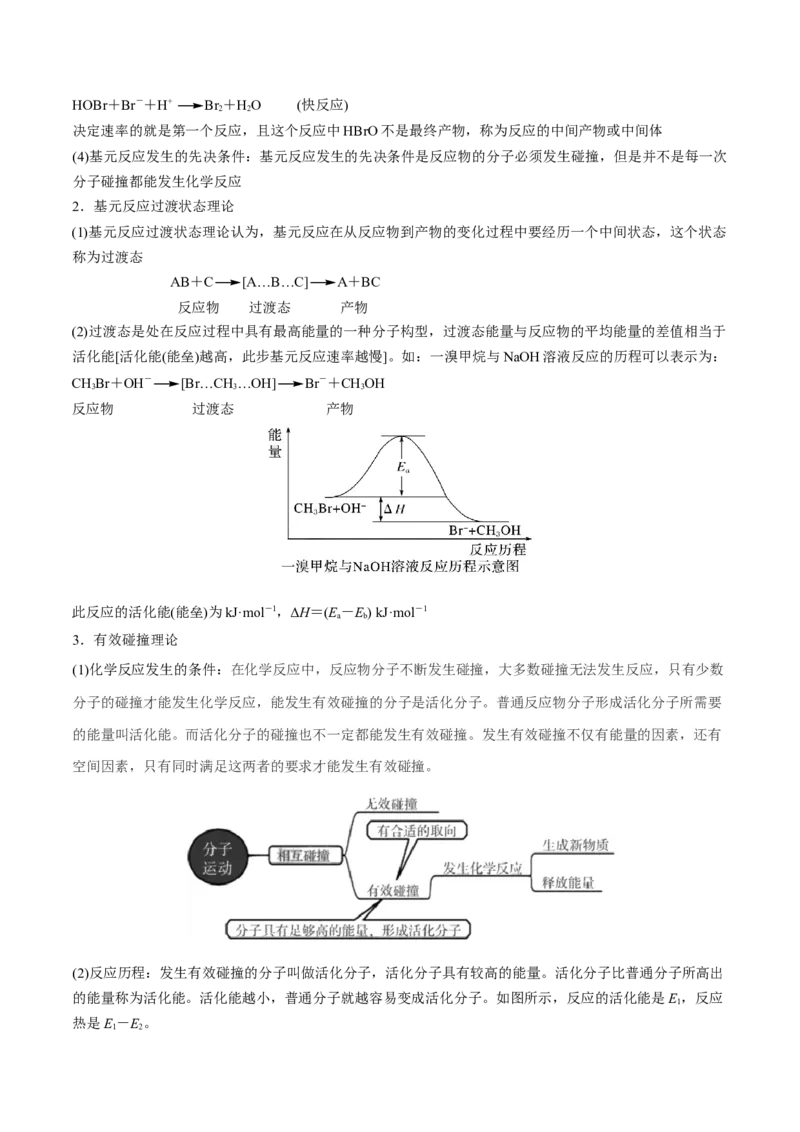
典例01(2023·北京卷)一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表 或
中的一种。下列说法正确的是A.a、c分别是
B. 既可以是 ,也可以是
C.已知 为副产物,则通入水蒸气可减少 的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
典例02(2022·山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法
错误的是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
1.基元反应与反应历程
(1)基元反应:大多数的化学反应往往经过多个反应步骤才能实现。其中每一步反应都称为基元反应
如:2HI===H+I 的2个基元反应为2HI H+2I·、2I· I
2 2 2 2
(2)反应机理:先后进行的基元反应反映了化学反应的反应历程,反应历程又称反应机理
(3)许多化学反应都不是基元反应,而是由两个或多个基元步骤完成的。假设反应:A +B===AB是分两个
2 2
基元步骤完成的
第一步 A 2A (慢反应)
2
第二步 2A+B AB (快反应)
2
对于总反应来说,决定反应速率的肯定是第一个基元步骤,即这种前一步的产物作为后一步的反应物的连
串反应的。决定速率的步骤是最慢的一个基元步骤
如:过氧化氢HO 在水溶液中把溴化氢HBr氧化为溴Br 的反应:HO + 2H+ +2Br- Br + 2H O
2 2 2 2 2 2 2
反应机理为
HO+H++Br- HOBr+HO (慢反应)
2 2 2HOBr+Br-+H+ Br +HO (快反应)
2 2
决定速率的就是第一个反应,且这个反应中HBrO不是最终产物,称为反应的中间产物或中间体
(4)基元反应发生的先决条件:基元反应发生的先决条件是反应物的分子必须发生碰撞,但是并不是每一次
分子碰撞都能发生化学反应
2.基元反应过渡状态理论
(1)基元反应过渡状态理论认为,基元反应在从反应物到产物的变化过程中要经历一个中间状态,这个状态
称为过渡态
AB+C [A…B…C] A+BC
反应物 过渡态 产物
(2)过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与反应物的平均能量的差值相当于
活化能[活化能(能垒)越高,此步基元反应速率越慢]。如:一溴甲烷与NaOH溶液反应的历程可以表示为:
CHBr+OH- [Br…CH…OH] Br-+CHOH
3 3 3
反应物 过渡态 产物
此反应的活化能(能垒)为kJ·mol-1,ΔH=(E-E) kJ·mol-1
a b
3.有效碰撞理论
(1)化学反应发生的条件:在化学反应中,反应物分子不断发生碰撞,大多数碰撞无法发生反应,只有少数
分子的碰撞才能发生化学反应,能发生有效碰撞的分子是活化分子。普通反应物分子形成活化分子所需要
的能量叫活化能。而活化分子的碰撞也不一定都能发生有效碰撞。发生有效碰撞不仅有能量的因素,还有
空间因素,只有同时满足这两者的要求才能发生有效碰撞。
(2)反应历程:发生有效碰撞的分子叫做活化分子,活化分子具有较高的能量。活化分子比普通分子所高出
的能量称为活化能。活化能越小,普通分子就越容易变成活化分子。如图所示,反应的活化能是E,反应
1
热是E-E。
1 2在一定条件下,活化分子所占的百分数是固定不变的。活化分子的百分数越大,单位体积内活化分子数越
多,单位时间内有效碰撞的次数越多,化学反应速率越快。活化能越大,反应速率越慢,化学反应取决于
最慢的一步。
4.常见反应历程(或机理)图像分析
(1)催化剂与化学反应
①在无催化剂的情况下:E 为正反应的活化能;E 为逆反应的活化能;E-E 为此反应的焓变(ΔH)。
1 2 1 2
②有催化剂时,总反应分成了两个反应步骤(也可能为多个,如模拟演练题1中图像所表示的),反应①为
吸热反应,产物为总反应的中间产物,反应②为放热反应,总反应为放热反应。
③催化剂的作用:降低E 、E ,但不影响ΔH,反应是放热反应还是吸热反应取决于起点(反应物)能量和终
1 2
点(生成物)能量的相对大小。
【特别提醒】认识催化剂的五大误区
误区1、认为催化剂不参加化学反应,实质是:催化剂不是不参加化学反应,而是在化学反应前后,催化
剂的化学性质基本不变。
误区2、认为一个反应只有一种催化剂,实质是:一个反应可以有多种催化剂,只是我们常选用催化效率
高的,对环境污染小,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也可以是氯化铁,当然
还可以硫酸铜等。
误区3、认为催化剂都是加快化学反应速率,实质是:催化剂有正催化剂与负催化剂,正催化剂加快化学
反应速率,负催化剂是减慢化学反应速率的。
误区4、认为催化剂的效率与催化剂的量无关,实质是:催化剂参与了化学反应,是第一反应物。既然是
反应物,催化剂的表面积,催化剂的浓度大小必然影响化学反应速率。比如高锰酸钾氧化草酸,开始慢,后来速率突然加快,就是开始时生成二价锰离子浓度小,后来生成锰离子浓度大了,氧化速率突然就加快
了。催化剂的用量是会改变催化效率的。
误区5、认为催化剂反应前后的性质不变,实质是:催化剂反应前后的化学性质不变,物理性质会发生改
变,比如,反应前是块状的,反应后变成了粉末状的。
(2)“环式”反应机理
对于“环式”反应过程图像,位于“环上”的物质一般是催化剂或中间体,如⑤、⑥、⑦和⑧,“入环”
的物质为反应物,如①和④,“出环”的物质为生成物,如②和③。在机理图中,先找到确定的反应物,
反应物一般是通过一个箭头进入整个历程的物质,(产物一般多是通过一个箭头最终脱离这个历程的物质)
与之同时反应的就是催化剂,并且经过一个完整循环之后又会生成;中间产物则是这个循环中的任何一个
环节。如下图中,MoO 则是该反应的催化剂,图中剩余的三个物质均为中间产物。
3
(3)能垒与决速步骤
①能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,
②决速步:包含此能垒的反应我们称之为决速步骤,也成为慢反应。例如下图中,从第一个中间态到过渡
态2的能量就是能垒,而HCOO*+H*=CO +2H*是在Rh做催化剂时该历程的决速步骤。
2【特别提醒】①能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
5.突破能量变化的能垒图
(1)通览全图,理清坐标的含义。能量变化的能垒图的横坐标一般表示反应的历程,横坐标的不同阶段
表示一个完整反应的不同阶段。纵坐标表示能量的变化,不同阶段的最大能垒即该反应的活化能;
(2)细看变化,分析各段反应。仔细观察曲线(直线)的变化趋势,分析每一阶段发生的反应是什么,各段
反应是放热还是吸热,能量升高的为吸热,能量下降的为放热;
(3)综合分析,做出合理判断。综合整合各项信息,回扣题目要求,做出合理判断。如利用盖斯定律将
各步反应相加,即得到完整反应;催化剂只改变反应的活化能,但不改变反应的反应热,也不会改变反应
的转化律。
6.反应机理题的解题思路
(1)通览全图,找准一“剂”三“物”
①催化剂:催化剂在机理图中多数是以完整的循环出现的,以催化剂粒子为主题的多个物种一定在机理图
中的主线上
②反应物:通过一个箭头进入整个历程的物质一般是反应物;
③生成物:通过一个箭头最终脱离整个历程的物质多是产物;
④中间体:通过一个箭头脱离整个历程,但又生成的是中间体,通过两个箭头进入整个历程的中间物质也
是中间体,中间体有时在反应历程中用“[ ]”标出。
(2)逐项分析得答案:根据第一步由题给情境信息,找出催化剂、反应物、生成物、中间体,再结合每一选
项设计的问题逐项分析判断,选出正确答案
考向01 反应历程能垒图像的分析与应用
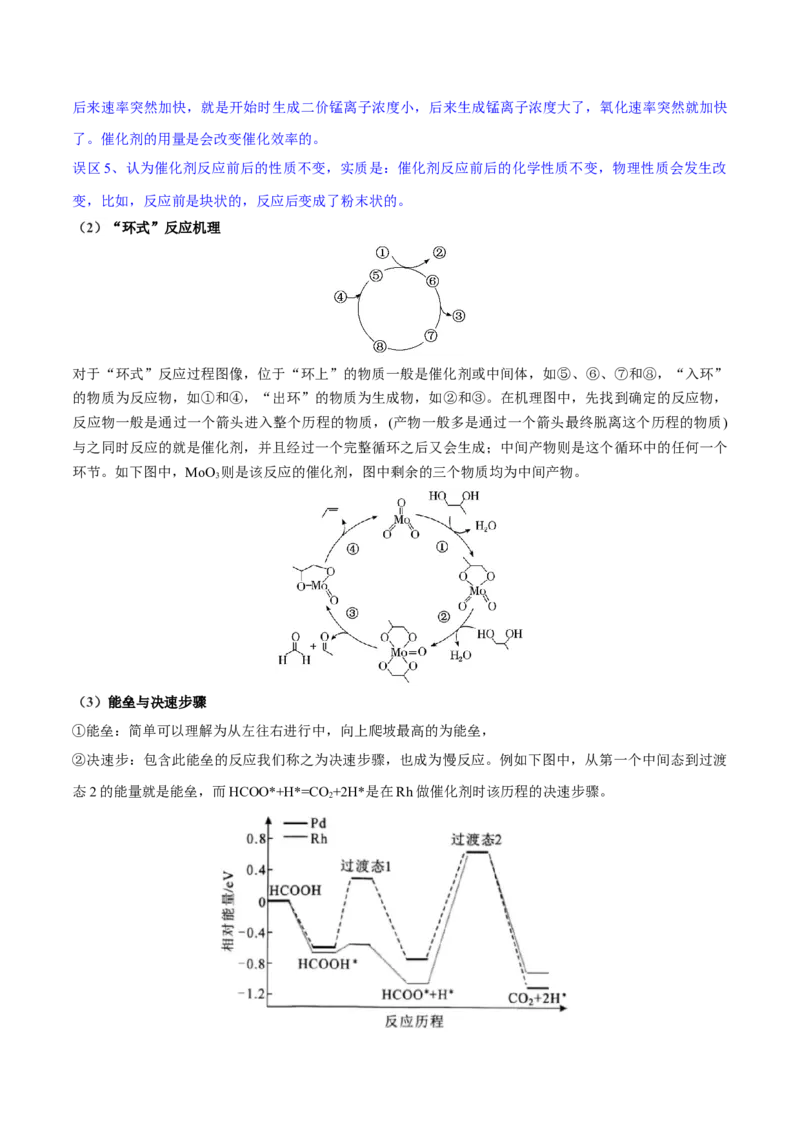
1.(2023·浙江绍兴·统考二模)NO是《联合国气候变化框架公约》所列六种温室气体之一。CO和NO
2 2
在Fe+作用下转化为N 和CO,反应的能量变化及反应历程如图所示,两步基元反应为:① NO+Fe
2 2 2
+=N +FeO+ K,②CO+FeO+=CO +Fe+ K。下列说法不正确的是
2 1 2 2A.该反应ΔH<0
B.两步反应中,决定总反应速率的是反应①
C.升高温度,可提高 NO 的平衡转化率
2
D.Fe+增大了活化分子百分数,加快了化学反应速率,但不改变反应的ΔH
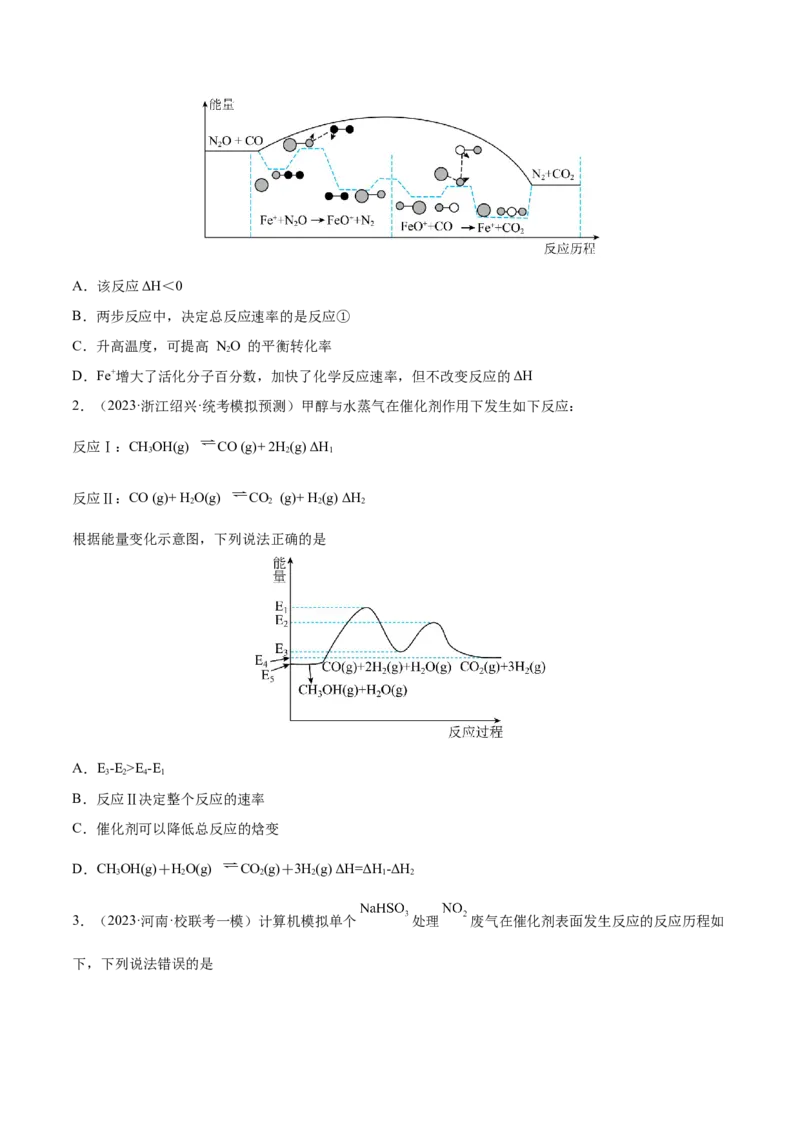
2.(2023·浙江绍兴·统考模拟预测)甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CHOH(g) CO (g)+ 2H (g) ΔH
3 2 1
反应Ⅱ:CO (g)+ H O(g) CO (g)+ H (g) ΔH
2 2 2 2
根据能量变化示意图,下列说法正确的是
A.E-E >E-E
3 2 4 1
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CHOH(g)+HO(g) CO(g)+3H(g) ΔH=ΔH -ΔH
3 2 2 2 1 2
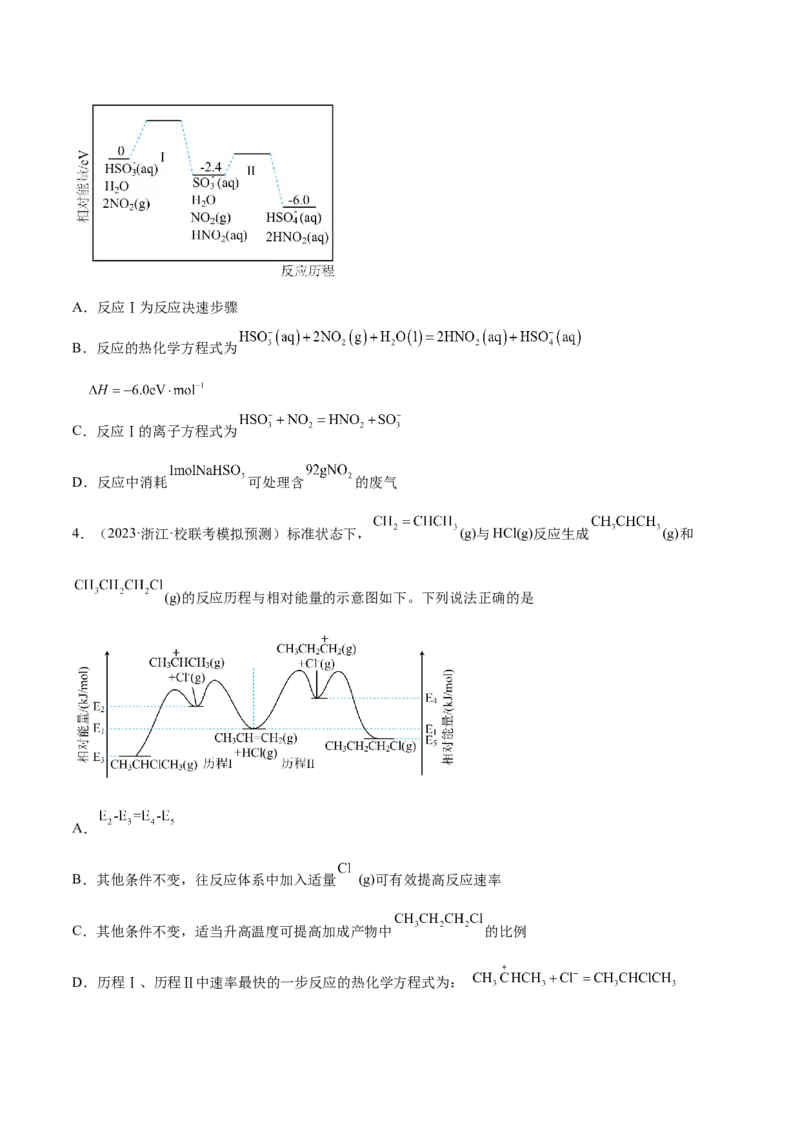
3.(2023·河南·校联考一模)计算机模拟单个 处理 废气在催化剂表面发生反应的反应历程如
下,下列说法错误的是A.反应Ⅰ为反应决速步骤
B.反应的热化学方程式为
C.反应Ⅰ的离子方程式为
D.反应中消耗 可处理含 的废气
4.(2023·浙江·校联考模拟预测)标准状态下, (g)与HCl(g)反应生成 (g)和
(g)的反应历程与相对能量的示意图如下。下列说法正确的是
A.
B.其他条件不变,往反应体系中加入适量 (g)可有效提高反应速率
C.其他条件不变,适当升高温度可提高加成产物中 的比例
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:5.(2023·山东德州·统考三模)苯和甲醇在催化剂 上反应生成甲苯的计算机模拟反应能线图
如下。下列有关说法正确的是(已知:TS代表反应过渡态;Int代表反应中间体。)
A.反应过程中决速步的 为
B.反应过程中不存在 键的形成
C.反应过程中铝元素的化合价发生了变化
D.降低温度能够增大苯的平衡转化率
考向02 反应历程过渡态图像的分析与应用
1.(2023·浙江·校联考模拟预测)下面是丙烷(用 表示)的氯化和溴化反应时的相对能量变化图(已知
)及产率关系。有关说法不正确的是A. 完全生成 放热
B. 比 稳定
C.以丙烷、卤素、氢氧化钠溶液为原料制备2-丙醇, 优于
D.溴代和氯代第一步都是决速反应
2.(2023·江西·江西师大附中校联考模拟预测) 是锂离子电池的一种电解质, ,
在水中水解的反应历程如图所示。已知:甲分子的P原子3d能级参与杂化。TS代表过渡态,M代表产
物。下列叙述正确的是
A.总反应的焓变 小于0B.按照VSEPR理论,甲分子中P原子采用 杂化
C.上述分步反应中 的能垒最大
D.丁挥发时要克服极性键
3.(2023·浙江·校联考模拟预测) 时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水
过程与相对能量变化如图所示:
下列说法不正确的是
A.乙醇通过氢键吸附于固体酸分子筛表面并放出热量
B.生成产物1有4个基元反应
C.生成产物1的热化学方程式为:
D.升高温度、延长反应时间可提高产物1的产率
4.(2023·河南·统考二模)某反应可有效降低汽车尾气污染物的排放,其反应热 。一
定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是(
)
A.三个基元反应中只有③是放热反应
B.该化学反应的速率主要由反应②决定C.该过程的总反应为
D.
5.(2023·河北·校联考三模) 选择性催化还原( )是目前最有效且应用最广的除去 的方
法,在 催化剂上发生反应的机理如图所示,其中TS表示过渡态。下列说法正确的是
A.反应历程中最大的能垒为
B.历程中 的
C.该反应分3步进行
D.在反应历程中有极性共价键和非极性共价键的断裂与形成
考向03 反应机理图像的分析与应用
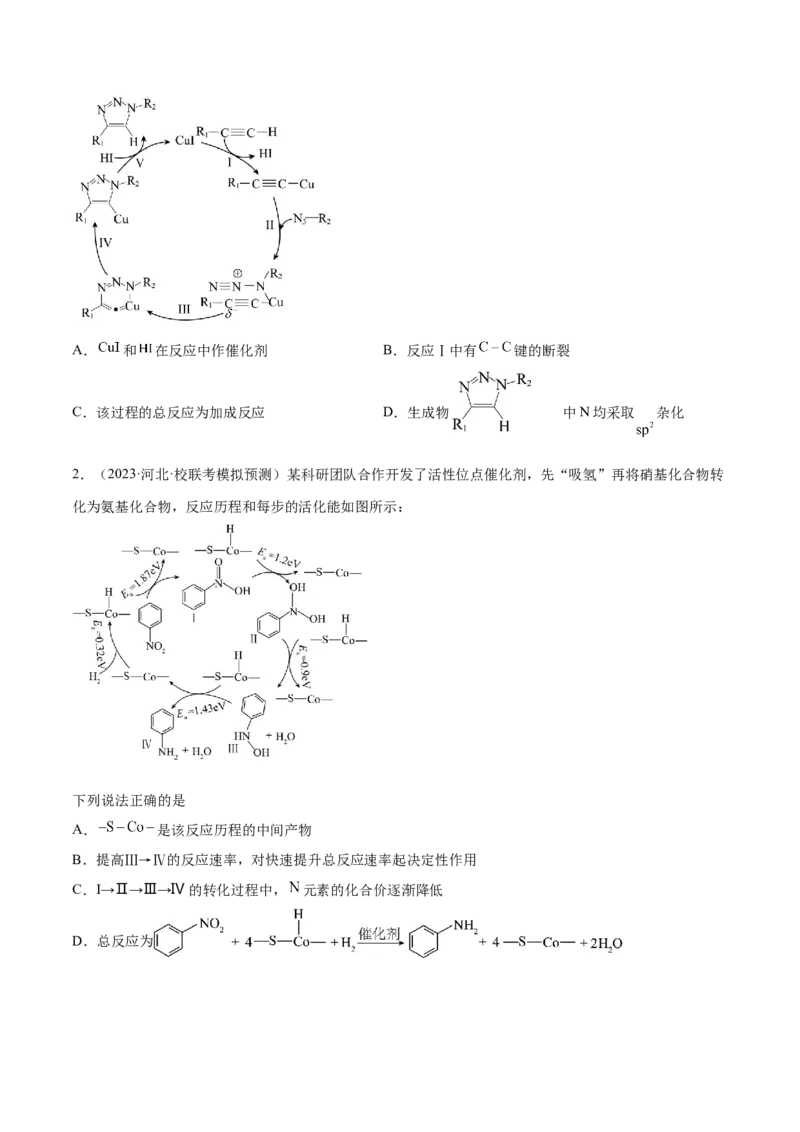
1.(2023下·云南·高二校联考阶段练习)2022年诺贝尔化学奖授予对点击化学和生物正交化学做出贡献
的三位科学家。点击化学的代表反应为叠氮——炔基成环反应,部分原理如图所示。下列说法正确的是A. 和 在反应中作催化剂 B.反应Ⅰ中有 键的断裂
C.该过程的总反应为加成反应 D.生成物 中N均采取 杂化
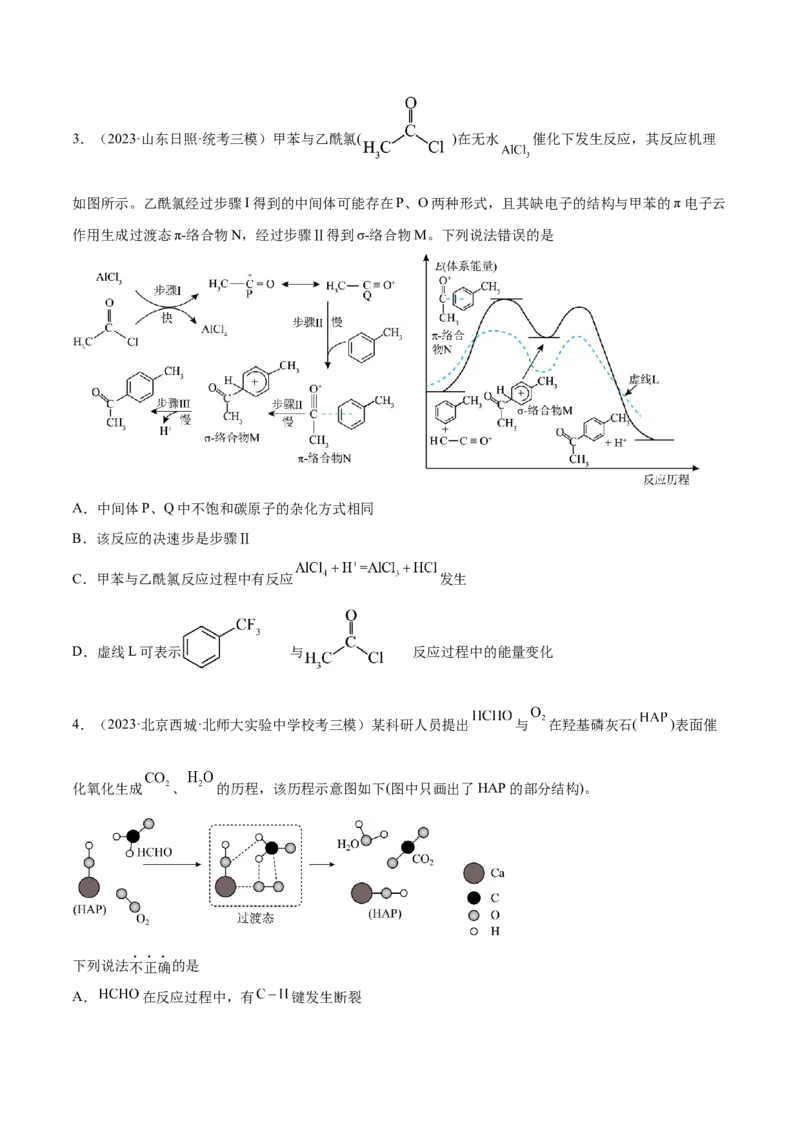
2.(2023·河北·校联考模拟预测)某科研团队合作开发了活性位点催化剂,先“吸氢”再将硝基化合物转
化为氨基化合物,反应历程和每步的活化能如图所示:
下列说法正确的是
A. 是该反应历程的中间产物
B.提高Ⅲ→Ⅳ的反应速率,对快速提升总反应速率起决定性作用
C.I→Ⅱ→Ⅲ→Ⅳ的转化过程中, 元素的化合价逐渐降低
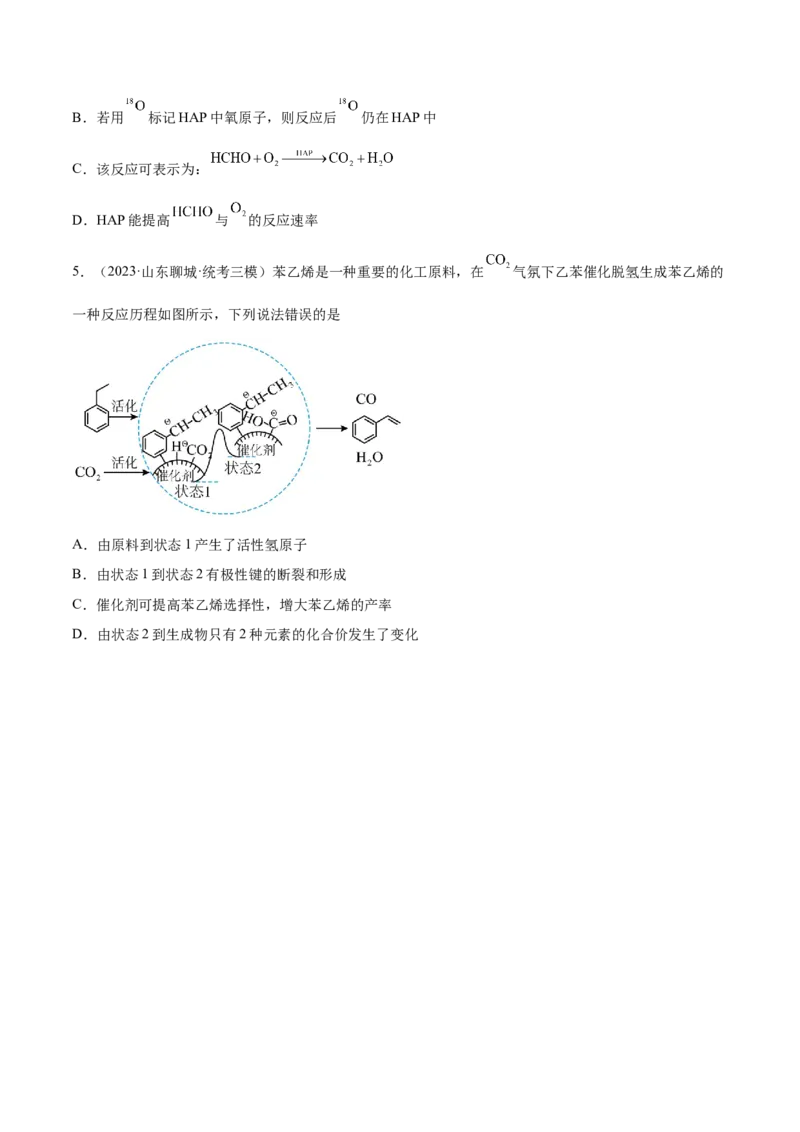
D.总反应为3.(2023·山东日照·统考三模)甲苯与乙酰氯( )在无水 催化下发生反应,其反应机理
如图所示。乙酰氯经过步骤I得到的中间体可能存在P、O两种形式,且其缺电子的结构与甲苯的π电子云
作用生成过渡态π-络合物N,经过步骤Ⅱ得到σ-络合物M。下列说法错误的是
A.中间体P、Q中不饱和碳原子的杂化方式相同
B.该反应的决速步是步骤Ⅱ
C.甲苯与乙酰氯反应过程中有反应 发生
D.虚线L可表示 与 反应过程中的能量变化
4.(2023·北京西城·北师大实验中学校考三模)某科研人员提出 与 在羟基磷灰石( )表面催
化氧化生成 、 的历程,该历程示意图如下(图中只画出了HAP的部分结构)。
下列说法不正确的是
A. 在反应过程中,有 键发生断裂B.若用 标记HAP中氧原子,则反应后 仍在HAP中
C.该反应可表示为:
D.HAP能提高 与 的反应速率
5.(2023·山东聊城·统考三模)苯乙烯是一种重要的化工原料,在 气氛下乙苯催化脱氢生成苯乙烯的
一种反应历程如图所示,下列说法错误的是
A.由原料到状态1产生了活性氢原子
B.由状态1到状态2有极性键的断裂和形成
C.催化剂可提高苯乙烯选择性,增大苯乙烯的产率
D.由状态2到生成物只有2种元素的化合价发生了变化