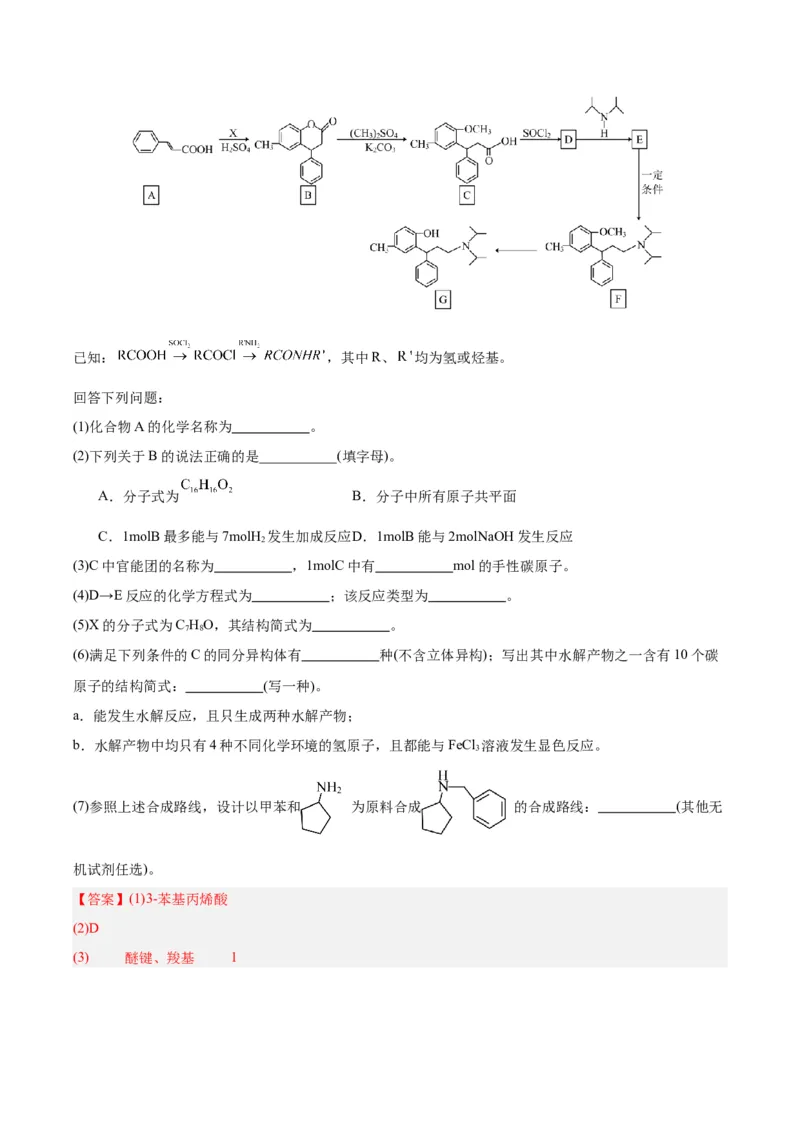
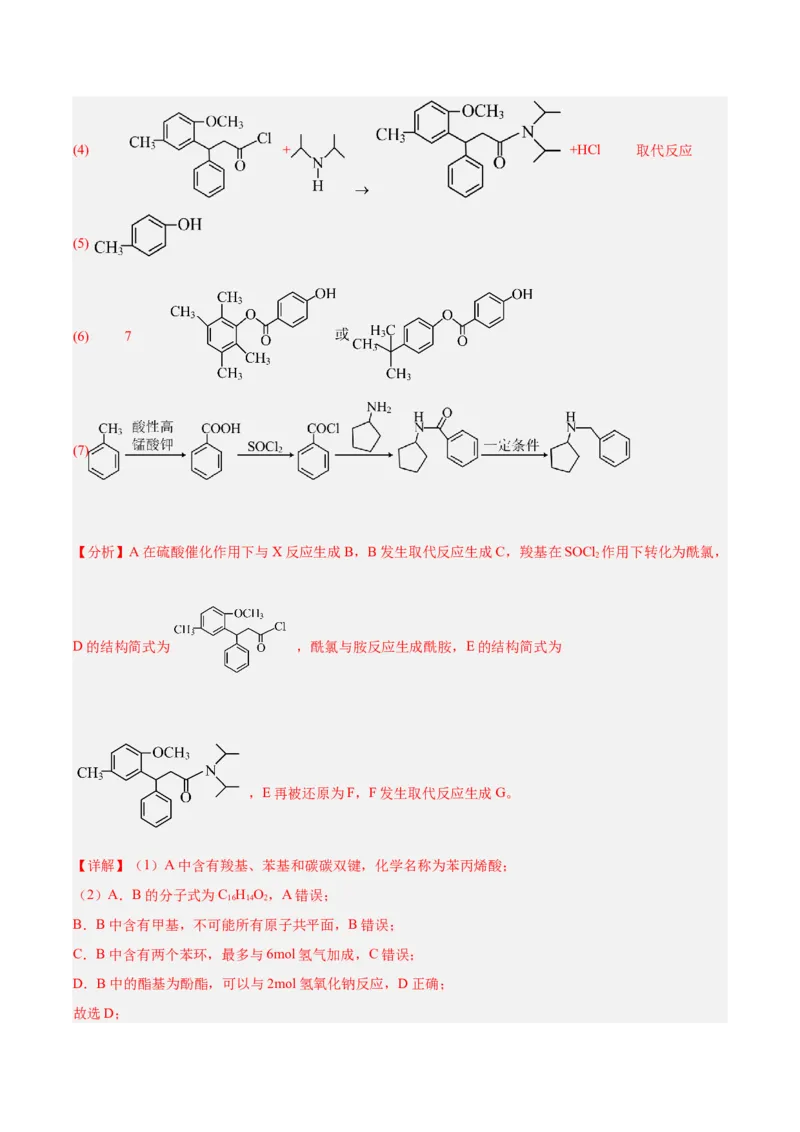
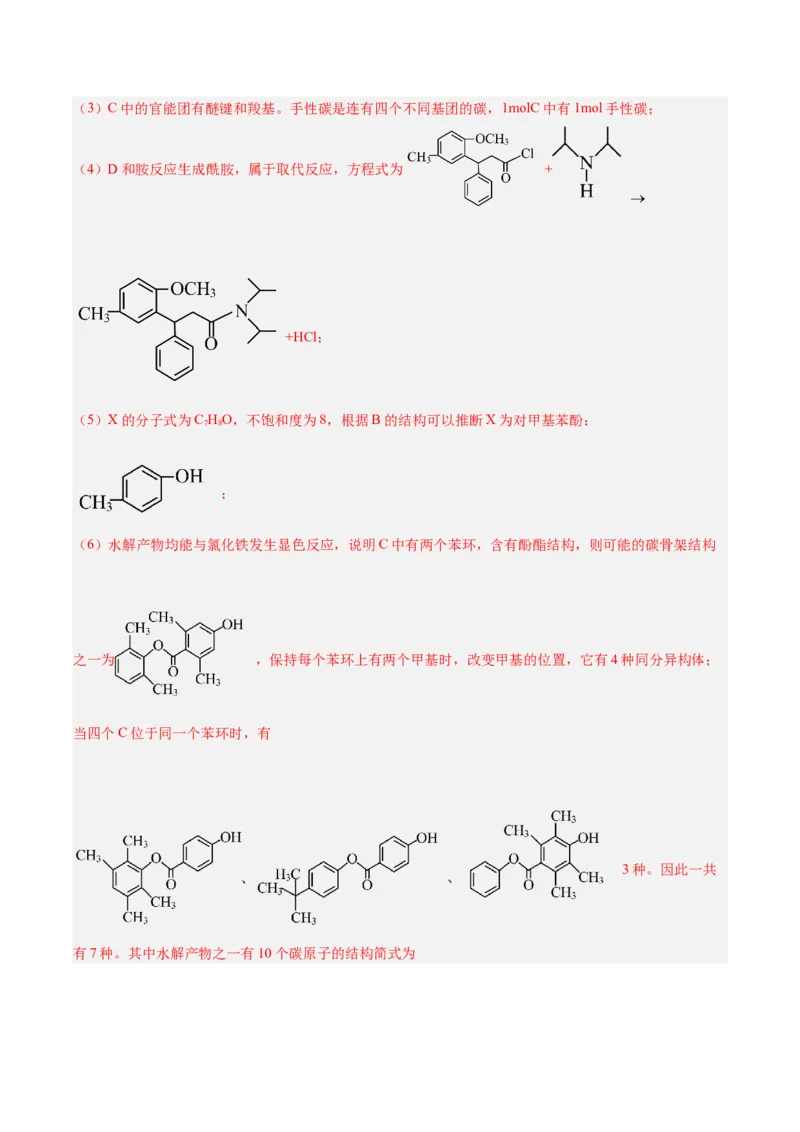
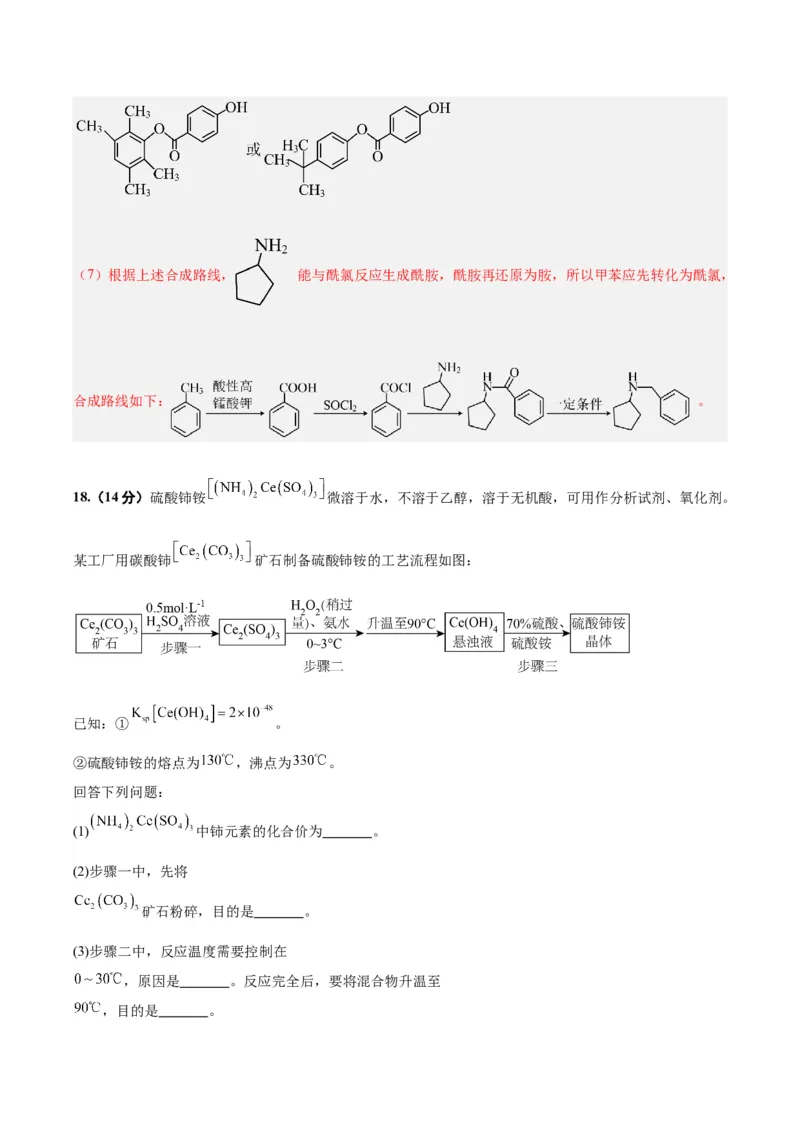
文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟(北京专用)
黄金卷01
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 S 32 Fe 56 Ce 140
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
1.下列“一带一路”特色贸易商品中,主要有机成分不属于糖类的是
A.吉尔吉斯坦蜂蜜 B.内蒙古羊绒 C.新疆棉花 D.俄罗斯大列巴
【答案】B
【详解】羊绒主要有机成分为蛋白质,不属于糖类。
故选:B。
2.2023年10月24日,新修订的海洋保护法获得通过。以下过程未涉及氧化还原反应的是
A.量子点技术应用于深海探测与光学传感 B.高铁酸钠(NaFeO)处理水
2 4
C.利用风电技术对海水进行原位电解制氢 D.热空气吹出法从海水中提溴
【答案】A
【详解】A.量子点发光未发生化学变化,A正确;
B.高铁酸钠(NaFeO)利用其强氧化性消杀病毒,涉及氧化还原,B错误;
2 4
C.水制备氢气,涉及价态变化,C错误;
D.海水中溴以溴离子存在,将其转化为溴单质,存在价态变化,D错误;
故选:A。
3.下列化学用语表述正确的是A. 的球棍模型: B.NaCl晶体的晶胞:
C.丁二烯的键线式: D.基态Cr原子的价层电子轨道式:
【答案】D
【详解】A.该模型为 的空间充填模型而非球棍模型,A错误;
B.晶胞要求是“无隙并置”,B选项给出的立方体平移一个单位后,顶点并不能重叠,所以不是NaCl的
晶胞,B错误;
C.丁二烯的键线式为 ,C错误;
D.Cr是第24号元素,价电子排布式为 。根据洪特规则,基态原子中,填入简并轨道的电子总是先
单独分占,且自旋平行,所以Cr的3d能级的电子分占简并轨道且自旋平行,但4s与3d不是简并轨道,
自旋方向不一定平行,D正确;
故选:D。
4.下列事实不能用勒夏特列原理(平衡移动原理)解释的是
A.在含有 的溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
B.实验室中常用排饱和食盐水的方法收集
C.工业上生产硫酸时,充入过量的空气以提高 的转化率
D.由 、 蒸气、HI组成的平衡体系,加压(减小容器容积)后颜色变深
【答案】D
【详解】A.Fe(SCN) 溶液中存在化学平衡Fe(SCN) Fe3++3SCN-,加入铁粉,发生反应Fe3++Fe=3Fe2+,
3 3
Fe3+的浓度减小,平衡正向移动,溶液颜色变浅或褪去,能用勒夏特列原理解释,故A不选;
B.氯水中存在平衡Cl+H O HClO+H++Cl-,排饱和食盐水时,c(Cl-)增大,平衡逆向移动,Cl 的溶解度
2 2 2
减小,能用勒夏特列原理解释,故B不选;
C.工业上生产硫酸时发生反应2SO +O 2SO ,充入过量的空气平衡正向移动,可以提高 的转化率,
2 2 3
能用勒夏特列原理解释,故C不选;D.加压后2HI(g) H(g)+I (g)不移动,气体颜色变深与平衡移动无关,不能用勒夏特列原理解释,故D
2 2
选;
故选D。
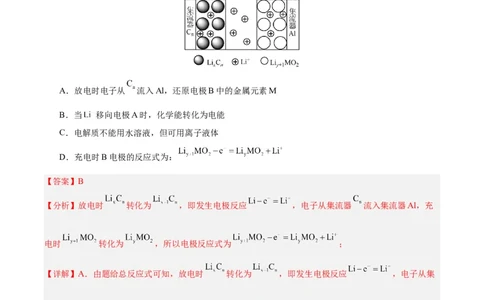
5.某过渡金属(M)—锂离子电池的结构如图所示,总反应式为 ,下
列说法不正确的是
A.放电时电子从 流入Al,还原电极B中的金属元素M
B.当 移向电极A时,化学能转化为电能
C.电解质不能用水溶液,但可用离子液体
D.充电时B电极的反应式为:
【答案】B
【分析】放电时 转化为 ,即发生电极反应 ,电子从集流器 流入集流器Al,充
电时 转化为 ,所以电极反应式为 ;
【详解】A.由题给总反应式可知,放电时 转化为 ,即发生电极反应 ,电子从集
流器 流入集流器Al,发生反应: ,金属元素M被还原,选项A正确;
B.当 移向电极A时,是 转化为 ,由总反应可知是充电过程,是电能转化为化学能,选项
B不正确;
C.因Li能与水发生反应,所以电解质不能用水溶液,可以用常温下呈液态又可以导电的离子液体,选项
C正确;D.由总反应及电池结构可知,充电时 转化为 ,所以电极反应式为
,选项D正确;
答案选B。
6.下列指定反应的离子方程式正确的是
A.碘化亚铁溶液通入少量的氯气:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2
B.用HO 从酸化的海带灰浸出液中制取碘:2I-+H O+2H+=I +2H O
2 2 2 2 2 2
C.Fe(OH) 胶体的制备:Fe3++3NH•H O=Fe(OH) (胶体)+3NH
3 3 2 3
D.等物质的量的NaHCO 溶液与Ca(OH) 溶液混合:2HCO +Ca2++2OH-=CaCO ↓+CO
3 2 3
【答案】B
【详解】A.碘化亚铁溶液通入少量的氯气,只有碘离子被氧化为碘单质, ,A错误;
B.双氧水能将碘离子氧化成碘单质,用HO 从酸化的海带灰浸出液中提取碘: ,
2 2
B正确;
C.制取 红褐色胶体应该向煮沸的蒸馏水中滴加饱和氯化铁溶液至溶液变红褐色;
,C错误;
D.等物质的量的NaHCO 溶液与Ca(OH) 溶液混合,氢氧根离子过量,碳酸氢根离子完全反应生成碳酸
3 2
钙沉淀水:HCO +Ca2++OH-=CaCO ↓+H O,D错误;
3 2
故选B。
7.一种制备乙酸乙酯的实验装置如图所示(夹持装置已略去)。下列说法正确的是A.浓硫酸起到催化剂、吸水剂、脱水剂的作用
B.仪器a的作用是冷凝回流,b中碎瓷片的作用是防暴沸
C.仪器b中加入试剂的顺序是浓硫酸、无水乙醇、冰醋酸
D.反应完全后,可用仪器a、b蒸馏得到产品
【答案】B
【详解】A.酯化反应中浓硫酸的作用是催化剂和吸水剂,故A错误;
B.仪器a是冷凝管,作用是冷凝回流,使乙酸和乙醇能充分反应,b中的碎瓷片可以防止液体爆沸,故B
正确;
C.加入试剂的顺序是先加乙醇,再加浓硫酸,冷却后再加入乙酸,防止加入硫酸放热使液体沸腾造成产
率降低,故C错误;
D.分离乙酸乙酯需要蒸馏,蒸馏要用到蒸馏烧瓶,圆底烧瓶不能蒸馏,故D错误;
答案选B。
8.用下列装置(夹持仪器已略去)进行相关实验,其装置正确且能达到实验目的的是
A.用图甲装置测定醋酸浓度
B.图乙为向容量瓶中转移溶解后放置至室温的液体
C.用图丙装置制备Cl 可达到随用随制的目的
2
D.用图丁装置模拟侯氏制碱法制备NaHCO
3
【答案】B
【详解】A.用图甲装置测定醋酸浓度,应该用酚酞,NaOH溶液应该用碱式滴定管,故A不符合题意;B.固体溶解后放置至室温才能转移到容量瓶中,并用玻璃棒引流,故B符合题意;
C.高锰酸钾易溶于水,因此不能用图丙装置制备Cl,不能达到随用随制的目的,故C不符合题意;
2
D.模拟侯氏制碱法制备NaHCO 时向饱和食盐水中通入过量氨气,再通入二氧化碳反应生成NaHCO ,故
3 3
D不符合题意。
综上所述,答案为B。
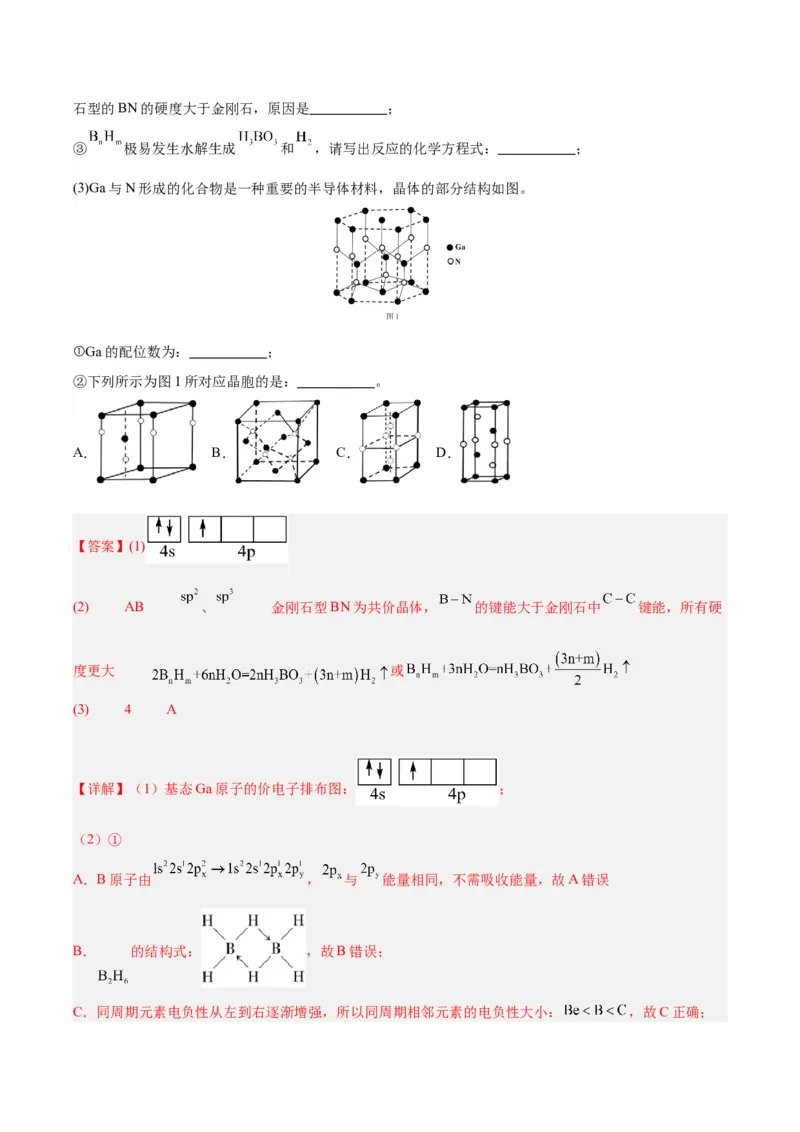
9.氟康唑是一种抗真菌药物,用于治疗真菌感染。其结构如图所示,其中 五元环中所有原子都在
同一个平面上。关于氟康唑的说法正确的是
A.氟康唑分子中所有原子共平面
B.氟康唑分子中有1个手性碳原子
C.氟康唑分子中C原子的杂化方式为sp2、sp3
D.氟康唑分子所有原子都满足8电子稳定结构
【答案】C
【详解】A.氟康唑分子中含有饱和碳原子,所有原子不可能共平面,A错误;
B.氟康唑分子中不存在手性碳原子,B错误;
C.氟康唑分子中环上的C原子的杂化方式为sp2,饱和碳原子是sp3,C正确;
D.氟康唑分子氢原子满足2电子稳定结构,D错误;
答案选C。
10.下列性质的比较,不正确的是
A.电负性: B.热稳定性:
C.酸性: D.第一电离能:
【答案】B
【详解】A. 已知S和Cl是同一周期的元素,同一周期从左往右主族元素的电负性依次增强,则电负性:
,A正确;
B. 已知O和S为同一主族的元素,同一主族从上往下元素的非金属性依次减弱,简单气态氢化物的热稳定性与其非金属性一致,则热稳定性: ,B错误;
C. 已知S和P是同一周期的元素,同一周期从左往右主族元素的非金属性依次增强,则最高价氧化物对应
水化物的酸性与其非金属性一致,则酸性: ,C正确;
D. 已知O和S为同一主族的元素,同一主族从上往下元素的第一电离能依次减小,则第一电离能: ,
D正确;
故答案为:B。
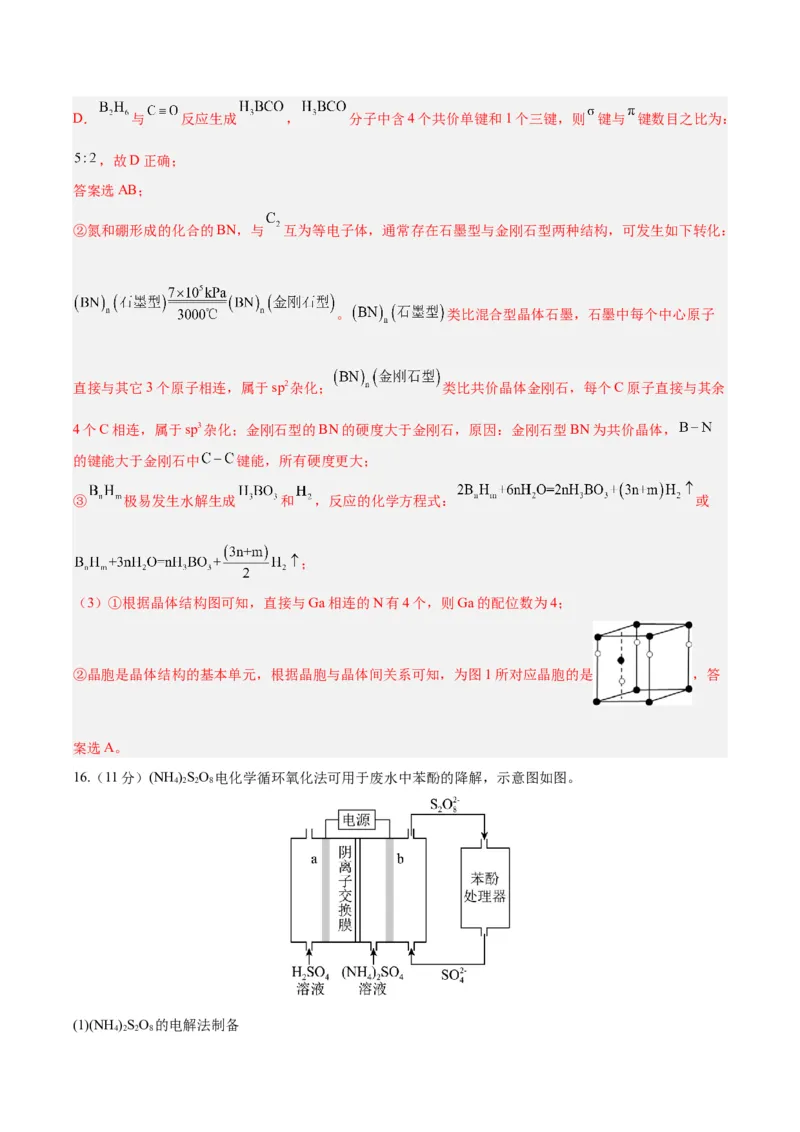
11.下列反应可制备导电高分子化合物:
下列说法错误的是
A.X分子中所有碳原子共平面 B.Y能使酸性高锰酸钾溶液褪色
C.X和Y生成Z的反应为加聚反应 D.X和Y的核磁共振氢谱中,峰的组数相同
【答案】A
【详解】A.饱和碳原子直接相连的原子为四面体结构,故X分子中所有碳原子不会共平面,A错误;
B.Y中含有不饱和碳碳键,能使酸性高锰酸钾溶液褪色,B正确;
C.X和Y生成Z的反应为单体通过加成反应生成高聚物的反应,为加聚反应,C正确;
D.X为对称结构,存在5种氢;Y为不对称结构,存在5种氢;故核磁共振氢谱中,峰的组数相同,D正
确;
故选A。
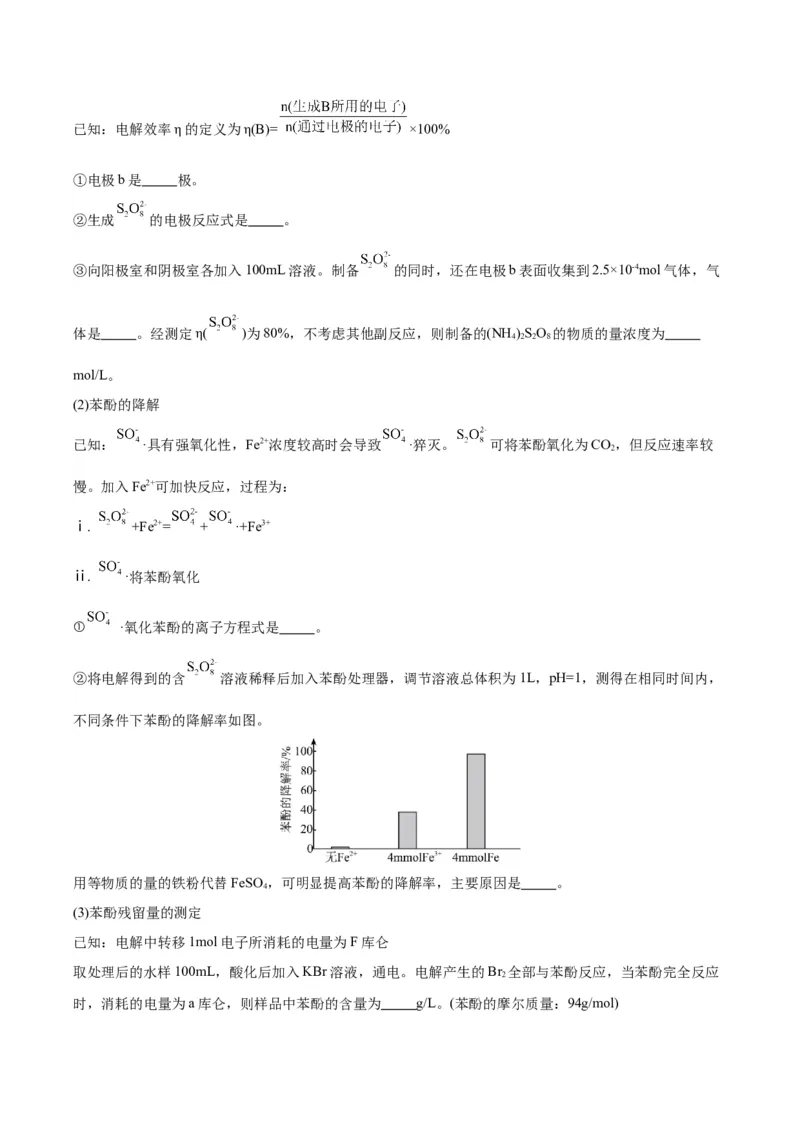
12.油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄
褪色的主要原因是发生了以下两种化学反应:下列说法正确的是
A.反应I和II中,元素 和 都被氧化
B.反应I和II中,氧化 转移的电子数之比为
C. 和 的空间结构都是正四面体形
D.反应I和II中,参加反应的 :I