文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学和生活、科技、社会发展息息相关,下列说法正确的是
A.华为新上市的mate60 pro手机引发关注,其CPU基础材料是SiO
2
B.三星堆黄金面具出土时光亮且薄如纸,说明金不活泼和有很好的延展性
C.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO
D.医用外科口罩使用的材料聚丙烯,能使酸性高锰酸钾溶液褪色
【答案】B
【解析】A.华为新上市的mate60 pro手机引发关注,其CPU基础材料是晶体Si,而不是SiO,A错误;
2
B.三星堆黄金面具是文物,历经年代久远,但出土时光亮且薄如纸,说明金不活泼和有很好的延展性,B
正确;
C.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为Fe O,C 错误;
2 3
D.医用外科口罩使用的材料聚丙烯,聚丙烯分子中无不饱和的碳碳双键,因此不能被酸性高锰酸钾溶液
氧化,因此不能使酸性高锰酸钾溶液褪色,D错误;
故选B。
2.下列化学用语表示正确的是
A.溴的简化电子排布式:
B.1-丁醇的键线式:
C. 形成的 键模型:
D.水的VSEPR模型:
【答案】D
【解析】A.溴位于周期表中第4周期第ⅤⅡA族,核外电子数35,电子排布式为 ,选项
A错误;
B.1-丁醇的键线式为 ,而 为1-丙醇,选项B错误;
C. 形成的 键模型: ,选项C错误;
D.HO中价层电子对个数=2+ =4,且含有2个孤电子对,所以HO的VSEPR模型为四面体
2 2,选项D正确;
故选D。
3.N 为阿伏加德罗常数的值。下列说法不正确的是
A
A.标准状况下,11.2 L NO与11.2 L O 混合后的分子数目为0.75 N
2 A
B.0.1 mol H 和0.1 mol I 于密闭容器中充分反应后,分子总数为0.2 N
2 2 A
C.7.2 g CaO 和CaS的混合物中,含有的阴阳离子总数为0.2 N
2 A
D.向1 L 0.1mol/L盐酸中滴加氨水至中性,溶液中含有的 数目为0.1 N
A
【答案】A
【解析】A.标准状况下,11.2 L NO(物质的量为0.5mol)与11.2 L O(物质的量为0.5mol)混合后反应生成
2
0.5molNO ,还剩余0.25mol O ,由于2NO NO,因此混合后的分子数目小于0.75 N ,且标况下二氧
2 2 2 2 4 A
化氮不是气体,故A错误;
B.H+ I 2HI是等体积反应,0.1 mol H 和0.1 mol I 于密闭容器中充分反应后,分子总数为0.2 N ,故
2 2 2 2 A
B正确;
C.CaO 含有一个钙离子和过氧根离子,CaO 和CaS的摩尔质量相同,阴阳离子数目相同,因此7.2 g
2 2
CaO 和CaS(物质的量为0.1mol)的混合物中,含有的阴阳离子总数为0.2 N ,故C正确;
2 A
D.向1 L 0.1mol/L盐酸中滴加氨水至中性,氯化铵物质的量为0.1mol,根据电荷守恒和呈中性,的溶液中
的铵根离子数目等于氯离子数目,因此溶液中含有的 数目为0.1 N ,故D正确;
A
故选A。
4.下列离子方程式书写正确的是
A.向 溶液中通入过量 :
B.CuO溶于 溶液:
C.向 溶液中通入 :
D.Fe与稀硝酸反应,当 时:
【答案】D
【解析】A.向 溶液中通入过量 生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为
,故A错误;
B.CuO溶于 溶液生成硫酸钠、硫酸铜、水,反应的离子方程式为 ,故B
错误;
C.向 溶液中通入 ,二氧化硫被氧化为硫酸根离子,硝酸根被还原为NO,反应的离子方程式为
,故C错误;
D.Fe与稀硝酸反应,当 时:设参加反应的铁共1mol,xmolFe被氧化为Fe3+、(1-
x)molFe被氧化为Fe2+,根据得失电子守恒、电荷守恒,被还原的硝酸为 ,表现酸性的硝
酸为 , ,解得x=0.25mol,即氧化生成Fe3+、Fe2+的比为1:3,所以反应方程式为 ,故D正确;
故选D。
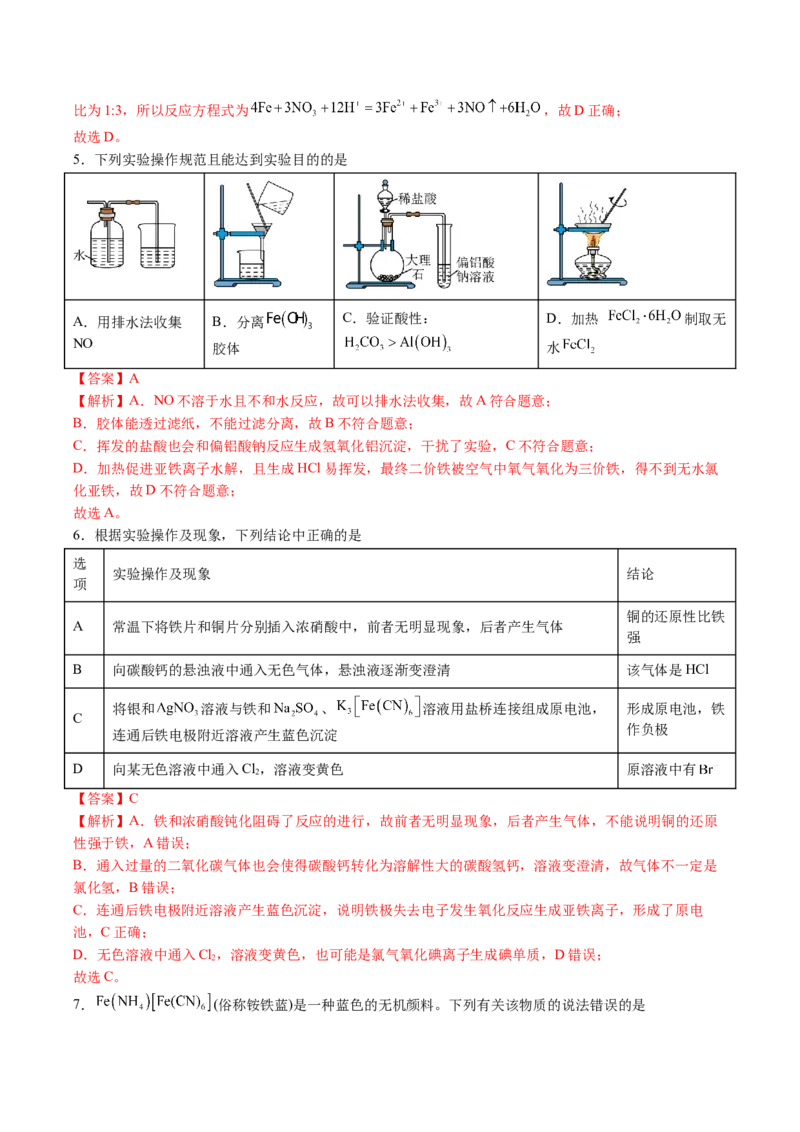
5.下列实验操作规范且能达到实验目的的是
A.用排水法收集 B.分离 C.验证酸性: D.加热 制取无
NO 胶体 水
【答案】A
【解析】A.NO不溶于水且不和水反应,故可以排水法收集,故A符合题意;
B.胶体能透过滤纸,不能过滤分离,故B不符合题意;
C.挥发的盐酸也会和偏铝酸钠反应生成氢氧化铝沉淀,干扰了实验,C不符合题意;
D.加热促进亚铁离子水解,且生成HCl易挥发,最终二价铁被空气中氧气氧化为三价铁,得不到无水氯
化亚铁,故D不符合题意;
故选A。
6.根据实验操作及现象,下列结论中正确的是
选
实验操作及现象 结论
项
铜的还原性比铁
A 常温下将铁片和铜片分别插入浓硝酸中,前者无明显现象,后者产生气体
强
B 向碳酸钙的悬浊液中通入无色气体,悬浊液逐渐变澄清 该气体是HCl
将银和 溶液与铁和 、 溶液用盐桥连接组成原电池, 形成原电池,铁
C
作负极
连通后铁电极附近溶液产生蓝色沉淀
D 向某无色溶液中通入Cl,溶液变黄色 原溶液中有
2
【答案】C
【解析】A.铁和浓硝酸钝化阻碍了反应的进行,故前者无明显现象,后者产生气体,不能说明铜的还原
性强于铁,A错误;
B.通入过量的二氧化碳气体也会使得碳酸钙转化为溶解性大的碳酸氢钙,溶液变澄清,故气体不一定是
氯化氢,B错误;
C.连通后铁电极附近溶液产生蓝色沉淀,说明铁极失去电子发生氧化反应生成亚铁离子,形成了原电
池,C正确;
D.无色溶液中通入Cl,溶液变黄色,也可能是氯气氧化碘离子生成碘单质,D错误;
2
故选C。
7. (俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该物质的说法错误的是A.电负性:
B.铵铁蓝中铁元素有两种化合价
C. 中 的键角比 中的 的键角大
D.铵铁蓝中的配体是 ,该配体中 键与 键的数目之比是
【答案】D
【解析】A.同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则电负性: ,故
A正确;
B.由化合物中正、负化合价的代数和为0可知,铵铁蓝中铁元素有 和 两种化合价,故B正确;
C.根据价层电子对互斥理论可知, 的空间结构为正四面体形, 的空间结构为三角锥形,
中 的键角比 中的 的键角大,故C正确;
D. 中C和N之间是三键,与氮气互为等电子体,1个 中有1个 键和2个 键,则该配体中 键
与 键的数目之比是 ,故D错误。
故选D。
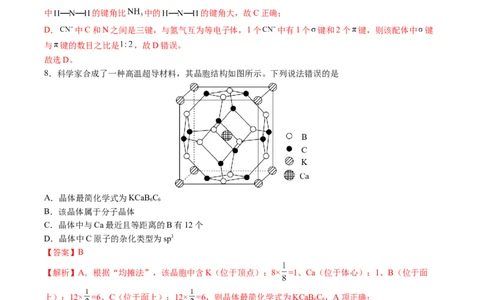
8.科学家合成了一种高温超导材料,其晶胞结构如图所示。下列说法错误的是
A.晶体最简化学式为KCaB C
6 6
B.该晶体属于分子晶体
C.晶体中与Ca最近且等距离的B有12个
D.晶体中C原子的杂化类型为sp3
【答案】B
【解析】A.根据“均摊法”,该晶胞中含K(位于顶点):8× =1、Ca(位于体心):1、B(位于面
上):12× =6、C(位于面上):12× =6,则晶体最简化学式为KCaB C ,A项正确;
6 6
B.该晶体是一种高温超导材料,该晶体不可能属于分子晶体,B项错误;
C.由晶胞结构可知,Ca位于体心,B位于面上,晶体中与Ca最近等距离的B有12个,C项正确;
D.C位于面上,结合晶胞结构知,C的价层电子对数为4,C原子采取sp3杂化,D项正确;
故选B。
9.7-羟基香豆素是香豆素家族的天然产物,是一种荧光化合物,可用作防晒剂和药物;它的结构简式如图
所示。下列说法错误的是A.分子式为C HO
9 6 3
B.该物质的官能团是碳碳双键、羟基、酯基
C.1mol该物质与足量H 反应,最多消耗4molH
2 2
D.该物质不能发生取代反应
【答案】D
【解析】A.观察其结构简式知,一分子含9个C,6个H,3个O,故分子式为C HO,A不符合题意;
9 6 3
B.观察其结构简式知,该物质的官能团是碳碳双键、羟基、酯基,B不符合题意;
C.7-羟基香豆素结构中含一个苯环、一个碳碳双键,分别可与三分子氢气、一分子氢气发生加成反应,
故1mol该物质与足量H 反应时最多消耗4molH ,C不符合题意;
2 2
D.由于含酚羟基,可与浓溴水发生取代反应;所含的酯基可以发生水解反应,也属于取代反应,D符合
题意;
故选D。
10.在直流电源作用下,双极膜中间层中的 解离为 和 。某技术人员利用双极膜(膜c、膜d)电
解技术从含葡萄糖酸钠(用GCOONa表示)的溶液中提取NaOH和葡萄糖酸(GCOOH),工作原理如图所示。
下列说法错误的是
A.M为阴极
B.③室和④室所得产物相同
C.膜a为阳离子交换膜,膜b为阴离子交换膜
D.N极电极反应式为
【答案】B
【分析】在直流电源作用下高效制备HSO 和NaOH由图可知,M极为阴极,电极反应式为2HO+2e-
2 4 2
=H ↑+2OH-,左侧葡萄糖酸钠溶液中钠离子透过膜a向左侧迁移,葡萄糖酸根离子透过膜b向右侧迁移,
2
故膜a为阳离子交换膜,膜b为阴离子交换膜,水解离出的氢离子经过膜c向左侧迁移,膜c为阳离子交
换膜,N极为阳极,电极反应式为2HO-4e-=O ↑+4H+,右侧葡萄糖酸钠溶液中葡萄糖酸根离子透过膜f向
2 2
右侧迁移,钠离子透过膜e向左侧迁移,故膜e为阳离子交换膜,膜f为阴离子交换膜,水解离出的氢氧
根离子经过膜d向右侧迁移,膜d为阴离子交换膜;
【解析】A.根据分析可知,M极为阴极,选项A正确;
B.葡萄糖酸根离子透过膜b向右侧迁移,水解离出的氢离子经过膜c向左侧迁移,③室产生葡萄糖酸;钠
离子透过膜e向左侧迁移,水解离出的氢氧根离子经过膜d向右侧迁移,④室产生氢氧化钠,两室产物不
相同,选项B错误;
C.左侧葡萄糖酸钠溶液中钠离子透过膜a向左侧迁移,葡萄糖酸根离子透过膜b向右侧迁移,故膜a为阳
离子交换膜,膜b为阴离子交换膜,选项C正确;D.N极为阳极,电极反应式为2HO-4e-=O ↑+4H+,选项D正确;
2 2
故选B。
11.离子液体常用作有机合成的溶剂和催化剂,在生物、化学等多领域都有广泛的应用。大多数的离子液
体含有体积很大的阴、阳离子。某离子液体的结构如下图。其中X、Y、Z、W、E、Q均为短周期主族非
金属元素,且原子序数依次增大。下列说法错误的是
A.YQ 是一种直线形分子
2
B.氢化物的沸点:E>W>Y
C.化合物ZX 的水溶液显碱性
2 4
D.简单离子的半径:Q>Z>W>E
【答案】B
【分析】由题干信息可知,X、Y、Z、W、E、Q均为短周期主族非金属元素,且原子序数依次增大,结
合题干离子液体的结构中X、E均只形成1个共价键,Y周围形成4个共价键,Z形成3个共价键,W形成
2个共价键,Q形成6个共价键,故可推知X为H,Y为C,Z为N,W为O,E为F,Q为S,据此分析解
题。
【解析】A.由分析可知,Y为C,Q为S,YQ 即CS,其中心S原子周围的价层电子对数为:2+
2 2
=2,故CS 是一种直线形分子,A正确;
2
B.由分析可知,Y为C,W为O,E为F,由于碳的氢化物有很多,且沸点相差很大,故无法比较碳的氢
化物与其他两种氢化物的沸点,B错误;
C.由分析可知,Z为N,X为H,化合物ZX 即NH 的水溶液显碱性,其原理为:NH+H O
2 4 2 4 2 4 2
NH·H O +OH-,C正确;
2 4 2
D.由分析可知,Q为S,Z为N,W为O,E为F,其中S2-比其他离子多一个电子层,其他三种离子具有
相同的核外电子排布,且核电荷数为F>O>N,故简单离子的半径大小为:S2->N3->O2->F-,D正确;
故选B。
12.利用含镍电极废料制备 的过程可表示为:
已知:①含镍电极废料中除 外还含有少量 , 和不溶性杂质
②“酸浸”后溶液中含有 和少量的 和 ,除杂后方可氧化下列说法错误的是
A.由工业流程可知: 的氧化性大于
B.氧化过程的离子方程式:
C.除杂过程中利用了 、 和 的溶度积的不同通过调节 后过滤
D.利用电解碱性 悬浊液也可以制备 ,为提高电解效率可以适当加入一定量 溶液
【答案】B
【分析】含镍电极废料(除Ni外还含有少量Al O,Fe O 和不溶性杂质)中加稀硫酸酸浸,“酸浸”后溶液
2 3 2 3
中含有Ni2+和少量的Al3+和Fe2+,调节pH,将Al3+和Fe2+转化为沉淀过滤除去,除杂后加KClO溶液将
Ni2+氧化为NiOOH,据此分析解答。
【解析】A.“酸浸”时发生反应: ,则氧化性: ,A项正确;
B. 经过 的氧化,得到 ,反应的离子方程式为
,B项错误;
C.除杂过程包括:调节 ,将 和 转化为沉淀,再过滤除去不溶性杂质,利用了 、
和 的溶度积的不同,C项正确;
D.电解碱性 悬浊液制备 ,阳极反应为: ,若加入
一定量的 ,氯离子在阳极上失电子生成氯气,氯气在碱性条件下生成 , 将 氧化为
,有助于提高生产效率,D项正确;
故选B。
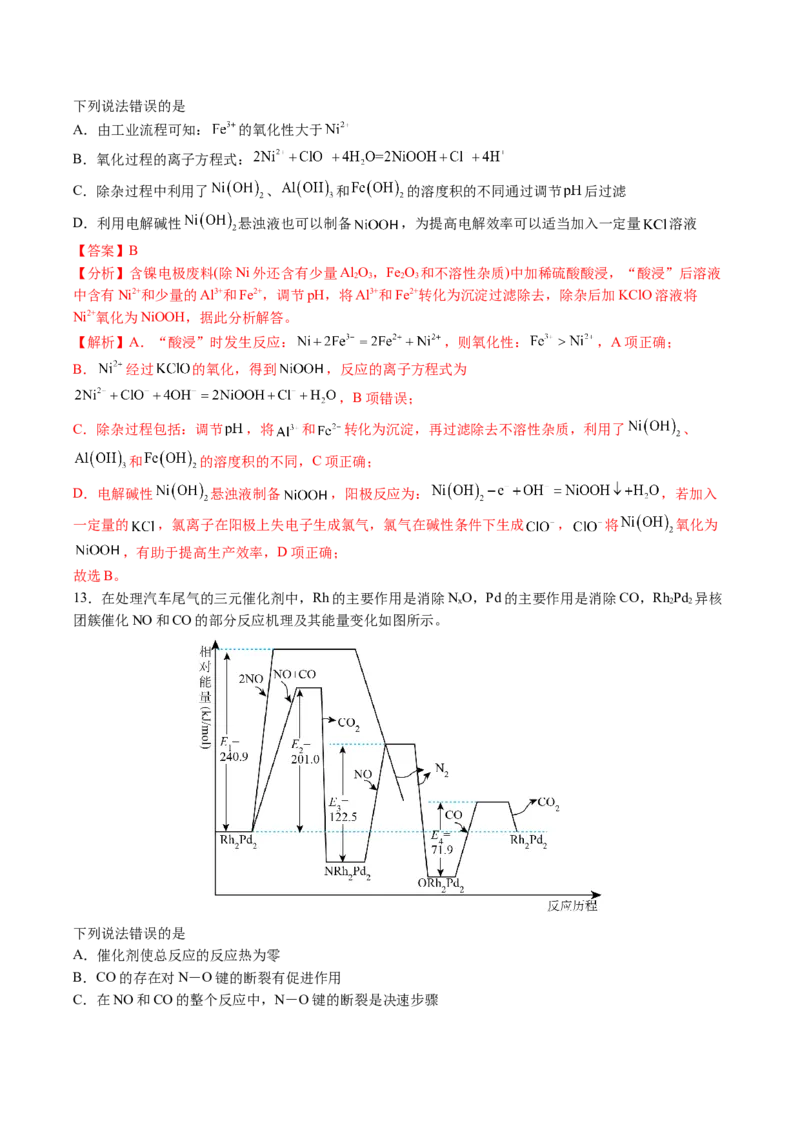
13.在处理汽车尾气的三元催化剂中,Rh的主要作用是消除NO,Pd的主要作用是消除CO,Rh Pd 异核
x 2 2
团簇催化NO和CO的部分反应机理及其能量变化如图所示。
下列说法错误的是
A.催化剂使总反应的反应热为零
B.CO的存在对N-O键的断裂有促进作用
C.在NO和CO的整个反应中,N-O键的断裂是决速步骤D.催化反应方程式为2CO+2NO 2CO+N
2 2
【答案】A
【解析】A.催化剂不能够改变反应的焓变,A错误;
B.图像分析可知,CO存在,N-O断裂化学键吸收能量降低,CO的存在对N-O键的断裂有促进作用,B
正确;
C.N-O键的断裂需要的能量最高,反应速率最慢,在NO和CO的整个反应中,N-O键的断裂是决速步
骤,C正确;
D.图像分析可知催化反应的总反应为一氧化氮和一氧化碳反应生成氮气和二氧化碳,反应的化学方程式
为:2CO+2NO 2CO+N ,D正确;
2 2
故选A。
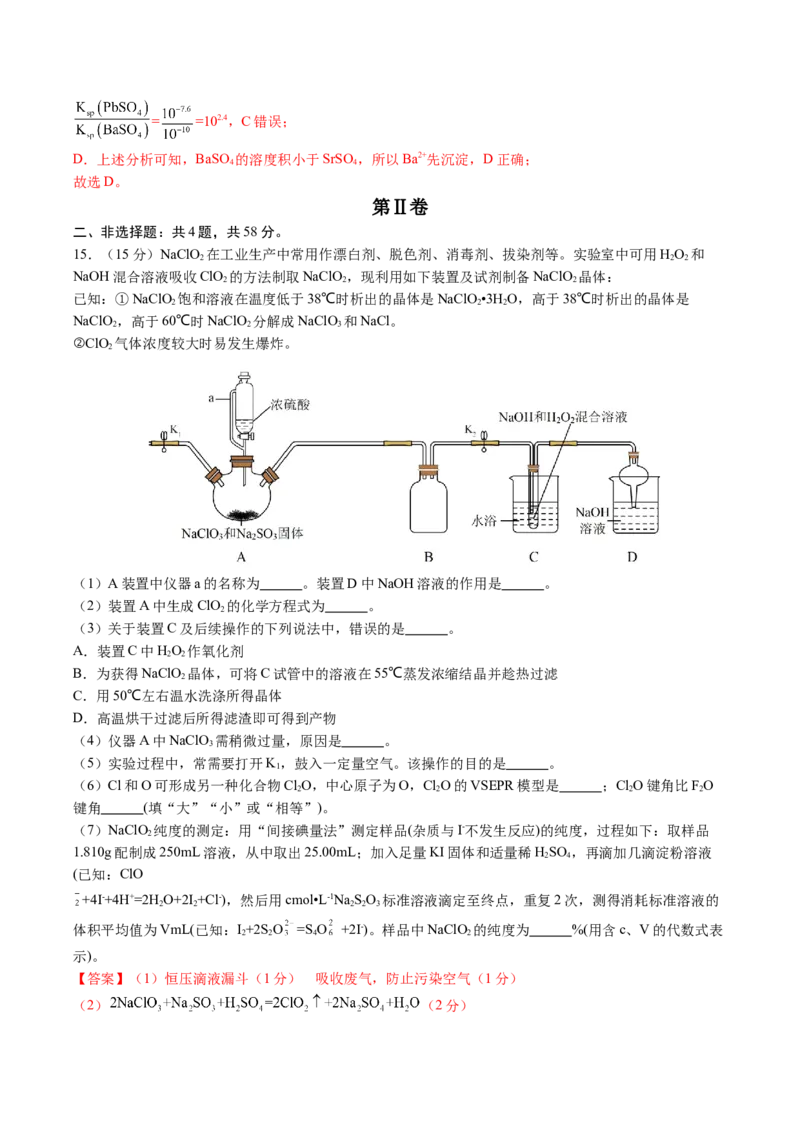
14.T℃下,三种硫酸盐 (M表示 或 或 )的沉淀溶解平衡曲线如图所示。已知
, 。下列说法正确的是
A. 在任何条件下都不可能转化为
B.X点和Z点分别是 和 的饱和溶液,对应的溶液中
C.T℃下,反应 的平衡常数为
D.T℃时,用 溶液滴定 浓度均为 和 的混合溶
液, 先沉淀
【答案】D
【分析】已知 , ,结合C、B、A点数据,则K (BaSO)=
sp 4
c(Ba2+)c(SO )=10-10,K (PbSO )= c(Pb2+)·c(SO )=10-7.6,K (SrSO )= c(Sr2+)·c(SO )=10-6.4。
sp 4 sp 4
【解析】A.因SrSO 、PbSO 、BaSO 为同类型沉淀,再结合题图可知,
4 4 4
K (BaSO)