文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷02
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 I 127 Cs 133 Pb 207
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与生活生产密切相关。下列说法错误的是
A.葡萄酒中添加的 既可杀菌,又可防止营养成分被氧化
B.加酶洗衣粉不宜洗涤真丝织品,会使真丝中的蛋白质变性
C.常见无机含氯消毒剂有氯气、次氯酸盐、 等
D.不锈钢是一种含合金元素 和 的合金钢
【答案】B
【解析】A.SO 可以抑制细菌生长,也具有还原性,在葡萄酒中可以杀菌,也可用于防氧化,A正确;
2
B.真丝织品的主要成分是蛋白质,加酶洗衣粉不宜洗涤真丝织品,是因为酶使真丝中的蛋白质水解,B
错误;C.常见无机含氯消毒剂有氯气、次氯酸盐、 ClO D.不锈钢主要含有Fe、Cr、Ni和少量
2 等,C正确;
的碳,D正确;故选B。
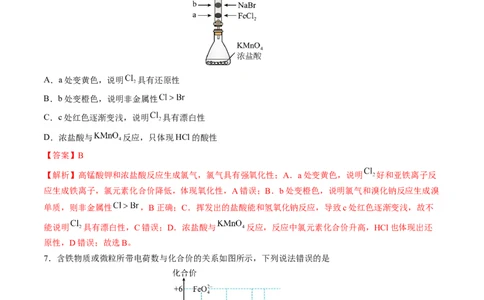
2.学习小组用废弃的铝制易拉罐按如下流程制备明矾,并测定明矾中结晶水的含量。
上述实验中不需要用到的操作是
A. B. C. D.
【答案】D
【解析】废弃的铝制易拉罐加入氢氧化钾碱溶后分液得到滤液,然后加入稀硫酸调节pH得到硫酸铝钾溶
液,然后经过一系列操作得到明矾晶体;A.溶液Ⅱ得到明矾晶体需要蒸发浓缩操作,故A不符合题意;
B.测定明矾中结晶水的含量,故实验中需要灼烧操作,故B不符合题意;C.加入氢氧化钾溶解铝后需要
过氯分离出滤液,故C不符合题意;D.实验中不需要萃取分液操作,不用分液漏斗,,故D符合题意;
故选D。
3.元素及其化合物在化工生产中有着重要的用途.下列说法正确的是
A.工业上以二氧化硅为原料制备高纯硅,还需要用到焦炭、氢气、氯化氢等原料
B.工业上制硫酸是用98.3%的硫酸吸收二氧化硫
C.工业上生产玻璃和水泥时均使用纯碱和石灰石作为原料
D.工业上制取钠单质普遍采用电解熔融的氢氧化钠【答案】A
【解析】A.工业上以二氧化硅为原料制备高纯硅,用焦炭还原二氧化硅得到粗硅,粗硅用氯气反应得到
四氯化硅与杂质分离,再用氢气还原四氯化硅得到高纯度硅单质,需要用到焦炭、氢气、氯气等原料,A
正确;B.工业上制硫酸是用98.3%的浓硫酸吸收三氧化硫,B错误;C.水泥的原料是粘土和石灰石,玻
璃的原料是纯碱、石灰石和石英,所以工业上生产玻璃和水泥时均使用的原料中均有石灰石,C错误;
D.工业上制取钠单质普遍采用电解熔融的氯化钠,氢氧化钠的成本较高,不适合工业生产, D错误;故
本题选A。
4.设 为阿伏伽德罗常数的值。下列说法正确的是
A.7.8g 中所含阴离子数为
B.1mol 完全反应制成胶体后,其中含有氢氧化铁胶粒数为
C.1mol 和3mol 在一定条件下充分反应生成的 分子数为
D.常温下pH=2的醋酸溶液中含有的氢离子数为
【答案】A
【解析】A. 中含有 和 ,7.8g 物质的量为0.1mol,则阴离子数为 ,A正确;B.
1mol 完全反应制成胶体后,其中含有氢氧化铁胶粒数小于 ,B错误;C.反应为可逆反应,生成
的 分子数小于 ,C错误;D.题没有给出醋酸溶液的体积,无法算出氢离子数,D错误;故选
A。
5.已知在有机化合物中,吸电子基团(吸引电子云密度靠近)能力:
,推电子基团(排斥电子云密度偏离)能力:
,一般来说,体系越缺电子,酸性越强;体系越富电子,
碱性越强。下列说法错误的是
A.碳原子杂化轨道中s成分占比:
B.羟基的活性:
C.酸性:
D.碱性:
【答案】D
【详解】A.碳碳三键中C原子杂化方式为sp杂化,碳碳双键中C原子杂化方式为sp2杂化,故碳原子杂
化轨道中s成分占比: ,A正确;
B.苯环为吸电子基团,乙基为推电子基团,故羟基的活性:苯甲醇>乙醇,B正确;C.吸电子能力Cl>Br,故酸性 ,C正确;
D.甲基为推电子基团,故 中六元环的电子云密度大,碱性强,D错误;
故选D。
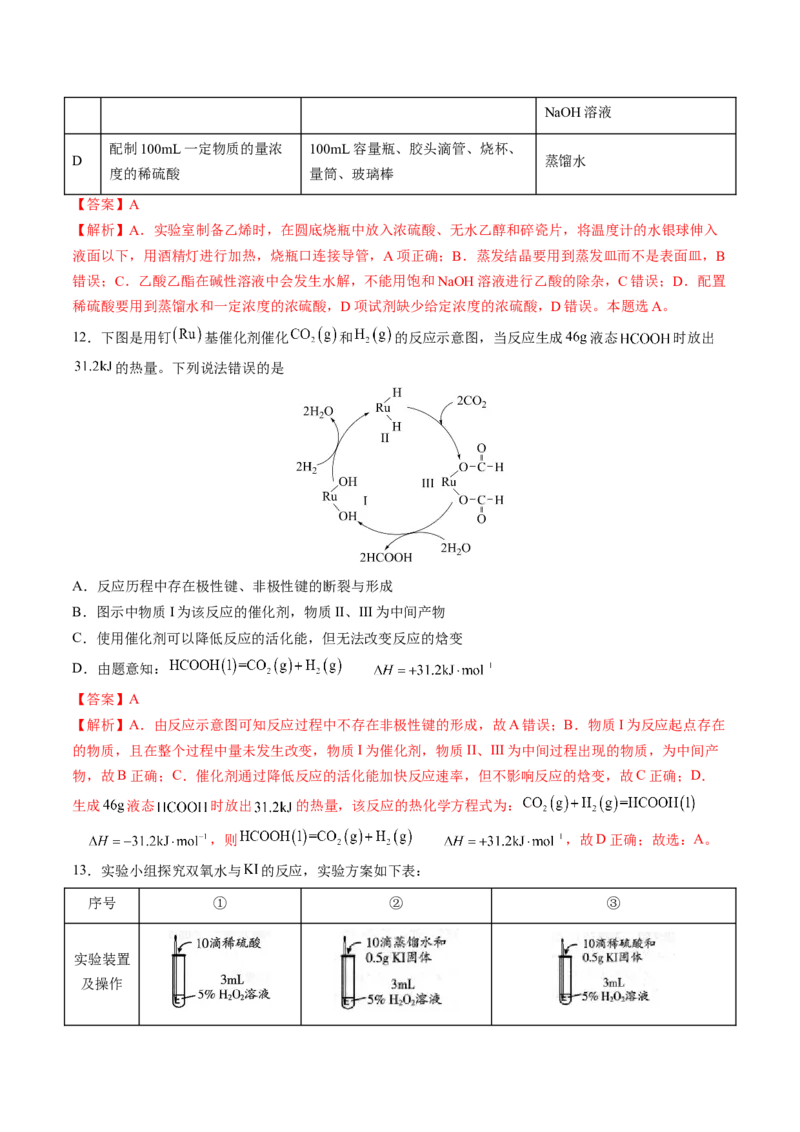
6.将浓盐酸加到 中进行如图(a~c均为浸有相应试液的棉花)所示的探究实验,反应一段时间后,
下列分析正确的是
A.a处变黄色,说明 具有还原性
B.b处变橙色,说明非金属性
C.c处红色逐渐变浅,说明 具有漂白性
D.浓盐酸与 反应,只体现HCl的酸性
【答案】B
【解析】高锰酸钾和浓盐酸反应生成氯气,氯气具有强氧化性;A.a处变黄色,说明 好和亚铁离子反
应生成铁离子,氯元素化合价降低,体现氧化性,A错误;B.b处变橙色,说明氯气和溴化钠反应生成溴
单质,则非金属性 ,B正确;C.挥发出的盐酸能和氢氧化钠反应,导致c处红色逐渐变浅,故不
能说明 具有漂白性,C错误;D.浓盐酸与 反应,反应中氯元素化合价升高,HCl也体现出还
原性,D错误;故选B。
7.含铁物质或微粒所带电荷数与化合价的关系如图所示,下列说法错误的是
A.M可能是
B.R为铁单质,常温下遇浓硫酸发生钝化
C.N可用 溶液检验D. 与强氧化剂在碱性条件下反应可以生成
【答案】C
【解析】A.M中Fe元素为+2价,且电荷数为0,可能是 ,故A正确;B.R中Fe元素为0价,
且电荷数为0,为Fe单质,铁单质在常温下遇浓硫酸发生钝化,故B正确;C.N中Fe元素为+2价,且电
荷数为+2,为Fe2+,Fe2+不能用 溶液检验,故C错误;D. 中Fe元素为+6价,据图可知
在碱性环境中稳定存在,所以Fe3+与氧化剂在碱性条件下反应可生成 ,故D正确;故选C。
8.某抗氧化剂Z可由图中反应制得:
下列关于化合物X、Y、Z的说法正确的是
A.化合物Z中采用 杂化和 杂化的碳原子个数比为3∶5
B.化合物Y中含有3个手性碳原子
C.化合物X可使溴水褪色,1molX最多可消耗
D.化合物Z中第一电离能最大的元素为氧元素
【答案】A
【解析】A.根据有机物Z的结构简式可知,采用 杂化的碳原子有6个,采用 杂化的碳原子有10个,
因此二者比为3∶5,A正确;B.连有四个不同基团的碳原子为手性碳原子,化合物Y中含有一个手性碳
原子,B错误;C.化合物X中,酚羟基的两个邻位碳可以与两个 发生取代反应,碳碳双键可以与一个
发生加成,因此1molX最多可消耗 ,C错误;D.同周期从左向右,元素的第一电离能逐渐增
大,但N>O,因此化合物Z中第一电离能最大的元素为氮元素,D错误。本题选A。
9.短周期主族元素Q、X、Y、Z质子数之和为37,Q与X、Y、Z位于不同周期,Q与Z位于同一主族。
X、Y、Z最外层电子数分别为x、y、z,且依次增大,x、y、z之和为15, 。下列说法正确的是
A.Q是原子半径最小的元素
B.最高正价含氧酸的酸性:
C. 分子中各原子最外层达到8电子结构
D.Z的氢化物不可能含有非极性共价键
【答案】C
【解析】由题意,x、y、z之和为15, ,可推知y=5,x=3或4,z=7或6,又由Q、X、Y、Z质子
数之和为37,Q与X、Y、Z位于不同周期,Q与Z位于同一主族,可推出X为C,Y为N,Z为O,Q为
S。A.根据元素周期律,同周期元素,原子序数越大,原子半径越小;同主族元素,原子序数越大,原子
半径越大,得Z是原子半径最小的元素,故A错误;B.同周期元素的非金属性随原子序数增大而递增,元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,非金属性XI (As)>I (Se)的原因是___________。
1 1 1 1
(3)三氟乙脒的结构如图所示,其中σ键 与π键数目之比为___________, 碳原子的杂化类型为
___________; 测量HF相对分子质量测量值经常偏大的原因是___________。
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长a pm,则该物质的化学式为
___________; 晶体中Pb2+与Cs+最短距离为___________ pm; 晶体的密度ρ=___________ g · cm-3(设阿伏
加德罗常数的值为N ,用含a、N 的代数式表示;可能用到相对原子质量: Cs: 133 Pb: 207 I:
A A
127)
【答案】(除标明外,每空2分)
(1)7(1分) 6s26p2(1分)
(2)As、Se和Br为同周期元素,同周期元素从左至右,第一电离能呈现增大的趋势;但由于基态As原
子的p能级轨道处于半充满状态,能量更低更稳定,故其第一电离能大于Se的
(3)9:1(1分) sp2和sp3(1分) HF分子间存在氢键,形成缔合分子(HF) 导致HF相对分子质量
n
测量值偏大
(4)CsPbI (1分) (1分)
3
【解析】(1)基态碘原子的核外电子排布为: ,价层电子的运动状态
有7种;基态Pb原子的价层电子排布式为6s26p2,故答案为:7;6s26p2;
(2)同周期元素从左至右,第一电离能呈现增大的趋势,As、Se和Br为同周期元素,核电荷数依次增加,
第一电离能呈增大趋势,但由于基态As原子的p能级轨道处于半充满状态,能量更低更稳定,故其第一电
离能大于Se,故答案为:As、Se和Br为同周期元素,同周期元素从左至右,第一电离能呈现增大的趋势;
但由于基态As原子的p能级轨道处于半充满状态,能量更低更稳定,故其第一电离能大于Se;
(3)由结构简式可知该物质中含9个σ键 与1个π键,个数比为9:1;其中单键碳原子采用sp2杂化,双
键碳原子采用sp3杂化;HF分子间存在氢键,易形成缔合分子(HF) 导致HF相对分子质量测量值偏大,故
n
答案为:9:1;sp2和sp3;HF分子间存在氢键,形成缔合分子(HF) 导致HF相对分子质量测量值偏大;
n
(4)Cs+有8个位于顶点个数为: ;I-有6个位于面心,个数为: ,Pb2+有1个位于体心,则该晶胞的化学式:CsPbI ,晶体中Pb2+与Cs+最短距离为体对角线的一半,即为 pm;晶胞质量为:
3
,晶胞体积为: ,则晶胞密度为: ,故答案为:CsPbI ; ;
3
。
17.(12分)硼氢化钠 在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为
,含少量杂质 )制取 ,其工艺流程如下:
已知:硼氢化钠 常温下能与水反应,易溶于异丙胺(沸点为 )。
(1) 和 都是硼酸盐,请写出一元弱酸硼酸 在水中的电离方程式
_______。
(2)粉碎的目的是_______;滤渣的成分是_______(写化学式、下同)。
(3)操作1的步骤是____、冷却结晶;操作2、操作3的名称分别为_____、_______。
(4)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是_______。
(5)流程中可循环利用的物质是_______。写出副产物硅酸钠的一种用途_______。
(6) 被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含
氢还原剂的还原能力相当于多少克 的还原能力。 的有效氢含量为_____(保留两位小数)。
【答案】(除标明外,每空2分)
(1)
(2)增大硼镁矿与碱液的接触面积,提高浸取率(或提高原料的利用率)和加快反应速率(或者使反应更快
更充分) 和
(3)蒸发浓缩(1分) 过滤(1分) 蒸馏(1分)
(4)除去反应器中的空气,防止空气中的水、氧气与原料钠、氢气反应(1分)
(5)异丙胺(1分) 可做防火剂或黏合剂(1分)
(6)0.21
【解析】硼镁矿粉碎后加入氢氧化钠碱溶,氢氧化钠和四氧化三铁不反应、和镁离子生成氢氧化镁沉淀,得到滤渣 和 ,滤液中含硼,为蒸发浓缩、冷却结晶得到 ,脱水后高温合成
得到 、 ,加入异丙胺提取出 ,蒸馏分离出取异丙胺得到 ;
(1)一元弱酸硼酸 在水溶液中部分电离, ;
(2)粉碎的目的是增大硼镁矿与碱液的接触面积,提高浸取率(或提高原料的利用率)和加快反应速率(或
者使反应更快更充分);氢氧化钠和四氧化三铁不反应、和镁离子生成氢氧化镁沉淀,故滤渣的成分是
和 ;
(3)操作1从溶液中得到晶体,则操作为蒸发浓缩、冷却结晶;操作2为分离固液的操作,是过滤;硼氢
化钠 常易溶于异丙胺(沸点为 ),操作3为从硼氢化钠的异丙胺溶液中得到硼氢化钠的操作,
为蒸馏;
(4)钠、氢气均可与空气中氧气反应,高温合成过程中,加料之前需先在反应器中通入氩气,该操作的
目的是除去反应器中的空气,防止空气中的水、氧气与原料钠、氢气反应;
(5)操作3蒸馏出的异丙胺,可以在操作2中重复使用,故流程中可循环利用的物质是异丙胺。副产物硅
酸钠可做防火剂或黏合剂等;
(6) 中氢元素化合价为-1,可以失去电子变为+1;氢气中氢失去电子变为+1,根据电子守恒可知,
,则有效氢含量为 。
18.(12分)20℃下,制作网红“天气瓶”流程如下,请根据下述制作流程,结合下列信息和所学知识,
回答问题:
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
硝酸钾溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
氯化铵溶解度/g 29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3
樟脑( )是一种白色晶体,易溶于酒精、难溶于水。
(1)樟脑难溶于水,易溶于酒精的原因主要是___________________。
(2)由硝酸钾、氯化铵制备得到“溶液b”的过程中需要用到的玻璃仪器有__________________________。
得到“溶液c”时需控制温度50℃,可采取的方法是_______________。
(3)实验中发现硝酸钾溶解速率很慢,请推测原因________________________。
(4)温度改变,天气瓶内或清澈干净,或浑浊朦胧,或产生大片美丽的结晶。请通过计算说明0℃时出现的是樟脑晶体_________________,推测晶体产生的原因________。
(5)从晶体生长析出的角度分析,“天气瓶”制作中硝酸钾和氯化铵的作用是______________。
【答案】(除标明外,每空2分)
(1)水分子极性较强,而樟脑和乙醇均为弱极性分子
(2)烧杯、玻璃棒、量筒 水浴加热(1分)
(3)氯化铵在溶液的水解反应为吸热反应,溶液温度降低(1分)
(4)0℃时硝酸钾溶解度为13.3g,氯化铵29.4g,33g溶剂水能溶解硝酸钾4.4g,氯化铵9.7g 樟脑在酒
精中的溶解度随温度升高而增大,溶解速率随温度降低而减小
(5)控制樟脑晶体高速生长过程中的连续成核(或:减缓樟脑晶体的生长速度),便于得到较大晶体
【解析】(1)水分子极性较强,而樟脑和乙醇均为弱极性分子,由相似相溶原理可知,樟脑难溶于水,
易溶于酒精,故答案为:水分子极性较强,而樟脑和乙醇均为弱极性分子;
(2)由硝酸钾、氯化铵制备得到“溶液b”的过程为固体溶解的过程,溶解时需要用到的玻璃仪器为烧杯、
玻璃棒、量筒;得到“溶液c”时的控制温度小于100℃,所以采取的加热方式为水浴加热,故答案为:烧
杯、玻璃棒、量筒;水浴加热;
(3)由表格数据可知,硝酸钾在温度较低时,溶解度小,氯化铵是强酸弱碱盐,在溶液中的水解反应为
吸热反应,所以氯化铵溶解时吸收热量,使溶液温度降低导致硝酸钾溶解速率很慢,故答案为:氯化铵在
溶液的水解反应为吸热反应,溶液温度降低;
(4)由表格数据可知,0℃时33g水溶解硝酸钾、氯化铵的质量分别为 ≈4.4g、
≈9.7g,硝酸钾和氯化铵在溶液中能够溶解的最大质量均大于2.5g,所以0℃时出现的晶体是樟脑晶体,不
可能是硝酸钾和氯化铵;0℃时出现樟脑晶体说明樟脑在酒精中的溶解度随温度升高而增大,导致溶解速
率随温度降低而减小,故答案为:0℃时硝酸钾溶解度为13.3g,氯化铵29.4g,33g溶剂水能溶解硝酸钾
4.4g,氯化铵9.7g;樟脑在酒精中的溶解度随温度升高而增大,溶解速率随温度降低而减小;
(5)从晶体生长析出的角度可知,“天气瓶”制作中硝酸钾和氯化铵的作用是控制樟脑晶体高速生长过
程中的连续成核,减缓樟脑晶体的生长速度,便于得到较大晶体,故答案为:控制樟脑晶体高速生长过程
中的连续成核(或:减缓樟脑晶体的生长速度),便于得到较大晶体。
19.(12分)茚三酮能与任何含α一氨基的物质形成深蓝色或红色物质,可用于鉴定氨基酸、蛋白质、多
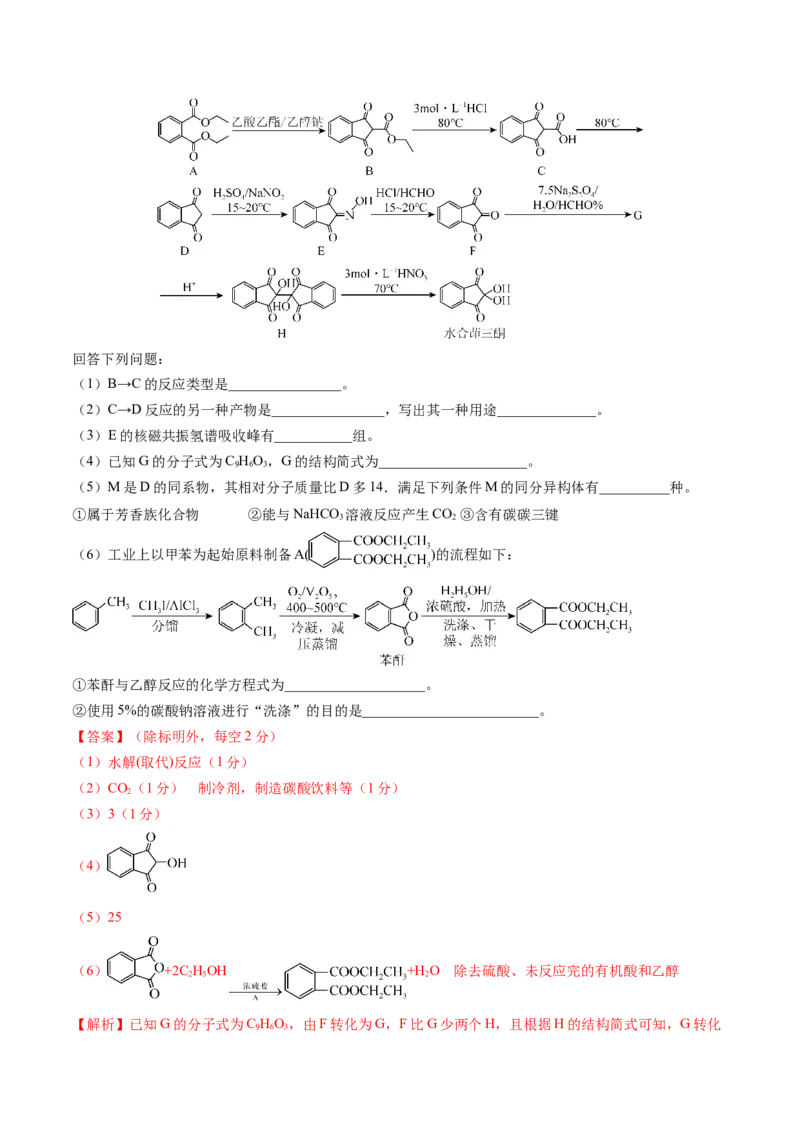
肽等,物证技术中常用水合茚三酮显现指纹。其合成路线如下:回答下列问题:
(1)B→C的反应类型是________________。
(2)C→D反应的另一种产物是________________,写出其一种用途______________。
(3)E的核磁共振氢谱吸收峰有___________组。
(4)已知G的分子式为C HO,G的结构简式为_____________________。
9 6 3
(5)M是D的同系物,其相对分子质量比D多14.满足下列条件M的同分异构体有__________种。
①属于芳香族化合物 ②能与NaHCO 溶液反应产生CO ③含有碳碳三键
3 2
(6)工业上以甲苯为起始原料制备A( )的流程如下:
①苯酐与乙醇反应的化学方程式为____________________。
②使用5%的碳酸钠溶液进行“洗涤”的目的是_________________________。
【答案】(除标明外,每空2分)
(1)水解(取代)反应(1分)
(2)CO(1分) 制冷剂,制造碳酸饮料等(1分)
2
(3)3(1分)
(4)
(5)25
(6) +2C HOH +H O 除去硫酸、未反应完的有机酸和乙醇
2 5 2
【解析】已知G的分子式为C HO,由F转化为G,F比G少两个H,且根据H的结构简式可知,G转化
9 6 3为H时为酸化,H的分子式为G的两倍,结合结构简式推知G为 ;
(1)根据B和C的结构简式可知,B→C是B中的酯基水解生成C和乙醇,反应类型是水解反应或取代反
应;
(2)根据C和D的结构简式可知,C→D反应是C反应生成D和CO,故另一种产物是CO,其用途有制
2 2
冷剂,制造碳酸饮料等;
(3)根据结构简式可知,E中含有三种不同环境的氢原子,核磁共振氢谱吸收峰有3组;
(4)根据分析可知,G的结构简式为 ;
(5)D为 ,M是D的同系物,其相对分子质量比D多14,则可能多一个CH,满足条件①属于
2
芳香族化合物;②能与NaHCO 溶液反应产生CO ,则含有羧基;③含有碳碳三键,若苯环上只有一个取
3 2
代基,则取代基为-CH(COOH)-C CH 、-CH-C C-COOH 、-C C-CH-COOH ,则有三种;若苯环上有
2 2
两个取代基,则取代基为-COOH和-CHC CH、-COOH和-C C-CH、-CH 和-C C-COOH、-C CH和-
2 3 3
CHCOOH,每种均有邻、间、对位,故共有4 3=12种;若苯环上有三个取代基,则有-C CH、-COOH
2
和-CH,结构有10种;故总共有同分异构体25种;
3
(6)①苯酐与两分子乙醇反应生成 和水,反应的化学方程式为 +2C HOH
2 5
+H O;
2
②使用5%的碳酸钠溶液进行“洗涤”的目的是除去硫酸、未反应完的有机酸和乙醇。
20.(12分)“低碳经济”已成为全世界科学家研究的重要课题。根据所学知识回答下列问题:
I.在一定条件下,CO
2
(g) +4H
2
(g)⇌CH
4
(g)+2H
2
O(g) ΔH
1
。
已知:①常温常压下,H 和CH 的燃烧热(ΔH)分别为- 285.5kJ ·mol-1和-890.0 kJ ·mol-1;
2 4
②HO(l)=HO(g) ΔH=+44.0 kJ ·mol-1。
2 2 2
(1)ΔH=_______ kJ ·mol-1。
1
(2)在某一恒容密闭容器中加入CO、H,其分压分别为15 kPa、30 kPa,加入催化剂并加热使其发生反
2 2
应CO
2
(g) +4H
2
(g)⇌CH
4
(g)+ 2H
2
O(g)。研究表明CH
4
的反应速率v(CH
4
)=1.2×10-6 p(CO
2
)·p4(H
2
) kPa·s-1,某
时刻测得HO(g)的分压为10 kPa,则该时刻v(H )=_______。
2 2
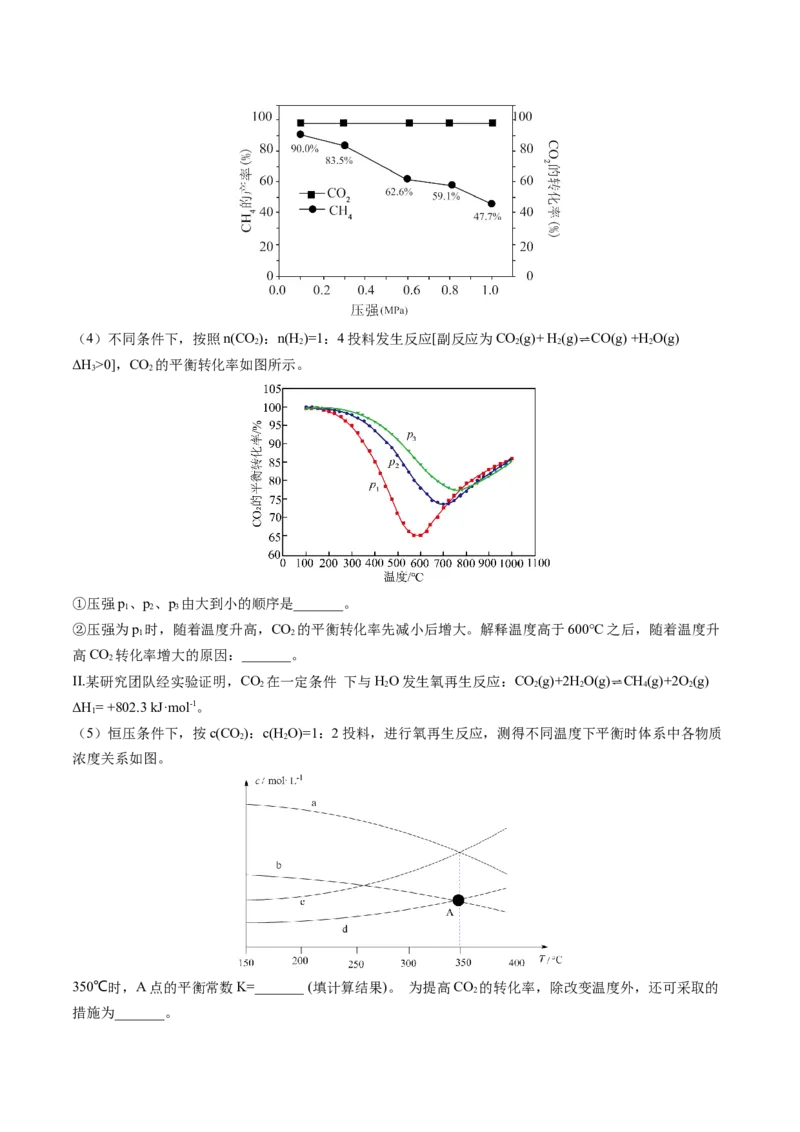
(3)其他条件一定时,不同压强下,CO 的转化率和CH 的产率如图所示。则CO 甲烷化应该选择的压强
2 4 2
约为_______MPa;CH 的产率小于CO 的转化率的原因是_______。
4 2(4)不同条件下,按照n(CO
2
):n(H
2
)=1:4投料发生反应[副反应为CO
2
(g)+ H
2
(g)⇌CO(g) +H
2
O(g)
ΔH>0],CO 的平衡转化率如图所示。
3 2
①压强p、p、p 由大到小的顺序是_______。
1 2 3
②压强为p 时,随着温度升高,CO 的平衡转化率先减小后增大。解释温度高于600°C之后,随着温度升
1 2
高CO 转化率增大的原因:_______。
2
II.某研究团队经实验证明,CO
2
在一定条件 下与H
2
O发生氧再生反应:CO
2
(g)+2H
2
O(g)⇌CH
4
(g)+2O
2
(g)
ΔH= +802.3 kJ·mol-1。
1
(5)恒压条件下,按c(CO):c(HO)=1:2投料,进行氧再生反应,测得不同温度下平衡时体系中各物质
2 2
浓度关系如图。
350℃时,A点的平衡常数K=_______ (填计算结果)。 为提高CO 的转化率,除改变温度外,还可采取的
2
措施为_______。【答案】(除标明外,每空2分)
(1)-164. 0
(2)0.48 kPa·s-1
(3)0.1(1分) 有其他含碳的副产物生成(1分)
(4)①p> p>p ②温度超过600℃时,副反应进行程度较大,CO 的转化率上升(1分)
3 2 1 2
(5)1 减小投料比[c(CO):c(HO)](或及时移出产物) (1分)
2 2
【解析】(1)常温常压下,H 和CH 的燃烧热(ΔH)分别为-285.5kJ ·mol-1和-890.0 kJ ·mol-1,则有③2H(g)
2 4 2
+O (g)=2HO(l) ΔH =-571kJ ·mol-1,④CH(g)+2O(g)=CO (g)+2HO(l) ΔH =-890.0kJ ·mol-1,根据盖斯定律可
2 2 3 4 2 2 2 4
知,2③-④+2②可得反应CO
2
(g) +4H
2
(g)⇌CH
4
(g)+2H
2
O(g),则ΔH
1
=2ΔH
3
-ΔH
4
+2ΔH
2
=2(-571kJ
·mol-1)-(-890.0kJ ·mol-1)+2(+44.0kJ ·mol-1)=-164.0kJ ·mol-1。
(2)同温同体积下,气体的压强和气体的物质的量成正比,CO、H 的起始分压分别为15kPa、30kPa,
2 2
某时刻测得HO(g)的分压为10kPa,Δp(H O)=10kPa,则Δp(CO)=5kPa,Δp(H )=20kPa,此时,
2 2 2 2
p(CO)=10kPa,Δp(H )=10kPa,v(CH)=1.2×10-610104kPa·s-1=0.12kPa·s-1,v(H )=4v(CH )=0.48kPa·s-1。
2 2 4 2 4
(3)如图所示,随着压强增大,CO 的转化率变化不大,CH 的产率逐渐减小,故CO 甲烷化应该选择的
2 4 2
压强约为0.1MPa;CH 的产率小于CO 的转化率的原因是有其他含碳的副产物生成。
4 2
(4)①CO
2
(g) +4H
2
(g)⇌CH
4
(g)+2H
2
O(g)是放热反应,低温时,主要发生该反应,该反应是气体体积减小
的反应,增大压强,平衡正向移动,CO 的平衡转化率增大,故p>p>p;
2 3 2 1
②压强为p 时,温度低于600℃时,主反应进行程度大,该反应是放热反应,升高温度,平衡逆向移动,
1
CO 的转化率下降,温度超过600℃时,副反应进行程度较大,该反应是吸热反应,升高温度,平衡正向
2
移动,CO 的转化率上升。
2
(5)恒压条件下,按c(CO):c(HO)=1:2投料,并结合方程式可知,曲线a表示HO的浓度变化,曲线
2 2 2
b表示CO 的浓度变化,曲线c表示O 的浓度变化,曲线d表示CH 的浓度变化;350℃时,
2 2 4
c(CO)=c(CH ),c(HO)=c(O),K= =1;为提高CO 的转化率,除改变温度外,还可采取
2 4 2 2 2
的措施为减小投料比[c(CO):c(HO)],或及时移出产物。
2 2