文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(山东专用)
黄金卷04
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 V 51
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.化学与食品密切相关.下列说法正确的是
A.健康食品不含任何添加剂 B.烘焙面包用小苏打作膨松剂
C.氮气防腐是利用了氮气的物理性质 D.食品袋中放置生石灰可防止氧化变质
【答案】B
【解析】A.健康食品可以含有在法律范围内许可的食品添加剂,不添加食品添加剂会加快食物的腐败变
质,容易对人体产生毒害作用,存在安全隐患,故A 错误;B.碳酸氢钠固体加热时开始逐渐分解生成碳
酸钠、水和二氧化碳气体,常利用此特性作为制作饼干、糕点、馒头、面包的膨松剂,故B正确;C.空
气中分离出来的氮气用于食品防腐,是利用了氮气的稳定性,属于化学性质,故C错误;D.生石灰不具
有还原性,不能防止食品氧化变质,生石灰具有吸水性,可以作干燥剂,故D错误;故选B。
2.下列各项实验的基本操作,其中正确的是
A.用湿润的pH试纸测定硫酸溶液的pH
B.用浓硫酸干燥二氧化硫
C.金属钠着火时,用泡沫灭火器灭火
D.蒸发操作中,将蒸发皿放在铁架台的铁圈上,并垫上石棉网加热
【答案】B
【解析】A.用pH试纸测定硫酸溶液的pH时,pH试纸不能润湿,A项错误;
B.浓硫酸有吸水性,且不与 反应,可用浓硫酸干燥 ,B项正确;
C.泡沫含水,钠与水反应,钠的燃烧产物 与水及 也反应,导致燃烧更加剧烈,所以不能用泡
沫灭火器灭火,C项错误;
D.蒸发时,蒸发皿可以放在铁圈上直接加热,蒸发皿耐高温,不用垫石棉网,D项错误。
故答案选B。
3.下列说法错误的是
A.顺-2-丁烯和反-2-丁烯加氢产物相同
B.苯酚和甲醛通过加聚反应可制得高分子材料
C.可用酸性KMnO 溶液鉴别甲苯和环已烷
4
D.淀粉和纤维素在酸作用下水解的最终产物都是葡萄糖
【答案】B
【解析】A.顺-2-丁烯和反-2-丁烯加氢产物都是丁烷,产物相同,A项正确;
B.苯酚和甲醛通过缩聚反应可制得高分子材料酚醛树脂,B项错误;
C.甲苯能使酸性高锰酸钾褪色,环己烷不能使酸性高锰酸钾褪色,可以用可用酸性高锰酸钾溶液鉴别甲苯和环已烷,C项正确;
D.淀粉和纤维素在酸作用下水解的最终产物都是葡萄糖,D项正确;
答案选B。
4.向含 的废水中加入铁粉和 可制备 ,反应如下
,下列说法正确的是
A. 的电子式为
B.加入 的作用是提供 和调节
C. 电离方程式:
D.反应中每生成 转移 电子
【答案】B
【解析】A. 中存在共价键,电子式为 ,A错误;B.反应后生成的化合物中含有钾离子,
故碳酸钾的作用为提供钾离子,并消耗 ,调节pH,B正确 ;C. 的电离方程式为:
,C错误;D.该反应中铁元素化合价升高2价,故每生成2mol二氧化碳
转移2mol电子,则每生成1mol二氧化碳转移1mol电子,D错误;故选B。
5.物质的结构决定物质的性质。设N 为阿伏加德罗常数的值。下列说法错误的是
A
A.DNA通过氢键结合成稳定的双螺旋结构
B.46g由二甲醚(CHOCH )和乙醇组成的混合物中,杂化方式为sp2杂化的原子数为2N
3 3 A
C.键角:CO >NF >P
3 4
D.基态Mn原子中,两种自旋状态的电子数之比为2∶3
【答案】B
【解析】A.DNA分子的双螺旋结构是相对稳定的,这是因为在DNA分子双螺旋结构的内侧,通过氢键
形成的碱基,A正确;
B.在二甲醚和乙醇中,碳原子和氧原子均为 杂化,B错误;
C.CO 中C的价层电子对为3,且不含孤电子对,为平面三角形,键角为120°;NF 中N的价层电子对
3
为3,含1对孤电子对,为三角锥形,键角为107°;P 为正四面体结构,键角为60°;键角:CO >NF >
4 3
P,C正确;
4
D.基态Mn原子的电子排布图为:
,两种自旋状
态的电子数之比为2∶3,D正确;
故选B。
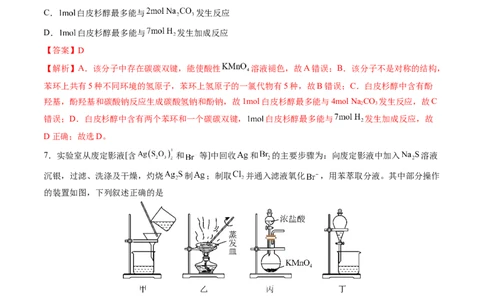
6.近日北京大学肿瘤医院发现,天然小分子白皮杉醇在胃癌治疗中有重要应用价值。其结构如图所示,下列有关白皮杉醇的说法正确的是
A.不能使酸性 溶液褪色
B.苯环上氢原子的一氯代物有4种
C. 白皮杉醇最多能与 发生反应
D. 白皮杉醇最多能与 发生加成反应
【答案】D
【解析】A.该分子中存在碳碳双键,能使酸性 溶液褪色,故A错误;B.该分子不是对称的结构,
苯环上共有5种不同环境的氢原子,苯环上氢原子的一氯代物有5种,故B错误;C.白皮杉醇中含有酚
羟基,酚羟基和碳酸钠反应生成碳酸氢钠和酚钠,故1mol白皮杉醇最多能与4mol Na CO 发生反应,故C
2 3
错误;D.白皮杉醇中含有两个苯环和一个碳碳双键, 白皮杉醇最多能与 发生加成反应,故
D正确;故选D。
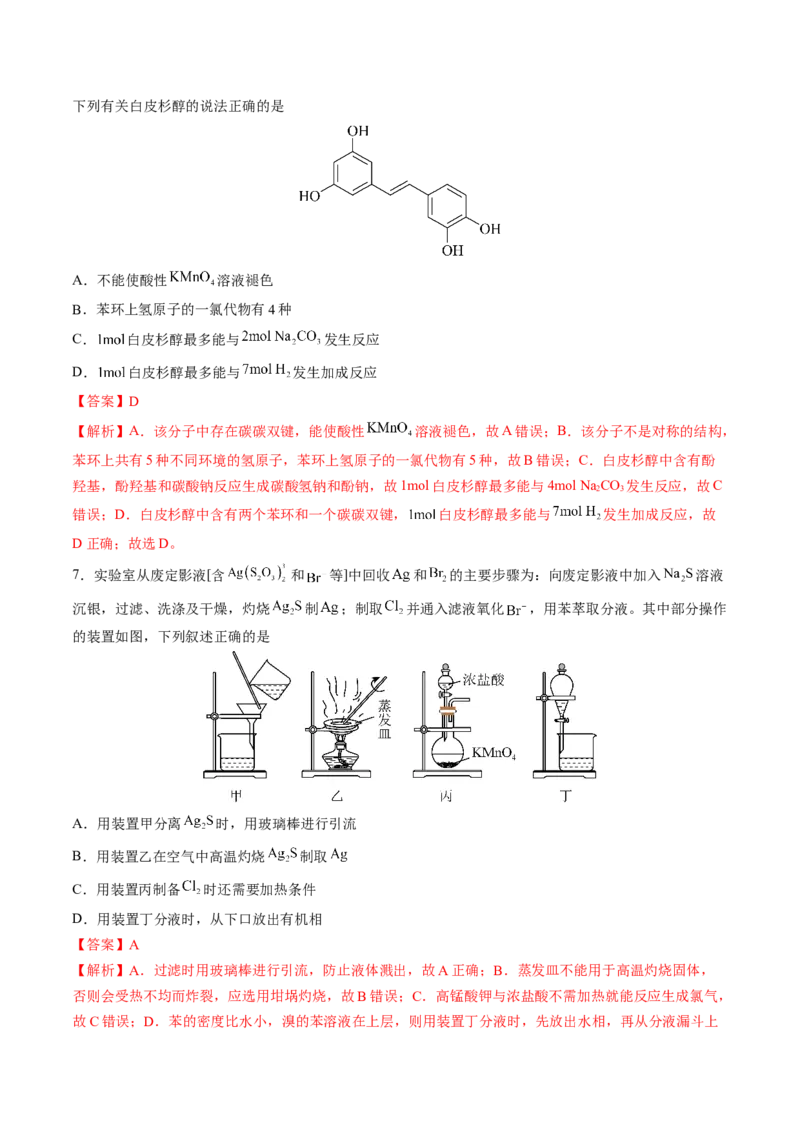
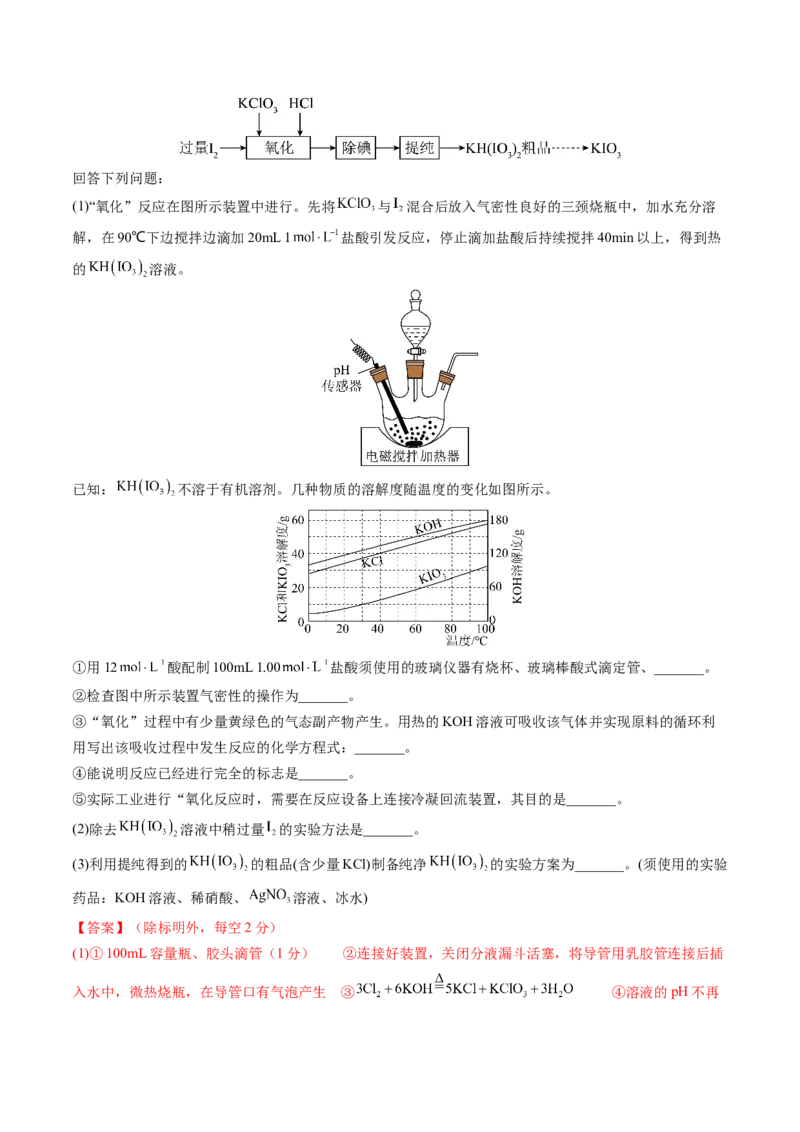
7.实验室从废定影液[含 和 等]中回收 和 的主要步骤为:向废定影液中加入 溶液
沉银,过滤、洗涤及干燥,灼烧 制 ;制取 并通入滤液氧化 ,用苯萃取分液。其中部分操作
的装置如图,下列叙述正确的是
A.用装置甲分离 时,用玻璃棒进行引流
B.用装置乙在空气中高温灼烧 制取
C.用装置丙制备 时还需要加热条件
D.用装置丁分液时,从下口放出有机相
【答案】A
【解析】A.过滤时用玻璃棒进行引流,防止液体溅出,故A正确;B.蒸发皿不能用于高温灼烧固体,
否则会受热不均而炸裂,应选用坩埚灼烧,故B错误;C.高锰酸钾与浓盐酸不需加热就能反应生成氯气,
故C错误;D.苯的密度比水小,溴的苯溶液在上层,则用装置丁分液时,先放出水相,再从分液漏斗上口倒出有机相,故D错误;故选A。
8.检验 的反应有如下两种途径。下列说法正确的是
A.反应①中 被还原
B.乙醚与 中的铬元素形成共价键,有利于蓝色现象的观察
C.反应②为:
D.反应③中溶液的 越小,反应速率越慢
【答案】B
【解析】A.反应① 、CrO 中Cr元素化合价均为+6,此反应不是氧化还原反应,A错误;B.由题
5
中信息乙醚与 中的铬元素形成共价键,蓝色可稳定几分钟,有利于蓝色现象的观察,B正确;C.由
信息反应②为: ,C错误;D.反应③
+8H++3H O=3O ↑+2Cr3++7H O,中溶液的 越小,H+浓度越大,反应速率越快,D错误;故答案选B。
2 2 2 2
9.室温下,下列实验探究方案能达到探究目的的是
选项 探究方案 探究目的
将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液,观察 食品脱氧剂样品中有无+3价
A
溶液颜色变化 铁
B 用pH计测量等浓度的醋酸、盐酸的pH,比较溶液pH大小 是弱电解质
炭可与浓HNO 反应生成
3
C 向浓HNO 中插入红热的炭,观察生成气体的颜色
3
NO
2
向淀粉溶液中加适量20%H SO 溶液,加热,冷却后加NaOH溶液 淀粉溶液在稀硫酸和加热条
2 4
D
至碱性,再加少量碘水,观察溶液颜色变化 件下是否水解
【答案】B
【解析】A.由于该反应2Fe3++Fe=3Fe2+溶液中可能不存在Fe3+,而无法使KSCN显色检测Fe3+,A不符合
题意;
B.CHCOOH为弱电解质电离程度小,其电离出的H+比等浓度的盐酸电离出的H+少,从而两者的pH有
3
差异,测定两者的pH即可确定CHCOOH为弱电解质,B项符合题意;
3C.浓HNO 受热会分解产生NO 从而无法确定炭与浓HNO 是否发生反应产生NO ,C项不符合题意;
3 2 3 2
D.I 与NaOH反应而无法与淀粉显色,从而无法确定淀粉水解情况,D不符合题意;
2
故选B。
10.X、Y、Z、W、Q是原子序数依次增大且不超过20的主族元素。X是地壳中含量最多的元素,Y基态
原子核外s能级和p能级电子数相等,Z与X同主族,Q的焰色试验呈紫色。列说法正确的是
A.简单离子半径;
B.X的第一电离能比同周期的相邻元素的大
C.Z的简单气态氢化物的热稳定性比W的强
D.Q最高价氧化物对应水化物的碱性比Y的弱
【答案】A
【解析】X、Y、Z、W、Q是原子序数依次增大且不超过20的主族元素;X是地壳中含量最多的元素,X
为O;Y基态原子核外s能级和p能级电子数相等,Y为Mg;Z与X同主族,Z为S;Q的焰色试验呈紫色,
Q为K,则W为Cl。A.由分析可知,X为O,Y为Mg,Z为S;电子层数越多,简单离子的半径越大;
电子层数相同时,核电荷数越大,简单离子的半径越小;故简单离子半径; ,A正确;
B.由分析可知,X为O;同一周期,从左到右,随着原子序数变大,元素的第一电离能变大,N的2p轨
道为半充满稳定状态,第一电离能大于同周期相邻元素,故N、O的第一电离能大小:N>O;而不是氧的
第一电离能比同周期的相邻元素的大,B错误;C.由分析可知,Z为S,W为Cl;元素的非金属性越强,
其简单氢化物稳定性越强,非金属性:Cl>S,则S的简单气态氢化物的热稳定性比W的Cl,C错误;
D.由分析可知,Y为Mg,Q为K;元素金属性越强,最高价氧化物对应水化物的碱性越强;金属性:K
>Mg,K最高价氧化物对应水化物的碱性比Mg的强,D错误;故选A。
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11.以铁硼矿(主要成分为 和 ,还有少量 、FeO、CaO、 和 等)为原料
制备硼酸 的工艺流程如图所示:
下列说法错误的是
A.浸渣中的物质是 、 和
B.“净化除杂”需先加 溶液再调节溶液的pH
C.操作a为蒸发浓缩、冷却结晶
D.“粗硼酸”中的主要杂质是氢氧化铝
【答案】AD
【解析】以铁硼矿(主要成分为 和 ,还有少量 和 等)为
原料制备硼酸(H BO),根据流程可知,加硫酸溶解,只有SiO 不溶,CaO转化为微溶于水的CaSO,“净
3 3 2 4化除杂”需先加入氧化剂,将Fe2+氧化为Fe3+,调节溶液的pH,使Fe3+、Al3+均转化为沉淀,则滤渣为氢
氧化铝、氢氧化铁,然后蒸发浓缩、冷却结晶、过滤分离出HBO。A.由分析可知,“浸渣”为 ,
3 3
,A错误;B.“净化除杂”先加 溶液将 转化为 ,再调节溶液的pH,生成氢氧化铝
和氢氧化铁,B正确;C.由分析可知,操作a为蒸发浓缩、冷却结晶,C正确;D.最后浓缩结晶时硫酸
镁易结合水以晶体析出,则粗硼酸中的主要杂质是七水硫酸镁,D错误;故选AD。
12.实验室分别进行如下实验:①向 溶液中滴加酸性 溶液,溶液由蓝色变为淡黄色;②向
溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝。已知 ;蓝色; :淡黄色、强氧化
性。下列说法错误的是
A.①中氧化剂与还原剂物质的量之比为
B.②的离子反应为
C.由①②可知,氧化性:
D. 溶液中滴加 可发生反应
【答案】A
【解析】A.向VOSO 溶液中滴加酸性KMnO 溶液,溶液由蓝色变为淡黄色,说明酸性环境下高锰酸根
4 4
将VO2+氧化为 ,高锰酸根被还原成Mn2+,由电子守恒可知存在KMnO ~ 5VOSO ~ 5e-,则①中氧化
4 4
剂与还原剂物质的量之比为1:5,A项错误;
B.向(VO )SO 溶液中滴加浓盐酸,产生黄绿色气体,溶液变蓝,说明浓盐酸能把 还原为VO2+,Cl-失
2 2 4
去电子生成氯气,由电子、电荷及原子守恒可知离子方程式为:2 +4H++2Cl-= 2VO2++Cl↑+2H O,B项
2 2
正确;
C.氧化剂的氧化性大于氧化产物的氧化性,则由①可知,氧化性: MnO > , 由②可知,氧化性:
> Cl ,所以氧化性MnO > >Cl,C项正确;
2 2
D. 具有较强的氧化性,(VO )SO 溶液中滴加FeSO 会发生氧化还原反应,则 被还原为VO2+,
2 2 4 4
Fe2+被氧化为Fe3+,D项正确;
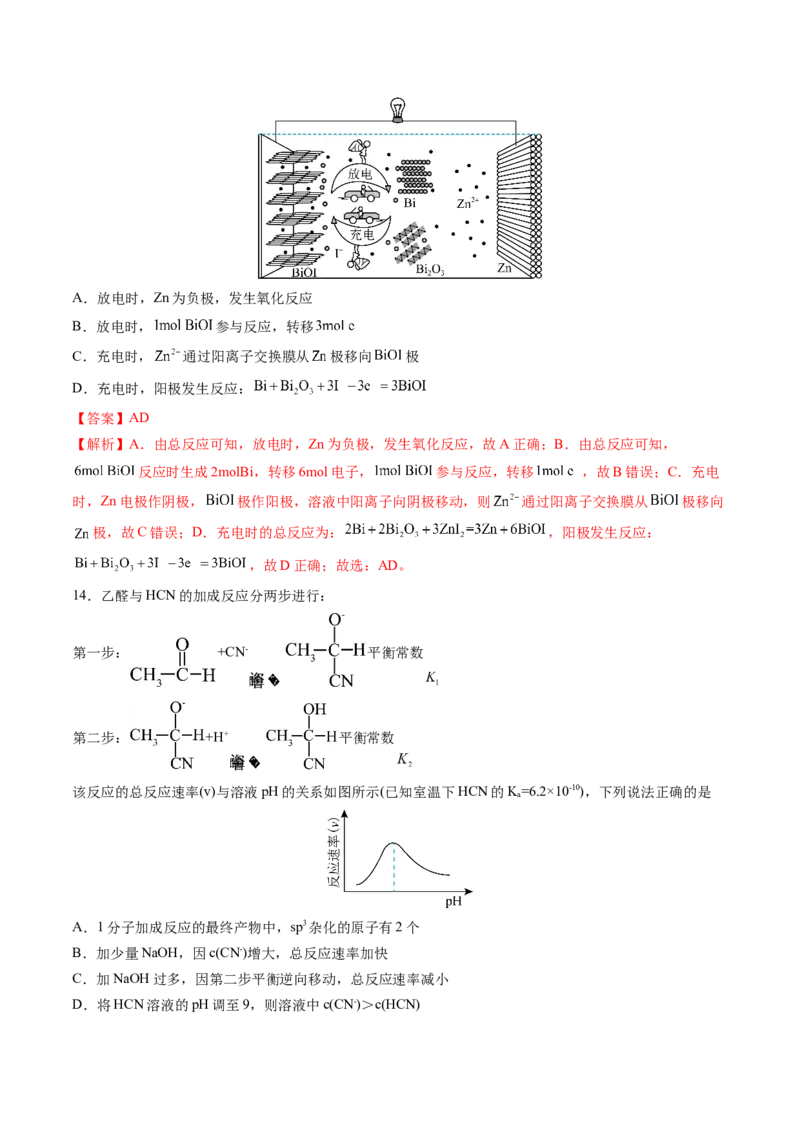
故答案选A。
13.我国科学家利用 电池,以 水溶液作为锌离子电池的介质,可实现快速可逆的协同转化
反应。如图所示,放电时该电池总反应为: 。下列说法正确的是A.放电时,Zn为负极,发生氧化反应
B.放电时, 参与反应,转移
C.充电时, 通过阳离子交换膜从 极移向 极
D.充电时,阳极发生反应:
【答案】AD
【解析】A.由总反应可知,放电时,Zn为负极,发生氧化反应,故A正确;B.由总反应可知,
反应时生成2molBi,转移6mol电子, 参与反应,转移 ,故B错误;C.充电
时,Zn电极作阴极, 极作阳极,溶液中阳离子向阴极移动,则 通过阳离子交换膜从 极移向
极,故C错误;D.充电时的总反应为: ,阳极发生反应:
,故D正确;故选:AD。
14.乙醛与HCN的加成反应分两步进行:
第一步: +CN- 平衡常数
第二步: +H+ 平衡常数
该反应的总反应速率(v)与溶液pH的关系如图所示(已知室温下HCN的K=6.2×10-10),下列说法正确的是
a
A.1分子加成反应的最终产物中,sp3杂化的原子有2个
B.加少量NaOH,因c(CN-)增大,总反应速率加快
C.加NaOH过多,因第二步平衡逆向移动,总反应速率减小
D.将HCN溶液的pH调至9,则溶液中c(CN-)>c(HCN)【答案】B
【解析】A.1分子加成反应的最终产物为 ,其中的饱和碳为sp3杂化,另外氧原子也是sp3杂化,
则一共有3个,A错误;B.加入少量氢氧化钠可以和HCN反应生成CN-,则其浓度增大,反应速率增快,
B正确;C.加NaOH过多,则溶液中氢离子浓度会比较低,导致第二步反应较慢,成为影响总反应速率
的主要因素,故总反应速率较慢,C错误;D.将HCN溶液的pH调至9,则c(H+)=1.0×10-9,根据题意K
a
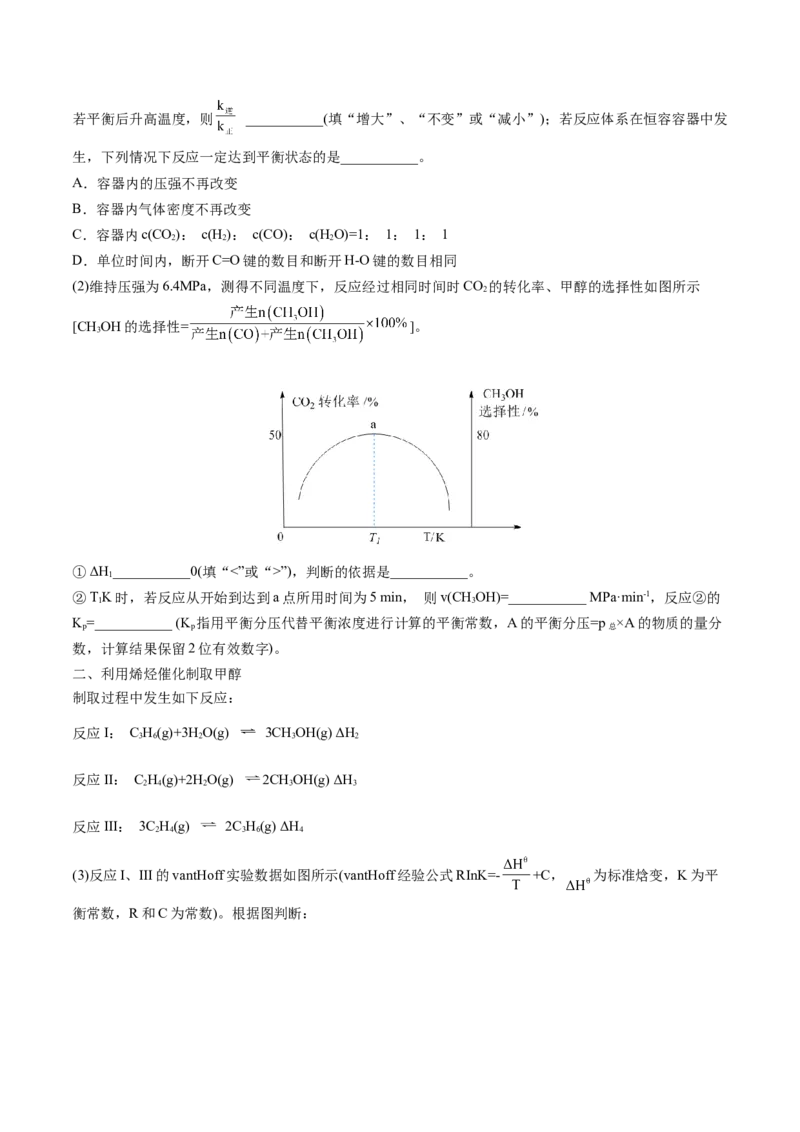
,将c(H+)=1.0×10-9代入可知, ,故c(CN-)”),判断的依据是___________。
1
②TK时,若反应从开始到达到a点所用时间为5 min, 则v(CHOH)=___________ MPa·min-1,反应②的
1 3
K=___________ (K 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=p ×A的物质的量分
p p 总
数,计算结果保留2位有效数字)。
二、利用烯烃催化制取甲醇
制取过程中发生如下反应:
反应I: C H(g)+3HO(g) 3CHOH(g) ΔH
3 6 2 3 2
反应II: C H(g)+2HO(g) 2CHOH(g) ΔH
2 4 2 3 3
反应III: 3C H(g) 2C H(g) ΔH
2 4 3 6 4
(3)反应I、III的vantHoff实验数据如图所示(vantHoff经验公式RInK=- +C, 为标准焓变,K为平
衡常数,R和C为常数)。根据图判断:ΔH=___________(用含ΔH 和ΔH 的计算式表示),反应III的 ___________ kJ ·mol-1。
3 2 4
【答案】(除标明外,每空1分)
(1)减小 AD
(2)①< 温度高于T 时,相同时间内测得二氧化碳转化率随温度的增大而下降,而反应②温度升高,平衡
1
正向移动,二氧化碳转化率随温度的增大而增大,所以反应①温度升高,平衡逆向移动,二氧化碳转化率
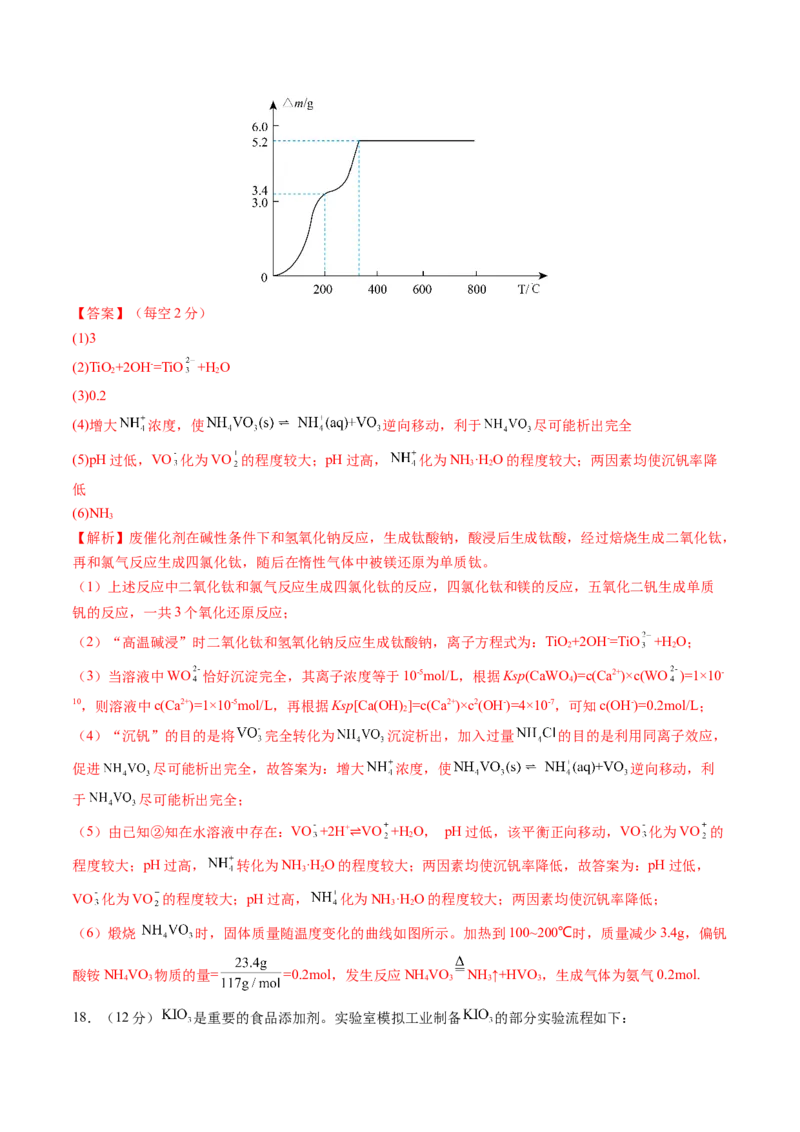
随温度的增大而减小,即证明 ΔH<0 ②0.16(2分) 0.059(2分)
(3) (2分) -100(2分)
【解析】(1)反应达到平衡状态时v = v ,k c(CO)·c(H)=k c(HO) ·c(CO), = =
正 逆 正 2 2 逆 2
,反应②为吸热反应,随温度升高平衡正向移动,K增大,则 减小;A.该反应虽然前后气体分子数
相等,但整个体系还存在反应①,整体压强为变量,则容器内的压强不再改变,能说明反应到达平衡状态;
B.容器体积不变,气体质量反应前后不变,则容器内气体密度始终不变,不能据此说明反应到达平衡状
态;
C.容器内c(CO):c(H):c(CO):c(HO)=1:1:1:1,不能说明各组分浓度不再改变,因此不能据此判
2 2 2
断平衡;D.单位时间内,断开C=O键的数目和断开H-O键的数目相同,可知消耗二氧化化碳和消耗水的
速率相等,即正反应速率等于逆反应速率,反应达到平衡状态;故答案为:减小;AD;
(2)①温度高于T 时,相同时间内测得二氧化碳转化率随温度的增大而下降,而反应②温度升高,平衡
1
正向移动,二氧化碳转化率随温度的增大而增大,所以反应①温度升高,平衡逆向移动,二氧化碳转化率
随温度的增大而减小,即证明 ΔH<0,故答案为:<;温度高于T 时,相同时间内测得二氧化碳转化率随
1 1
温度的增大而下降,而反应②温度升高,平衡正向移动,二氧化碳转化率随温度的增大而增大,所以反应
①温度升高,平衡逆向移动,二氧化碳转化率随温度的增大而减小,即证明 ΔH<0;
②TK时,根据图1可知,二氧化碳转化率为50%,甲醇的选择性为80%,投n(H )=3mol,n(CO)=1mol,
1 2 2
则生成甲醇的物质的量为1mol×50%×80%=0.4mol,根据反应可知,a点时,各物质的物质的量分别为:
n(CO)=lmol-1mol×50%=0.5mol,n(H )=3mol-3mol×0.4mol-0.1mol=1.7mol,n(CHOH)=0.4mol。
2 2 3
n(H O)=0.4mol+0.1mol=0.5mol,n(CO)=0.lmol,n =0.5+1.7+0.1+0.5+0.4=3.2mol,所以各物质的分压为:
2 总
、 、 、
、 ,若反应从开始到达a点所用时间为5min,则 ;根据平衡常数表达式可知反应②的Kp=
,故答案为:0.16;0.059;
(3)由盖斯定律可知反应II= ,则ΔH= ;结合图中信息即题中公式可得:RlnK=-
3
+C=34;RlnK=- +C=30.4;联立方程解得: =-100,故答案为:
;-100。