文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷06
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.创造美好幸福生活离不开化学。下列有关叙述错误的是
A.家用天然气灶具需安装报警装置,因为天然气是可燃气体,漏气易发生危险
B.食品袋里的去氧剂(一般含铁粉、活性炭和食盐)可以减缓食品变质速率
C.杭州第19届亚运会主火炬首次采用甲醇作燃料,实现了零碳排放
D.冰、干冰常用作制冷剂,冰融化和干冰升华时都要吸收热量
2.下列化学用语表达正确的是
A. 的离子结构示意图:
B. 分子中,碳原子与氧原子之间形成的共价键类型为 键
C.基态氧原子核外电子轨道表示式:
D. 分子的空间结构:三角锥形
3.设 为阿伏加德罗常数的值,下列说法正确的是
A. 溶液中所含 数目为
B. 中 杂化的碳原子数目为1
C.标准状况下, 中含有的电子数目为
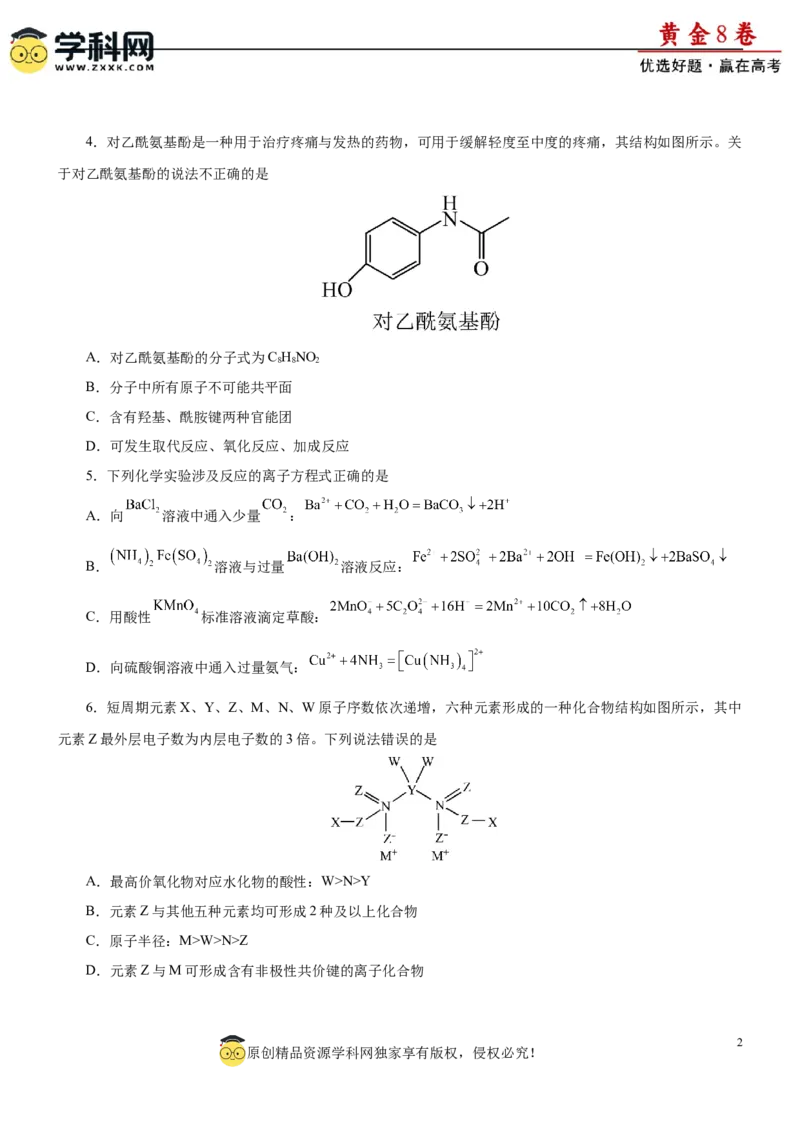
D.常温下,将 投入足量浓硝酸中,反应转移电子数目为4.对乙酰氨基酚是一种用于治疗疼痛与发热的药物,可用于缓解轻度至中度的疼痛,其结构如图所示。关
于对乙酰氨基酚的说法不正确的是
A.对乙酰氨基酚的分子式为C HNO
8 8 2
B.分子中所有原子不可能共平面
C.含有羟基、酰胺键两种官能团
D.可发生取代反应、氧化反应、加成反应
5.下列化学实验涉及反应的离子方程式正确的是
A.向 溶液中通入少量 :
B. 溶液与过量 溶液反应:
C.用酸性 标准溶液滴定草酸:
D.向硫酸铜溶液中通入过量氨气:
6.短周期元素X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,其中
元素Z最外层电子数为内层电子数的3倍。下列说法错误的是
A.最高价氧化物对应水化物的酸性:W>N>Y
B.元素Z与其他五种元素均可形成2种及以上化合物
C.原子半径:M>W>N>Z
D.元素Z与M可形成含有非极性共价键的离子化合物
2
原创精品资源学科网独家享有版权,侵权必究!7.利用废旧镀锌铁皮制备 胶体粒子的流程如图所示,已知: 溶于强碱时生成易溶于水的
,下列说法正确的是
A.用氢氧化钠溶液处理废旧镀锌铁皮,主要目的是为了处理表面的油污
B.“酸溶”的离子方程式为
C.“氧化”后溶液中存在的阳离子有 、 、
D. 胶体粒子可通过过滤操作得到
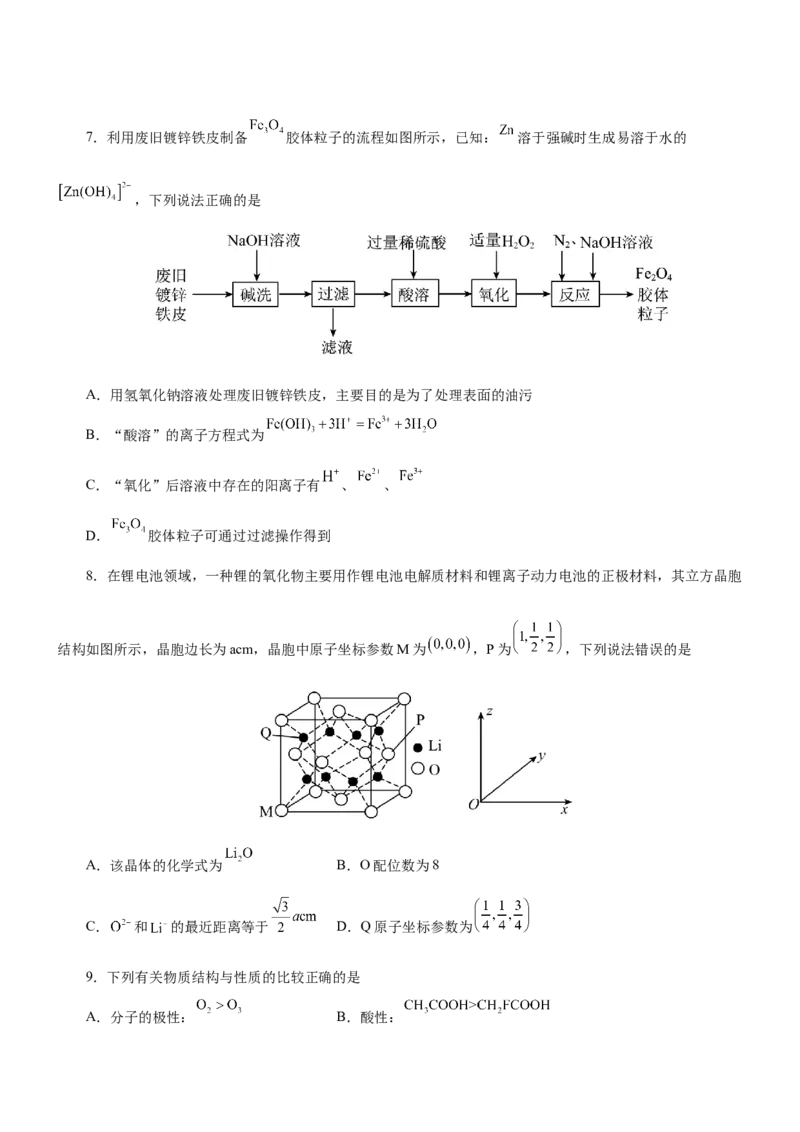
8.在锂电池领域,一种锂的氧化物主要用作锂电池电解质材料和锂离子动力电池的正极材料,其立方晶胞
结构如图所示,晶胞边长为acm,晶胞中原子坐标参数M为 ,P为 ,下列说法错误的是
A.该晶体的化学式为 B.O配位数为8
C. 和 的最近距离等于 D.Q原子坐标参数为
9.下列有关物质结构与性质的比较正确的是
A.分子的极性: B.酸性:C.键角: D.基态原子未成对电子数:Mn>Cr
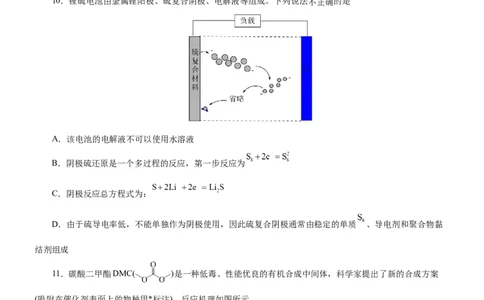
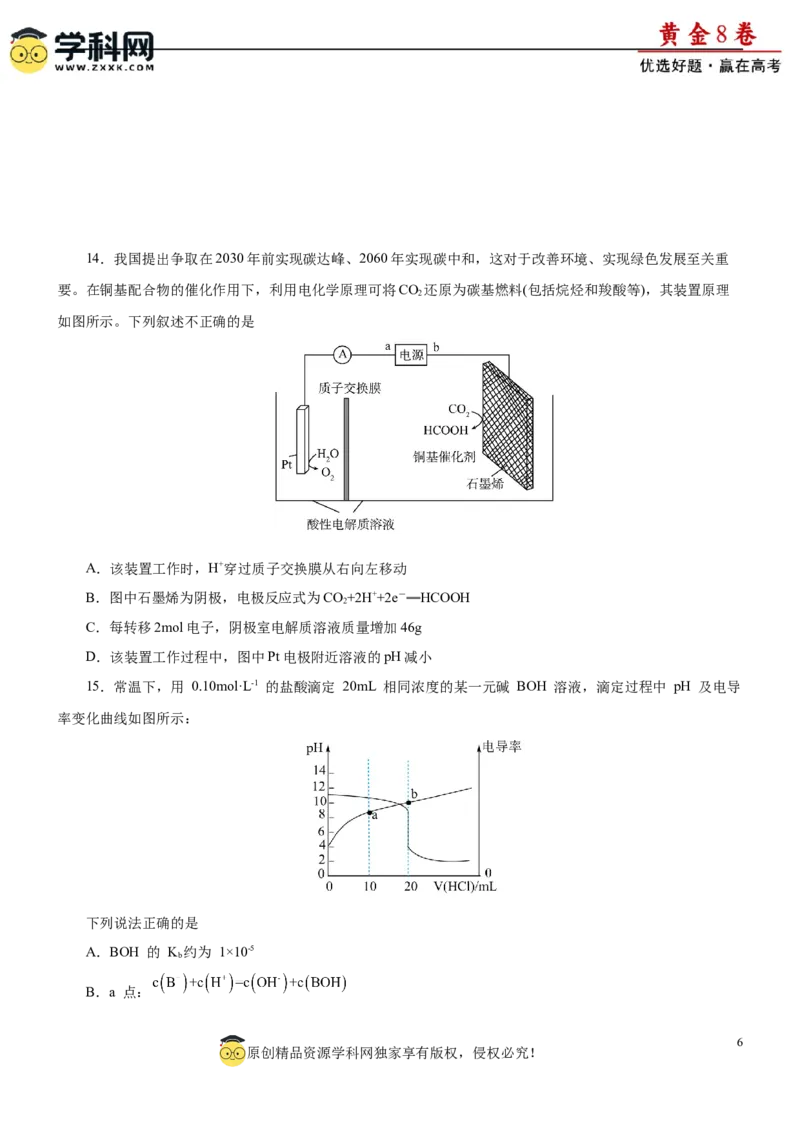
10.锂硫电池由金属锂阳极、硫复合阴极、电解液等组成。下列说法不正确的是
A.该电池的电解液不可以使用水溶液
B.阴极硫还原是一个多过程的反应,第一步反应为
C.阴极反应总方程式为:
D.由于硫导电率低,不能单独作为阴极使用,因此硫复合阴极通常由稳定的单质 、导电剂和聚合物黏
结剂组成
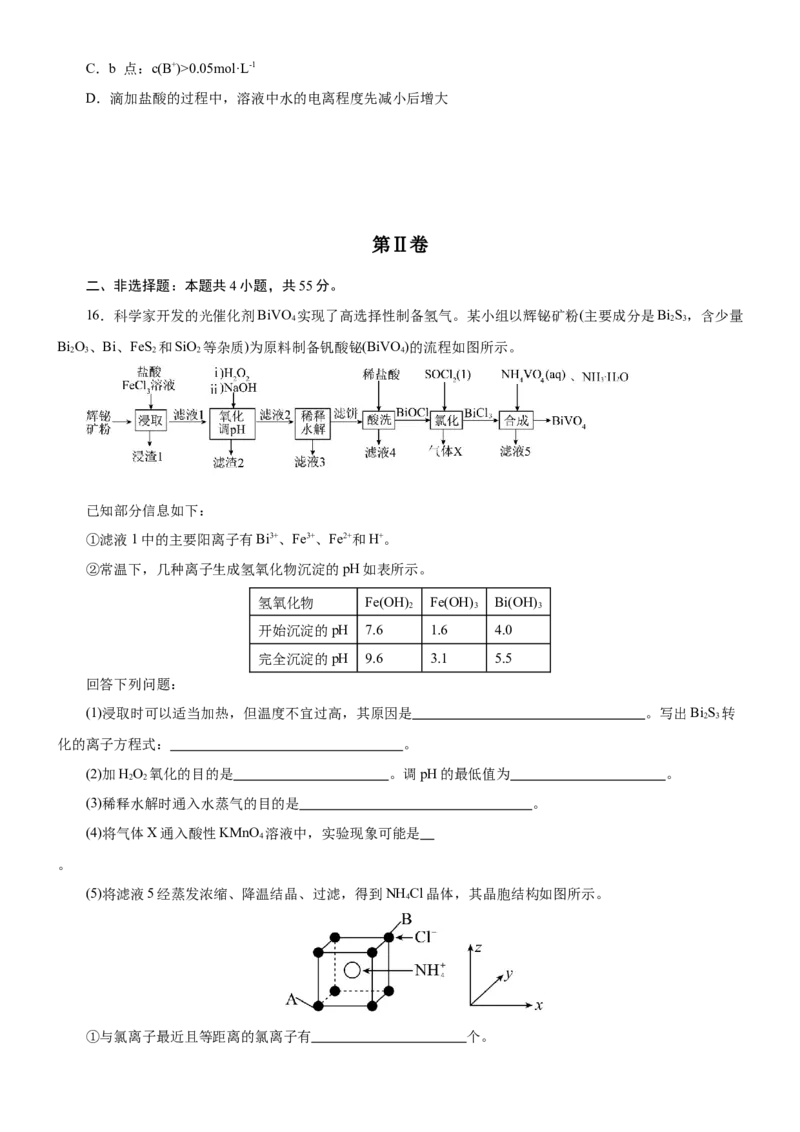
11.碳酸二甲酯DMC( )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案
(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是
4
原创精品资源学科网独家享有版权,侵权必究!A.HO·提高了反应的活化能
B.过程CHOH*+HO·*=CH O·*+HO*是该反应的决速步骤
3 3 2
C.过程中既有H-O键的断裂,又有H-O键的形成
D.吸附和脱附过程中共吸收1.126×104 eV的能量
12.过氧化钙(CaO)可用于治理赤潮、应急供氧等。2.76gCaO ·8H O样品(含杂质)受热分解过程的热重曲线
2 2 2
(样品质量随温度变化曲线,在140℃时恰好完全脱水,杂质受热不分解)如图所示。已知:过氧化钙常温下干燥
品很稳定,在350℃时能迅速分解。
下列说法不正确的是
A.CaO 能与水发生反应,反应的化学方程式为
2
B.该样品中CaO 的含量约为26.09%
2
C.在60℃时, 中x = 3
D.在350℃时,剩余的固体(杂质除外)的化学式为CaO
13.煤炭燃烧过程中会释放出大量的SO ,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以
2
CaSO 的形式固定,从而降低SO 的排放。但是煤炭燃烧过程中产生的CO又会与CaSO 发生化学反应,降低脱
4 2 4
硫效率。相关反应的热化学方程式如下:
CaSO(s)+CO(g) CaO(s)+SO (g)+CO (g) △H =+218.4 kJ/mol(反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s)+4CO (g) △H =-175.6 kJ/mol (反应Ⅱ)
4 2 2
下列有关说法正确的是
A.提高反应体系的温度,能提高该反应体系中SO 生成量
2
B.反应Ⅱ在较高的温度下可自发进行
C.用生石灰固硫的反应为:4CaO(s)+4SO (g) 3CaSO(s)+CaS(s) △H ,则△H>△H
2 4 3 3 2
D.由反应Ⅰ和反应Ⅱ可计算出反应CaSO(s) CaO(s)+SO (g)的焓变
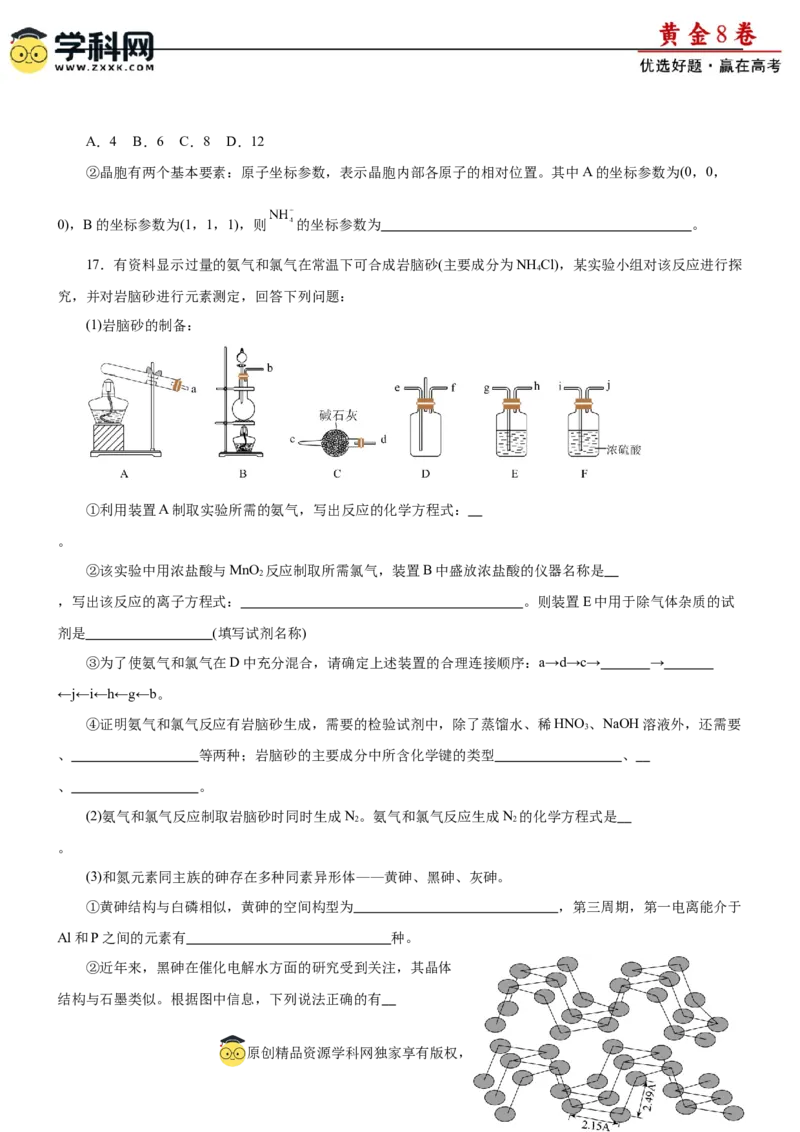
4 314.我国提出争取在2030年前实现碳达峰、2060年实现碳中和,这对于改善环境、实现绿色发展至关重
要。在铜基配合物的催化作用下,利用电化学原理可将CO 还原为碳基燃料(包括烷烃和羧酸等),其装置原理
2
如图所示。下列叙述不正确的是
A.该装置工作时,H+穿过质子交换膜从右向左移动
B.图中石墨烯为阴极,电极反应式为CO+2H++2e-═HCOOH
2
C.每转移2mol电子,阴极室电解质溶液质量增加46g
D.该装置工作过程中,图中Pt电极附近溶液的pH减小
15.常温下,用 0.10mol·L-1 的盐酸滴定 20mL 相同浓度的某一元碱 BOH 溶液,滴定过程中 pH 及电导
率变化曲线如图所示:
下列说法正确的是
A.BOH 的 K 约为 1×10-5
b
B.a 点:
6
原创精品资源学科网独家享有版权,侵权必究!C.b 点:c(B+)>0.05mol·L-1
D.滴加盐酸的过程中,溶液中水的电离程度先减小后增大
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.科学家开发的光催化剂BiVO 实现了高选择性制备氢气。某小组以辉铋矿粉(主要成分是BiS,含少量
4 2 3
BiO、Bi、FeS 和SiO 等杂质)为原料制备钒酸铋(BiVO)的流程如图所示。
2 3 2 2 4
已知部分信息如下:
①滤液1中的主要阳离子有Bi3+、Fe3+、Fe2+和H+。
②常温下,几种离子生成氢氧化物沉淀的pH如表所示。
氢氧化物 Fe(OH) Fe(OH) Bi(OH)
2 3 3
开始沉淀的pH 7.6 1.6 4.0
完全沉淀的pH 9.6 3.1 5.5
回答下列问题:
(1)浸取时可以适当加热,但温度不宜过高,其原因是 。写出BiS 转
2 3
化的离子方程式: 。
(2)加HO 氧化的目的是 。调pH的最低值为 。
2 2
(3)稀释水解时通入水蒸气的目的是 。
(4)将气体X通入酸性KMnO 溶液中,实验现象可能是
4
。
(5)将滤液5经蒸发浓缩、降温结晶、过滤,得到NH Cl晶体,其晶胞结构如图所示。
4
①与氯离子最近且等距离的氯离子有 个。A.4 B.6 C.8 D.12
②晶胞有两个基本要素:原子坐标参数,表示晶胞内部各原子的相对位置。其中A的坐标参数为(0,0,
0),B的坐标参数为(1,1,1),则 的坐标参数为 。
17.有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH Cl),某实验小组对该反应进行探
4
究,并对岩脑砂进行元素测定,回答下列问题:
(1)岩脑砂的制备:
①利用装置A制取实验所需的氨气,写出反应的化学方程式:
。
②该实验中用浓盐酸与MnO 反应制取所需氯气,装置B中盛放浓盐酸的仪器名称是
2
,写出该反应的离子方程式: 。则装置E中用于除气体杂质的试
剂是 (填写试剂名称)
③为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:a→d→c→ →
←j←i←h←g←b。
④证明氨气和氯气反应有岩脑砂生成,需要的检验试剂中,除了蒸馏水、稀HNO、NaOH溶液外,还需要
3
、 等两种;岩脑砂的主要成分中所含化学键的类型 、
、 。
(2)氨气和氯气反应制取岩脑砂时同时生成N。氨气和氯气反应生成N 的化学方程式是
2 2
。
(3)和氮元素同主族的砷存在多种同素异形体——黄砷、黑砷、灰砷。
①黄砷结构与白磷相似,黄砷的空间构型为 ,第三周期,第一电离能介于
Al和P之间的元素有 种。
②近年来,黑砷在催化电解水方面的研究受到关注,其晶体
结构与石墨类似。根据图中信息,下列说法正确的有
8
原创精品资源学科网独家享有版权,侵权必究!(填标号)。
a.黑砷中As—As键的键能均相同
b.黑砷与C 都属于混合型晶体
60
c.黑砷单层中As原子与As—As键的个数比为2:3
d.黑砷层与层之间的作用力为范德华力
18.二氧化碳利用技术已成为当今世界研究热点。回答下列问题:
(1)空气中CO2含量过高造成的环境问题是 。
(2)氢气还原二氧化碳是处理二氧化碳的方法之一,常见反应原理有
, 。
① 。
②在上述反应涉及的分子中,属于极性分子的有 。甲醇的沸点(64.7℃)高于二甲醚的
沸点(-29.5℃),原因是 °
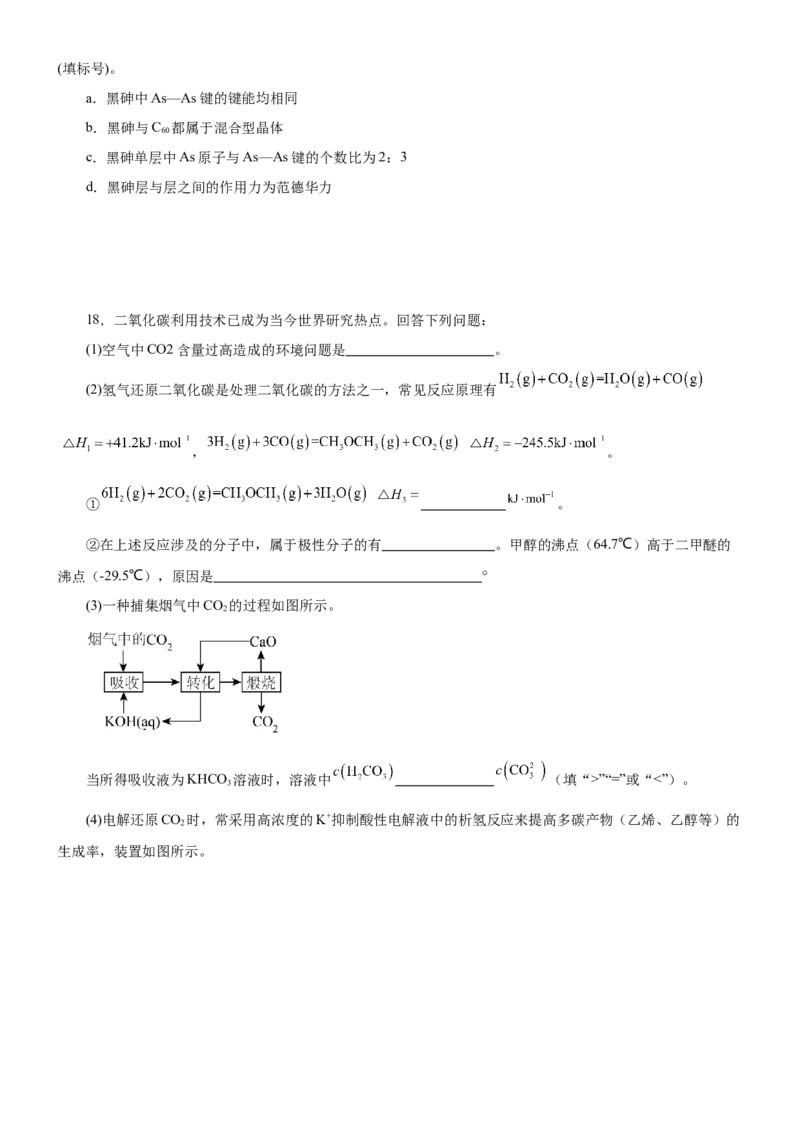
(3)一种捕集烟气中CO 的过程如图所示。
2
当所得吸收液为KHCO 溶液时,溶液中 (填“>”“=”或“<”)。
3
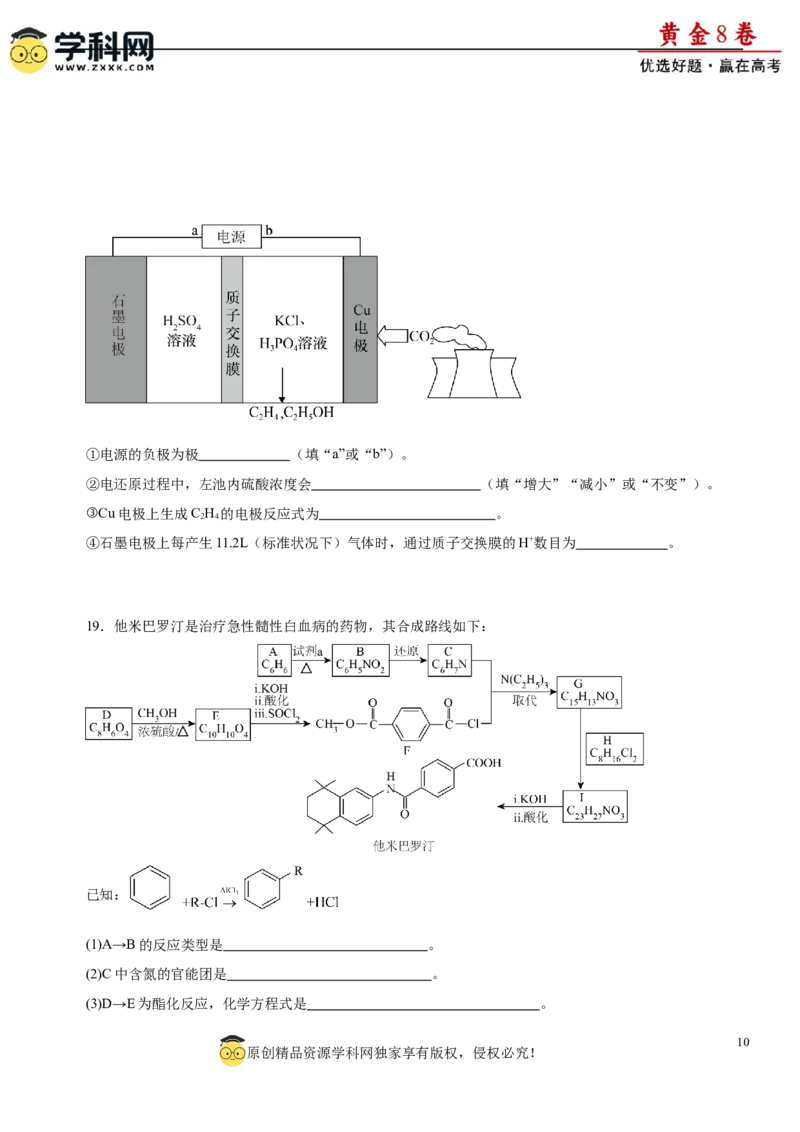
(4)电解还原CO 时,常采用高浓度的K+抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的
2
生成率,装置如图所示。①电源的负极为极 (填“a”或“b”)。
②电还原过程中,左池内硫酸浓度会 (填“增大”“减小”或“不变”)。
③Cu电极上生成C H 的电极反应式为 。
2 4
④石墨电极上每产生11.2L(标准状况下)气体时,通过质子交换膜的H+数目为 。
19.他米巴罗汀是治疗急性髓性白血病的药物,其合成路线如下:
已知:
(1)A→B的反应类型是 。
(2)C中含氮的官能团是 。
(3)D→E为酯化反应,化学方程式是 。
10
原创精品资源学科网独家享有版权,侵权必究!(4)C和F反应得到G为可逆反应,推测N(C H)(一种有机碱)的作用是 。
2 5 3
(5)I的结构简式是 。
(6)H是制他米巴罗汀的重要中间体,以C H 为原料合成H的路线如下:
2 2
已:
①试剂b的结构简式是 。
②N→H的化学方程式是 。