文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷07
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cr 52 Fe 56 Pb 106
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. “逐梦苍穹之上,拥抱星辰大海”,航天科技的发展与化学密切相关。下列选项正确的是
A.“北斗三号”导航卫星搭载计时铷原子钟,铷是第ⅠA族元素
B.“嫦娥五号”探测器配置砷化镓太阳能电池,太阳能电池将化学能直接转化为电能
C.“祝融号”火星车利用正十一烷储能,正十一烷属于不饱和烃
D.“神舟十三号”航天员使用塑料航天面窗,塑料属于无机非金属材料
2.化学实验是化学探究的一种重要途径。下列有关实验的描述正确的是
A.用湿润的蓝色石蕊试纸检验
B.中学实验室中,可将未用完的钠放回原试剂瓶
C.进行焰色试验时,可用玻璃棒替代铂丝
D.酸碱中和滴定实验中,应先用待测液润洗锥形瓶
3.对于下列实验,能正确描述其反应的离子方程式是
A.将闪锌矿浸没在足量的蓝矾溶液:ZnS+Cu2+=CuS+Zn2+
B.向小苏打溶液中滴加少量苛性钠溶液:HCO +OH-=H O+CO↑
2 2
C.用醋酸溶液处理水垢中的碳酸钙:CaCO +2H+=Ca2++H O+CO↑
3 2 2
D.向明矾溶液中加入过量的氨水:Al3++4NH•H O=AlO +4NH +2H O
3 2 2
4.植物对氮元素的吸收过程如下,下列说法正确的是
A.高温有利于加快过程① B.浇水和松土有利于过程②
C.过程③中 被还原 D.过程④叫做氮的固定
5.用 表示阿伏加德罗常数的值。下列说法正确的是
A.常温下, 铁与足量浓硝酸充分反应转移的电子数为
B. 溶于足量的水充分反应转移的电子数为
C.标准状况下, 所含原子数为
D. 与 反应时,转移电子的数目为6.科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元
素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前
者的一种核素为 。下列有关叙述正确的是
A.核素 的质量数为288 B.核素 的质量数与中子数之差为173
C.113号元素属于非金属元素 D.115号元素的最高正化合价是
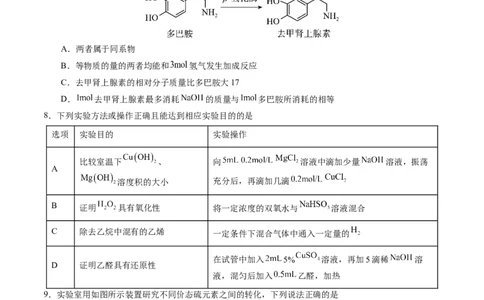
7.我们所感受的各种情绪从本质上讲都是一种化学体验,多巴胺和去甲肾上腺素均属于神经递质。下列
有关两者说法正确的是
A.两者属于同系物
B.等物质的量的两者均能和 氢气发生加成反应
C.去甲肾上腺素的相对分子质量比多巴胺大17
D. 去甲肾上腺素最多消耗 的质量与 多巴胺所消耗的相等
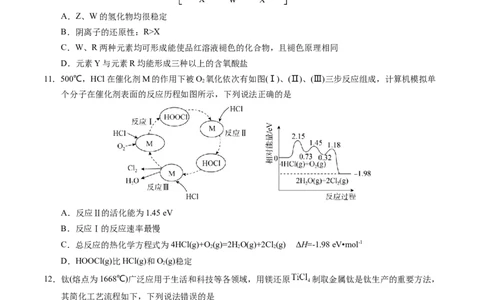
8.下列实验方法或操作正确且能达到相应实验目的的是
选项 实验目的 实验操作
比较室温下 、 向 溶液中滴加少量 溶液,振荡
A
溶度积的大小 充分后,再滴加几滴
B 证明 具有氧化性 将一定浓度的双氧水与 溶液混合
C 除去乙烷中混有的乙烯 一定条件下混合气体中通入一定量的
在试管中加入 5% 溶液,再加5滴稀 溶
D 证明乙醛具有还原性
液,混匀后加入 乙醛,加热
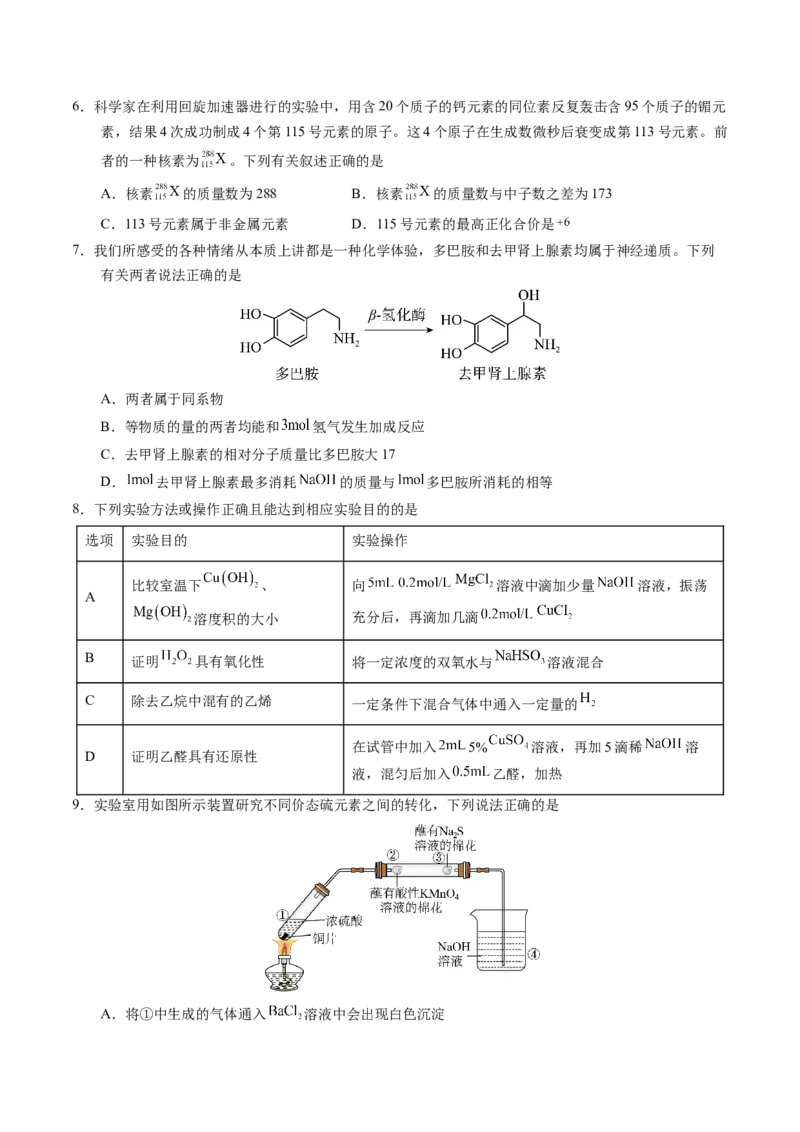
9.实验室用如图所示装置研究不同价态硫元素之间的转化,下列说法正确的是
A.将①中生成的气体通入 溶液中会出现白色沉淀B.②中棉花紫色褪去,体现 的还原性
C.③中有黄色固体生成,氧化剂与还原剂物质的量之比为1∶2
D.向④的小烧杯中加入少量苯可起到防倒吸作用
10.某化合物(结构如图所示)是一种家用杀虫剂。X、Y、Z、W、R为原子序数逐渐增大的短周期元素,Z
与R不在同一周期。下列叙述正确的是
A.Z、W的氢化物均很稳定
B.阴离子的还原性:R>X
C.W、R两种元素均可形成能使品红溶液褪色的化合物,且褪色原理相同
D.元素Y与元素R均能形成三种以上的含氧酸盐
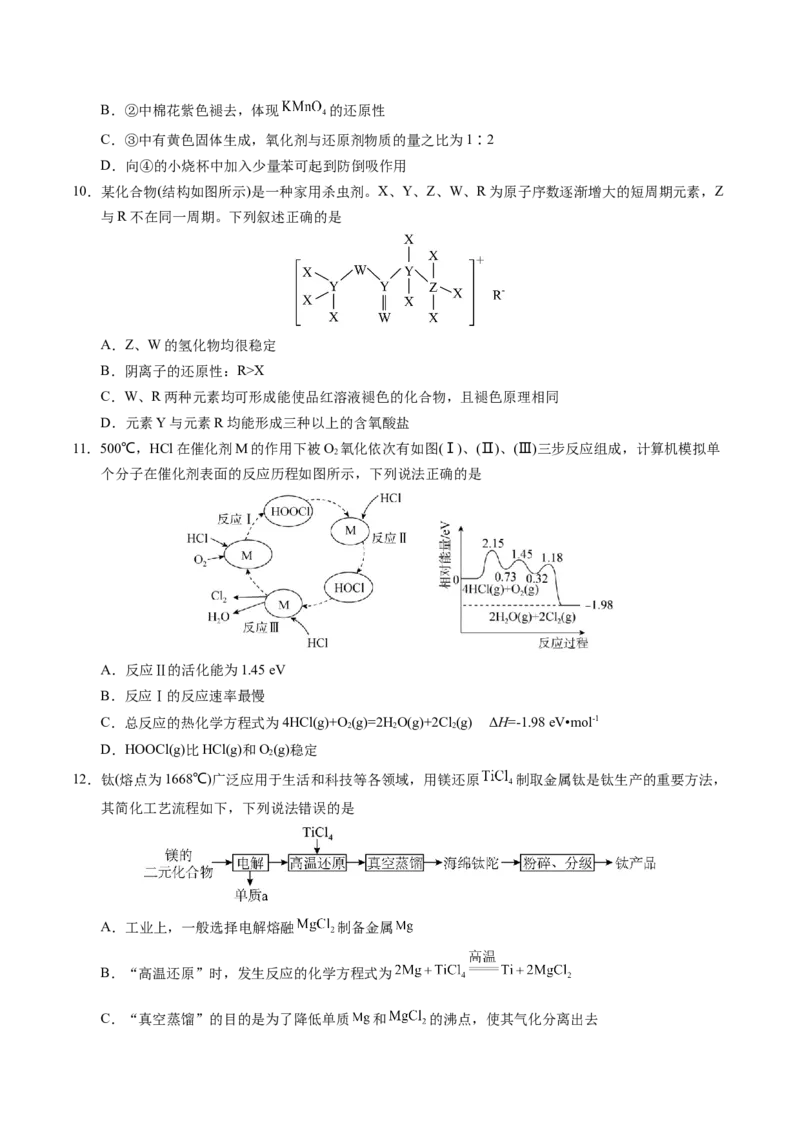
11.500℃,HCl在催化剂M的作用下被O 氧化依次有如图(Ⅰ)、(Ⅱ)、(Ⅲ)三步反应组成,计算机模拟单
2
个分子在催化剂表面的反应历程如图所示,下列说法正确的是
A.反应Ⅱ的活化能为1.45 eV
B.反应Ⅰ的反应速率最慢
C.总反应的热化学方程式为4HCl(g)+O (g)=2HO(g)+2Cl (g) ΔH=-1.98 eV•mol-1
2 2 2
D.HOOCl(g)比HCl(g)和O(g)稳定
2
12.钛(熔点为1668℃)广泛应用于生活和科技等各领域,用镁还原 制取金属钛是钛生产的重要方法,
其简化工艺流程如下,下列说法错误的是
A.工业上,一般选择电解熔融 制备金属
B.“高温还原”时,发生反应的化学方程式为
C.“真空蒸馏”的目的是为了降低单质 和 的沸点,使其气化分离出去D.“电解”时,阴极上生成单质a,可用作其他联产过程的氧化剂
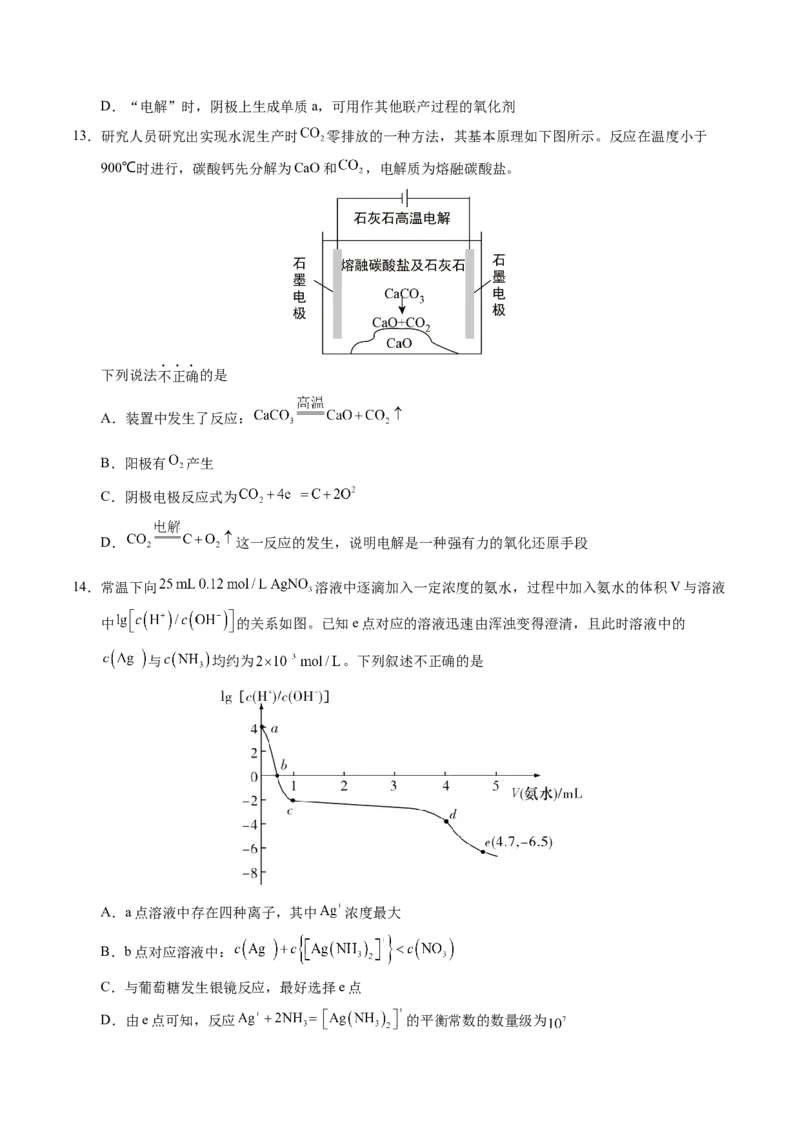
13.研究人员研究出实现水泥生产时 零排放的一种方法,其基本原理如下图所示。反应在温度小于
900℃时进行,碳酸钙先分解为CaO和 ,电解质为熔融碳酸盐。
下列说法不正确的是
A.装置中发生了反应:
B.阳极有 产生
C.阴极电极反应式为
D. 这一反应的发生,说明电解是一种强有力的氧化还原手段
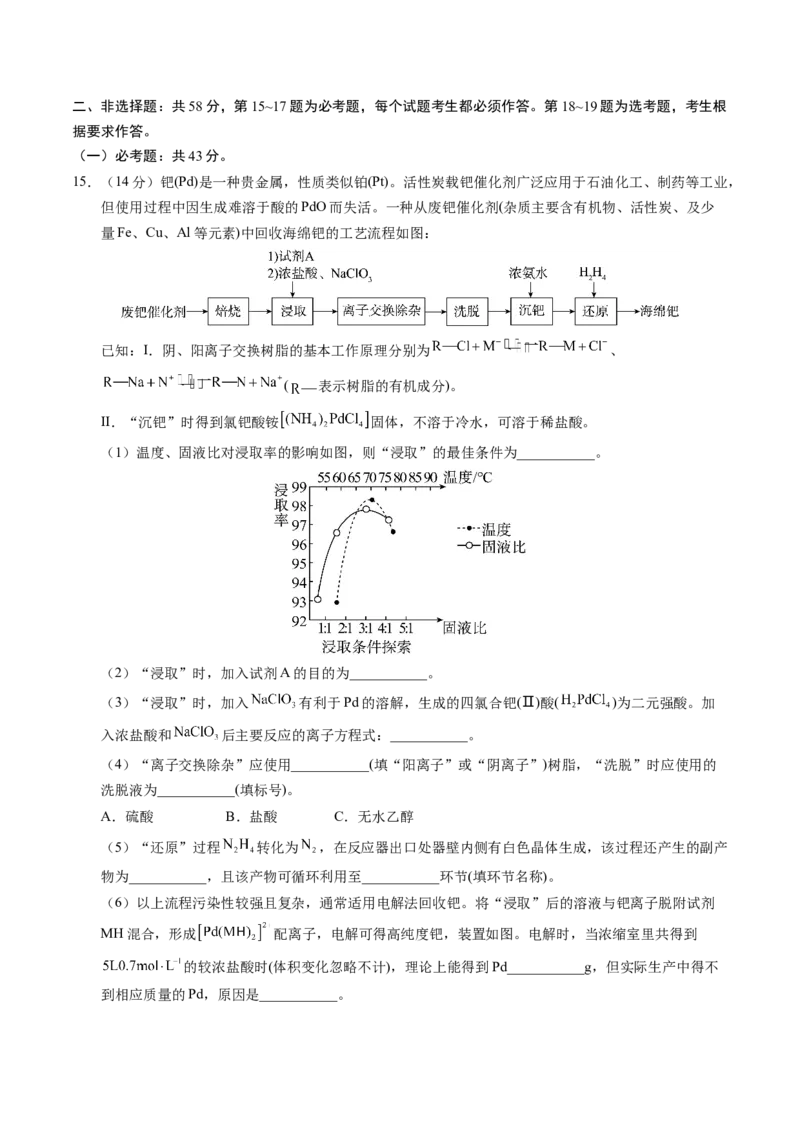
14.常温下向 溶液中逐滴加入一定浓度的氨水,过程中加入氨水的体积V与溶液
中 的关系如图。已知e点对应的溶液迅速由浑浊变得澄清,且此时溶液中的
与 均约为 。下列叙述不正确的是
A.a点溶液中存在四种离子,其中 浓度最大
B.b点对应溶液中:
C.与葡萄糖发生银镜反应,最好选择e点
D.由e点可知,反应 的平衡常数的数量级为二、非选择题:共58分,第15~17题为必考题,每个试题考生都必须作答。第18~19题为选考题,考生根
据要求作答。
(一)必考题:共43分。
15.(14分)钯(Pd)是一种贵金属,性质类似铂(Pt)。活性炭载钯催化剂广泛应用于石油化工、制药等工业,
但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有机物、活性炭、及少
量Fe、Cu、Al等元素)中回收海绵钯的工艺流程如图:
已知:I.阴、阳离子交换树脂的基本工作原理分别为 、
( 表示树脂的有机成分)。
II.“沉钯”时得到氯钯酸铵 固体,不溶于冷水,可溶于稀盐酸。
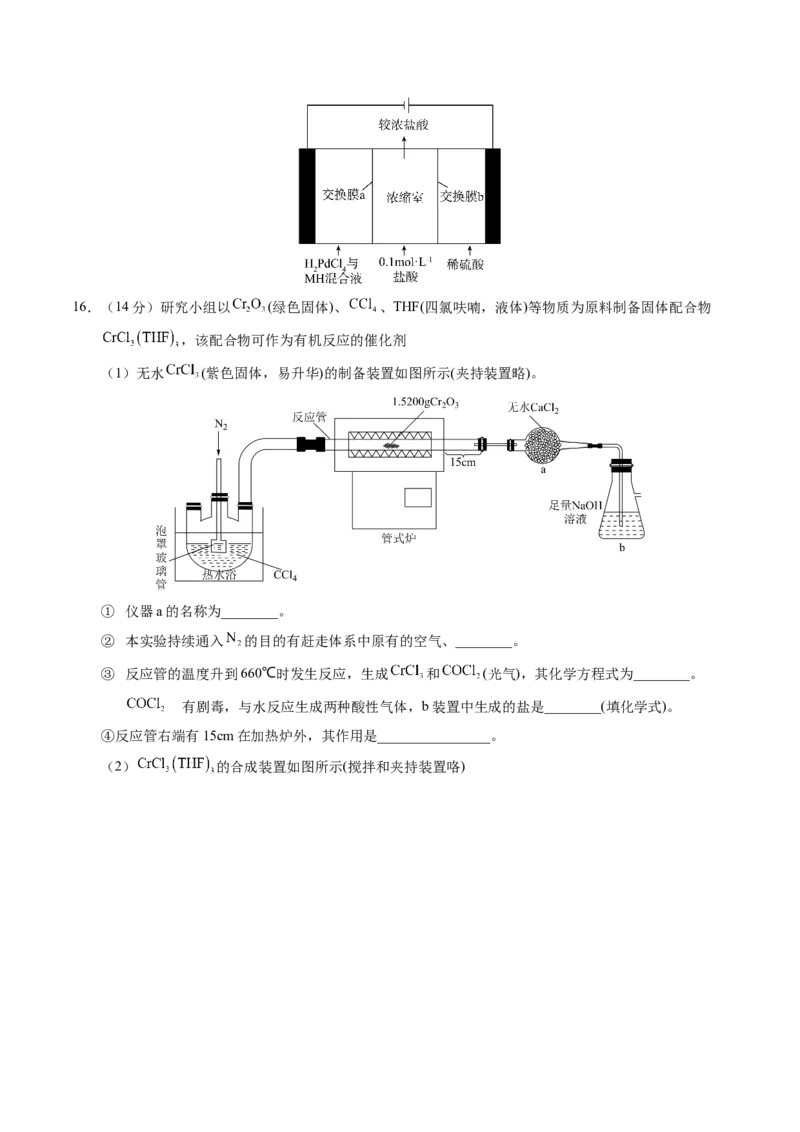
(1)温度、固液比对浸取率的影响如图,则“浸取”的最佳条件为___________。
(2)“浸取”时,加入试剂A的目的为___________。
(3)“浸取”时,加入 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加
入浓盐酸和 后主要反应的离子方程式:___________。
(4)“离子交换除杂”应使用___________(填“阳离子”或“阴离子”)树脂,“洗脱”时应使用的
洗脱液为___________(填标号)。
A.硫酸 B.盐酸 C.无水乙醇
(5)“还原”过程 转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产
物为___________,且该产物可循环利用至___________环节(填环节名称)。
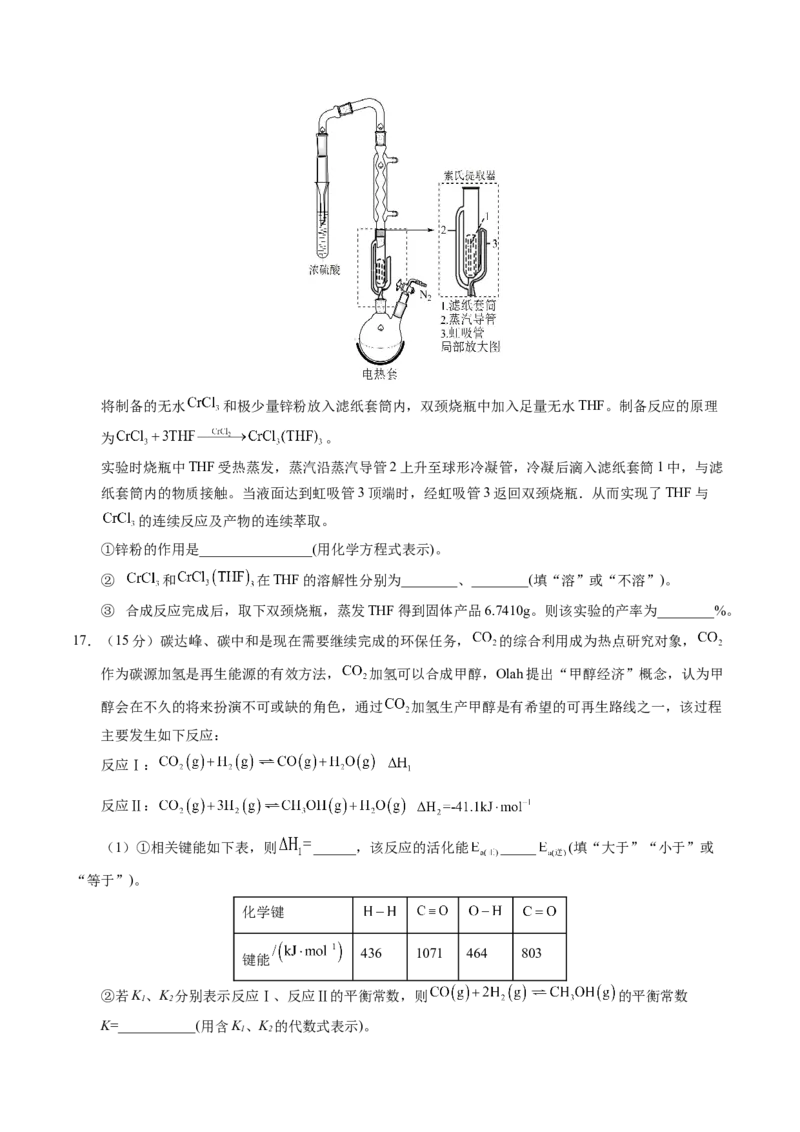
(6)以上流程污染性较强且复杂,通常适用电解法回收钯。将“浸取”后的溶液与钯离子脱附试剂
MH混合,形成 配离子,电解可得高纯度钯,装置如图。电解时,当浓缩室里共得到
的较浓盐酸时(体积变化忽略不计),理论上能得到Pd___________g,但实际生产中得不
到相应质量的Pd,原因是___________。16.(14分)研究小组以 (绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
① 仪器a的名称为________。
② 本实验持续通入 的目的有赶走体系中原有的空气、________。
③ 反应管的温度升到660℃时发生反应,生成 和 (光气),其化学方程式为________。
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________(填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________。
(2) 的合成装置如图所示(搅拌和夹持装置咯)将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理
为 。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤
纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与
的连续反应及产物的连续萃取。
①锌粉的作用是________________(用化学方程式表示)。
② 和 在THF的溶解性分别为________、________(填“溶”或“不溶”)。
③ 合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________%。
17.(15分)碳达峰、碳中和是现在需要继续完成的环保任务, 的综合利用成为热点研究对象,
作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,Olah提出“甲醇经济”概念,认为甲
醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程
主要发生如下反应:
反应Ⅰ:
反应Ⅱ:
(1)①相关键能如下表,则 ______,该反应的活化能 _____ (填“大于”“小于”或
“等于”)。
化学键
436 1071 464 803
键能
②若K 、K 分别表示反应Ⅰ、反应Ⅱ的平衡常数,则 的平衡常数
1 2
K=___________(用含K 、K 的代数式表示)。
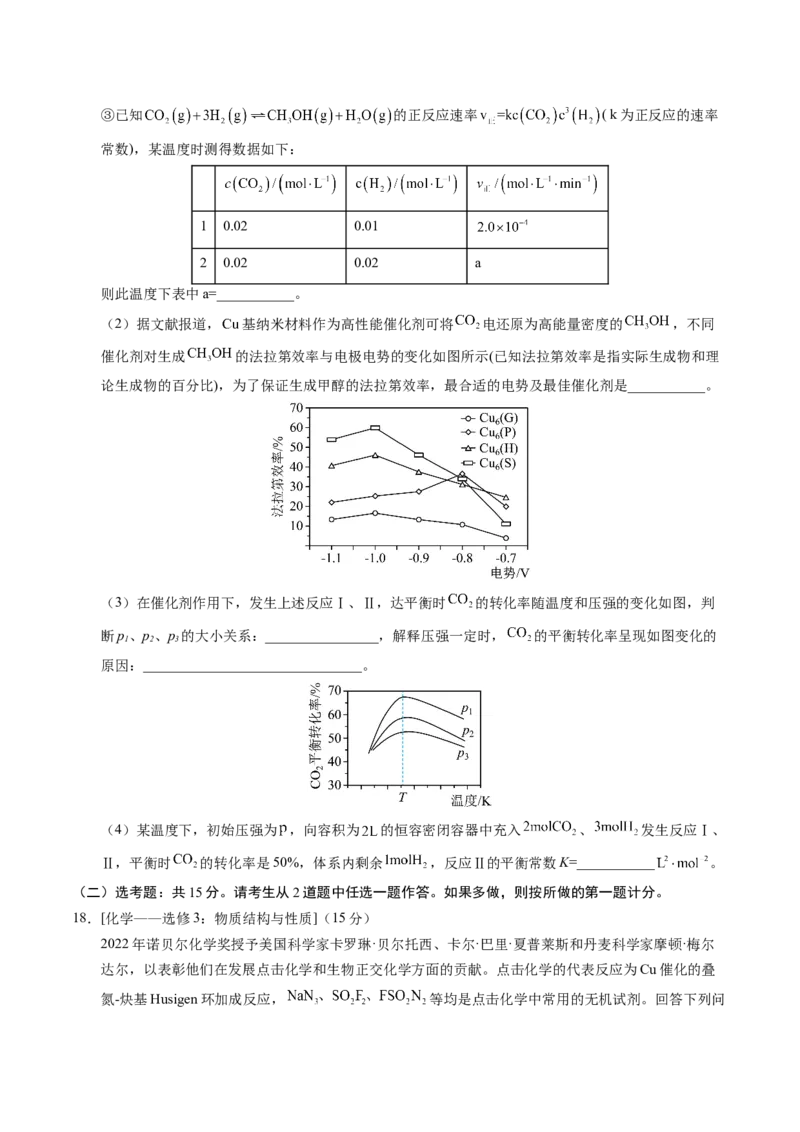
1 2③已知 的正反应速率 ( k为正反应的速率
常数),某温度时测得数据如下:
1 0.02 0.01
2 0.02 0.02 a
则此温度下表中a=___________。
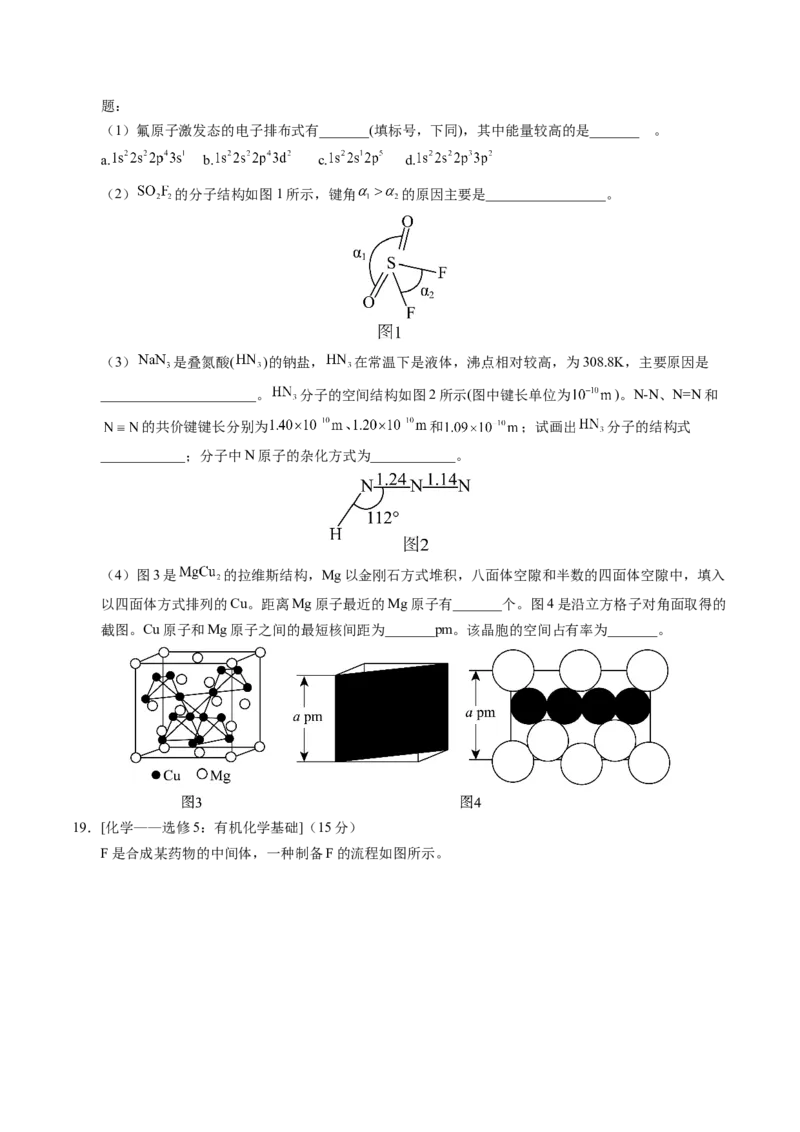
(2)据文献报道, 基纳米材料作为高性能催化剂可将 电还原为高能量密度的 ,不同
催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理
论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是___________。
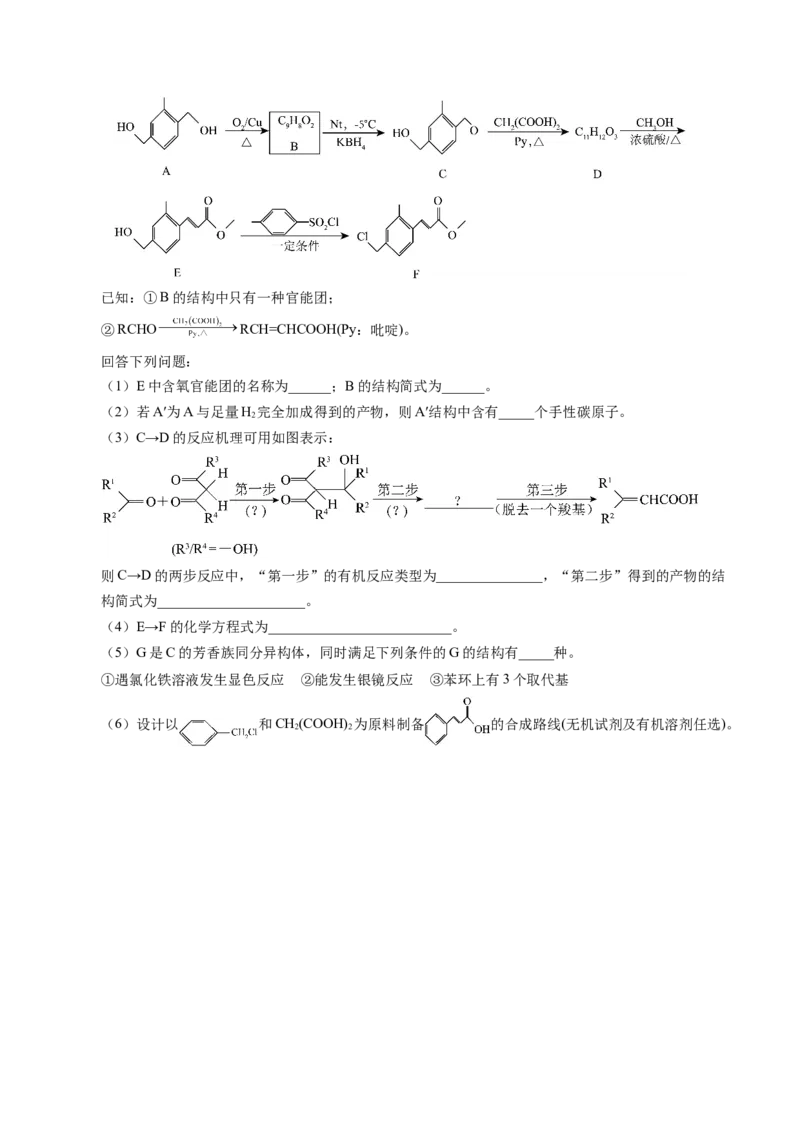
(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时 的转化率随温度和压强的变化如图,判
断p、p、p 的大小关系:________________,解释压强一定时, 的平衡转化率呈现如图变化的
1 2 3
原因:_______________________________。
(4)某温度下,初始压强为 ,向容积为 的恒容密闭容器中充入 、 发生反应Ⅰ、
Ⅱ,平衡时 的转化率是50%,体系内剩余 ,反应Ⅱ的平衡常数K=___________ 。
(二)选考题:共15分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。
18.[化学——选修3:物质结构与性质](15分)
2022年诺贝尔化学奖授予美国科学家卡罗琳·贝尔托西、卡尔·巴里·夏普莱斯和丹麦科学家摩顿·梅尔
达尔,以表彰他们在发展点击化学和生物正交化学方面的贡献。点击化学的代表反应为Cu催化的叠
氮-炔基Husigen环加成反应, 等均是点击化学中常用的无机试剂。回答下列问题:
(1)氟原子激发态的电子排布式有_______(填标号,下同),其中能量较高的是_______ 。
a. b. c. d.
(2) 的分子结构如图1所示,键角 的原因主要是_________________。
(3) 是叠氮酸( )的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
______________________。 分子的空间结构如图2所示(图中键长单位为 )。N-N、N=N和
的共价键键长分别为 和 ;试画出 分子的结构式
____________;分子中N原子的杂化方式为____________。
(4)图3是 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入
以四面体方式排列的Cu。距离Mg原子最近的Mg原子有_______个。图4是沿立方格子对角面取得的
截图。Cu原子和Mg原子之间的最短核间距为_______pm。该晶胞的空间占有率为_______。
19.[化学——选修5:有机化学基础](15分)
F是合成某药物的中间体,一种制备F的流程如图所示。已知:①B的结构中只有一种官能团;
②RCHO RCH=CHCOOH(Py:吡啶)。
回答下列问题:
(1)E中含氧官能团的名称为______;B的结构简式为______。
(2)若A′为A与足量H 完全加成得到的产物,则A′结构中含有_____个手性碳原子。
2
(3)C→D的反应机理可用如图表示:
则C→D的两步反应中,“第一步”的有机反应类型为_______________,“第二步”得到的产物的结
构简式为_____________________。
(4)E→F的化学方程式为__________________________。
(5)G是C的芳香族同分异构体,同时满足下列条件的G的结构有_____种。
①遇氯化铁溶液发生显色反应 ②能发生银镜反应 ③苯环上有3个取代基
(6)设计以 和CH(COOH) 为原料制备 的合成路线(无机试剂及有机溶剂任选)。
2 2