文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷07
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cr 52 Fe 56 Pb 106
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. “逐梦苍穹之上,拥抱星辰大海”,航天科技的发展与化学密切相关。下列选项正确的是
A.“北斗三号”导航卫星搭载计时铷原子钟,铷是第ⅠA族元素
B.“嫦娥五号”探测器配置砷化镓太阳能电池,太阳能电池将化学能直接转化为电能
C.“祝融号”火星车利用正十一烷储能,正十一烷属于不饱和烃
D.“神舟十三号”航天员使用塑料航天面窗,塑料属于无机非金属材料
【答案】A
【解析】A.铷是碱金属,位于第ⅠA族,故A正确;
B.太阳能电池是将太阳能转化为电能,故B错误;
C.正十一烷属于饱和烃,故C错误;
D.塑料属于有机合成材料,故D错误;
故选A。
2.化学实验是化学探究的一种重要途径。下列有关实验的描述正确的是
A.用湿润的蓝色石蕊试纸检验
B.中学实验室中,可将未用完的钠放回原试剂瓶
C.进行焰色试验时,可用玻璃棒替代铂丝
D.酸碱中和滴定实验中,应先用待测液润洗锥形瓶
【答案】B
【解析】A. 溶于水呈碱性,可以用湿润的红色石蕊试纸检验 ,故A错误;
B.易燃物如钠、钾等不能随便丟弃,中学实验室可以将未用完的钠、钾等放回原试剂瓶,故B正确;
C.玻璃的成分里边有硅酸钠,钠盐的焰色试验为黄色,对其他元素的试验存在干扰,进行焰色试验时,
不可用玻璃棒替代铂丝,故C错误;
D.酸碱中和滴定实验中,洗锥形不能用待测液润洗,否则会导致测量结构偏大,故D错误;
故选B。
3.对于下列实验,能正确描述其反应的离子方程式是
A.将闪锌矿浸没在足量的蓝矾溶液:ZnS+Cu2+=CuS+Zn2+
B.向小苏打溶液中滴加少量苛性钠溶液:HCO +OH-=H O+CO↑
2 2C.用醋酸溶液处理水垢中的碳酸钙:CaCO +2H+=Ca2++H O+CO↑
3 2 2
D.向明矾溶液中加入过量的氨水:Al3++4NH•H O=AlO +4NH +2H O
3 2 2
【答案】A
【解析】A.CuS比ZnS难溶,将闪锌矿浸没在足量的蓝矾溶液中,发生沉淀的转化,反应的离子方程式
为ZnS+Cu2+=CuS+Zn2+,故A正确;
B.向小苏打溶液中滴加少量苛性钠溶液反应生成碳酸钠和水,反应的离子方程式为
,故B错误;
C.醋酸为弱酸,应保留化学式,正确的离子方程式为 ,
故C错误;
D.Al(OH) 不溶于氨水,正确的离子方程式为 ,故D错误;
3
故选A。
4.植物对氮元素的吸收过程如下,下列说法正确的是
A.高温有利于加快过程① B.浇水和松土有利于过程②
C.过程③中 被还原 D.过程④叫做氮的固定
【答案】B
【解析】A.过程①有根瘤菌参与催化,不能高温下进行,A错误;
B.过程②是 和O 反应生成 ,浇水和松土有利于过程②的反应,B正确;
2
C.过程③中 转化为NO ,N的化合价由+3价升高到+5价, 作还原剂被氧化,C错误;
D.氮的固定是将空气中游离态的氮转化为含氮化合物的过程,过程④是氮的化合物中氮的转变,D错误;
故答案为:B。
5.用 表示阿伏加德罗常数的值。下列说法正确的是
A.常温下, 铁与足量浓硝酸充分反应转移的电子数为
B. 溶于足量的水充分反应转移的电子数为
C.标准状况下, 所含原子数为
D. 与 反应时,转移电子的数目为
【答案】D
【解析】A.常温下,铁遇浓硝酸钝化,A错误;
B. 与水不能完全反应,存在化学平衡,转移电子数不足1mol,B错误;
C.标准状况下, 是固体,C错误;
D.碘离子的还原性比亚铁离子强,碘离子先与氯气反应, 中含 , 与恰好完全反应生成 和 ,转移电子 ,电子数为 ,D正确;
故选D。
6.科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元
素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前
者的一种核素为 。下列有关叙述正确的是
A.核素 的质量数为288 B.核素 的质量数与中子数之差为173
C.113号元素属于非金属元素 D.115号元素的最高正化合价是
【答案】A
【分析】核素的表示方法为:元素符号左下角为质子数,左上角为质量数;
【解析】A.核素 的质量数为288,A项正确;
B.核素 的中子数为288-115=173,核素 的质量数与中子数之差为288-173=115,B项错误;
C.113号元素与B元素位于同一主族,该族元素从Al开始为金属元素,所以113号元素属于金属元素,C
项错误;
D.115号元素位于第ⅤA族,最外层有5个电子,最高价为+5价,D项错误;
故选A。
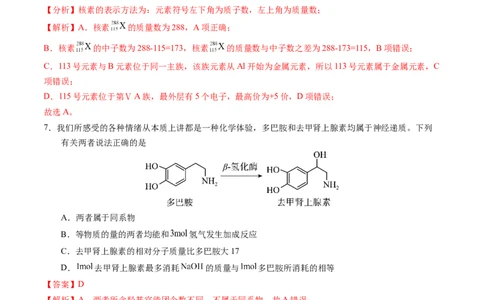
7.我们所感受的各种情绪从本质上讲都是一种化学体验,多巴胺和去甲肾上腺素均属于神经递质。下列
有关两者说法正确的是
A.两者属于同系物
B.等物质的量的两者均能和 氢气发生加成反应
C.去甲肾上腺素的相对分子质量比多巴胺大17
D. 去甲肾上腺素最多消耗 的质量与 多巴胺所消耗的相等
【答案】D
【解析】A.两者所含羟基官能团个数不同,不属于同系物,故A错误;
B.两者的物质的量不确定,不能确定加成氢气的物质的量,故B错误;
C.去甲肾上腺素比多巴胺多一个氧原子,相对分子质量多16,故C错误;
D.两者均只有酚羟基与NaOH反应,1mol中均含2mol酚羟基,消耗2molNaOH,故D正确;
故选:D。
8.下列实验方法或操作正确且能达到相应实验目的的是
选项 实验目的 实验操作
A
比较室温下 、 向 溶液中滴加少量 溶液,振荡溶度积的大小 充分后,再滴加几滴
B 证明 具有氧化性 将一定浓度的双氧水与 溶液混合
C 除去乙烷中混有的乙烯 一定条件下混合气体中通入一定量的
在试管中加入 5% 溶液,再加5滴稀 溶
D 证明乙醛具有还原性
液,混匀后加入 乙醛,加热
【答案】A
【解析】A.向5mL0.2mol/LMgCl 溶液中滴加少量NaOH溶液,氢氧化钠全部转化成氢氧化镁,振荡充分
2
后,再滴加几滴0.2mol/LCuCl 溶液,如果白色沉淀转化成蓝色沉淀,说明氢氧化镁的溶度积大于氢氧化铜
2
的溶度积,故A正确;
B.过氧化氢与亚硫酸钠反应,利用过氧化氢的氧化性,将HSO 氧化成SO ,本身被还原成水,因为该
反应没有明显现象,因此无法判断是否发生反应,故B错误;
C.乙烯虽然与氢气发生加成反应生成乙烷,但氢气为气体,且无色,如果通入氢气过量,引入新的杂质,
一般通过溴水中,除去乙烷中的乙烯,故C错误;
D.乙醛与新制氢氧化铜悬浊液反应,NaOH需要过量,题中所给氢氧化钠不足,故D错误;
答案为A。
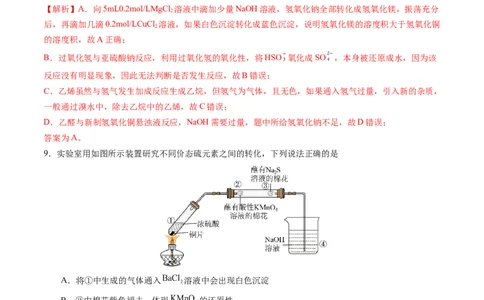
9.实验室用如图所示装置研究不同价态硫元素之间的转化,下列说法正确的是
A.将①中生成的气体通入 溶液中会出现白色沉淀
B.②中棉花紫色褪去,体现 的还原性
C.③中有黄色固体生成,氧化剂与还原剂物质的量之比为1∶2
D.向④的小烧杯中加入少量苯可起到防倒吸作用
【答案】C
【解析】A. 不能与 反应,不会出现白色沉淀,选项A错误;
B. 与 反应, 被还原,体现 的氧化性,选项B错误;
C.③中 与 反应有黄色固体硫生成, 作氧化剂, 作还原剂,氧化剂与还原剂物质的量之比
为1∶2,选项C正确;D.苯的密度比NaOH溶液小,苯在上层,不能起到防倒吸的效果,选项D错误;
答案选C。
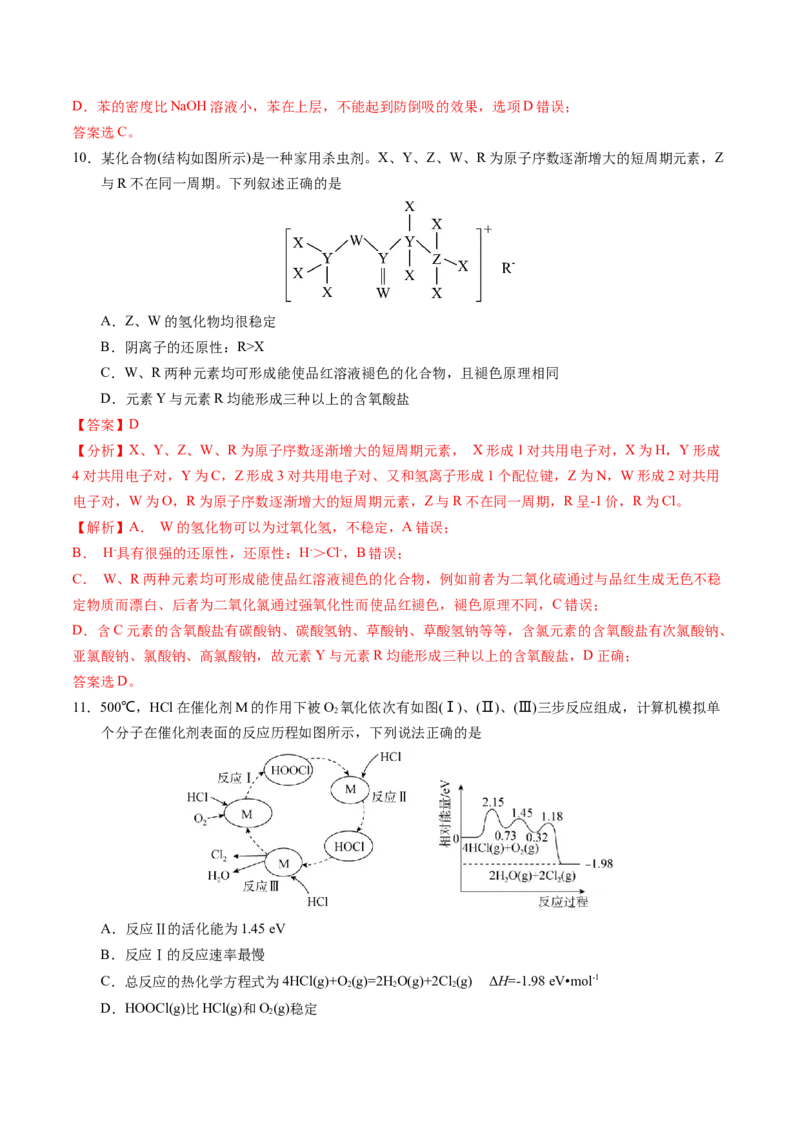
10.某化合物(结构如图所示)是一种家用杀虫剂。X、Y、Z、W、R为原子序数逐渐增大的短周期元素,Z
与R不在同一周期。下列叙述正确的是
A.Z、W的氢化物均很稳定
B.阴离子的还原性:R>X
C.W、R两种元素均可形成能使品红溶液褪色的化合物,且褪色原理相同
D.元素Y与元素R均能形成三种以上的含氧酸盐
【答案】D
【分析】X、Y、Z、W、R为原子序数逐渐增大的短周期元素, X形成1对共用电子对,X为H,Y形成
4对共用电子对,Y为C,Z形成3对共用电子对、又和氢离子形成1个配位键,Z为N,W形成2对共用
电子对,W为O,R为原子序数逐渐增大的短周期元素,Z与R不在同一周期,R呈-1价,R为Cl。
【解析】A. W的氢化物可以为过氧化氢,不稳定,A错误;
B. H-具有很强的还原性,还原性:H->Cl-,B错误;
C. W、R两种元素均可形成能使品红溶液褪色的化合物,例如前者为二氧化硫通过与品红生成无色不稳
定物质而漂白、后者为二氧化氯通过强氧化性而使品红褪色,褪色原理不同,C错误;
D.含C元素的含氧酸盐有碳酸钠、碳酸氢钠、草酸钠、草酸氢钠等等,含氯元素的含氧酸盐有次氯酸钠、
亚氯酸钠、氯酸钠、高氯酸钠,故元素Y与元素R均能形成三种以上的含氧酸盐,D正确;
答案选D。
11.500℃,HCl在催化剂M的作用下被O 氧化依次有如图(Ⅰ)、(Ⅱ)、(Ⅲ)三步反应组成,计算机模拟单
2
个分子在催化剂表面的反应历程如图所示,下列说法正确的是
A.反应Ⅱ的活化能为1.45 eV
B.反应Ⅰ的反应速率最慢
C.总反应的热化学方程式为4HCl(g)+O (g)=2HO(g)+2Cl (g) ΔH=-1.98 eV•mol-1
2 2 2
D.HOOCl(g)比HCl(g)和O(g)稳定
2【答案】B
【解析】A.反应Ⅱ的活化能为 ,A错误;
B.反应Ⅰ的能垒最高,所以反应Ⅰ的化学反应速率最慢,B正确;
C.图像给出的是单个分子参与反应时的能量变化,总反应的热化学方程式为
,C错误;
D.由反应Ⅰ可知 的总能量比 和 的总能量高,能量越高,物质越不稳定,D错误;
故选B。
12.钛(熔点为1668℃)广泛应用于生活和科技等各领域,用镁还原 制取金属钛是钛生产的重要方法,
其简化工艺流程如下,下列说法错误的是
A.工业上,一般选择电解熔融 制备金属
B.“高温还原”时,发生反应的化学方程式为
C.“真空蒸馏”的目的是为了降低单质 和 的沸点,使其气化分离出去
D.“电解”时,阴极上生成单质a,可用作其他联产过程的氧化剂
【答案】D
【分析】工业生产一般采用电解熔融 的方法制镁,则a为氯气,所得Mg通过“高温还原” 、
发生反应 制取金属钛,再经过真空蒸馏提纯钛等步骤得到钛产品。
【解析】A.由于 的熔点高,电解 制备金属 能耗大,工业生产一般采用电解熔融 的方
法,A项正确;
B.还原时,发生反应的化学方程式为 ,B项正确;
C.真空蒸馏时,需要将金属 、 分离除去,由于金属钛的熔点很高,因此真空蒸馏的目的是为了
降低单质 和 的沸点,C项正确;
D.工业生产中,阳极上发生反应为: , 可用作其他联产过程的氧化剂,D项错误;
答案选D。13.研究人员研究出实现水泥生产时 零排放的一种方法,其基本原理如下图所示。反应在温度小于
900℃时进行,碳酸钙先分解为CaO和 ,电解质为熔融碳酸盐。
下列说法不正确的是
A.装置中发生了反应:
B.阳极有 产生
C.阴极电极反应式为
D. 这一反应的发生,说明电解是一种强有力的氧化还原手段
【答案】C
【解析】A.根据题目,反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO,所以发生反应:
2
,故A正确;
B.阳极的电极反应时碳酸根离子失电子生成氧气的过程,电极反应为: ↑,故B
正确;
C.阴极是二氧化碳得到电子生成碳,依据电子守恒和传导离子配平书写电极反应为:
,故C错误;
D. 这一反应的发生,说明电解是一种强有力的氧化还原手段,可以让不能自发进行的
反应发生,故D正确;
选C。
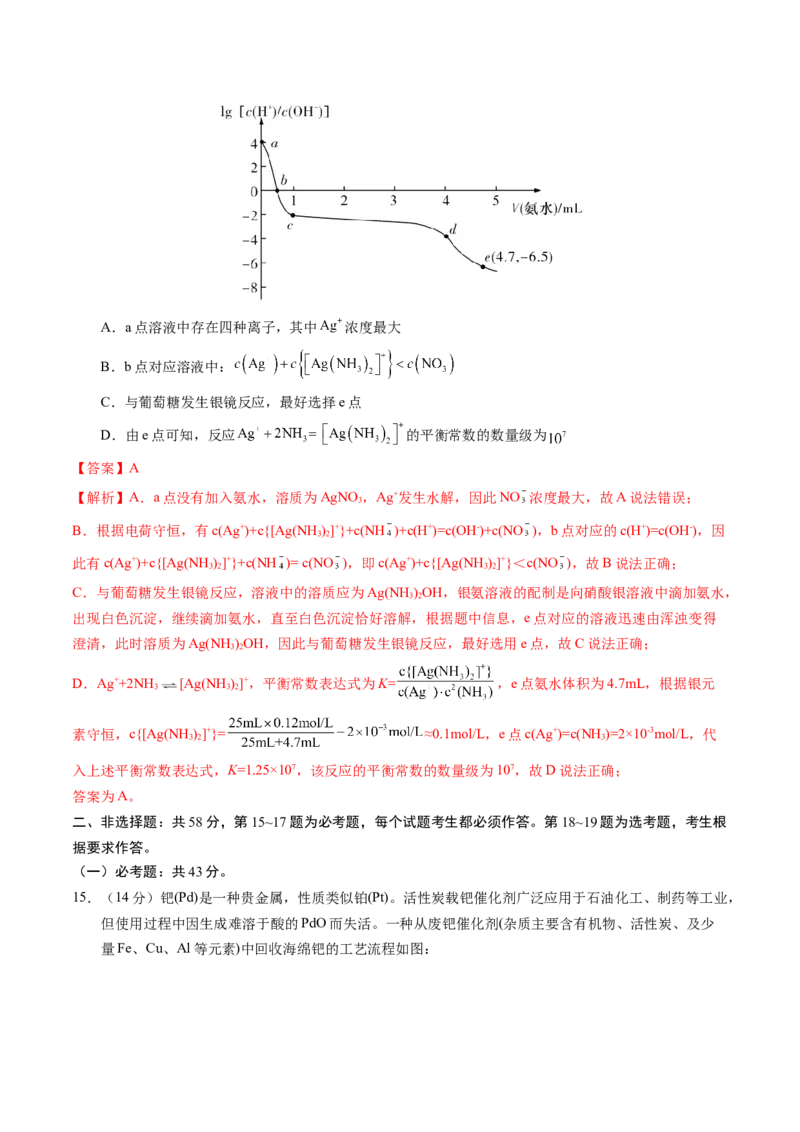
14.常温下向 溶液中逐滴加入一定浓度的氨水,过程中加入氨水的体积V与溶液
中 的关系如图。已知e点对应的溶液迅速由浑浊变得澄清,且此时溶液中的
与 均约为 。下列叙述不正确的是A.a点溶液中存在四种离子,其中 浓度最大
B.b点对应溶液中:
C.与葡萄糖发生银镜反应,最好选择e点
D.由e点可知,反应 的平衡常数的数量级为
【答案】A
【解析】A.a点没有加入氨水,溶质为AgNO,Ag+发生水解,因此NO 浓度最大,故A说法错误;
3
B.根据电荷守恒,有c(Ag+)+c{[Ag(NH )]+}+c(NH )+c(H+)=c(OH-)+c(NO ),b点对应的c(H+)=c(OH-),因
3 2
此有c(Ag+)+c{[Ag(NH )]+}+c(NH )= c(NO ),即c(Ag+)+c{[Ag(NH )]+}<c(NO ),故B说法正确;
3 2 3 2
C.与葡萄糖发生银镜反应,溶液中的溶质应为Ag(NH)OH,银氨溶液的配制是向硝酸银溶液中滴加氨水,
3 2
出现白色沉淀,继续滴加氨水,直至白色沉淀恰好溶解,根据题中信息,e点对应的溶液迅速由浑浊变得
澄清,此时溶质为Ag(NH)OH,因此与葡萄糖发生银镜反应,最好选用e点,故C说法正确;
3 2
D.Ag++2NH [Ag(NH)]+,平衡常数表达式为K= ,e点氨水体积为4.7mL,根据银元
3 3 2
素守恒,c{[Ag(NH)]+}= ≈0.1mol/L,e点c(Ag+)=c(NH)=2×10-3mol/L,代
3 2 3
入上述平衡常数表达式,K=1.25×107,该反应的平衡常数的数量级为107,故D说法正确;
答案为A。
二、非选择题:共58分,第15~17题为必考题,每个试题考生都必须作答。第18~19题为选考题,考生根
据要求作答。
(一)必考题:共43分。
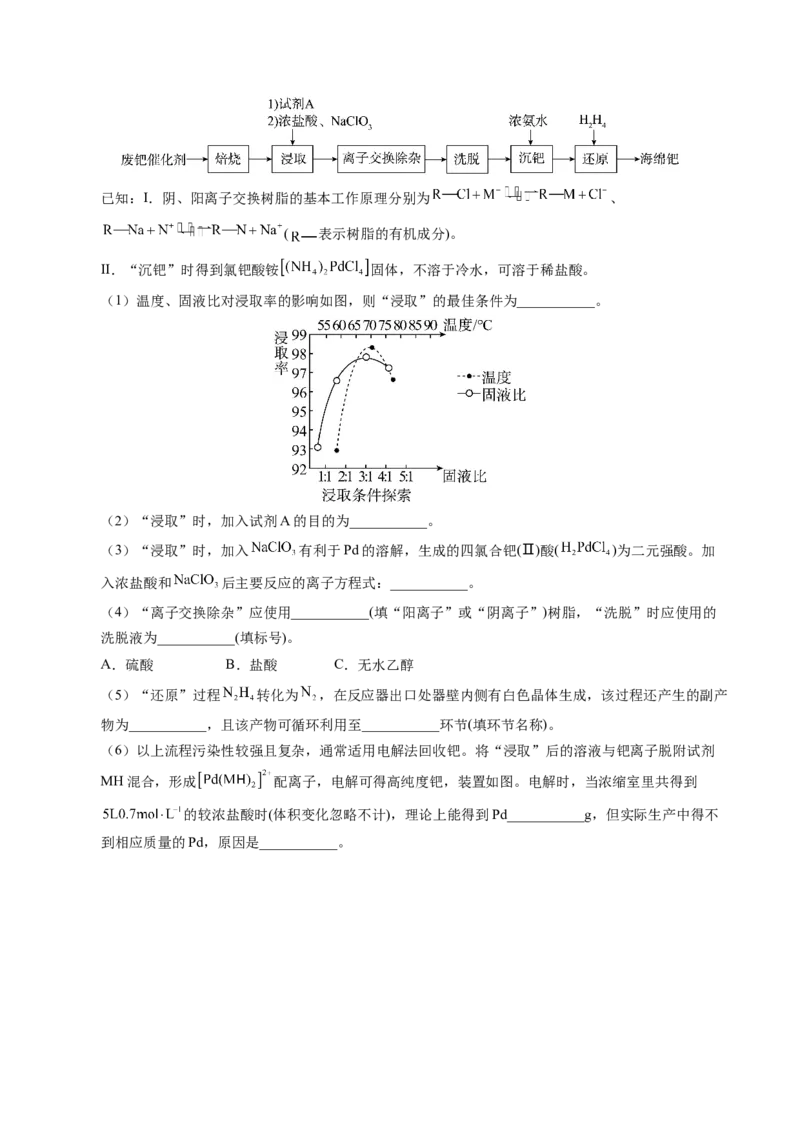
15.(14分)钯(Pd)是一种贵金属,性质类似铂(Pt)。活性炭载钯催化剂广泛应用于石油化工、制药等工业,
但使用过程中因生成难溶于酸的PdO而失活。一种从废钯催化剂(杂质主要含有机物、活性炭、及少
量Fe、Cu、Al等元素)中回收海绵钯的工艺流程如图:已知:I.阴、阳离子交换树脂的基本工作原理分别为 、
( 表示树脂的有机成分)。
II.“沉钯”时得到氯钯酸铵 固体,不溶于冷水,可溶于稀盐酸。
(1)温度、固液比对浸取率的影响如图,则“浸取”的最佳条件为___________。
(2)“浸取”时,加入试剂A的目的为___________。
(3)“浸取”时,加入 有利于Pd的溶解,生成的四氯合钯(Ⅱ)酸( )为二元强酸。加
入浓盐酸和 后主要反应的离子方程式:___________。
(4)“离子交换除杂”应使用___________(填“阳离子”或“阴离子”)树脂,“洗脱”时应使用的
洗脱液为___________(填标号)。
A.硫酸 B.盐酸 C.无水乙醇
(5)“还原”过程 转化为 ,在反应器出口处器壁内侧有白色晶体生成,该过程还产生的副产
物为___________,且该产物可循环利用至___________环节(填环节名称)。
(6)以上流程污染性较强且复杂,通常适用电解法回收钯。将“浸取”后的溶液与钯离子脱附试剂
MH混合,形成 配离子,电解可得高纯度钯,装置如图。电解时,当浓缩室里共得到
的较浓盐酸时(体积变化忽略不计),理论上能得到Pd___________g,但实际生产中得不
到相应质量的Pd,原因是___________。【答案】(除标明外,每空2分)
(1)70℃,固液比 (1分)
(2)将PdO还原为Pd
(3)
(4) 阴离子(1分) B(1分)
(5) HCl 浸取与洗脱(1分)
(6)159 阴极有 得电子生成
【分析】本题是一道工业流程题,通过废钯催化剂制备海绵钯,将原料焙烧后加入盐酸和还原剂从而生成
单质钯,再结合氯酸钠生成 ,通过离子交换除杂后,得到较纯净的 ,洗脱后用浓氨水沉钯,
在用 处理后得到产品,以此解题。
【解析】(1)由图可知,“浸取”的最佳条件为70℃,固液比 ;
(2)加入试剂A可以将PdO中的钯还原为单质,便于后期处理,故加入试剂A的理由是:将PdO还原为
Pd;
(3)根据题给信息可知,加入 后和单质钯反应生成四氯合钯(Ⅱ),则根据元素守恒可知,离子方
程式为: ;
(4)离子交换时发生的反应为阴、阳离子交换树脂的基本工作原理分别为 ,
其中氯离子被除掉,故应该选用阴离子交换膜;由给信息可知洗脱时得到 ,则此时应该选用盐酸,
故选B;
(5)由流程图可知,还原时 和 反应生成单质钯,根据反应器出口处器壁内侧有白色
晶体生成和元素守恒可知,副产物为HCl;由于在浸取与洗脱时都使用了盐酸故可以循环至浸取与洗脱循
环利用;
(6)盐酸的浓度由 变为 ,则生成的氯化氢的物质的量n(HCl)=5×( -
)=3mol,则此时转移电子的物质的量n(e-)=3mol,根据Pb~2e-,则生成Pd的物质的量=1.5mol,
其质量=106g/mol×1.5mol=159g;而实际电解过程中可能有氢离子在阴极得到电子,故但实际生产中得不到
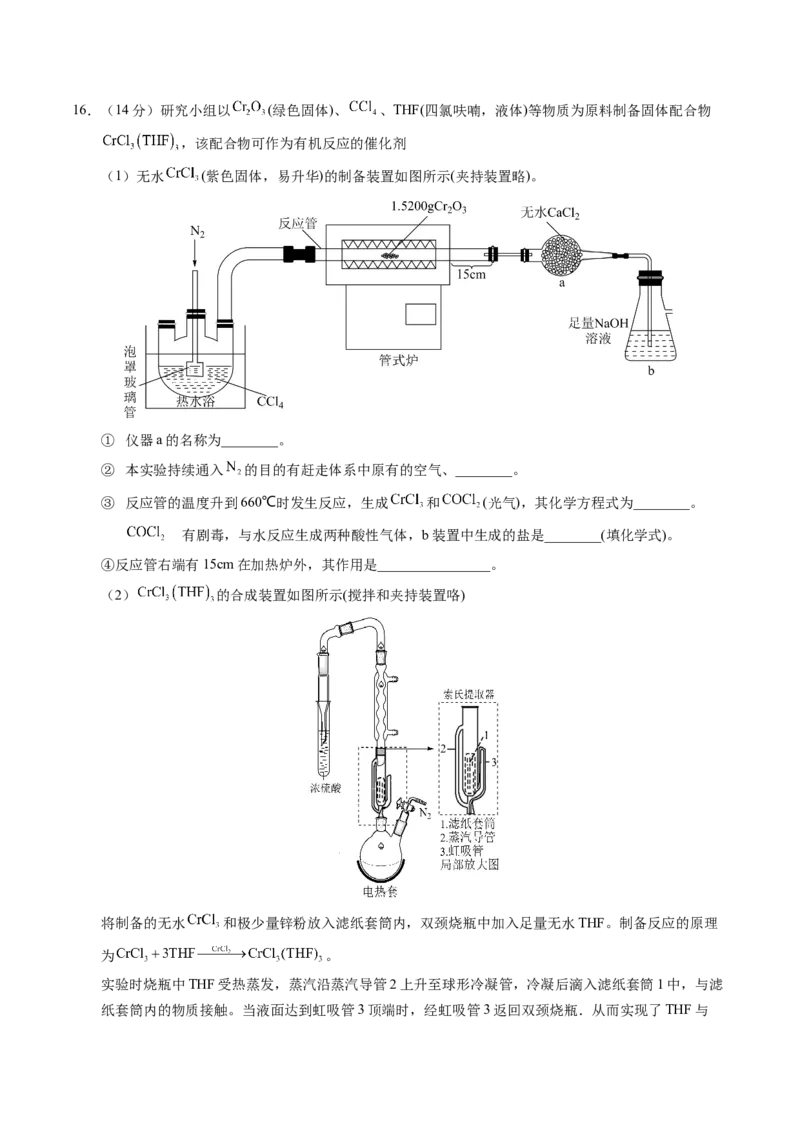
相应质量的Pd。16.(14分)研究小组以 (绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
① 仪器a的名称为________。
② 本实验持续通入 的目的有赶走体系中原有的空气、________。
③ 反应管的温度升到660℃时发生反应,生成 和 (光气),其化学方程式为________。
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________(填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理
为 。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤
纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与的连续反应及产物的连续萃取。
①锌粉的作用是________________(用化学方程式表示)。
② 和 在THF的溶解性分别为________、________(填“溶”或“不溶”)。
③ 合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________%。
【答案】(除标明外,每空2分)
(1)①干燥管(1分) ②将气态四氯化碳吹入管式炉(1分)
③Cr O+3CCl 2CrCl +3COCl Na CO 和NaCl ④使 凝华
2 3 4 3 2 2 3
(2) ① ②不溶(1分) 溶(1分) ③90%
【分析】实验室制备无水CrCl 的反应原理为:Cr O+3CCl 2CrCl +3COCl 。利用氮气和热水加热将
3 2 3 4 3 2
四氯化碳转化为气态进入管式炉与氧化铬反应得到氯化铬,利用无水氯化钙防止水蒸气进入管式炉,并用
氢氧化钠溶液吸收COCl ;合成 首先在圆底烧瓶中加入无水四氢呋喃,在滤纸套筒加入无水
2
和锌粉,开始加热四氢呋喃蒸气通过联接管进入提取管在冷凝管中冷凝回流到滤纸套筒中进行反应,
从而生成产物。
【解析】(1)①根据图示,仪器a是干燥管;
②热水加热将四氯化碳转化为气态,利用氮气将气态四氯化碳吹入管式炉;
③根据题意,以 (绿色固体)、 为原料制备固体无水 ,生成 和 (光气),反应的
化学方程式为Cr O+3CCl 2CrCl +3COCl ; 与水反应生成两种酸性气体:
2 3 4 3 2
COCl +H O=CO+2HCl,b装置中盛放足量NaOH溶液,所以生成的盐是NaCO 和NaCl;无水 易升
2 2 2 2 3
华,所以反应管右端有15cm在加热炉外,是为了使 凝华;
(2)①加入锌可以把三价铬还原为二价铬,方程式为: ;
②由实验步骤③中实验原理可知,四氢呋喃在圆底烧瓶和滤纸套筒中循环,
只有 不溶于四氢呋喃、 ,溶于四氢呋喃方能实现四氢呋喃与 的连续反应及产物的
连续萃取,故 和 在THF的溶解性分别为不溶,溶;
③由题目中的反应方程式Cr O+3CCl 2CrCl +3COCl 、 ,可知如
2 3 4 3 2
下对应关系式: ,理论产量 ,产率为
。
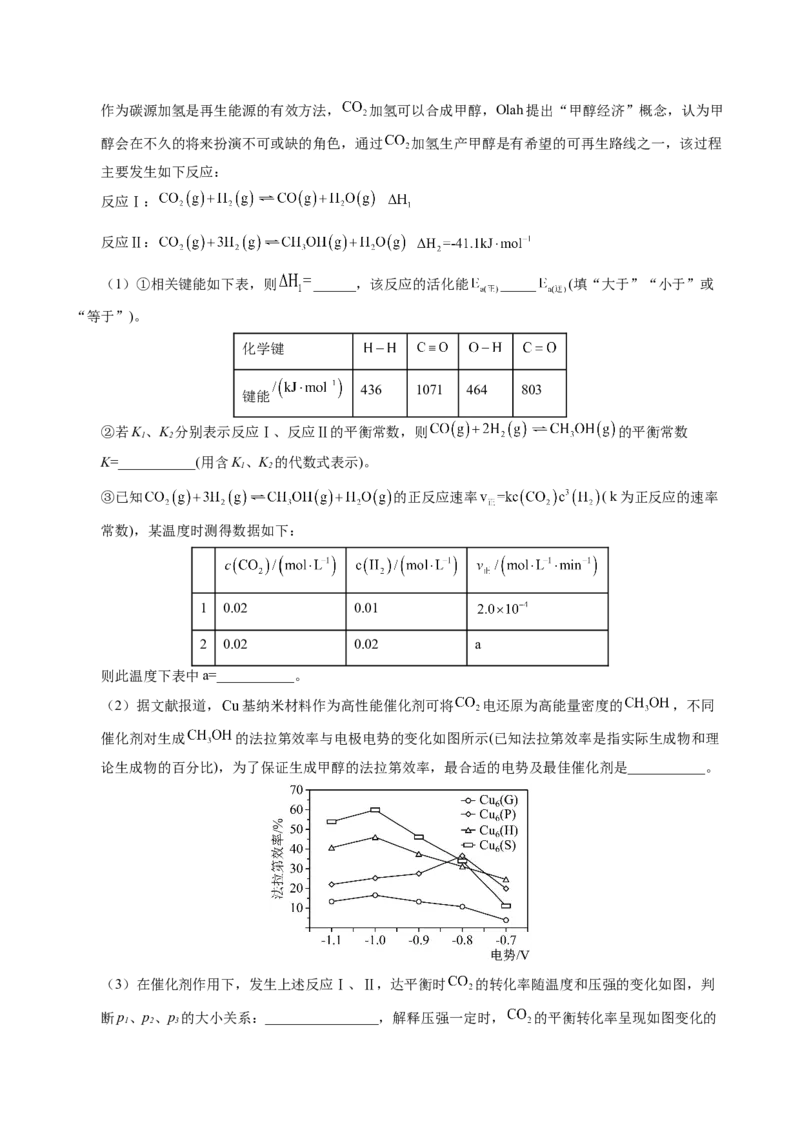
17.(15分)碳达峰、碳中和是现在需要继续完成的环保任务, 的综合利用成为热点研究对象,作为碳源加氢是再生能源的有效方法, 加氢可以合成甲醇,Olah提出“甲醇经济”概念,认为甲
醇会在不久的将来扮演不可或缺的角色,通过 加氢生产甲醇是有希望的可再生路线之一,该过程
主要发生如下反应:
反应Ⅰ:
反应Ⅱ:
(1)①相关键能如下表,则 ______,该反应的活化能 _____ (填“大于”“小于”或
“等于”)。
化学键
436 1071 464 803
键能
②若K 、K 分别表示反应Ⅰ、反应Ⅱ的平衡常数,则 的平衡常数
1 2
K=___________(用含K 、K 的代数式表示)。
1 2
③已知 的正反应速率 ( k为正反应的速率
常数),某温度时测得数据如下:
1 0.02 0.01
2 0.02 0.02 a
则此温度下表中a=___________。
(2)据文献报道, 基纳米材料作为高性能催化剂可将 电还原为高能量密度的 ,不同
催化剂对生成 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是指实际生成物和理
论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电势及最佳催化剂是___________。
(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时 的转化率随温度和压强的变化如图,判
断p、p、p 的大小关系:________________,解释压强一定时, 的平衡转化率呈现如图变化的
1 2 3原因:_______________________________。
(4)某温度下,初始压强为 ,向容积为 的恒容密闭容器中充入 、 发生反应Ⅰ、
Ⅱ,平衡时 的转化率是50%,体系内剩余 ,反应Ⅱ的平衡常数K=___________ 。
【答案】(除标明外,每空2分)
(1)① 大于(1分) ② ③1.6×10−3
(2)−1.0V、Cu (S)
6
(3)p>p>p TK之前以反应Ⅰ为主,转化率随着温度升高而增大,TK之后以反应Ⅱ为主,转化率随着
1 2 3
温度升高而降低
(4)2
【解析】(1)①反应热与反应物的键能之和与生成物的键能之和的差值相等,则反应Ⅰ的焓变
ΔH=(2×803+436)kJ/mol—(1071+2×464)kJ/mol=+43 kJ/mol,该反应为吸热反应,所以正反应的活化能大于
1
逆反应的活化能,故答案为:+43 kJ/mol;大于;
②由盖斯定律可知,反应Ⅱ—反应Ⅰ得到反应 ,则反应的平衡常数K= ,
故答案为: ;
③由速率公式可得:2.0×10−4=k×0.02×0.013,解得k=1×104,则a=1×104×0.02×0.023=1.6×10−3,故答案为:
1.6×10−3;
(2)由图可知,电极电势为−1.0V、Cu (S)做催化剂时生成甲醇的法拉第效率最高,则最合适的电势及最
6
佳催化剂是−1.0V、Cu (S),故答案为:−1.0V、Cu (S);
6 6
(3)反应Ⅰ是气体体积不变的反应,增大压强,平衡不移动,反应Ⅱ是气体体积减小的反应,增大压强,
平衡向正反应方向移动,二氧化碳的转化率增大,由图可知,压强为p、p、p 时,二氧化碳的转化率依
1 2 3
次减小,则压强的大小顺序为p>p>p;反应Ⅰ是吸热反应,升高温度,平衡向正反应方向移动,反应Ⅱ
1 2 3
是放热反应,升高温度,平衡向逆反应方向移动,由图可知,压强一定时,温度升高,二氧化碳的转化率
先增大后减小,说明TK之前以反应Ⅰ为主,转化率随着温度升高而增大,TK之后以反应Ⅱ为主,转化率
随着温度升高而降低,故答案为:p>p>p;TK之前以反应Ⅰ为主,转化率随着温度升高而增大,TK之后
1 2 3
以反应Ⅱ为主,转化率随着温度升高而降低;
(4)设平衡时一氧化碳、甲醇的物质的量分别为xmol、ymol,平衡时二氧化碳的转化率是50%,由碳原
子个数守恒可得:x+y=1,体系内剩余1mol氢气,由方程式和氢原子个数守恒可得:2x+x+y=2,解得x=y=0.5,则反应Ⅱ的平衡常数K= ,故答案为:2。
(二)选考题:共15分。请考生从2道题中任选一题作答。如果多做,则按所做的第一题计分。
18.[化学——选修3:物质结构与性质](15分)
2022年诺贝尔化学奖授予美国科学家卡罗琳·贝尔托西、卡尔·巴里·夏普莱斯和丹麦科学家摩顿·梅尔
达尔,以表彰他们在发展点击化学和生物正交化学方面的贡献。点击化学的代表反应为Cu催化的叠
氮-炔基Husigen环加成反应, 等均是点击化学中常用的无机试剂。回答下列问
题:
(1)氟原子激发态的电子排布式有_______(填标号,下同),其中能量较高的是_______ 。
a. b. c. d.
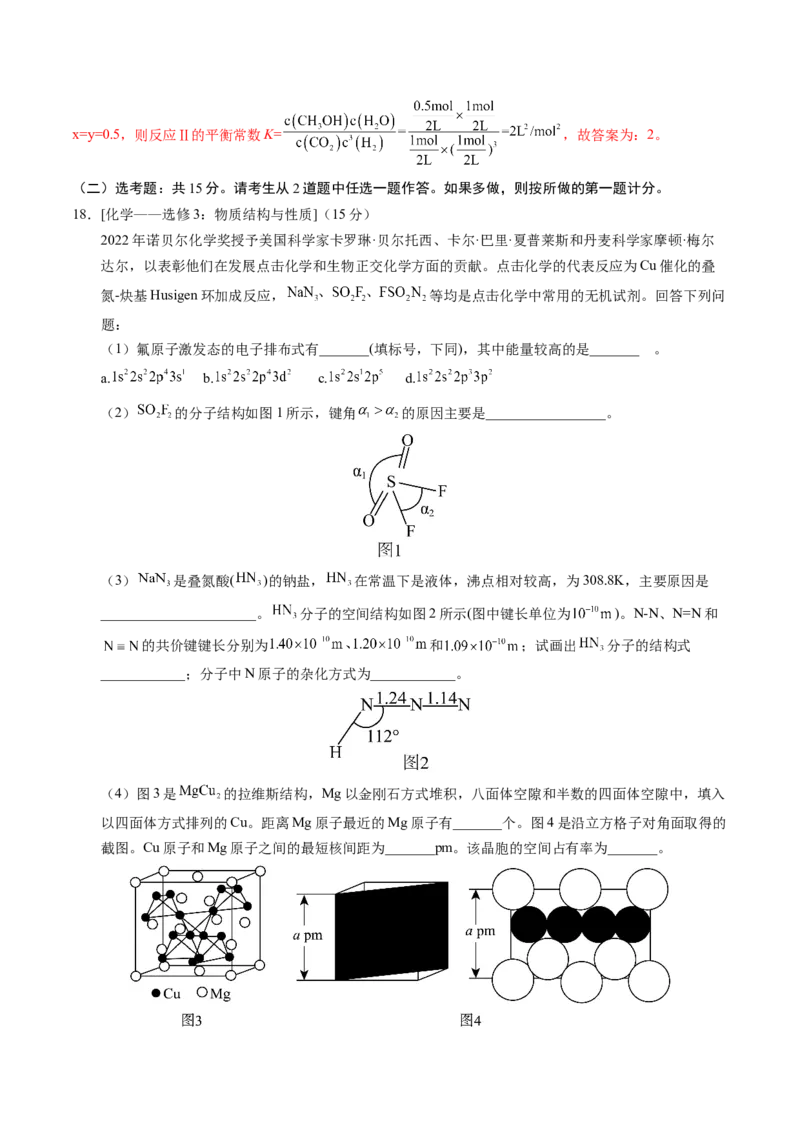
(2) 的分子结构如图1所示,键角 的原因主要是_________________。
(3) 是叠氮酸( )的钠盐, 在常温下是液体,沸点相对较高,为308.8K,主要原因是
______________________。 分子的空间结构如图2所示(图中键长单位为 )。N-N、N=N和
的共价键键长分别为 和 ;试画出 分子的结构式
____________;分子中N原子的杂化方式为____________。
(4)图3是 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入
以四面体方式排列的Cu。距离Mg原子最近的Mg原子有_______个。图4是沿立方格子对角面取得的
截图。Cu原子和Mg原子之间的最短核间距为_______pm。该晶胞的空间占有率为_______。【答案】(除标明外,每空2分)
(1)ad (1分) d(1分)
(2)双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用
(3)HN 分子间可形成氢键
3
(4)4(1分)
【解析】(1)F的核外电子数为9,其基态原子核外电子排布式为 ,a. 是基态氟原子
2p能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;
b. ,核外共10个电子,不是氟原子,b错误;
c. ,核外共8个电子,不是氟原子,c错误;
d. 是基态氟原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;故选
ad;同一原子3p能级的能量比3s能级的能量高,因此能量最高的是 ,故选d;
(2)双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用;
(3) 在常温下是液体,沸点相对较高,为308.8K,主要原因是 分子间存在氢键;根据题给化学
键的键长可画出叠氮酸的结构式为 。根据HN 的结构可知,HN 分子中形成一个单键和一个
3 3
双键的N原子为 杂化,形成三键的N原子为sp杂化;
(4)Mg以金刚石方式堆积,距离Mg原子最近的Mg原子有4个。
第一步:计算Cu原子和Mg原子的半径:由图4可知,Cu原子的半径为面对角线长的 ,由于边长是
,则面对角线长是 ,则Cu原子的半径为 ;Mg原子的半径为晶胞体对角线长的 ,体
对角线长是 ,则Mg原子的半径 。故Cu原子和Mg原子之间的最短核间距为 。
第二步:根据均摊法计算每个晶胞中Cu原子和Mg原子个数:根据晶胞结构可知,该晶胞中Mg原子的个
数是 ,Cu原子位于晶胞体内,个数为16。
第三步:计算晶胞中Cu原子和Mg原子的体积:Cu原子和Mg原子的体积为
。
第四步:计算晶胞的体积和空间占有率:晶胞边长是 ,则晶胞的体积是 。晶胞的空间占有率是
。
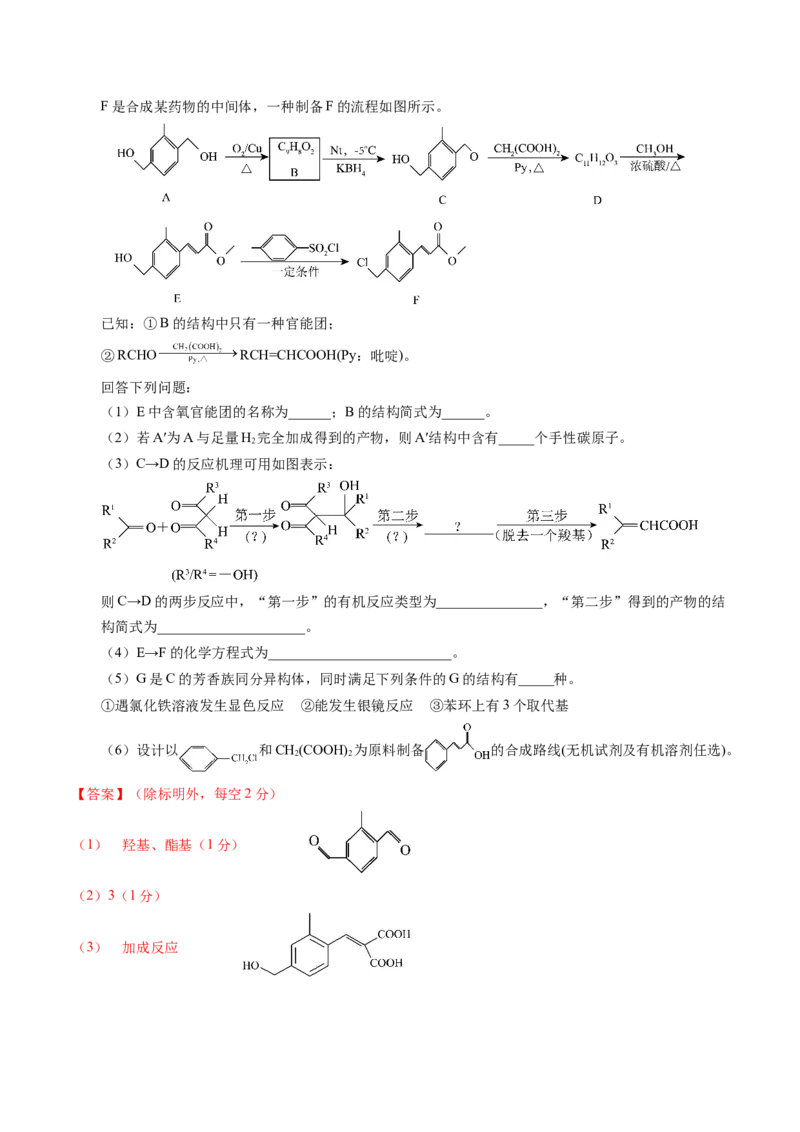
19.[化学——选修5:有机化学基础](15分)F是合成某药物的中间体,一种制备F的流程如图所示。
已知:①B的结构中只有一种官能团;
②RCHO RCH=CHCOOH(Py:吡啶)。
回答下列问题:
(1)E中含氧官能团的名称为______;B的结构简式为______。
(2)若A′为A与足量H 完全加成得到的产物,则A′结构中含有_____个手性碳原子。
2
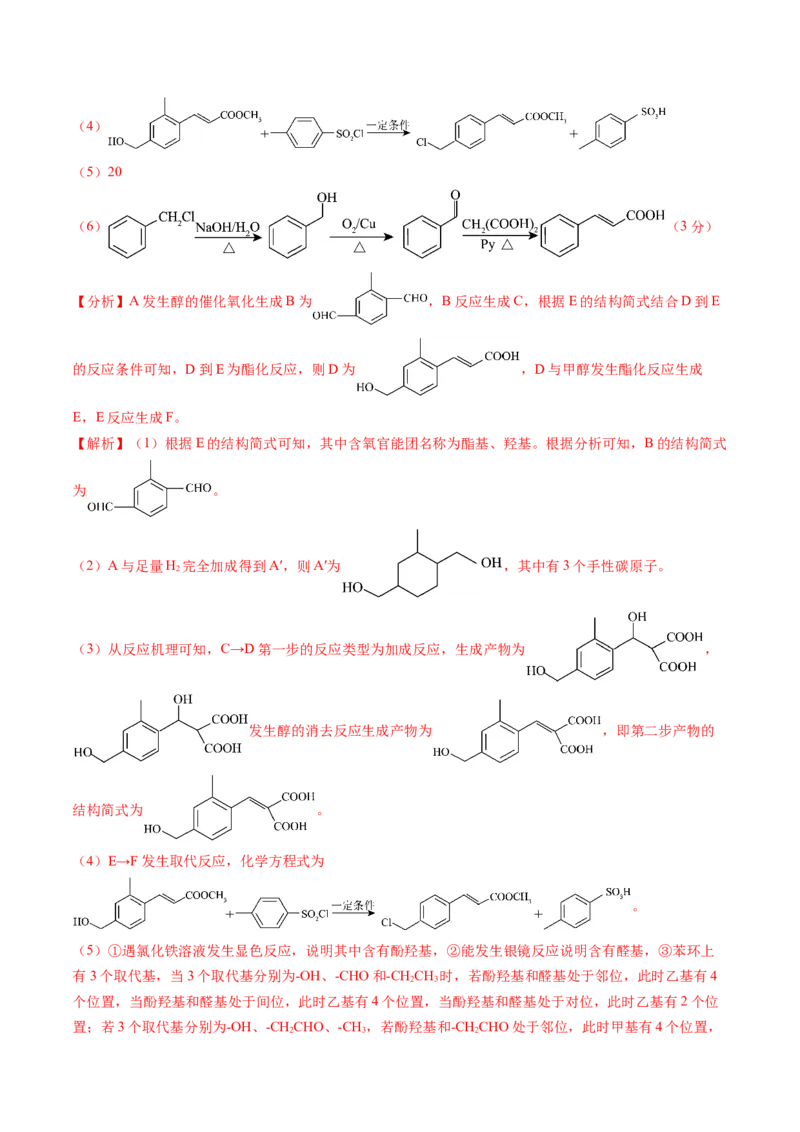
(3)C→D的反应机理可用如图表示:
则C→D的两步反应中,“第一步”的有机反应类型为_______________,“第二步”得到的产物的结
构简式为_____________________。
(4)E→F的化学方程式为__________________________。
(5)G是C的芳香族同分异构体,同时满足下列条件的G的结构有_____种。
①遇氯化铁溶液发生显色反应 ②能发生银镜反应 ③苯环上有3个取代基
(6)设计以 和CH(COOH) 为原料制备 的合成路线(无机试剂及有机溶剂任选)。
2 2
【答案】(除标明外,每空2分)
(1) 羟基、酯基(1分)
(2)3(1分)
(3) 加成反应(4)
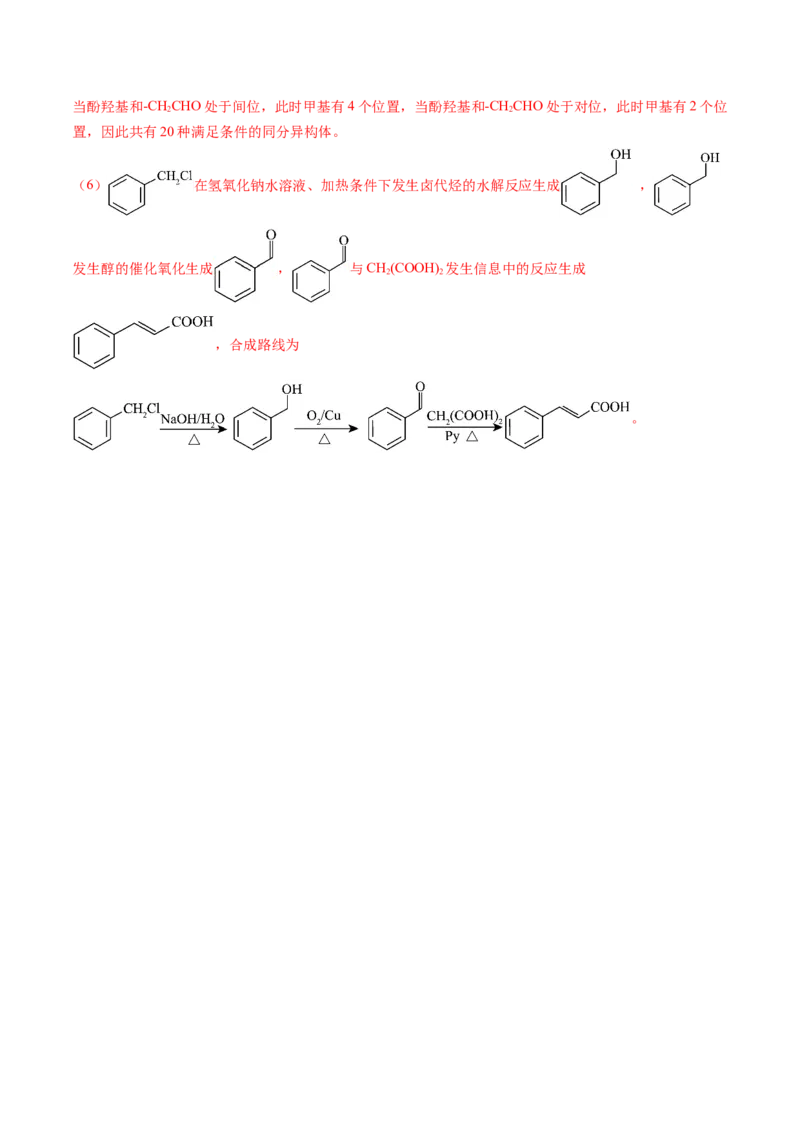
(5)20
(6) (3分)
【分析】A发生醇的催化氧化生成B为 ,B反应生成C,根据E的结构简式结合D到E
的反应条件可知,D到E为酯化反应,则D为 ,D与甲醇发生酯化反应生成
E,E反应生成F。
【解析】(1)根据E的结构简式可知,其中含氧官能团名称为酯基、羟基。根据分析可知,B的结构简式
为 。
(2)A与足量H 完全加成得到A′,则A′为 ,其中有3个手性碳原子。
2
(3)从反应机理可知,C→D第一步的反应类型为加成反应,生成产物为 ,
发生醇的消去反应生成产物为 ,即第二步产物的
结构简式为 。
(4)E→F发生取代反应,化学方程式为
。
(5)①遇氯化铁溶液发生显色反应,说明其中含有酚羟基,②能发生银镜反应说明含有醛基,③苯环上
有3个取代基,当3个取代基分别为-OH、-CHO和-CHCH 时,若酚羟基和醛基处于邻位,此时乙基有4
2 3
个位置,当酚羟基和醛基处于间位,此时乙基有4个位置,当酚羟基和醛基处于对位,此时乙基有2个位
置;若3个取代基分别为-OH、-CHCHO、-CH,若酚羟基和-CHCHO处于邻位,此时甲基有4个位置,
2 3 2当酚羟基和-CHCHO处于间位,此时甲基有4个位置,当酚羟基和-CHCHO处于对位,此时甲基有2个位
2 2
置,因此共有20种满足条件的同分异构体。
(6) 在氢氧化钠水溶液、加热条件下发生卤代烃的水解反应生成 ,
发生醇的催化氧化生成 , 与CH(COOH) 发生信息中的反应生成
2 2
,合成路线为
。