文档内容
(9)化学反应速率与化学平衡——2025届高考化学二轮复习易错重难提
升【新高考】
一、易错点分析
考点一 外界条件对化学反应速率的影响
1.掌握计算化学反应速率的两种方法
(1)根据定义式及图表中数据计算:
微点拨①计算时一定要注意溶液的体积,不能盲目地把Δn当作Δc代入公式进行计算;②还要
注意单位及规范书写。
(2)根据“比例关系”计算。
对于反应“mA(g)+nB(g) pC(g)+qD(g)”,则有v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
2.从不同角度认识反应速率常数
(1)假设基元反应(能够一步完成的反应)为aA(g)+bB(g) === cC(g)+dD(g),其速率可表示为
v=kca(A)cb(B),式中的k称为反应速率常数或速率常数。
微点拨①反应速率常数(k)表示单位浓度下的化
学反应速率,与浓度无关,但受温度、催化剂、固体表面积等因素的影响;②通常反应速率常数
越大,反应进行得越快。
(2)正、逆反应的速率常数与平衡常数的关系。
3.从“有效碰撞”角度认识外界条件对化学反应速率的影响
(1)活化分子和有效碰撞。
①能够发生有效碰撞的分子叫作活化分子。活化能是指为了能发生化学反应,普通分子(具有平
均能量的分子)变成活化分子所需要吸收的最低能量,即活化分子比普通分子多出的那部分能量。
②能够发生化学反应的碰撞叫作有效碰撞。
发生有效碰撞的两个条件:一是反应物分子必须具有足够的能量(即活化分子);二是分子碰撞时
要有合适的取向。
PS:活化能是影响化学反应速率的内因。相同条件下,不同化学反应的速率不同,主要是活化能大小不同引起。一般情况,反应的活化能越小,化学反应速率越大,反之,反应的活化能越大,反
应速率越小。
(2)影响化学反应速率的外界因素。
(3)“惰性气体”(非反应气体)对化学反应速率的影响。
考点二 化学平衡、化学平衡常数及有关计算
1.判断化学平衡状态的“三要素”
(1)分析反应条件,看清反应体系是恒温恒容、恒温恒压还是绝热容器。
(2)分析反应特点,看清反应前后气体分子总数是否发生变化,确定反应过程中气体总物质的量、
总压强是否变化。
(3)巧用“正逆相等,变量不变”作出判断。PS:分析可逆反应时,要注意反应的特殊情况,看清是否有固体参加或生成,是否存在固体的分
解反应等。
2.掌握化学平衡移动的判断方法
(1)根据勒夏特列原理判断。
通过比较改变外界条件,平衡破坏瞬间的正、逆反应速率的相对大小来判断平衡移动的方向。
(2)根据浓度商(Q)与平衡常数(K)的关系判断(相同温度)。
根据比较浓度商(Q)与化学平衡常数(K)的大小来判断平衡移动的方向。
①若Q>K,平衡向逆反应方向(或向左)移动;
②若Q=K,平衡不发生移动;
③若Q65.6 kJ
D.平衡反应速率:容器②>容器①
5.已知下列反应的平衡常数:① 。则反
应 的平衡常数是( )A. B. C. D.
6.下列关于各图象的解释或得出的结论不正确的是( )
A.由甲图可知,反应在 时刻可能改变了压强或使用了催化剂
B.由乙图可知,反应在m点可能达到了平衡状态
C.由丙图可知,反应过程中 的点是C点
D.由丁图可知,交点A表示反应一定处于平衡状态,此时
7.某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白( )和黄金雨中黄色的PbI 。
2
室温下 和 在不同的溶液中分别达到溶解平衡时, 与 或
的关系如图所示:
下列说法错误的是( )
A. 对应的是 与 的关系变化
B.p点 的结晶速率小于其溶解速率
C.将 浸泡到饱和KI溶液中几乎不能转化为
D.q点是 对应溶液的悬浊液,通过加水可以使浊液由q点向m点方向移动
8.已知: 。试管a中溶液做参照,对
试管b中溶液依次进行如下操作:①微热,溶液变为黄色②将其置于冷水中,溶液变为蓝色③滴加氨水至过量,蓝色沉淀增多,后又逐渐消失变为深蓝色溶液。下列说法正确的是( )
A.由步骤①可推知该反应的
B.由步骤②可说明降低温度,该反应平衡正向移动
C.步骤③深蓝色溶液中
D.试管b中生成的 中均含配位键
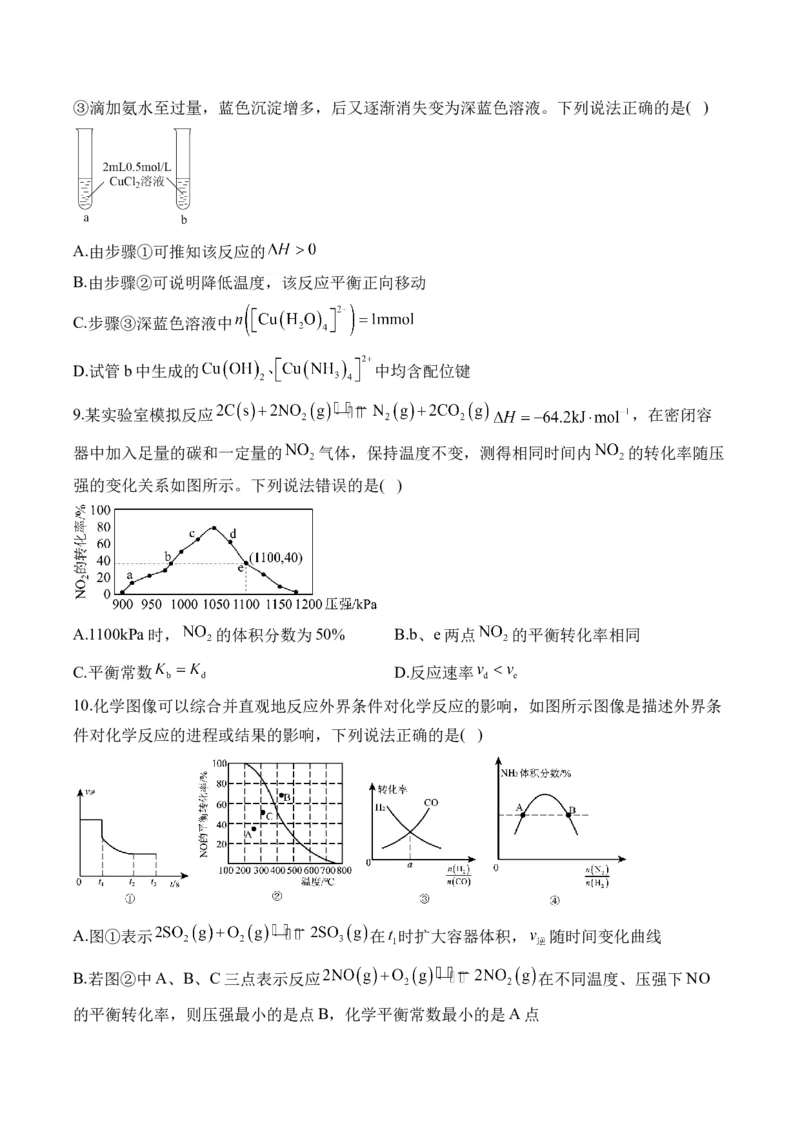
9.某实验室模拟反应 ,在密闭容
器中加入足量的碳和一定量的 气体,保持温度不变,测得相同时间内 的转化率随压
强的变化关系如图所示。下列说法错误的是( )
A.1100kPa时, 的体积分数为50% B.b、e两点 的平衡转化率相同
C.平衡常数 D.反应速率
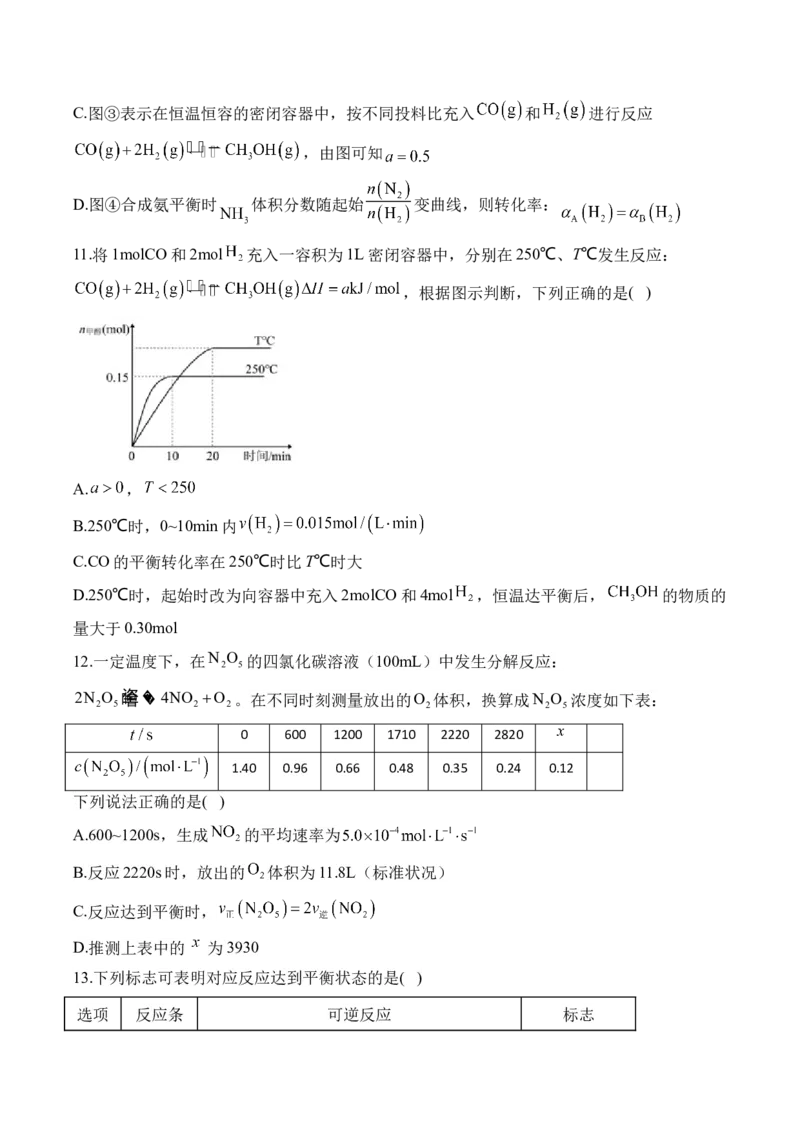
10.化学图像可以综合并直观地反应外界条件对化学反应的影响,如图所示图像是描述外界条
件对化学反应的进程或结果的影响,下列说法正确的是( )
A.图①表示 在 时扩大容器体积, 随时间变化曲线
B.若图②中A、B、C三点表示反应 在不同温度、压强下NO
的平衡转化率,则压强最小的是点B,化学平衡常数最小的是A点C.图③表示在恒温恒容的密闭容器中,按不同投料比充入 和 进行反应
,由图可知
D.图④合成氨平衡时 体积分数随起始 变曲线,则转化率:
11.将1molCO和2mol 充入一容积为1L密闭容器中,分别在250℃、T℃发生反应:
,根据图示判断,下列正确的是( )
A. ,
B.250℃时,0~10min内
C.CO的平衡转化率在250℃时比T℃时大
D.250℃时,起始时改为向容器中充入2molCO和4mol ,恒温达平衡后, 的物质的
量大于0.30mol
12.一定温度下,在N O 的四氯化碳溶液(100mL)中发生分解反应:
2 5
2N O 噲垐 �� 4NO O 。在不同时刻测量放出的O 体积,换算成N O 浓度如下表:
2 5 2 2 2 2 5
0 600 1200 1710 2220 2820
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是( )
A.600~1200s,生成 的平均速率为
B.反应2220s时,放出的 体积为11.8L(标准状况)
C.反应达到平衡时,
D.推测上表中的 为3930
13.下列标志可表明对应反应达到平衡状态的是( )
选项 反应条 可逆反应 标志件
恒温恒 混合气体的密
A
容 度不变
恒温恒 混合气体颜色
B
容 不变
在混合气
恒温恒
C 体中的
压
百分含量不变
恒温恒
D
压
A.A B.B C.C D.D
14. 和CO是环境污染性气体,可利用反应 将其转
化为无害气体。
(1)在恒容密闭容器中投入适量 和 ,在一定温度下发生上述反应,下列情况
表明该反应达到平衡状态的是_________________(填字母)。
A.混合气体的密度保持不变 B.混合气体的平均摩尔质量保持不变
C.混合气体的压强保持不变 D. 的体积分数保持不变
(2)在 和CO投料比一定的条件下,在催化剂作用下发生上述反应,测得单位时间内
CO的转化率、催化剂的催化效率与温度的关系如图所示。
图中在_____________(填“450~600℃”或“600~750℃”)温度范围内,温度是影响单位时间
内CO转化率的主要因素;450~600℃内随着温度的升高,单位时间内CO的转化率减小,其
原因是___________________________________。
(3) 时,在体积为2L的恒容密闭容器中加入 、 和催化剂,发生反应: ,10min时反应达到平衡,测得此时
。
①其他条件不变,温度升高到 ,反应达到平衡时, ,由此可推知,
____________0(填“>”“<”或“=”)。
② 时,反应的平衡常数 ___________( 为用各组分的分压计算的平衡常数,分压
=总压×物质的量分数)。
③ 时,向1L恒容密闭容器中投入0.4molCO(g)、 、 和
,此时化学反应将_______(填字母)。
A.向左进行 B.向右进行 C.处于平衡状态 D.无法判断
(4)已知:
请写出CO还原FeO的热化学方程式:___________________________。
15.“事物的双方既相互对立又相互统一”的哲学观点在化学中有着诸多体现。
Ⅰ.硫和氮两种元素与人们的生活密切相关,自然界中硫、氮的循环是维持生态平衡的重要物
质基础。
(1)下列说法错误的是__________(填标号)。
A.合成氨很大程度上解决了地球上因粮食不足而导致的饥饿问题
B.组成生命体的蛋白质中含有硫和氮
C.豆科植物的根瘤菌可实现自然固氮
D.二氧化硫有毒,不可用作食品添加剂
(2)一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:该聚合物由X( )和Y()聚合而成,下列说法正确的
是____________(填标号)。
A.X中碳氧双键比碳氮双键更容易与Y发生反应
B.生成该聚合物反应的原子利用率为100%
C.其自修复性可能与—S—S—有关
D.废弃的聚合物直接焚烧处理即可
Ⅱ.含硫、氨物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用
化学原理处理含硫、氨的废气、废液等具有重要意义。
(3)二氧化氯( )可用于烟气中 和NO的脱除。研究发现 氧化 和NO时
涉及以下基元反应。
脱硝:ⅰ.
ⅱ.
脱硫:ⅲ.
ⅳ.
其中k为速率常数。对于基元反应: ,其速率方程表达式为
实验测得: 分别单独氧化纯 、纯NO以及同时氧化二者混合物的氧化率随时间(t)
的变化情况如图所示。①其它因素都相同时, 氧化 的活化能___(填“>”或“<”) 氧化NO的活化能。
②请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响 氧化 的速率并
说明理由:___。
(4)CO也可以与NO反应生成无污染物: 。
已知:ⅰ.在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
ⅱ.气体的相对分压等于其分压(单位为kPa)除以 。
在某温度下,原料组成 ,初始总压为100kPa的恒容容器中进行上述反应,
达到平衡时 的分压为40kPa,则该反应的相对压力平衡常数 _______。
(5)污水中的硝基苯可用铁炭混合物在酸性条件下处理。硝基苯转化过程如下:
① 的电极反应式为_______。
②其他条件一定,相同时间内,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的
去除率越低的原因可能是_______。答案以及解析
1.答案:D
解析:①C的生成速率等于C的消耗速率,正逆反应速率相等,反应达到平衡,①正确;
②单位时间内生成amolA的同时生成3amolB,两者均表示逆反应速率,不能说明反应达到平
衡,②错误;
③恒容密闭容器中随着反应进行A、B、C的浓度不断变化,A、B、C浓度不变说明反应达
到平衡,③正确;
④反应在恒容密闭容器中进行,且产物中存在固体,混合气体的密度不再改变,说明气体的
总质量不再改变,反应达到平衡,④正确;
⑤该反应不是等体积反应,随着反应进行,气体的总压强不断变化,混合气体的总压强不变
说明反应达到平衡,⑤正确;
⑥该反应生成物中存在固体且不是等体积反应,混合气体的总物质的量不断变化,混合气体
的总物质的量不变时说明反应达到平衡,⑥正确;
⑦A、B、C、D浓度之比为1:3:2:2,首先D为固体没有浓度,其次A、B、C浓度比为1:3:2
与初始投料比和反应进行程度有关,不能说明反应达到平衡,⑦错误;
故正确的为①③④⑤⑥,故选D。
2.答案:C
解析:C.据图可知B、D点之后继续升高温度 的消耗速率变大的更多,即逆反应速率大
于正反应速率,平衡逆向移动,故C正确。
3.答案:B
解析:B.反应 的 ,常温下不能自发进行,则 ,
H TS 0
即 ,故B正确。
4.答案:C
解析:容器①中消耗1 mol CO放出41 kJ热量,若放出32.8 kJ热量时,参加反应的32.8kJ
n(CO) 1mol0.8mol
,则CO的转化率= ,A正确;设容器体
41kJ
积为V L,容器①中的反应可列如下三段式(单位:mol):
n(始):1 4 0 0
n(转):0.8 0.8 0.8 0.8
n(平):0.2 3.2 0.8 0.8
则容器①中反应的 ,平衡常数只与温度有关,B正确;由于容器①②中反应
的K相等,故二者中CO的转化率相等,则容器②中参加反应的
n(CO)2mol80%1.6mol,故Q1.6mol41kJmol1 65.6kJ,C错误;容器②中反应物
浓度较容器①大,则平衡反应速率容器②>容器①,D正确。
5.答案:C
解析:根据盖斯定律,由反应②-反应①,可得 ,其平衡常
K
K 2
数 。故选C。
K
1
6.答案:D
解析:A项,改变条件后,正逆反应速率增大且相等,可能是加了催化剂;对前后气体分子
数相等的化学反应,也可能是加压,故A不符合题意;
B项,已知生成物的百分含量随温度的升高而增大,m为曲线的最高点,生成物的百分含量
达到最大值,即建立了相应温度下的平衡状态;继续升温生成物的百分含量减小,说明升温
反应向相反方向移动,故B不符合题意;
C项,曲线上B点表示在此温度下反应达到平衡时所能达到的最大转化率,A位于曲线以上,
表示超过该温度下的最大转化率,此时平衡会向逆反应方向移动, ;C点位于曲线以
下,表示未达到该温度下的最大转化率,此时平衡会向正反应方向移动,v v ,故C不符
正 逆
合题意;
D项,A点时c(反应物)=c(生成物),不一定达到平衡状态,故D符合题意;
故选D。
7.答案:B解析:结合化学式和题图中曲线数量关系可知, 对应的是 与 的关系变
化,A项正确;
p点对于 来说是过饱和溶液,析出晶体,结晶速率大于其溶解速率,B项错误;
从题图中可以算出 , ,将 浸泡到饱和KI溶液中,
发生反应: ,该反应的平衡常数 ,所以几乎不能转化为
,C项正确;
q点是 的悬浊液,q点溶液中, ,加水稀释 减小,
增大,所以通过加水可使浊液由q点向m点方向移动,D项正确。
8.答案:A
解析:A.由步骤①可推知,升温,平衡正向移动,则该反应的 >0,故A正确;B.由步骤
②可说明降低温度,该反应平衡逆向移动,故B错误;C.步骤③深蓝色溶液中
,故C错误;D.试管b中生成的 中含配位键,
中无配位键,故D错误;故选:A。
9.答案:B
解析:B.b点反应未达平衡,此时的转化率不是平衡转化率,延长反应时间,反应物的转化
率将增大,e点时反应达平衡,此时NO 的转化率为平衡转化率,则b、e两点 的平衡转
2
化率不相同,故B错误;
C.温度一定,则平衡常数不变,即平衡常数K K ,故C正确;
b d
D.由图可知,压强: ,温度一定时压强越大,反应速率越快,即反应速率v v ,故D
d e
正确;
故选:B。
10.答案:A
解析:A项,图①中 时刻 在减小,且到 新平衡建立的时候, 持续减小,说明平衡逆
向移动,所以适用于 在 时扩大容器体积,即减压平衡逆向移
动。
B项,由图②中图像可知,随着温度的升高NO的转化率下降,说明平衡逆向移动,则该反应的正向为放热反应。A、B、C三点A点温度最低,此时平衡正向程度最大,K值最大。
C项,图③表示在恒温恒容的密闭容器中,按不同投料比充入 和 进行反应
,可计算知 。
D项,图④中A、B两点是平衡时 体积分数相同的点,图中的最高点是 和 恰好按
照方程式系数1∶3开始反应的平衡点,A点 过量,B点 过量,故压的转化率不会相同。
11.答案:D
解析:A.依据先拐先平衡的判断法可知, ,升高温度甲醇的物质的量减少,平衡逆
向移动,所以正反应为放热反应, ,即 ,故A错;
B.0~10min内甲醇的物质的量增加了0.5mol,根据方程式氢气的变化量为:
,所以 ,故B错;
C.已知该反应 ,而且 ,温度越低CO的转化率越大,所以CO的转化率:T℃
时大于250℃时,故C错;
答案选D。
12.答案:D
解析:A项,600~1 200g, ,则
,不正确;B项,起始至反应2220s时,
, ,放出的 在标准状
况下体积 ,不正确;C项,反应达到平衡时,
,不正确;D项,根据题表中数据可知, 浓度每减少一半所用时
间均为1110s,所以 2820+1110=3930,正确;故选D。
13.答案:B
解析:A.反应前后气体的总质量不变,容器容积不变,故容器内混合气体的密度始终不变,
故混合气体的密度不变无法判断反应是否达到平衡状态,故A错误;
B.二氧化氮为红棕色气体,容器内混合气体的颜色不变,二氧化氮浓度不变,正反应速率想
等,化学反应达到平衡状态,故B正确;
C.反应中氨气和二氧化碳的生成量之比始终为2:1,故 在混合气体中的百分含量始终保持不变,故 在混合气体中的百分含量不变无法判断反应是否达到平衡状态,故C错误;
D. ,无法判断正反应速率想等,故无法判断化学反应是否达到平衡状态,
故D错误;
故选:B。
14.答案:(1)D
(2)600~750℃;450~600℃内随着温度的升高,催化剂的催化效率不断降低,最后趋近于
0,反应速率逐渐减慢
(3)<;0.375;A
(4)
解析:(1)A.混合气体的质量和体积都不变,密度始终不变,则密度不变时不一定达平衡状
态;
B.混合气体的质量和物质的量都不变,平均摩尔质量始终不变,则平均相对分子质量不变时,
不一定达平衡状态;
C.混合气体的体积、物质的量都不变,压强始终不变,则压强不变时不一定达平衡状态;
D. 的体积分数保持不变,则物质的量不变,反应达平衡状态。综合以上分析,只有D符
合题意;
故选:D;
(2)从图中可以看出,温度高于600℃时,催化效率接近0,所以在600~750℃温度范围内,
温度是影响单位时间内CO转化率的主要因素;450~600℃内随着温度的升高,单位时间内
CO的转化率减小,从图中可以看出,温度升高,催化效率降低,其原因是450~600℃内随着
温度的升高,催化剂的催化效率不断降低,最后趋近于0,反应速率逐渐减慢;
(3)其他条件不变,温度升高到 ,反应达到平衡时, ,由此可推知,升
高温度,平衡逆向移动, 。
15.答案:(1)D
(2)BC
(3)①>;②会影响, 显示单独氧化 时产生ClO过慢,同时氧化时由反应ⅰ产生的
ClO部分与 作用,使 的氧化率提高明显
(4)320(5)① ;②反应生成的 ,随着pH增大,转化为
沉淀覆盖在铁炭混合物表面,阻碍了反应的进行,降低了反应速率
解析:(1)食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用。
(2)X中碳氮双键比碳氧双键更容易与Y发生反应,废弃的聚合物直接焚烧处理,可能会产
生氮氧化物、硫氧化物等有毒气体。
(3)①根据表中数据, 与NO的两步反应的 、 均大于 与 反应的 、 ,
说明, 与NO反应更快,因此 氧化 的活化能大于 与NO反应的活化能
②根据图像可知, 单独氧化 时,氧化率较低,同时氧化 和NO时, 氧化
的氧化率有明显上升,结合ⅰ、ⅲ、ⅳ的速率常数可知, 显示单独氧化 时产生
ClO过慢,同时氧化时由反应ⅰ产生的ClO部分与 作用,使 的氧化率提高明显。
(4)相同条件下,气体压强之比等于其物质的量之比,起始时,CO、NO的分压均为
50KPa,达到平衡时 的分压为40KPa,则 的分压为20KPa,CO、NO的分压均为(50-
40)KPa=10KPa,该反应的相对压力平衡常数= =320。
(5)在酸性条件下, 时,转移电子数为 4 ,电极反应式:
。从图中可以看出,pH越大, 越大,
转化生成的 越多,沉积在铁炭表面的固体越多,硝基苯的去除率越低,原因是:反
应生成的 ,随着pH增大,转化为 沉淀覆盖在铁炭混合物表面,阻碍了反应的进
行,降低了反应速率。