文档内容
第 41 课时: 不同价态含硫物质的转化
【学习目标】
掌握韩流化合物的相互转化方式。
熟悉基本缺项氧化还原离子方程式配平。
【重点难点】
1.重点:含硫化合物的相互转化;
2.难点:含硫化合物转化中的相关计算。
【高频考点】
含硫化合物转化中方程式应用。
【教学内容】
一、0 价与+4 价转化
1.S 单质
S+O ===(点燃)SO
2 2
S+2H SO ====3SO ↑+2H O
2 4 2 2
2.SO
2
SO +2H S===3S↓+2H O
2 2 2
S+2H SO (浓)===(加热) 3SO ↑ +2H O
2 4 2 2
二、+4 价与+6 价转化
1.SO
2
第 1 页与各种氧化剂反应,体现二氧化硫还原性。
2SO +O (催化剂、加热)2SO
2 2↔ 3
SO +2H O+X ===2HX+H SO
2 2 2 2 4
SO + Fe3+ + === SO 2- + Fe2+ +
2 4
SO + NO3- + H+ === SO 2- + NO↑ +
2 4
SO + MnO4- + === SO 2- + Mn2+ +
2 4
2.硫酸
C+2H SO (浓)===(加热)CO ↑ +2SO ↑ +2H O
2 4 2 2 2
S+2H SO (浓)===(加热) 3SO ↑ +2H O
2 4 2 2
Cu+2H SO (浓)===(加热)CuSO +SO ↑ +2H O
2 4 4 2 2
注意硫酸变稀之后反应就会停止。
浓硫酸在与氢前金属反应时,
当硫酸变稀后,就无法产生二氧化硫。
第 2 页【经典例题】
1.将 SO 通入下列溶液中,产生沉淀的是( )
2
A.BaCl
2
B.CaCl
2
C.Ba(NO )
3 2
D.NaOH
2.将 SO 通入 BaCl 中没有明显现象,加入下
2 2
列物质后会产生沉淀,请写出沉淀种类。
①Cl ( )
2
②KMnO ( )
4
③NH ( )
3
④H S( )
2
⑤NaNO ( )
3
【本课小结】
0 价硫有较强的还原性,可被氧化为+4 价。
+4 价硫既有氧化性又有还原性。
+6 价硫元素具有氧化性,可以被还原为+4 价。
第 3 页【课后作业】
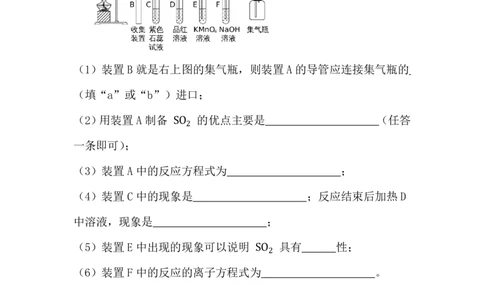
1. 实验室常用如图装置进行铜跟浓硫酸反应等一系列实验。请回答
下列问题:
(1)装置 B 就是右上图的集气瓶,则装置 A 的导管应连接集气瓶的
(填“a”或“b”)进口;
(2)用装置 A 制备 的优点主要是 (任答
一条即可); SO �
(3)装置 A 中的反应方程式为 ;
(4)装置 C 中的现象是 ;反应结束后加热 D
中溶液,现象是 ;
(5)装置 E 中出现的现象可以说明 具有 性;
(6)装置 F 中的反应的离子方程式为SO � 。
2. (1)工业上 (填“能”或“不能”)用铁质容器盛装冷的
浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下
探究活动:
【探究一】
(2)将已去除表面氧化物的铁钉(碳素钢)放入 浓硫酸中,
�入�⺁mL
第 4 页加热,充分反应后得到溶液 X 并收集到气体 Y。
①甲同学认为 X 中除 外还可能含有 。若要确认其中的
�� ��
,应选用 。Fe Fe
��
Fe
a. 溶液 b.铁粉和 溶液 c.浓氨水 d.酸性
溶液KSCN KSCN KMnO �
②乙同学取 (标准状况)气体Y 通入足量溴水中,发生反
应: ��� mL ,用单线桥表示电子转
移情况SO:� � Br � � �H � O ��� �HBr � H � S,O �然 后加入足量 溶
液,经适当操作后得干燥固体 。由 此推知气体Y中B aCl � 的
�
体积分数为 。 ���� g SO
【探究二】
分析上述实验中 体积分数的结果,丙同学认为气体Y 中还可能
含量有 和 SO �气 体。为此设计了下列探究实验装置(图中夹持
� �
仪器省略H)。 CO
(3)装置 B 中试剂的作用是 。
(4)认为气体 Y 中还含有 的理由是 (用化学方程
式表示)。 CO �
(5)为确认 的存在,需在装置中添加 M 于 ,M 中盛装的
是 。 CO �
第 5 页a.A 之前, 溶液 b.A B 间, 溶液
c.B C 间Na,O澄H清石灰水 d.C� D 间,Na澄O清H石灰水
( 6 )� 如 果 气 体 Y 中 含 有 �, 预 计 实 验 现 象 应
是 。 H �
3. 根据要求完成甲、乙两组实验。(a、b 为弹簧夹,加热及固定装
置已略去)
回答下列问题:
(1)制取 :写出铜与浓硫酸反应的化学方程
式: SO � 。
(2)用甲组装置验证酸性相对强弱:亚硫酸>碳酸>硅酸。
①操作步骤:连接仪器、 、加药品后,打开 a 关闭 b,
然后滴入浓硫酸,加热。
②甲组试管中的试剂分别是 A. 饱和溶液,B ,
C 。 试剂 B 的作用是 NaHCO � 。
③能说明酸性:亚硫酸>碳酸>硅酸的实验现象
是 。
第 6 页(3)用乙组装置验证 的某些性质。打开 b,关闭 a;
④ 溶液中有浅黄色SO浑�浊出现,反应的化学方程式
是 H � S 。 溶液中无明显现象,将其分成两份于
a、b两支试管中。 BaCl �
⑤试管 a 中滴加 溶液,产生白色沉淀的化学式
是 NaOH。
⑥试管 b 中滴加 溶液,也产生白色沉淀,产生白色沉淀的化
学式是 FeCl � 。
⑦上述④⑤⑥的反应分别验证 的性质依次是④ ;
⑤ ;⑥ 。S(O填� 序号)
A.酸性氧化物的通性 B.碱性氧化物的通性 C.还原性 D.氧化性
E.漂白性
(4)装置 G 中盛放的溶液是 。
【答案与解析】
1. (1)a
(2)可以控制反应的发生与停止、可以防止倒吸
(3) 浓 (3 分)
△
(4)溶液变红;� 溶�液恢复红色 � � �
Cu ��H SO � � ��� CuSO � SO ���H O
(5)还原性
(6)
� ��
SO � ��OH ��� SO� � H � O
第 7 页【解析】
本题主要考查铜、硫酸、二氧化硫的性质和相关实验操作。
(1)二氧化硫的密度大于空气的密度,可用向上排空气法收集 ,
因此装置 A 的导管应连接集气瓶的 a 进口。 SO �
(2)装置 A 中铜丝是可以抽出的,用装置 A 制备 的优点主要是
可以控制反应的发生与停止、可以防止倒吸。 SO �
(3)铜与浓硫酸在加热条件下反应生成硫酸铜、 和水,反应方
�
程式为 浓 SO 。
△
(4) Cu �溶�H于�水SO生� �成亚��硫��酸C,uS溶O液� �显S酸O �性�,�装�H置� OC 中紫色的石蕊试
液变红S;O � 能使品红溶液褪色,但 的漂白是不稳定的,因此
反应结束后SO加�热 D 中溶液,溶液的红色S恢O �复。
(5)高锰酸钾具有强氧化性, 通入至高锰酸钾溶液中溶液褪色,
说明高锰酸钾被 还原,可S以O �说明 具有还原性。
(6) 与氢氧S化O �钠反应生成亚硫酸钠SO和� 水,因此装置 F 中反应的
离子方S程O �式为 。
� ��
� � �
SO ��OH ��� SO � H O
2. (1)能
(2)d; ; (2 分)
(3)检验二氧化硫是否被除尽
����%
(4) (浓) (2 分)
△
(5)c � � � � �
C ��H SO ���CO ���SO ���H O
(6)氧化铜固体颜色变红,硫酸铜晶体颜色变蓝
第 8 页【解析】
(1)浓硫酸具有强的氧化性,常温下遇到铁发生钝化,形成致密氧
化膜阻止反应进行,工业上能用铁质容器盛装冷的浓硫酸。
(2)①d 项,二价铁离子具有强的还原性,能够使酸性的高锰酸钾
褪色,三价铁离子不具有还原性,不能使高锰酸钾褪色,所以可以用
来检验二价铁离子,故选 d 项;
a 项,溶液中含有三价铁离子,遇到硫氰酸钾显红色,对二价铁离子
检验造成干扰,故不选 a 项;
b 项,溶液中含有三价铁离子硫氰酸钾显红色,铁和铁离子反应生成
亚铁离子,不能检验出亚铁离子,故不选 b 项;
c 项,亚铁离子和浓氨水反应生成白色沉淀,但不稳定,立即转化为
黄绿色最终转化为红褐色沉淀,铁离子和浓氨水反应生成红褐色沉淀,
所以无论是否含有亚铁离子,加入浓氨水都产生红褐色沉淀,故不选
c 项。
综上所述,本题正确答案为 d。
② 具有还原性,通入足量溴水中,发生
SO
� ,用单线桥表示电子转移情况的SO化�学�方Br程� �式�为H:�
O �
� �
�HBr � H SO
混合气体 ,
⺁����L
�� � � ����L�mol � ⺁�⺁�入 mol
� �
SO � BaSO
� mol ��� g
� ���� g
第 9 页;
则� � ⺁�⺁的� m体o积l 分数: 。
⺁�⺁�
(3S)OA� 除去二氧化硫,⺁二�⺁�氧入 �化�硫⺁⺁能%使�品�红���溶%液褪色,所以 B 可以检
验 A 中是否完全除去二氧化硫。
(4)加热条件下, 和浓硫酸反应生成二氧化碳,所以认为气体 Y
中还含有 的理由C的反应方程式为: (浓)
CO � 。 C ��H � SO �
△
�(�5�)C实O �验��室�用SO澄�清��石�灰H �水O检验二氧化碳,但二氧化硫也能使澄清石
灰水变浑浊,要检验二氧化碳应该排除二氧化硫的干扰,所以在确定
不存在二氧化硫条件下,将气体通入澄清石灰水检验是否含有二氧化
碳,该检验装置应该在B— C之间,故 选c项。
综上所述,本题正确答案为c。
(6)氢气具有还原性,能还原性,能还原黑色的氧化铜生成红色的
铜单质,同时生成水,水能使无水硫酸铜变蓝色,这是检验水的特征
反应,所以如果 D 中氧化铜变红,E 中无水硫酸铜变蓝,则证明含有
氢气。
3. (1) 浓 (2 分)
△
(2)①检查装置的�气密� 性 � � �
Cu ��H SO � ����CuSO ��H O � SO �
②酸性高锰酸钾溶液;硅酸钠溶液;吸收二氧化硫,并检验二氧化硫
已经除净
③A 中溶液产生气泡,B 中紫红色溶液颜色变浅(或没有完全褪色),
第 10 页C 中出现白色沉淀(2 分)
(3)④ (2 分)
⑤ �H � S� SO � � �S ���H � O
⑥ BaSO �
⑦DB;aAS;O �C
(4) 溶液
【解析】NaOH
主要考查非金属性比较方法。
(1)铜和热的浓硫酸反应,反应中 元素的化合价由 0 升高到+2
价,作还原剂,产物为二氧化硫、硫酸铜Cu和水,反应的方程式为:
浓 。 Cu �
△
(2�)①� 装置 A 中反应制� 备气�体,在加� 入药品之前需要检查装置的气
�H SO � ����CuSO ��H O � SO �
密性。
②A 中碳酸氢钠的作用是和二氧化硫反应生成二氧化碳;B 中为酸性
高锰酸钾目的是除去二氧化硫,防止干扰二氧化碳和硅酸钠反应,若
紫红色溶液颜色变浅(或没有完全褪色)证明二氧化硫已经除净。C
中为硅酸钠,利用强酸制弱酸生成硅酸沉淀证明酸性:亚硫酸>碳酸
>硅酸。
③综合②所述,证明酸性:亚硫酸>碳酸>硅酸的现象为 A 中溶液产
生气泡,B 中紫红色溶液颜色变浅(或没有完全褪色),C 中出现白色
沉淀。
(3)④二氧化硫中硫元素的化合价是+4 价,有氧化性,二氧化硫气
第 11 页体与 溶液常温下反应,生成黄色固体硫(单质)和水,
H � S 。 �H � S�
S⑤O试� �管�aS中��滴�加H � O 溶液,二氧化硫和水反应生成亚硫酸,亚硫
酸和 反应生Na成OH亚硫酸钠,亚硫酸根离子和钡离子反应生成
N。aOH
B⑥a试SO管� b 中滴加 溶液, 具有氧化性,能把二氧化硫氧
化成+6 价的硫酸根Fe离Cl子� ,硫酸根F离eC子l �和钡离子反应生成 白色
沉淀。 BaSO �
⑦反应④中二氧化硫和硫化氢反应,二氧化硫被还原,所以体现的是
二氧化硫的氧化性,故选 D 项;
反应⑤中二氧化硫和碱反应,体现了二氧化硫酸性氧化物通性,故选
A 项;
反应⑥中二氧化硫被 氧化成硫酸根,体现了二氧化硫的还原
性,故选 C 项。 FeCl �
(4)G 的作用吸收尾气,防止污染空气,可盛放 溶液。
NaOH
第 12 页