文档内容
氧化还原反应2
重难点 题型 分值
1. 了解氧化剂还原剂的概念
重点 2. 知道常见的氧化剂与还原剂的常见反应
选择
3. 了解氧化还原反应的基本规律 8-12分
填空
1. 氧化还原反应的概念与应用
难点
2. 氧化还原反应规律的应用
核心知识点一:
氧化剂、还原剂、氧化性、还原性、氧化产物、还原产物的概念
1. 概念
氧化剂:在反应中得到电子(或电子对偏向)的物质。
还原剂:在反应中失去电子(或电子对偏移)的物质。
氧化性:氧化剂得电子的能力。在氧化还原反应中氧化剂具有氧化性,反应时本身被
还原。
还原性:还原剂失电子的能力。在氧化还原反应中还原剂具有还原性,反应时本身被
氧化。
第1页氧化产物:还原剂发生氧化反应后的生成物。
还原产物:氧化剂发生还原反应后的生成物。
2. 常见的氧化剂和还原剂
常见的氧化剂
(1)活泼的非金属单质:Cl、Br 、O、I、S等
2 2 2 2
(2)元素处于高价时的氧化物:CO、NO 、SO 、MnO 、PbO 等
2 2 3 2 2
(3)元素处于高价时的含氧酸:浓HSO 、HNO 等
2 4 3
(4)元素处于高价时的盐:KClO、KMnO 、FeCl 、KCr O 等
3 4 3 2 2 7
(5)过氧化物:NaO、HO 等
2 2 2 2
(6)次氯酸及其盐:HClO、Ca(ClO)、NaClO等
2
常见的还原剂
(1)活泼的金属单质:Na、Mg、Al、Zn、Fe
(2)某些非金属单质:H、C、Si
2
(3)元素处于低价时的氧化物:CO、SO
2
(4)元素处于低价时的酸:HCl、HI、HS、HSO 等
2 2 3
(5)元素处于低价时的盐:NaS、KI、NaSO 、FeSO 等
2 2 3 4
注意:大部分非金属单质都既有氧化性又有还原性,只是以氧化性为主。在同一氧
化还原反应中一定有氧化剂和还原剂,氧化剂和还原剂可以是不同的物质也可以是同种物
质。
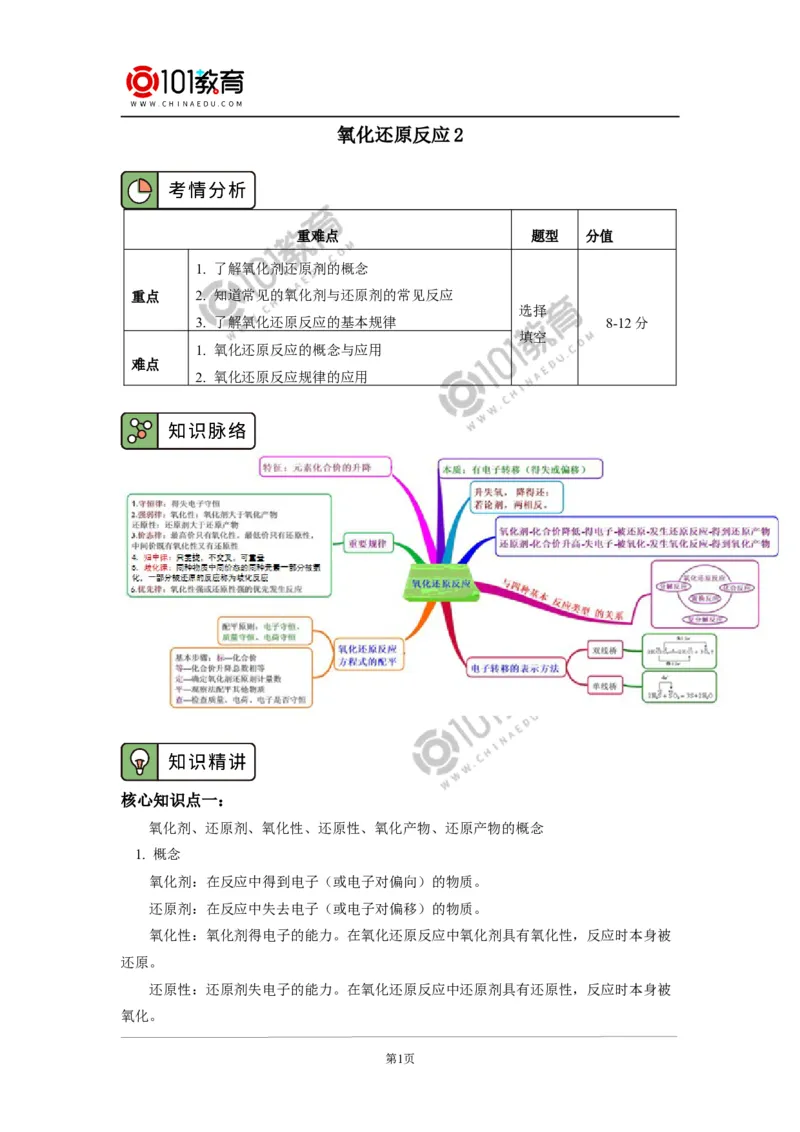
3. 氧化还原反应概念间的关系
核心知识点二:
一、氧化还原反应的规律
1. 守恒律
化合价升高总数与降低总数相等,实质是反应中失电子总数与得电子总数相等. 该规
律可应用于氧化还原反应方程式的配平及相关计算等。
2. 强弱律
第2页氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
强弱律的应用:在适宜条件下,用氧化性(还原性)较强的物质可制备氧化性(还原
性)较弱的物质;用于比较物质的氧化性或还原性的强弱。
3. 价态律
有多种价态的元素,处于最高价态时只具有氧化性(如 HSO 中的S元素),处于最
2 4
低价态时只具有还原性(如HS中的S元素),处于中间价态时既有氧化性又有还原性,
2
但是主要表现一种性质(如SO 中的S元素). 价态律可应用于判断物质的氧化性、还原性。
2
(注意:并不是说含有最高价元素的物质一定具有氧化性,比如 CaCO 、NaPO 等物质中,
3 2 3
C、P处于最高价,但它们无氧化性)
4. 归中律:只靠拢,不交叉,可重叠
同种元素不同价态间发生归中反应时,元素的化合价只接近而不交叉,最多达到同种
价态.
5. 歧化律
同种物质同价态的的同一元素一部分被氧化,一部分被还原的氧化还原反应叫歧化反
应;
6. 优先律
当存在多种还原剂(氧化剂)时,氧化剂(还原剂)通常先和还原性(氧化性)最强
的还原剂(氧化剂)反应。如向NaBr和NaI的混合溶液中通入Cl ,因I-的还原性强于Br
2
-,则先发生反应:2I-+Cl===2Cl-+I,然后发生反应:2Br-+Cl===2Cl-+Br
2 2 2 2
二、氧化还原反应的运用
实验室制备氧气、氢气等。
1. 制备某些物质。
工业上用还原剂冶炼金属。
强氧化剂Cl 、ClO 等对小型水厂、游泳池水、
2 2
2. 利用强氧化剂进行消毒、杀菌。
医院污水、工业污水的处理。
3. 燃料的燃烧,提供热能等。 电热厂供暖。
4. 化学电源的研制、开发及合理利用。 燃料电池及新型电池。
5. 电镀以防止金属的腐蚀。 铁上镀锡等。
核心知识点一:
某种飞船以NH 和NO 为动力源,发生反应:2NH+NO===3N +4HO,反应温度
2 4 2 4 2 4 2 4 2 2
第3页可高达2700℃,对于该反应,下列说法中正确的是( )
A. 该反应属于置换反应
B. NH 是氧化剂
2 4
C. NO 是还原剂
2 4
D. N 既是氧化产物又是还原产物
2
【考点】氧化剂还原剂的概念
【答案】D
【解析】该反应的反应物中无单质,不属于置换反应;该反应实际上是不同价态的氮
元素之间发生的归中反应,NH 是还原剂,NO 是氧化剂,N 既是氧化产物又是还原产物。
2 4 2 4 2
根据下列反应判断有关物质还原性由强到弱的顺序是( )
HSO +I+HO=2HI+HSO 2FeCl +2HI=2FeCl +2HCl+I
2 3 2 2 2 4 3 2 2
3FeCl +4HNO=2FeCl +NO↑+2HO+Fe(NO )
2 3 3 2 3 3
A. H SO >I->Fe2+>NO
2 3
B. I->Fe2+>H SO >NO
2 3
C. Fe2+>I->H SO >NO
2 3
D. NO>Fe2+>H SO >I-
2 3
【考点】本题考查氧化还原反应中物质的还原性强弱的比较.
【答案】A
【解析】从四个选项来看,各物质或微粒在反应中均有元素化合价变化,故解答此题
应依据还原剂的还原性大于还原产物的还原性来判断。由第一个方程式得还原性:HSO >I
2 3
-,由第二个方程式得还原性:I->Fe2+,由第三个方程式得还原性:Fe2+>NO,故选A。
核心知识点二:
已知常温下,在溶液中发生如下反应:
①16H++10Z-+2XO===2X2++5Z+8HO
2 2
②2A2++B ===2A3++2B-
2
③2B-+Z===B +2Z-
2 2
由此推断下列说法错误的是( )
A. 反应Z+2A2+===2A3++2Z-可以进行
2
B. Z元素在反应③中被还原,在反应①中被氧化
第4页C. 氧化性由强到弱的顺序是XO、Z、B 、A3+
2 2
D. 还原性由强到弱的顺序是Z-、B-、A2+、X2+
【考点】本题考查了氧化性还原性强弱的比较。
【答案】D
【解析】由题中信息知氧化性的强弱顺序为XO>Z >B >A3+,所以A、C正确;在
2 2
反应①中Z元素被氧化,在反应③中Z元素被还原,所以B项正确;还原性为A2+>B->
Z->X2+,D项错。
PbO 、KMnO 、Cl 、FeCl 、Cu的氧化性依次减弱。下列反应在水溶液中不可能发生
2 4 2 3
的是( )
A. Cu+2Fe3+===Cu2++2Fe2+
B. 10Cl-+2MnO+16H+===2Mn2++5Cl↑+8HO
2 2
C. 2Fe2++Cl===2Fe3++2Cl-
2
D. 5Pb2++2MnO+2HO===5PbO+2Mn2++4H+
2 2
【答案】D
【解析】氧化性:PbO >KMnO >Cl >FeCl >Cu,所以D项反应不可能发生,因为
2 4 2 3
该反应不符合反应规律:
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 在一定条件下,下列微粒的还原性顺序为Cl-