文档内容
铁及其化合物(1)
重难点 题型 分值
1. 掌握铁的化学性质及化学方程式;
重点
2. 铁的氧化物及铁的冶炼。 填 空 和
6-8分
选择
难点 1. 金属铁的化学性质及铁的冶炼
核心知识点一:
一、铁
1. 铁
(1)原子结构
铁位于元素周期表中第4周期Ⅷ族。
(2)物理性质
纯铁是银白色金属,熔、沸点高,具有良好的延展性,是电和热的良导体,抗腐蚀性,
具有能被磁铁吸引的特性,具有金属的通性。
(3)化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
第1页①与非金属单质的反应
常温下:铁被腐蚀生成铁锈,其主要成分为Fe O
2 3
O
2
点燃时:3Fe+2O=====Fe O
2 3 4
Cl 2Fe+3Cl=====2FeCl
2 2 3
S Fe+S=====FeS
②与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4HO(g)=====Fe O +
2 3 4
4H。
2
③与酸的反应
酸 化学方程式或现象
稀HSO Fe+HSO ===FeSO+H↑
2 4 2 4 4 2
Fe不足 Fe+4HNO===Fe(NO )+NO↑+2HO
3 3 3 2
稀
3Fe+8HNO===3Fe(NO )+2NO↑+
3 3 2
HNO Fe过量
3
4HO
2
浓HNO、浓HSO 常温下钝化
3 2 4
④与某些盐溶液CuSO 、FeCl 的反应
4 3
与CuSO 溶液反应的离子方程式为Fe+Cu2+===Fe2++Cu。
4
与FeCl 溶液反应的离子方程式为2Fe3++Fe===3Fe2+。
3
(4)工业上铁的冶炼:Fe O+3CO=====2Fe+3CO。
2 3 2
二、金属铁与水蒸气反应
1. 装置图:
第2页装置:①水蒸气发生
②水蒸气与铁粉反应
③检验产生的气体
2. 反应条件:红色的铁粉与水蒸气
3. 反应现象:有气体产生,吹起的肥皂泡遇火能够产生爆鸣声;灰黑色的粉末变成黑色
的晶体。
4. 反应原理:3Fe+4HO(g)=====Fe O+4H
2 3 4 2
5. 结论:产生氢气和四氧化三铁
三、金属与水反应的规律
1. K、Ca、Na和冷水剧烈反应,生成可溶性碱和H
2
2. Mg和冷水缓慢反应,与沸水迅速反应;Al与冷水难反应,与沸水能反应,生成不溶
性碱和H。
2
3. Zn、Fe、Sn、Pb和高温水蒸气反应,生成不溶性氧化物和H
2
4. Cu、Hg、Ag、Pt、Au不与水反应
核心知识点二
四、铁的氧化物
(1)物理性质
氧化物 FeO Fe O Fe O
2 3 3 4
颜色状态 黑色粉末 红棕色粉末 黑色晶体
铁的价态 + 2 + 3 + 2 、+ 3
溶解性 都不溶于水
第3页(2)化学性质
①稳定性: Fe O、Fe O 较稳定;FeO不稳定,受热能氧化为Fe O。
2 3 3 4 3 4
②与酸反应:FeO、Fe O 都是碱性氧化物,都能与酸反应生成盐和水。分别写出它们
2 3
与盐酸反应的离子方程式:FeO+2H+===Fe2++HO、Fe O+6H+===2Fe3++3HO。
2 2 3 2
(3)Fe O 理解
3 4
①从化学式来看,Fe O 可变式为Fe O·FeO
3 4 2 3
②Fe O 属于纯净物
3 4
③从元素的化合价了看,Fe有+2、+3价
④从氧化性还原性来看,+3价铁的氧化性较强,+2价铁的还原性较强。
⑤从跟酸(H+)的化学反应来看,例如
Fe O+8HCl=2FeCl + FeCl +4HO
3 4 3 2 2
Fe O+8H+=2Fe3++Fe2++4 HO
3 4 2
将Fe O 变式为Fe O·FeO,一些化学方程式或者离子方程式的书写就变的比较容易
3 4 2 3
五、铁的冶炼
1. CO还原氧化铁Fe O
2 3
(1)反应原理:Fe O+3CO=====2Fe+3CO
2 3 2
(2)反应步骤
①检查装置的气密性
②装入药品并固定装置
③向玻璃内通入一氧化碳气体
向玻璃内通入一氧化碳气体
目的是排出装置内的空气,以免加热时CO与空气混合可能会发生爆炸
④给氧化铁加热
⑤停止加热
⑥待试管冷却后停止通一氧化碳
目的:防止生成的铁重新被氧化
防止石灰水倒吸,玻璃管炸裂
CO:早出晚归
酒精灯:迟到早退
(3)实验现象:
①红棕色的固体逐渐变成黑色
②澄清的石灰水变浑浊。
(4)化学方程式
第4页Fe O+3CO=====2Fe+3CO
2 3 2
Ca(OH)+CO =CaCO ↓+H O
2 2 3 2
2. 工业炼铁
(1)设备:高炉
(2)炼铁的原料:
铁矿石:提供铁元素
焦炭:①提供热源、维持炉温
②制还原剂
石灰石:制造炉渣
提供氧气
(3)炼铁的原理:Fe O+3CO=====2Fe+3CO
2 3 2
在高温条件下,用还原剂一氧化碳从铁的氧化物中将铁还原出来。
(4)尾气的处理
尾气的成分含有CO,必须加以处理,方法有:
①用气球收集
②点燃
(5)检验实验中产生了铁:
①用磁铁吸引(物理方法)
②加盐酸或硫酸
(化学方法)
③加硫酸铜溶液
(化学方法)
3. 使金属矿物变成金属的过程,叫做金属的冶炼
(1)热分解法:有些不活泼的金属仅用热分解法就能制得。
(2)电解法:在金属活动性顺序中,钾、钠、钙、铝等几种金属的还原性很强,这些
金属都很容易失去电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,而只
能用通电分解即熔融盐或氧化物的方法来冶炼。
(3)热还原法,多数金属的冶炼过程属于热还原发。常用的还原剂有焦炭、一氧化碳、
氢气等。
核心知识点一:
第5页下列属于铁的物理性质的是( )
A. 铁在潮湿的空气中生锈
B. 铁投入盐酸中产生气泡
C. 铁是电和热的良导体
D. 铁放入CuSO 溶液中表面变成红色
4
【答案】C
【解析】A. 铁在潮湿的空气中生锈是铁与空气中的氧气、水发生反应,属于化学变化,
显示的是化学性质。
B. 铁投入盐酸中产生气泡,是铁与盐酸反应生辰氯化亚铁和氢气,属于化学变化,表
现出化学性质
C. 铁是电和热的良导体,属于物理性质
D. 铁放入CuSO 溶液中表面变成红色,是铁与硫酸铜反应生成硫酸亚铁和铜单质。属
4
于化学变化,表现出化学性质。
【考点】铁的化学反应
将铁片放入下列溶液中,溶液的质量减少的是( )
A. 稀HSO
2 4
B. FeSO 溶液
4
C. CuSO 溶液
4
D. 稀HCl
【答案】C
【解析】A. Fe与稀HSO 反应,生成硫酸亚铁和氢气,开始的溶液是稀硫酸,反应后
2 4
溶液是硫酸亚铁,当物质的量相同时,硫酸亚铁的质量比硫酸的大,所以溶液的质量是增
大的。
B. Fe与FeSO 溶液不反应,所以溶液质量不变。
4
C. Fe与CuSO 溶液反应,生成硫酸亚铁和铜单质,反应前的溶液是硫酸铜,反应后
4
的溶液是硫酸亚铁,当物质的量相同时,硫酸铜的质量比硫酸亚铁的质量大,所以溶液的
质量是减少的。
D. Fe与稀HCl反应,生成氯化亚铁和氢气,反应前溶液是盐酸,反应后溶液是氯化
亚铁,当物质的量相同时,盐酸的质量是小于氯化亚铁的质量的,所以溶液的质量是增大
的。
【考点】铁的相关化学性质
第6页核心知识点二:
判断正误
①在一氧化碳还原氧化铁的实验中,实验结束后应该先停止加热,冷却后再停止通
CO( )
②工业炼铁是在高温下,利用焦炭的还原性把铁从铁矿石中还原出来( )
【答案】①√②×
【解析】①在一氧化碳还原氧化铁的实验中,实验结束后应该先停止加热,冷却后再
停止通CO。目的:防止生成的铁重新被氧化,防止石灰水倒吸,玻璃管炸裂
②工业炼铁是在高温下,利用一氧化碳的还原性把铁从铁矿石中还原出来
【考点】铁的冶炼
下列变化过程不属于金属冶炼的是( )
A. 电解氧化铝
B. 铁在氧气中燃烧
C. 金属氧化物与焦炭在高温下反应
D. 高温下CO还原CuO
【答案】B
【解析】使金属矿物变成金属的过程,叫做金属的冶炼。B属于燃烧。
【考点】金属的冶炼。
关于铁的三种氧化物(FeO、Fe O、Fe O)的下列叙述中正确的是( )
2 3 3 4
A. 铁的三种氧化物中铁元素的化合价完全相同
B. 都是碱性氧化物,都能与盐酸反应生成氯化铁和水
C. 氧化亚铁在空气中加热可生成更稳定的四氧化三铁
D. 四氧化三铁中铁元素有+2价和+3价,它是一种混合物
【答案】C
【解析】FeO中的Fe是+2价,Fe O 中的Fe是+3价,Fe O 中的Fe是+2、+3价,所
2 3 3 4
以A是错误的。B中FeO、Fe O 是碱性氧化物,Fe O 不是碱性氧化物,故B错;氧化亚
2 3 3 4
铁在空气中加热可生成更稳定的四氧化三铁,C是正确的。四氧化三铁中铁元素有+2价和
+3价,它是一种纯净物,所以D错
第7页【考点】铁的氧化物
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 下列说法正确的是( )
A. 赤铁矿的主要成分是Fe O
3 4
B. Fe O 为碱性氧化物,可与水反应生成Fe(OH)
2 3 3
C. 铁锈的主要成分是Fe O
2 3
D. Fe O 中铁元素有+2价和+3价,Fe O 是混合物
3 4 3 4
2. 下列关于铁矿石的说法正确的是( )
A. 赤铁矿的主要成分是四氧化三铁
B. 铁矿石的主要成分与铁锈的主要成分相同
C. 硫铁矿可用于生产铁和硫酸
D. 铁的含量褐铁矿大于赤铁矿
3. 关于氧化铁和氧化亚铁的下列叙述中不正确的是( )
A. 都是碱性氧化物
B. 都能与酸反应生成盐和水
C. 都能与水反应生成氢氧化物
D. 都能被一氧化碳还原为铁
4. 在高温下用一氧化碳还原m克氧化铁得n克铁,氧的相对原子质量为16,则铁的相对
原子质量为( )
2(m−n)
A.
3n
24n
B.
m−n
m−n
C.
8n
n
D.
24(m−n)
5. 氧化铁和氧化铜的固体混合粉末Xg,高温下用足量的一氧化碳还原,得到金属混合物
2.4 g,将生成的二氧化碳气体用足量的澄清石灰水吸收后,产生5 g白色沉淀,则X的值
为( )
A. 2.45
B. 3.20
第8页C. 4.00
D. 7.40
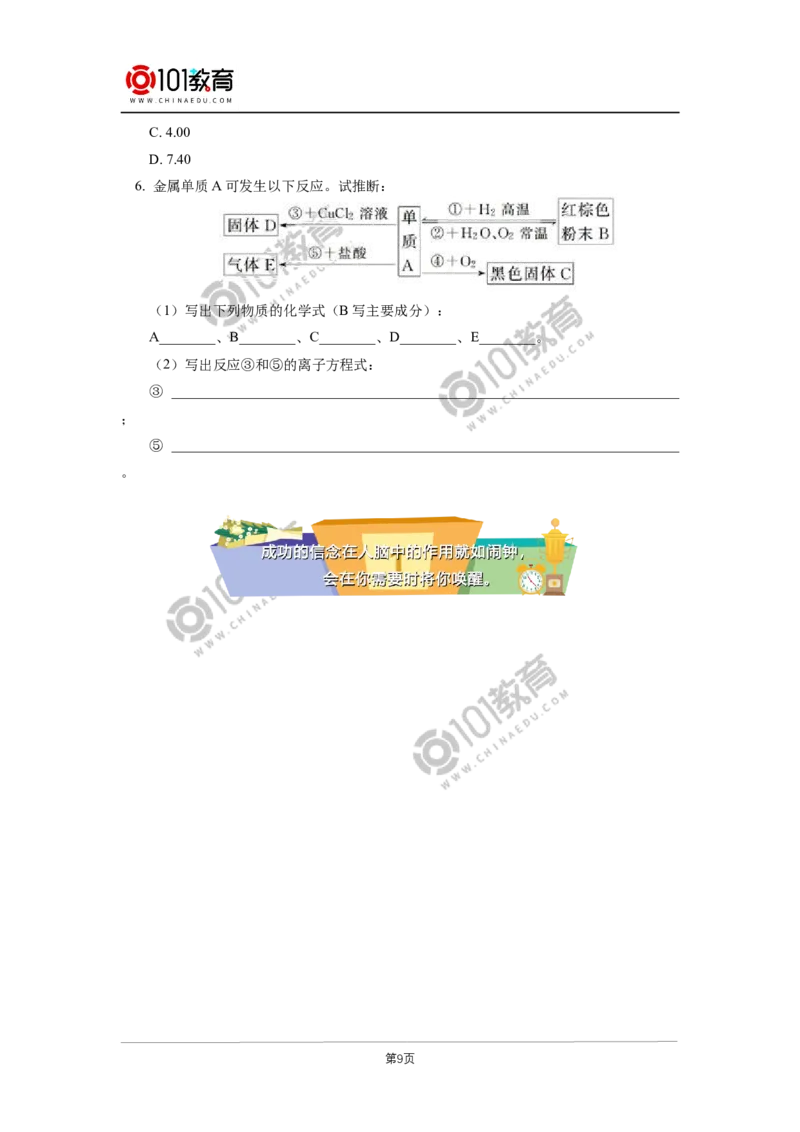
6. 金属单质A可发生以下反应。试推断:
(1)写出下列物质的化学式(B写主要成分):
A________、B________、C________、D________、E________。
(2)写出反应③和⑤的离子方程式:
③ ________________________________________________________________________
;
⑤ ________________________________________________________________________
。
第9页1.【答案】C
【解析】赤铁矿、铁锈的主要成分是 Fe O ,A错误,C正确;Fe O 为碱性氧化物,
2 3 2 3
但不与水反应,B错误;Fe O 为化合物,不是混合物,D错误。
3 4
2.【答案】C
【解析】铁矿石有多种:赤铁矿俗称铁红(主要成分是Fe O)、褐铁矿(主要成分是
2 3
Fe O·nHO)、磁铁矿(主要成分是Fe O )、硫铁矿(主要成分是FeS )等,而铁锈的主
2 3 2 3 4 2
要成分为氧化铁;硫铁矿与氧气反应得到氧化铁和二氧化硫可用于炼铁和制作硫酸。
3.【答案】C
【解析】氧化铁和氧化亚铁都是不溶于水的碱性氧化物,都不能与水反应生成氢氧化
物,都能与酸反应生成相应的盐和水,都具有氧化性,被氢气、一氧化碳、金属铝等还原
剂还原为铁单质。
4.【答案】B
【解析】设铁的相对原子质量为x,
Fe O+3CO=====2Fe+3CO
2 3 2
2x+48 2x
m n
24n
x=
m−n
5.【答案】B
【解析】有关的化学反应:
Fe O +3CO 2Fe+3CO 、CuO+CO Cu+CO 、CO +Ca(OH) ===CaCO
2 3 2 2 2 2 3
+HO;二氧化碳的物质的量=5 g÷100 g·mol-1=0.05 mol,1 mol一氧化碳可结合氧化物
2
中的1 mol氧原子,生成1 mol二氧化碳,氧化物中氧元素的质量=0.05 mol×16 g·mol-1
=0.80 g,金属氧化物的质量为2.40 g+0.80 g=3.20 g,即X=3.20。
6.【答案】(1)Fe Fe O Fe O Cu H
2 3 3 4 2
(2)Fe+Cu2+===Fe2++Cu Fe+2H+===Fe2++H↑
2
【解析】推断题的解题思路:根据物质的物理性质(特别是色、态)和化学性质(相
互转化关系、反应条件等),找出具有特征条件的物质,再由相互转化关系逐步推断。如
本题中结合B、C的颜色及与CuCl 、稀盐酸反应的性质可推知A为Fe。
2
第10页