文档内容
第一节 物质的分类及转化
第2课时 分散系及胶体
基础巩固
1.下列物质不属于分散系的是
A.油漆 B.CuSO ·5H O C.饱和食盐水 D.Fe(OH) 胶体
4 2 3
【答案】B
【解析】
油漆、饱和食盐水、Fe(OH) 胶体都属于分散系,分散系属于混合物,而CuSO ·5H O是纯净
3 4 2
物,不属于分散系,故答案为B
2.按溶液、浊液、胶体的顺序排列正确的是( )。
A.矿泉水、牛奶、豆浆
B.碘酒、泥水、血液
C.白糖水、食盐水、茶叶水
D.Ca(OH) 悬浊液、澄清石灰水、石灰浆
2
[答案]B
[解析]牛奶、豆浆、血液都是常见的胶体,食盐水属于溶液,石灰浆属于悬浊液,故B项正确。
3.向烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入6滴FeCl 饱和溶液。继续加热至液体呈
3
红棕色,停止加热,就制得了Fe(OH) 胶体。下列有关胶体的叙述不正确的是
3
A.胶体是一种分散系,属于混合物
B.胶体的本质特征是能发生丁达尔效应
C.胶体分散质粒子直径介于10-9 -10-7m之间
D.利用丁达尔现象是区分胶体和溶液的一种常用方法
【答案】B
【解析】A.分散系由分散质和分散剂组成,胶体是一种分散系,属于混合物,A正确;
B.胶体的本质特征是胶体粒子直径在1-100nm之间,B错误;
C.胶体分散质粒子直径介于1-100nm之间,即10-9 -10-7m之间,C正确;
D.胶体具有丁达尔现象,溶液不具有丁达尔现象,因此丁达尔现象是区分胶体和溶液的一种常用方法,
D正确;
答案选B。
4.朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的
灌木,落下参差的斑驳的黑影……”。结合这段文字及所学的化学知识判断下列说法正确的是( )
A.荷塘上方的薄雾是水蒸气
B.月光通过薄雾时产生了丁达尔效应
C.薄雾中的微观粒子直径大约是2.5 pm
D.“大漠孤烟直”中的孤烟成分和这种薄雾的成分相同
学科网(北京)股份有限公司[答案]B
【解析】荷塘上方的薄雾是空气中的小液滴,不是水蒸气,属于胶体,胶体粒子的直径为 1~100 nm,可
以产生丁达尔效应,A、C项错误,B项正确;“大漠孤烟直”中的孤烟指的是固体小颗粒,与这种薄雾
的成分不同,D项错误。
5.当光束通过下列物质时,不会出现丁达尔效应的是( )
①Fe(OH) 胶体 ②水 ③蔗糖溶液 ④FeCl 溶液 ⑤云、雾
3 3
A.②④⑤ B.③④⑤
C.②③④ D.①③④
【答案】C
【解析】
①Fe(OH) 胶体属于胶体,具有丁达尔效应,故①不选;
3
②水不属于胶体,不具有丁达尔效应,故②选;
③蔗糖溶液属于溶液,不具有丁达尔效应,故③选;
④FeCl 溶液是溶液,不具有丁达尔效应,故④选;
3
⑤云、雾是胶体,具有丁达尔效应,故⑤不选;
不会出现丁达尔效应的是②③④,故选C。
6.(2022·宁夏·银川二中高一期末)有关氢氧化铁胶体的说法正确的是
A.液体呈黄色
B.其分散质粒子直径小于1nm,不能透过滤纸
C.将FeCl 饱和溶液滴入沸水中,边滴边搅拌,即可制得氢氧化铁胶体
3
D.将大量FeCl 饱和溶液一次性加入沸水中,不能制得胶体
3
【答案】D
【解析】
A.氢氧化铁胶体呈红褐色,A错误;
B.胶体分散质粒子直径大小为1~100nm,胶体粒子能透过滤纸,B错误;
C.将FeCl 饱和溶液滴入沸水中,继续加热至溶液呈红褐色,可制得氢氧化铁胶体,不能搅拌,搅拌能
3
使胶体发生聚沉,C错误;
D.制备氢氧化铁胶体是,应向沸水中逐滴滴加1~2mL饱和FeCl 溶液,并继续加热至液体呈透明的红褐
3
色为止,不能一次性将大量FeCl 饱和溶液一次性加入沸水中,否则会发生聚沉现象,不能制得胶体,D
3
正确;
故答案为:D。
7.由空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶叫霾。当水汽凝结加剧、空气湿度增大时,霾就会
转化为雾。二氧化硫、氮氧化物和可吸入颗粒物是雾霾的主要组成。以下说法不正确的是( )
A.雾霾天,汽车车灯照出光亮“通路”的现象属于丁达尔效应
B.雾和霾都是混合物
C.防雾霾口罩的原理与过滤类似,防雾霾效果好的口罩往往呼吸阻力较大
D. 是指直径小于或等于 的污染物颗粒,该颗粒直径完全在胶体粒子的直径范围内
学科网(北京)股份有限公司【答案】D
【解析】雾霾中含有部分直径在 之间的微粒,故汽车车灯照出光亮“通路”的现象属于丁达
尔效应,A项正确;雾和霾中都含有多种物质,都是混合物,B项正确;防雾霾口罩的原理与过滤类似,
防雾霾效果好的口罩透气性较差,往往呼吸阻力较大,C项正确; 是指直径小于或等于 的污
染物颗粒,即粒子直径小于或等于 ,而胶体中分散质粒子的直径为 ,则 的
直径不完全在胶体粒子的直径范围内,D项错误。
8.下列说法正确的有
①“卤水点豆腐”“黄河入海口处三角洲的形成”都与胶体的性质有关
②在制备Fe(OH) 胶体实验中,可以长时间加热
3
③向Fe(OH) 胶体中加入过量稀硫酸,先有红褐色沉淀生成,然后沉淀溶解形成棕黄色溶液
3
④将饱和氯化铁溶液滴入NaOH溶液中,得到红褐色的Fe(OH) 胶体
3
⑤因为胶粒比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来
⑥不同品牌的墨水不能混用,与胶体聚沉有关
⑦所有胶体的分散质微粒都可以在外加电源作用下做定向移动
A.①③⑤ B.①③⑥⑦ C.①③⑥ D.①②③④⑦
【答案】C
【解析】
①“卤水点豆腐”“黄河入海口处三角洲的形成”与胶体的胶粒带电荷有关,海水中盐电离产生的离子使胶体
发生聚沉得到沙洲,①正确;
②在制备Fe(OH) 胶体实验中,当加热至液体呈红褐色就停止加热,而不能长时间加热,否则胶体会发生
3
聚沉,②错误;
③向Fe(OH) 胶体中加入过量稀硫酸,胶体先发生聚沉形成红褐色沉淀生成,然后发生酸碱中和反应,
3
Fe(OH) 沉淀溶解形成棕黄色溶液,③正确;
3
④将饱和氯化铁溶液滴入NaOH溶液中,发生复分解反应产生红褐色Fe(OH) 沉淀,④错误;
3
⑤因为胶粒比溶液中溶质粒子大,但小于悬浊液的固体小颗粒,能够通过滤纸,所以胶体不能用过滤的
方法把胶粒分离出来,⑤错误;
⑥不同品牌的墨水不能混用,否则胶体会发生聚沉形成沉淀而堵塞钢笔尖,写字不流畅,⑥正确;
⑦有的胶体的分散质微粒选择性吸附正电荷或负电荷,有的则不吸附电荷,因此不是所有胶体的分散质
微粒都可以在外加电源作用下做定向移动,⑦错误;
综上所述可知:说法正确的是①③⑥,故合理选项是C。
9.丁达尔效应是区分胶体与溶液的一种最常用的方法。
(1)如图是在实验室中进行 Fe(OH) 胶体丁达尔效应实验的示意图,该图中有一处明显错误是
3
______________________,原因是____________________(试从分散系分类的角度进行解释说明)。
(2)欲在树林中观察到丁达尔效应,你认为一天中最有可能观察到该现象的时间是________,理由是
___________________________________________________________________。
学科网(北京)股份有限公司[答案] (1)空气中也出现了光柱 进入烧杯前,光束穿过的空气不是胶体,不会产生丁达尔效应
(2)清晨 清晨树林中存在水雾,雾是胶体,光束穿过这些水雾产生丁达尔效应
[解析] (1)进入烧杯前,光束穿过的空气不是胶体,不会产生丁达尔效应。(2)雾是胶体,光束穿过这些
水雾产生丁达尔效应。
10.(2021·河南南阳市·南阳中学高一月考)取一定量Fe O 粉末(红棕色)加入适量某浓度的盐酸中,得
2 3
到呈棕黄色的饱和FeCl 溶液,利用此溶液进行以下实验:
3
(1)写出生成此溶液所发生反应的化学方程式为___________。
(2)取少量该FeCl 溶液置于试管甲中,滴入NaOH溶液,可以观察到有红褐色沉淀生成,反应的化学
3
方程式为___________,此反应属于___________(填基本反应类型)。
(3)在小烧杯甲中加入25 mL蒸馏水,加热至沸腾后,向___________中加入2-2滴___________,继续
煮沸至溶液呈___________ 色,即可制得Fe(OH) 胶体,反应方程式为___________。
3
(4)取丙烧杯中的少量Fe(OH) 胶体置于试管乙中,向试管乙中滴加一定量的稀硫酸,边滴加边振荡,
3
在此过程中可看到试管乙中生成的红褐色沉淀逐渐溶解,最终又得到棕黄色的溶液,发生此变化的化学
方程式为___________。
(5)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是___________。
3 3
A.Fe(OH) 胶体粒子的直径在1~100 nm之间
3
B.Fe(OH) 胶体具有丁达尔效应
3
C.Fe(OH) 胶体是均一的分散系
3
D.Fe(OH) 胶体的分散质能透过滤纸
3
【答案】(1)Fe O+6HCl=2FeCl +3H O
2 3 3 2
(2)FeCl +3NaOH=Fe(OH) ↓+3NaCl 复分解反应
3 3
(3)沸水 饱和氯化铁溶液 红褐色 FeCl +3H O Fe(OH) (胶体)+3HCl
3 2 3
(4)2Fe(OH) +3H SO =Fe (SO )+6H O
3 2 4 2 4 3 2
(5)A
【解析】
(1)Fe O 是金属氧化物,与HCl反应产生FeCl 、HO,反应的化学方程式为:
2 3 3 2
Fe O+6HCl=2FeCl +3H O。
2 3 3 2
(2)取少量该FeCl 溶液置于试管甲中,滴入NaOH溶液,二者发生复分解反应产生Fe(OH) 红褐色沉淀
3 3
和NaCl,反应的化学方程式为:FeCl +3NaOH=Fe(OH) ↓+3NaCl。
3 3
(3)在小烧杯甲中加入25 mL蒸馏水,加热至沸腾后,向沸水中加入2-3滴饱和氯化铁溶液,继续煮沸
至溶液呈红褐色停止加热,就制取得到Fe(OH) 胶体;该反应的化学方程式为:FeCl +3H O Fe(OH) (胶
3 3 2 3
体)+3HCl。
(4)取丙烧杯中的少量Fe(OH) 胶体置于试管乙中,向试管乙中滴加一定量的稀硫酸,边滴加边振荡,
3
首先会看到胶体由于聚沉形成红褐色沉淀,然后发生中和反应产生Fe (SO ) 和水,故最终沉淀溶解又得
2 4 3
到棕黄色的溶液,发生此变化的化学方程式为:2Fe(OH) +3H SO =Fe (SO )+6H O。
3 2 4 2 4 3 2
(5)Fe(OH) 胶体区别于FeCl 溶液最本质的特征是Fe(OH) 胶体粒子的直径在1~100 nm之间,大于溶
3 3 3
学科网(北京)股份有限公司液中溶质离子,故合理选项是A。
能力提升
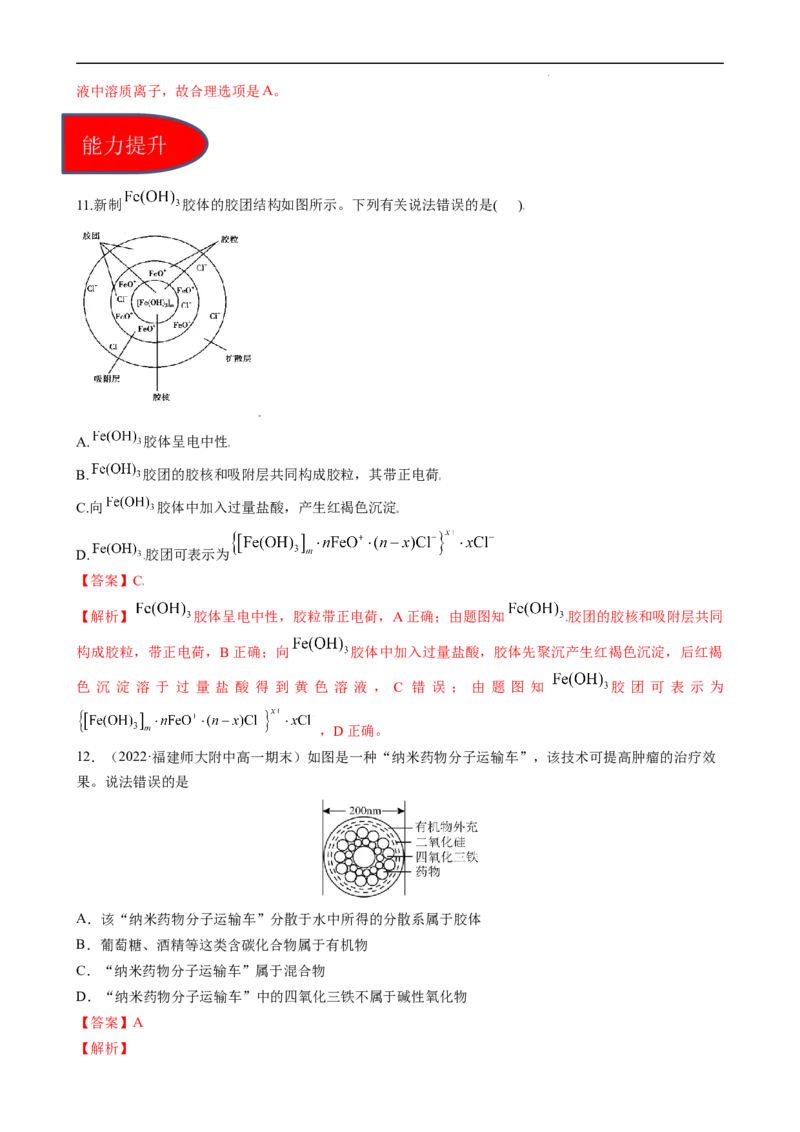
11.新制 胶体的胶团结构如图所示。下列有关说法错误的是( )
A. 胶体呈电中性
B. 胶团的胶核和吸附层共同构成胶粒,其带正电荷
C.向 胶体中加入过量盐酸,产生红褐色沉淀
D. 胶团可表示为
【答案】C
【解析】 胶体呈电中性,胶粒带正电荷,A正确;由题图知 胶团的胶核和吸附层共同
构成胶粒,带正电荷,B正确;向 胶体中加入过量盐酸,胶体先聚沉产生红褐色沉淀,后红褐
色 沉 淀 溶 于 过 量 盐 酸 得 到 黄 色 溶 液 , C 错 误 ; 由 题 图 知 胶 团 可 表 示 为
,D正确。
12.(2022·福建师大附中高一期末)如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效
果。说法错误的是
A.该“纳米药物分子运输车”分散于水中所得的分散系属于胶体
B.葡萄糖、酒精等这类含碳化合物属于有机物
C.“纳米药物分子运输车”属于混合物
D.“纳米药物分子运输车”中的四氧化三铁不属于碱性氧化物
【答案】A
【解析】
学科网(北京)股份有限公司A.该“纳米药物分子运输车”的直径为200nm,分散于水中所得的分散系属于浊液,故A错误;
B.葡萄糖、酒精属于有机物,故B正确;
C.“纳米药物分子运输车”含有二氧化硅、四氧化三铁、药物等,属于混合物,故C正确;
D.四氧化三铁中铁元素显+2、+3价,和盐酸反应生成氯化铁、氯化亚铁两种盐,不属于碱性氧化物,
故D正确;
选A。
13.用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。具
体操作步骤如下:
①取20%白磷的乙醚溶液 ,加蒸馏水 。
②先滴加1%氯化金水溶液 ,再滴加1%的 ,溶液 ,振荡变成棕红色。
③加热煮沸至液体变成透明红色。
④分离提纯,除去无机溶质。
所得分散系中金颗粒直径为 之间。
请回答下列问题:
(1)该分散系属于______,其分散质是______。
(2)用一束强光照射该分散系,从侧面可看到______。
(3)继续加热所得红色透明液体,______(填“能”或“不能”)保持其性质不变。
【答案】 胶体 金颗粒 一条“光亮”的通路 不能
【解析】
(1)所得分散系中金颗粒的直径在 之间,所以该分散系属于胶体,其分散质是金颗粒。
(2)该分散系属于胶体,胶体具有丁达尔效应,所以用一束强光照射该分散系,从侧面能看到一条“光
亮”的通路。
(3)若将所得红色液体继续加热,则会发生聚沉,不能保持其性质不变。
14.(2021·山西实验中学)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明
胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属
铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO ) 中铬元素是+3价,则其中铁元素是___价。CrO 是一种酸根离子,则Fe(CrO ) 属于
2 2 2 2
___(填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和KSO 溶液共同具备的性质是___(填序号)。
2 4
a.都不稳定,密封放置会产生沉淀
b.分散质粒子可通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下
列中的___(填序号)。
学科网(北京)股份有限公司A. B. C.
(4)实验室常用向煮沸的蒸馏水中滴加饱和FeCl 溶液制备Fe(OH) 胶体,证明有胶体生成的最常用的实
3 3
验操作是___。如向其中滴入过量稀硫酸,出现的现象是___。
(5)现有10mL明胶的水溶液与5mLK SO 溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯
2 4
中,设计实验证明SO 能够透过半透膜:___。
【答案】(1)+2 盐
(2)b
(3)C
(4)让一束可见光通过制得的分散系,从侧面观察到一条光亮的“通路",说明制得的是胶体 硫酸少
量时,有红褐色沉淀生成,硫酸过量时,沉淀溶解,溶液变成棕黄色
(5)取烧杯中的少量液体,向其中滴加BaCl [或Ba(NO )]溶液,有白色沉淀产生
2 3 2
【解析】
(1)Fe(CrO ) 中,氧元素的化合价是-2价,总的负价是-8价,铬元素的化合价是+3价,2个铬原子化合
2 2
价是+6价,所以铁元素化合价是+2价;Fe(CrO ) 是由亚铁离子和CrO 组成的盐;
2 2
(2)溶液很稳定,a项错误;胶体和溶液中的分散质粒子都能透过滤纸,b项正确;胶体具有丁达尔效应
而溶液没有,c项错误;故答案为b;
(3)胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜,所以当胶体中混有溶液时,
用渗析的方法来提纯,所以选C;
(4)利用丁达尔现象,具体操作为让一束可见光通过制得的分散系,从侧面观察到一条光亮的“通路",
说明制得的是胶体。氢氧化胶体遇到硫酸这种电解质的溶液时,先发生聚集沉淀,后逐渐溶解,即先生
成红褐色沉淀,后逐渐溶解,变为黄色溶液。
(5)硫酸根离子可以和钡离子之间反应产生白色不溶于硝酸的白色沉淀,具体方法为:取烧杯中的少量
液体,向其中滴加BaCl [或Ba(NO )]溶液,有白色沉淀产生。
2 3 2
学科网(北京)股份有限公司学科网(北京)股份有限公司