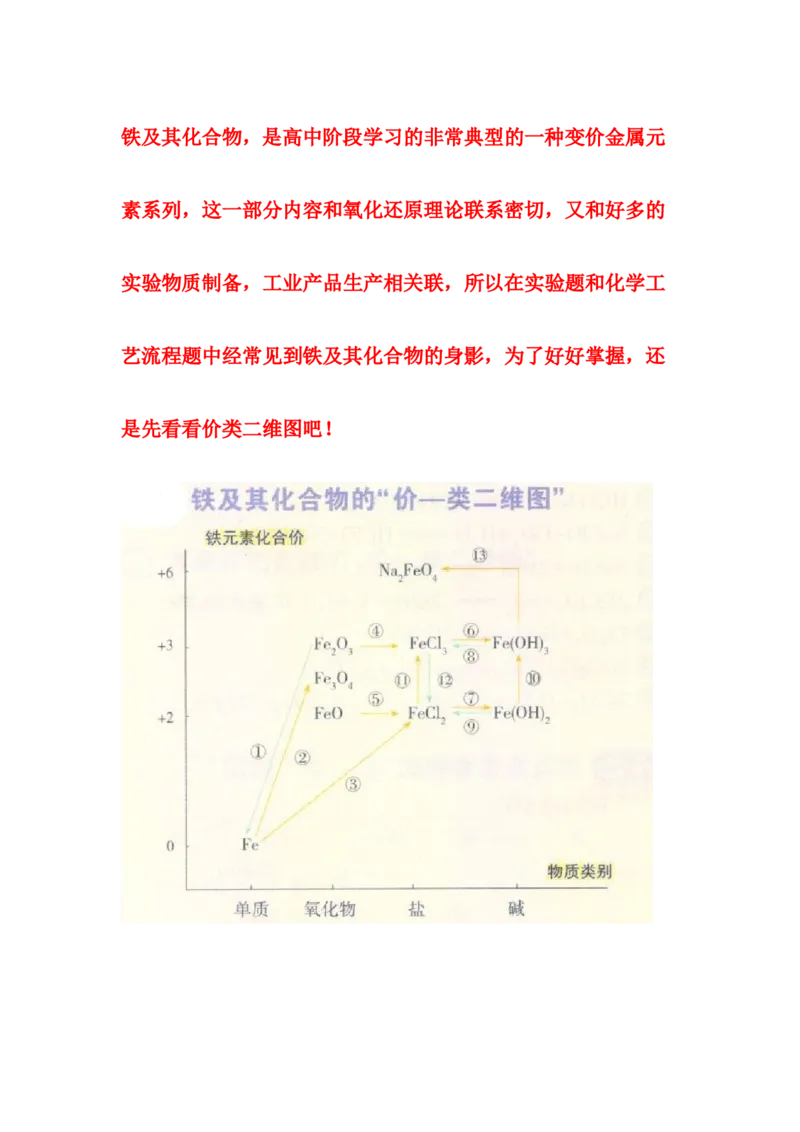
文档内容
铁及其化合物,是高中阶段学习的非常典型的一种变价金属元
素系列,这一部分内容和氧化还原理论联系密切,又和好多的
实验物质制备,工业产品生产相关联,所以在实验题和化学工
艺流程题中经常见到铁及其化合物的身影,为了好好掌握,还
是先看看价类二维图吧!1、铁的误区警示
常温下,铁与水不反应,只有在高温条件下,Fe才会与水蒸
气反应。
1.某研究小组为了探究“铁与水蒸气”能否发生反应及反应的
产物,进行了下列实验:
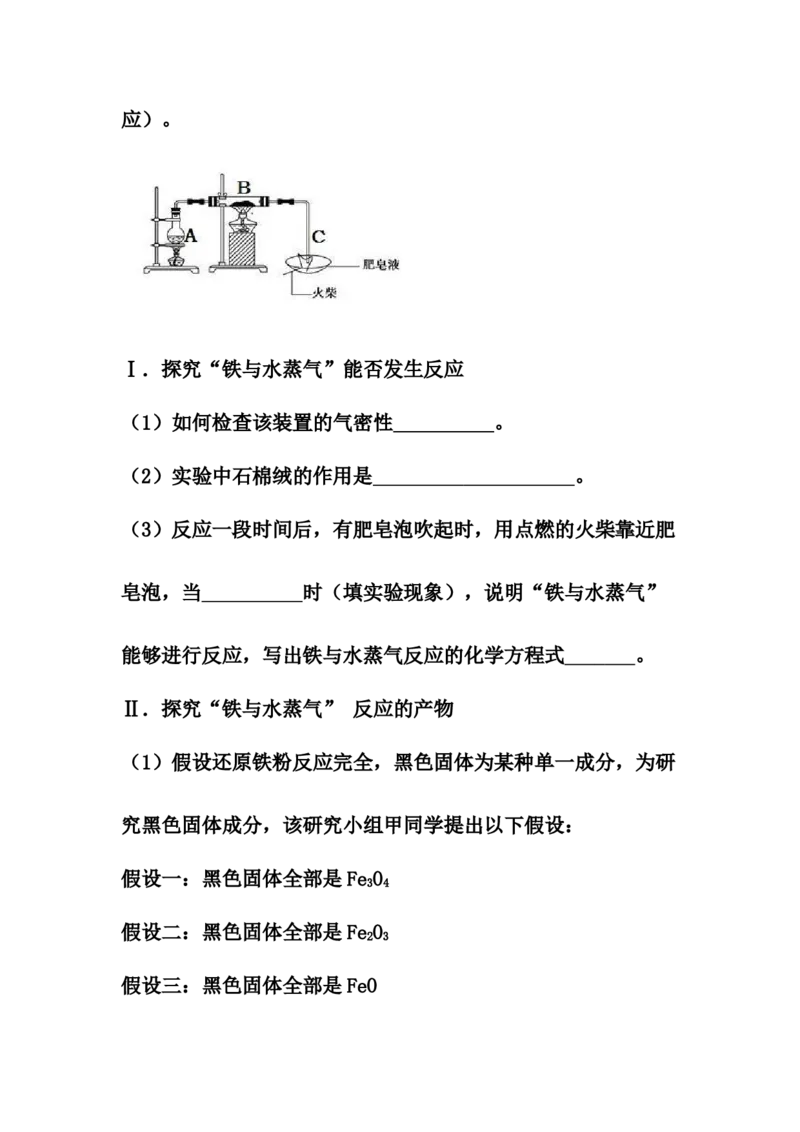
用如图所示实验装置,在硬质玻璃管B中放入还原铁粉和石棉
绒的混合物,再结合一些步骤,就可以完成高温下“Fe与水蒸
气的反应实验”(已知石棉绒是耐高温材料,不与水和铁反应)。
Ⅰ.探究“铁与水蒸气”能否发生反应
(1)如何检查该装置的气密性 。
(2)实验中石棉绒的作用是 。
(3)反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥
皂泡,当 时(填实验现象),说明“铁与水蒸气”
能够进行反应,写出铁与水蒸气反应的化学方程式 。
Ⅱ.探究“铁与水蒸气” 反应的产物
(1)假设还原铁粉反应完全,黑色固体为某种单一成分,为研
究黑色固体成分,该研究小组甲同学提出以下假设:
假设一:黑色固体全部是Fe O
3 4
假设二:黑色固体全部是Fe O
2 3
假设三:黑色固体全部是FeO乙同学认为即使不通过实验就可以否定甲同学的一个假设,你
认为乙同学否认的假设是 ,理由是
。
(2)若假设一正确,请设计实验加以验证,完成下列表格(仪
器自选)。
限选实验试剂:1 mol·L-1硫酸、2 mol·L-1NaOH溶液、新制氯
水、澄清石灰水、酸性KMnO 溶液、KSCN 溶液、品红溶液
4
实验步骤 预期实验现象与结论
取反应后干燥的固体于试管中,
加入足量的1mol·L-1硫酸溶解
【答案加评分标准】Ⅰ.(1)将C处导气管末端浸入水槽中,
微热A处圆底烧瓶,气管末端出现气泡,停止加热后气管末端
出现一段水柱,则气密性好,否则气密性不好(2分)(2)增
大铁粉与水蒸气的接触面积(1分)
△
(3)肥皂泡破裂,有爆鸣声(2分)3Fe+4H O(g)
2
Fe O +4H (2分)
3 4 2Ⅱ. (1)假设二(1分)由于Fe O 为红棕色粉末,则可以根据
2 3
固体颜色直接否定假设二(1分)
实验步骤 预期实验现象与结论
取反应后干燥的固体于试管中,加入足量的1mol·L-1硫酸硫酸溶
解
①取少量上述溶液于一试管
①溶液变红色,则反应后的固体
中,滴加1~2滴KSCN 溶液(1
中含有+3价的铁(1分)
分)
②溶液不显紫色,则反应后的固
②另取少量上述溶液于另一试
体中含有+2价的铁,综合上述步
管中,滴加2~3滴酸性KMnO
4 骤①②可知假设一正确。(2分)
溶液(1分)
【解析】
试题分析:Ⅰ.(1)气密性检查一般用液差法,即将C处导气
管末端浸入水槽中,微热A处圆底烧瓶,气管末端出现气泡,
停止加热后气管末端出现一段水柱,则气密性好,否则气密性
不好。
(2)石棉绒的接触面积大,可增大铁粉与水蒸气的接触面积,
加快反应速率。
(3)反应一段时间后,有肥皂泡吹起时,反应中有氢气产生,
因此用点燃的火柴靠近肥皂泡,当肥皂泡破裂,有爆鸣声时(填实验现象),说明“铁与水蒸气”能够进行反应,铁与水
△
蒸气反应的化学方程式为3Fe+4H O(g) Fe O +4H 。
2 3 4 2
Ⅱ.(1)由于Fe O 为红棕色粉末,则可以根据固体颜色是黄
2 3
色直接否定假设二。
(2)四氧化三铁中铁元素的价态有+2价和+3价,可以根据
亚铁离子和铁离子检验验证假设一正确,即
实验步骤 预期实验现象与结论
取反应后干燥的固体于试管中,加入足量的1mol·L-1硫酸硫酸溶
解
①取少量上述溶液于一试管
①溶液变红色,则反应后的固体中含
中,滴加1~2滴KSCN 溶液
有+3价的铁(1分)
(1分)
②溶液不显紫色,则反应后的固体中
②另取少量上述溶液于另一
含有+2价的铁,综合上述步骤①②可
试管中,滴加2~3滴酸性
知假设一正确。(2分)
KMnO 溶液(1分)
4
考点:考查铁与水蒸气反应实验设计与探究
2.铁的还原性
铁是变价金属,与强氧化剂反应生成三价铁,与弱氧化剂反
应生成二价铁。
(1)铁与弱氧化剂
如:H+、Cu2+、S、I 反应时,被氧化为+2价。
2
(2)铁与H O(g)、O 反应的氧化产物为Fe O 。
2 2 3 4
(3)铁与Cl 、Br 等反应时,被氧化为+3价。
2 22.下列反应中,铁只能生成高价化合物的是
A.过量的铁与稀HNO 反应 B.铁粉与硫蒸气反应
3
C.铁粉与氯气反应 D.红热的铁粉与水蒸气反应
【答案】C
【解析】
【分析】
铁遇到强的氧化剂反应生成三价铁离子,遇到弱的氧化剂反应
生成二价铁离子,据此解答.
【详解】
A.过量的铁与稀HNO 反应硝酸亚铁,故A不选;
3
B.铁粉与硫蒸气反应生成硫化亚铁,故B不选;
C.氯气具有强的氧化性,能够与铁反应生成氯化铁,故C选;
D.红热的铁粉与水蒸气反应生成四氧化三铁和氢气,故D不选;
故选:C。
3. 铁的氧化物
(1)铁的氧化物中Fe的常见化合价只有+2价和+3价,
Fe O 可以看成由FeO和Fe O 按物质的量之比1∶1组合而成的
3 4 2 3复杂氧化物,通常也可写成FeO·Fe O 的形式。
2 3
(2)FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物。
2 3 3 4
(3)Fe O 与盐酸反应可看作Fe O 、FeO分别与盐酸反应,然
3 4 2 3
后把两个反应式相加。
(4)FeO、Fe O 遇氧化性酸(如HNO )发生氧化还原反应,+2
3 4 3
价的铁均被氧化成+3价。
3.下列关于铁的氧化物说法不正确的是( )
A.铁的氧化物通常状况下都是有色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶
液中同时存在Fe2+和Fe3+
C.氧化铁是铁锈的主要成分,因此氧化铁俗称为铁锈
D.工业上常使用铁的氧化物做原料冶炼铁
【答案】C
【解析】
A、铁的氧化物通常状况下都是有色固体,如氧化铁是红棕色,
氧化亚铁和四氧化三铁都是黑色的,故A正确;B、四氧化三铁
是一种复杂的铁的氧化物,其中1/3是Fe2+、2/3是Fe3+,
Fe O 可看作是由FeO、Fe O 形成的化合物。[实质是
3 4 2 3
Fe(FeO ) ,偏铁酸亚铁盐],,它与盐酸反应后的溶液中同时存
2 2在Fe2+和Fe3+,B正确;C、铁锈的主要成分是Fe O ·XH O,故C
2 3 2
错误;D、 工业上常使用铁的氧化物做原料用一氧化碳冶炼铁,
故D正确;故选C。
4. Fe(OH) 制备时的注意事项
2
(1)Fe2+易被氧化,所以FeSO 溶液要现用现配,且配制
4
FeSO 溶液的蒸馏水要煮沸除去氧气。
4
(2)为了防止NaOH溶液加入时带入空气,可将吸有NaOH溶
液的长滴管伸入到FeSO 溶液的液面下,再挤出NaOH溶液。
4
(3)为防止Fe2+氧化,还可向盛有FeSO 溶液的试管中加入少
4
量煤油液封。
4.某实验小组在实验室利用氨气和新制备的硫酸亚铁溶液反应
制备氢氧化亚铁。
(一)制备硫酸亚铁溶液
(1)步骤①,加入稀硫酸的目的是_______。
(2)步骤②,加入还原铁粉后观察到的现象是_______。
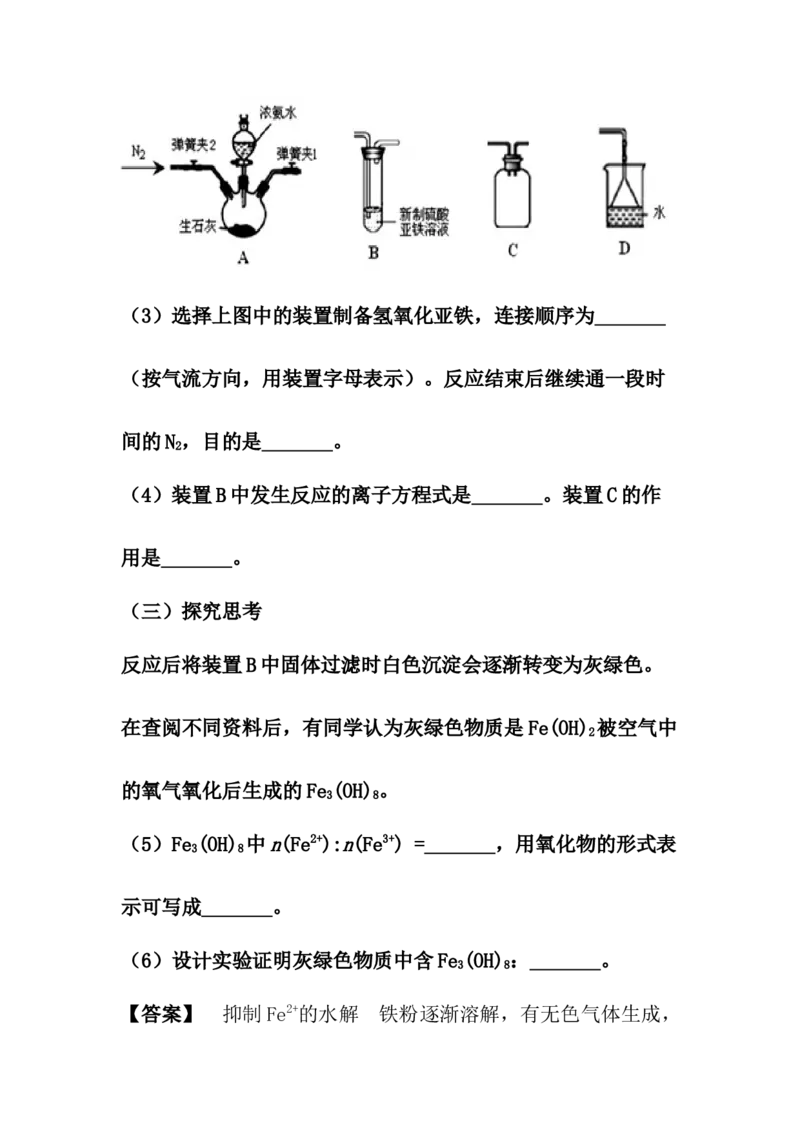
(二)制备氢氧化亚铁(3)选择上图中的装置制备氢氧化亚铁,连接顺序为_______
(按气流方向,用装置字母表示)。反应结束后继续通一段时
间的N ,目的是_______。
2
(4)装置B中发生反应的离子方程式是_______。装置C的作
用是_______。
(三)探究思考
反应后将装置B中固体过滤时白色沉淀会逐渐转变为灰绿色。
在查阅不同资料后,有同学认为灰绿色物质是Fe(OH) 被空气中
2
的氧气氧化后生成的Fe (OH) 。
3 8
(5)Fe (OH) 中n(Fe2+):n(Fe3+) =_______,用氧化物的形式表
3 8
示可写成_______。
(6)设计实验证明灰绿色物质中含Fe (OH) :_______。
3 8
【答案】 抑制Fe2+的水解 铁粉逐渐溶解,有无色气体生成,溶液由黄色逐渐变为浅绿色 A C B D 防止拆除装置时残留的
氨气逸出污染空气 Fe2+ + 2NH + 2H O= Fe(OH) + 2NH + 安全
3 2 2 4
瓶,防倒吸 1:2 FeO ·Fe O ·4H O 取少量灰绿色物质于
2 3 2
试管中,加入稀盐酸(或稀硫酸)溶解,将溶液分成两份,一
份滴入几滴KSCN溶液,变为血红色;另一份加入适量
K [Fe(CN) ]溶液,生成蓝色沉淀,则灰绿色物质中含Fe (OH)
3 6 3 8
【解析】该实验的目的是利用氨气和新制备的硫酸亚铁溶液反
应制备氢氧化亚铁。(一)制备硫酸亚铁溶液,向硫酸铁晶体
中加入去氧蒸馏水和稀硫酸,再加入过量的还原铁粉,将
Fe3+还原成Fe2+,得到硫酸亚铁溶液。(1)步骤①,加入稀硫
酸的目的是,目的是抑制Fe3+的水解;(2)步骤②,加入还原
铁粉后,铁粉和酸反应和Fe3+反应,观察到的现象是铁粉逐渐
溶解,有无色气体生成,溶液由黄色逐渐变为浅绿色;(二)
制备氢氧化亚铁,原理是将氨气通入硫酸亚铁溶液中,此过程
的关键是隔绝空气。(3)制备氢氧化亚铁的装置中,A装置的作用是将浓氨水滴到生石灰上,使生石灰和水反应放出热量,
放出氨气,氮气的作用是将装置中的空气全部排出,B装置的
作用是氨气和硫酸亚铁溶液反应产生氢氧化亚铁,C装置的作
用是作为安全瓶防止倒吸,D装置的作用是吸收尾气。故装置
连接顺序为A C B D;反应结束后继续通一段时间的N ,目
2
的是将装置中残留的氨气全部被吸收,防止拆除装置时残留的
氨气逸出污染空气;(4)装置B中发生反应的离子方程式是:
Fe2+ + 2NH + 2H O= Fe(OH) + 2NH +,装置C在A和B之间,故
3 2 2 4
C的作用是:安全瓶,防倒吸;(5)Fe (OH) 中,3个Fe带8
3 8
个正电荷,故n(Fe2+):n(Fe3+) =1:2,用氧化物的形式表示可
写成FeO ·Fe O ·4H O;(6)要设计实验证明灰绿色物质中
2 3 2
含Fe (OH) ,即要证明此物质中既有Fe2+又有Fe3+,Fe2+用
3 8
K [Fe(CN) ]溶液检验,Fe3+用KSCN溶液检验,故试验方法为:
3 6
取少量灰绿色物质于试管中,加入稀盐酸(或稀硫酸)溶解,
将溶液分成两份,一份滴入几滴KSCN溶液,变为血红色;另一份加入适量K [Fe(CN) ]溶液,生成蓝色沉淀,则灰绿色物质中
3 6
含Fe (OH) 。
3 8
点睛:实验题的关键是搞清楚实验目的:利用氨气和新制备的
硫酸亚铁溶液反应制备氢氧化亚铁。结合题意,先制备硫酸亚
铁溶液,向硫酸铁晶体中加入去氧蒸馏水和稀硫酸,再加入过
量的还原铁粉,将Fe3+还原成Fe2+,得到硫酸亚铁溶液,再制备
氢氧化亚铁,原理是将氨气通入硫酸亚铁溶液中,此过程的关
键是隔绝空气。就可知各装置的目的,各个措施的目的,就可
以顺利的解题。
5. 检验Fe2+的注意事项
(1)只含Fe2+的溶液
检验Fe2+加入试剂的顺序:待测液――→不变色――→ 红
色(含Fe2+,不含Fe3+)。
①加KSCN溶液前,不能加氧化性物质[如H O 、NO(H+)等],
2 2
防止Fe2+被氧化。
②氧化剂不能选用酸性KMnO 溶液,原因有:酸性KMnO 溶液
4 4
本身显紫红色,对Fe(SCN) 红色有干扰;酸性KMnO 溶液能氧
3 4
化KSCN,溶液不变红色,不能证明不含Fe2+。
(2)同时含有Fe2+和Fe3+的溶液Fe2+对检验Fe3+无干扰,可以滴加KSCN溶液检验Fe3+;
Fe3+对检验Fe2+有干扰,不能加KSCN溶液检验Fe2+,通常
向溶液中滴加适量酸性KMnO 溶液,溶液紫红色褪去说明含有
4
Fe2+(当然如果含有氯离子这个方法就不行了)。
5.为了检验某氯化亚铁溶液是否变质,可向溶液中加入( )
A.氢氧化钠溶液 B.铁片
C.硫氰酸钾溶液 D.酸性KMnO 溶液
4
【答案】C
【解析】FeCl 与 NaOH 溶液反应先生成 Fe(OH) ,后被 O 氧化为
2 2 2
Fe(OH) ,会干扰 Fe3+的检验,故 A 项不符合;Fe 与 Fe3+反应时,
3
溶液颜色变化不明显,故 B 项不符合;Fe2+与 SCN-不反应,但
Fe3+与 SCN-反应使溶液变红色,故 C 项符合;KMnO 只与 Fe2+反
4
应,不与Fe3+反应,故D项不符合。
6. Fe2+、Fe3+、Fe之间的相互转化关系
(1)Fe只具有还原性。可被弱氧化剂(H+、S等)氧化成Fe2
+,被强氧化剂(Cl 等)氧化成Fe3+。
2
(2)Fe2+既有氧化性又有还原性。可被强氧化剂[Cl 、
2
KMnO (H+)等]氧化为Fe3+;可被还原剂(Al、Zn、CO、C等)还原
4
为Fe。
(3)Fe3+只具有氧化性,可被弱还原剂(Fe、Cu等)还原为Fe2+,被强还原剂(Al、Zn、CO等)还原为Fe。
6.阅读下列材料后,回答相应问题。
一个体重50Kg的健康人,含铁2g。这2g铁在人体中不是以单
质金属的形式存在的,而是以Fe2+和Fe3+的形式存在。二价铁离
子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价
铁盐,如硫酸亚铁(FeSO )。服用维生素C,可使食物中的三价
4
铁离子还原成二价铁离子,有利与铁的吸收。
(1)人体中经常进行Fe2+ Fe3+的转化,A中Fe2+作______剂,B
中Fe3+作________剂。
(2)“服用维生素C,可使食物中的三价铁离子还原成二价铁离
子。”这句话指出维生素C在这一反应中作__________剂,具
有___________性。
【答案】还原 氧化 还原 还原
【解析】
(1)所含元素化合价升高的物质为还原剂,含元素化合价降低
的物质为氧化剂;(2)根据铁元素的化合价变化可知+3价Fe3+被还原来分析维生素
C的作用,并利用还原剂具有还原性来解答。
【详解】
(1)在A中铁元素的化合价由+2价升高到+3价,铁元素的化合
价升高,则A中Fe2+作还原剂,在B中铁元素的化合价由+3价
降低为+2价,铁元素的化合价降低,则B中Fe3+作氧化剂;
(2)由信息维生素C可使食物中的+3价Fe3+还原成+2价Fe2+,该
反应中铁元素的化合价降低,则维生素C中某元素的化合价升
高,即维生素C为还原剂,体现还原性。
【点睛】
本题属于信息习题,考查氧化还原反应中氧化剂、还原剂的概
念及其与氧化性、还原性的关系,明确元素的化合价变化来分
析是解答本题的关键。
7. 铁及其化合物的颜色
铁粉是黑色的;铁块是银白色的
Fe2+—浅绿色Fe O —黑色晶体
3 4
Fe(OH) —白色沉淀
2
Fe3+—黄色
Fe(OH) —红褐色沉淀
3
Fe(SCN) —血红色溶液
3
FeO—黑色粉末
Fe O —红棕色粉末
2 3
FeS—黑色固体
这部分内容有时候作为基础题考察记忆颜色的准确性,更多
的时候是作为一些推断题的突破口。所以就不再找习题了,仔
细在以后的题目中体会就行了。
8. 铁的归纳
(1)金属阳离子被还原不一定得到金属单质
如:Fe3+―→Fe2+。
(2)离子共存问题
①Fe3+与I-、S2-、HS-、SO、HSO等因发生氧化还原反应而
不能大量共存。
②Fe2+与MnO(H+)、NO(H+)、ClO-等因发生氧化还原反应而
不能大量共存。
(3)除杂问题(括号内为杂质)
①FeCl 溶液(FeCl ):加足量氯水或H O 或通入足量Cl 。
3 2 2 2 2
②FeCl 溶液(FeCl ):加足量铁粉,充分反应后过滤。
2 3
③FeSO 溶液(CuSO ):加足量铁粉,充分反应后过滤。
4 4
8.氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、
印染、造纸行业的污水处理。某课题小组设计如下方案制备氯
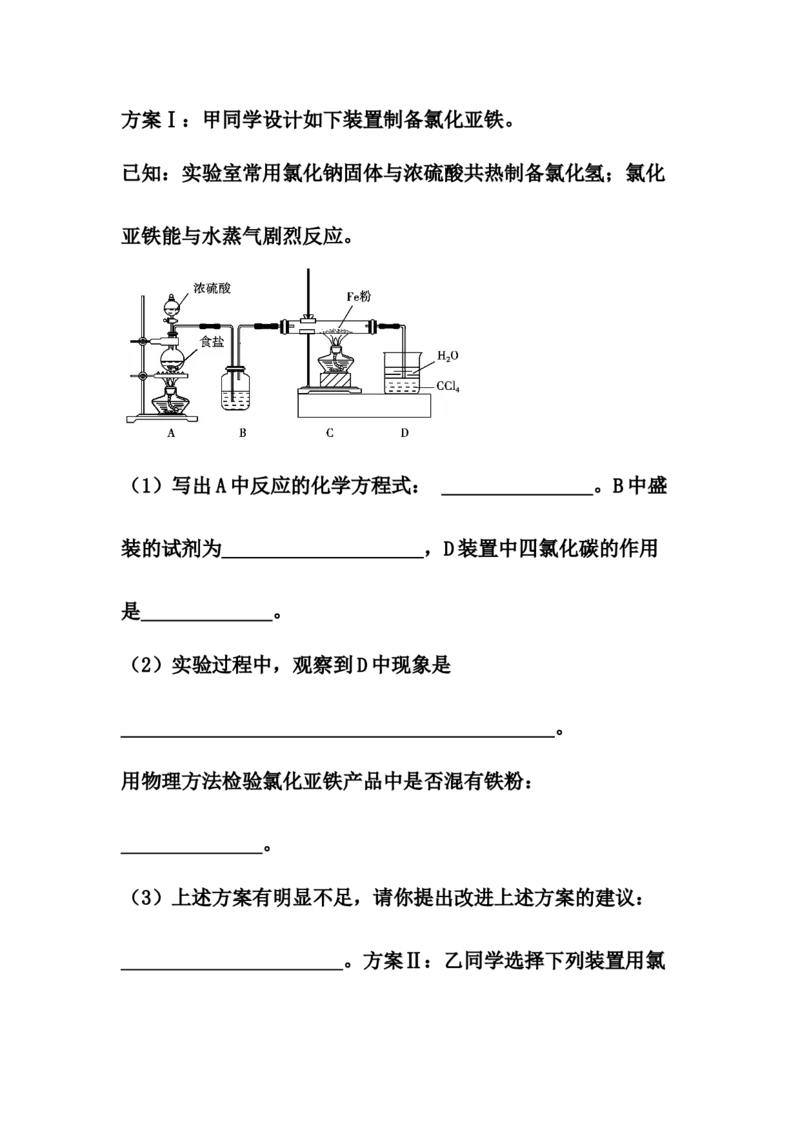
化亚铁并探究氯化亚铁(Fe2+)的还原性。方案Ⅰ:甲同学设计如下装置制备氯化亚铁。
已知:实验室常用氯化钠固体与浓硫酸共热制备氯化氢;氯化
亚铁能与水蒸气剧烈反应。
(1)写出A中反应的化学方程式: _______________。B中盛
装的试剂为____________________,D装置中四氯化碳的作用
是_____________。
(2)实验过程中,观察到D中现象是
___________________________________________。
用物理方法检验氯化亚铁产品中是否混有铁粉:
______________。
(3)上述方案有明显不足,请你提出改进上述方案的建议:
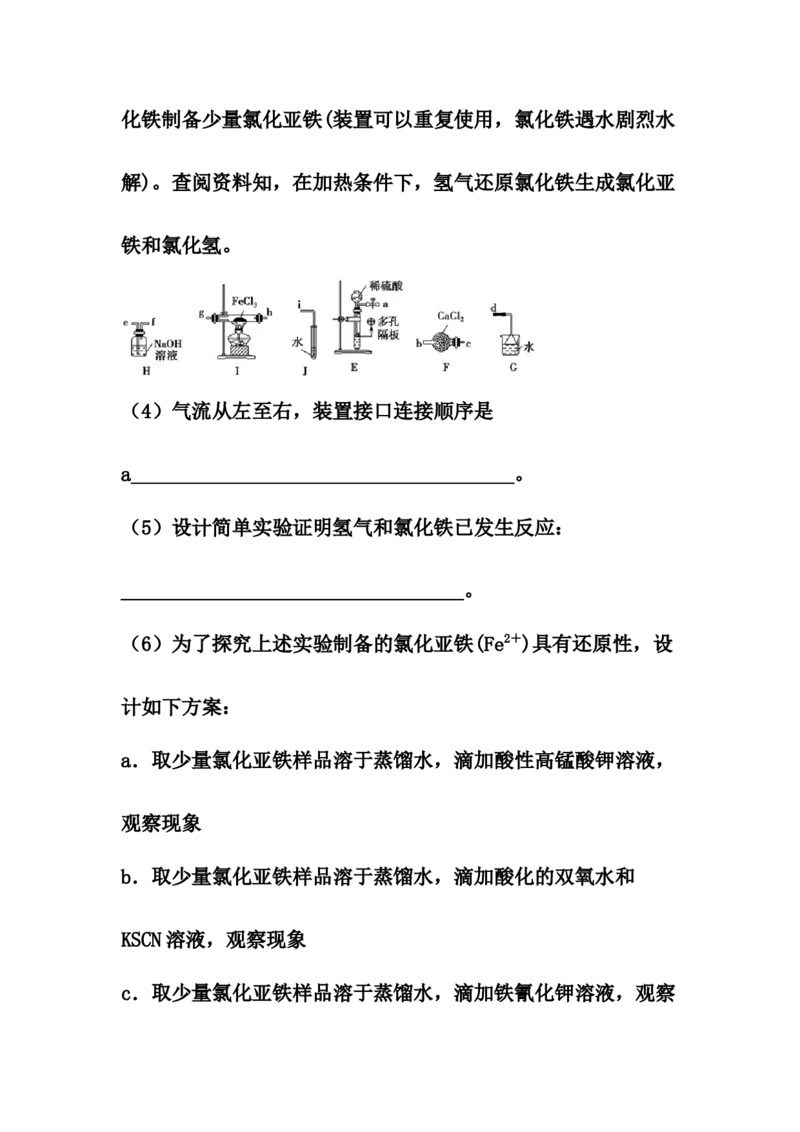
______________________。方案Ⅱ:乙同学选择下列装置用氯化铁制备少量氯化亚铁(装置可以重复使用,氯化铁遇水剧烈水
解)。查阅资料知,在加热条件下,氢气还原氯化铁生成氯化亚
铁和氯化氢。
(4)气流从左至右,装置接口连接顺序是
a______________________________________。
(5)设计简单实验证明氢气和氯化铁已发生反应:
__________________________________。
(6)为了探究上述实验制备的氯化亚铁(Fe2+)具有还原性,设
计如下方案:
a.取少量氯化亚铁样品溶于蒸馏水,滴加酸性高锰酸钾溶液,
观察现象
b.取少量氯化亚铁样品溶于蒸馏水,滴加酸化的双氧水和
KSCN溶液,观察现象
c.取少量氯化亚铁样品溶于蒸馏水,滴加铁氰化钾溶液,观察现象
d.取少量氯化亚铁样品溶于蒸馏水,先加KSCN溶液,后加氯
水,观察现象
上述方案合理的是________(填代号)。
【答案】2NaCl+H SO (浓) = Na SO +2HCl↑ 浓硫酸
2 4 2 4
防倒吸 有气泡逸出 用磁铁吸附,若有黑色粉末被吸起,
则混有铁粉;否则,没有混入铁粉 在C、D之间增加一个盛
有浓硫酸的试剂瓶(或将D换成盛装碱石灰的干燥管)
cb→gh→cb→d 在G中滴加硝酸银溶液,若产生白色沉淀,
则已发生反应;否则,未发生反应 d
【解析】
(1)氯化钠固体与浓硫酸共热生成硫酸钠和氯化氢;装置B中
加入的试剂是浓硫酸;四氯化碳与氯化氢不反应,四氯化碳起
防倒吸作用;
(2)磁铁可以吸附铁粉,若有黑色粉末被吸起,则混有铁粉;
否则,没有混入铁粉;(3)在C、D之间增加一个盛有浓硫酸的试剂瓶(或将D换成盛
装碱石灰的干燥管);
(4)该装置包括制取氯化氢、干燥、氯化氢与铁反应、干燥
(防止水蒸气与铁反应)、尾气吸收(防倒吸),气流从左至
右,装置接口连接顺序是a→cb→gh→cb→d;
(5)H +2FeCl =2FeCl +2HCl,检验氯化氢可以确认氢气与氯化
2 3 2
铁是否已发生反应;
(6)根据验证氯化亚铁中(Fe2+)具有还原性,要排除Cl-、
Fe3+的干扰进行判断。
【详解】
(1)氯化钠固体与浓硫酸共热生成硫酸钠和氯化氢,反应方程
式为:2NaCl+H SO (浓)=Na SO +2HCl↑,装置B中加入的试
2 4 2 4
剂是浓硫酸,四氯化碳与氯化氢不反应,四氯化碳起防倒吸作
用,故答案为:2NaCl+H SO (浓)=Na SO +2HCl↑,浓硫酸,
2 4 2 4
防倒吸。
(2)氯化氢与铁粉反应生成氯化亚铁和氢气,在D中逸出了氢气,用磁铁可以吸附铁粉,若有黑色粉末被吸起,则混有铁粉;
否则,没有混入铁粉,故答案为:有气泡逸出;用磁铁吸附,
若有黑色粉末被吸起,则混有铁粉;否则,没有混入铁粉。
(3)该装置包括制取氯化氢、干燥、氯化氢与铁反应、干燥
(防止水蒸气与铁反应)、尾气吸收(防倒吸),所以在C、D
之间增加一个盛有浓硫酸的试剂瓶(或将D换成盛装碱石灰的干
燥管),故答案为:在C、D之间增加一个盛有浓硫酸的试剂瓶
(或将D换成盛装碱石灰的干燥管)。
(4)该装置包括制取氯化氢、干燥、氯化氢与铁反应、干燥
(防止水蒸气与铁反应)、尾气吸收(防倒吸),气流从左至
右,装置接口连接顺序是a→cb→gh→cb→d,
故答案为:cb→gh→cb→d。
(5)H +2FeCl =2FeCl +2HCl,检验氯化氢可以确认氢气与氯化
2 3 2
铁是否已发生反应,方法为:在G中滴加硝酸银溶液,若产生
白色沉淀,则已发生反应;否则,未发生反应,故答案为:在G中滴加硝酸银溶液,若产生白色沉淀,则已发生反应;否则,
未发生反应。
(6)验证氯化亚铁中(Fe2+)具有还原性,要排除Cl-、Fe3+的干
扰。
a.氯离子能和酸性高锰酸钾溶液反应,也能使溶液褪色,故a
错误;
b.加入酸化的双氧水和KSCN溶液,可能有Fe3+的干扰,所以溶
液显红色不一定是Fe2+被氧化为Fe3+,故b错误;
c.加入铁氰化钾溶液,只能检验Fe2+,不能证明Fe2+具有还原
性,故C错误;
d.滴加KSCN溶液,无颜色变化,再滴加氯水,溶液变红色,说
明Fe2+具有还原性,故d正确。
故答案为:d。