文档内容
《配合物与超分子》第一课时 教学设计
课题 《配合物与超分子》 单元 3 学科 化学 年级 高二
本章内容比较系统地介绍了晶体结构与性质,内容比较丰富。第三章作
为选修性必修2结尾章,与前两章一起构成“原子、分子、晶体的结构与性
质”三位一体的物质结构与性质模块的基本内容。本节教学内容是人教版高中
化学选择性必修第二册第三章《晶体结构与性质》第四节《配合物与超分子》
第一课时。
教材
本节安排了“配合物与超分子”这部分内容。学生通过学习这部分知识,
分析
能从微观角度理解配位键的形成条件和表示方法,能判断常见的配合物。能利
用配合物的性质去推测配合物的组成,从而形成“结构决定性质”的认知模
型。了解超分子的结构特点与性质。
宏观辨识与微观探析:能从微观角度理解配位键的形成条件和表示方法,
能判断常见的配合物。
教学
目标
与核
证据推理与模型认知:能利用配合物的性质去推测配合物的组成,从而形
心素
成“结构决定性质”的认知模型。
养
重点 配合物与超分子
难点
教学过程
教学环节 教师活动 学生活 设计意图
动
导入新课 思考:无水CuSO 是白色的,为什么CuSO ·5H O晶体 思考 通过思
4 4 2
却是蓝色的? 考,引发
学生兴
趣,提高
学生学习
积极性。
讲授新课 第四节 配合物与超分子
一、配合物
实验3-2
向盛有下表中固体样品的试管中,分别加入足量的
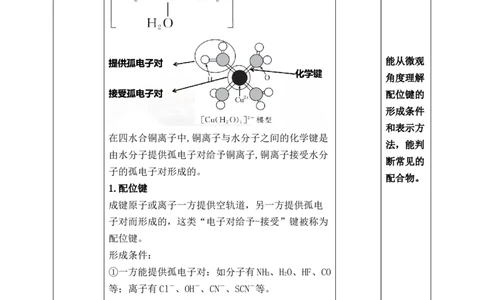
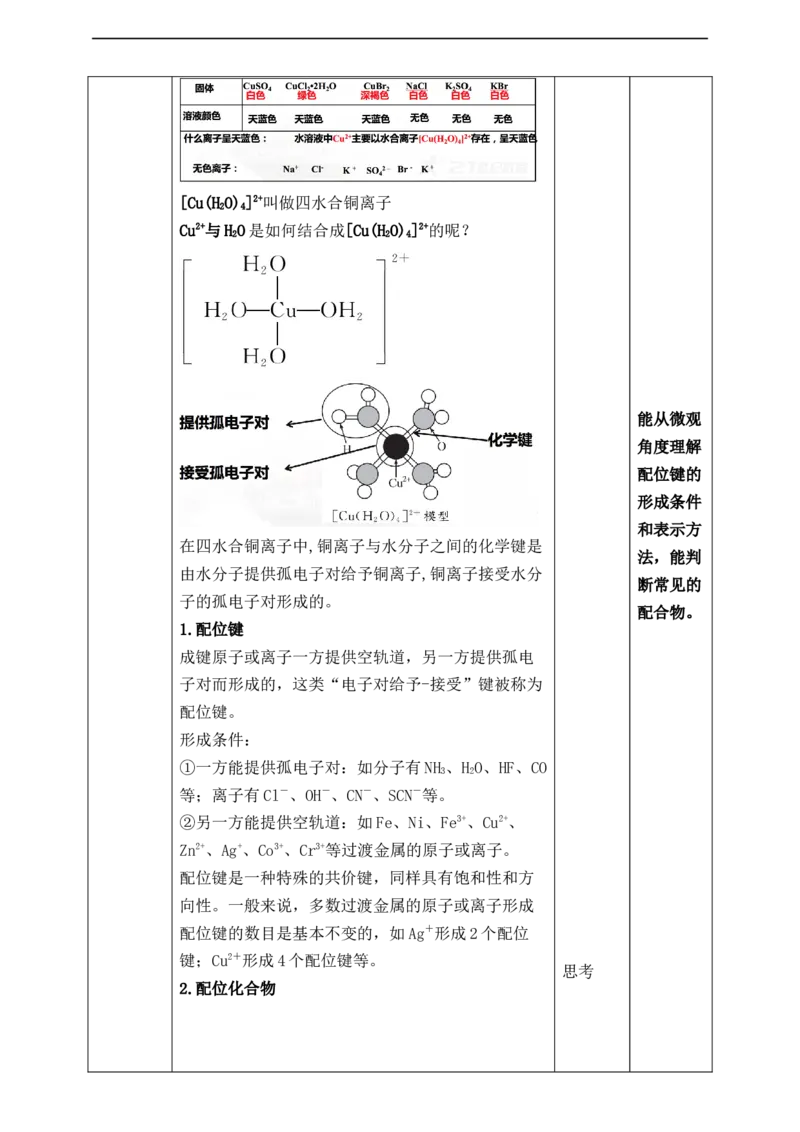
水,观察实验现象并填写下表[Cu(H O) ]2+叫做四水合铜离子
2 4
Cu2+与H O是如何结合成[Cu(H O) ]2+的呢?
2 2 4
能从微观
角度理解
配位键的
形成条件
和表示方
在四水合铜离子中,铜离子与水分子之间的化学键是
法,能判
由水分子提供孤电子对给予铜离子,铜离子接受水分
断常见的
子的孤电子对形成的。
配合物。
1.配位键
成键原子或离子一方提供空轨道,另一方提供孤电
子对而形成的,这类“电子对给予-接受”键被称为
配位键。
形成条件:
①一方能提供孤电子对:如分子有NH 、H O、HF、CO
3 2
等;离子有Cl-、OH-、CN-、SCN-等。
②另一方能提供空轨道:如Fe、Ni、Fe3+、Cu2+、
Zn2+、Ag+、Co3+、Cr3+等过渡金属的原子或离子。
配位键是一种特殊的共价键,同样具有饱和性和方
向性。一般来说,多数过渡金属的原子或离子形成
配位键的数目是基本不变的,如Ag+形成2个配位
键;Cu2+形成4个配位键等。
思考
2.配位化合物通常把金属离子或原子(称为中心离子或原子)与某
些分子或离子(称为配体或配位体)以配位键结合形
成的化合物称为配位化合物,简称配合物。
配位化合物一定含有配位键但含有配位键的化合物
不一定是配位化合物例如:CO、NH +、H O+、SO 2-、
4 3 4
P O
2 5
(1)中心原子(离子):提供空轨道的金属离子或原
子。一般是过渡金属,必须有空轨道。
(2)配位体:含有孤电子对的分子或离子
NH H O CO Cl- SCN- CN-
3 2
(3)配位原子:配位体中具有孤电子对的原子N O
P S,一般是ⅤA Ⅵ A ⅦA的非金属原子
(4)配位数:直接同中心原子配位的原子数目,一
般是2、4、6、8 能利用配
(5)配离子的电荷:等于中心离子和配体总电荷的 合物的性
代数和,如:[Fe(SCN) ]3- 质去推测
6
3.配合物的组成 配合物的
组成,从
认真思 而形成
考 “结构决
定性质”
的认知模
型。
对于配合物,外界在水溶液中易电离,但内界却难
电离。
实验3-3
实验操作
①向盛有4mL 0.1mol/L CuSO 溶液的试管里滴加几
4
滴1 mol/L 氨水
②继续添加氨水并振荡试管
③再向试管中加入极性较小的溶剂(如加入8 mL 95%
乙醇),并用玻璃棒摩擦试管壁
实验现象
①形成难溶物②难溶物溶解,得到深蓝色的透明溶液
③析出深蓝色晶体
实验原理
① Cu2+ + 2NH ·H O = Cu(OH) ↓+2NH +
3 2 2 4
② Cu(OH) + 4NH = [Cu(NH ) ](OH)
2 3 3 4 2
③深蓝色晶体为[Cu(NH ) ]SO ·H O,说明该配合物
3 4 4 2
在乙醇中的溶解度小于在水中的溶解度
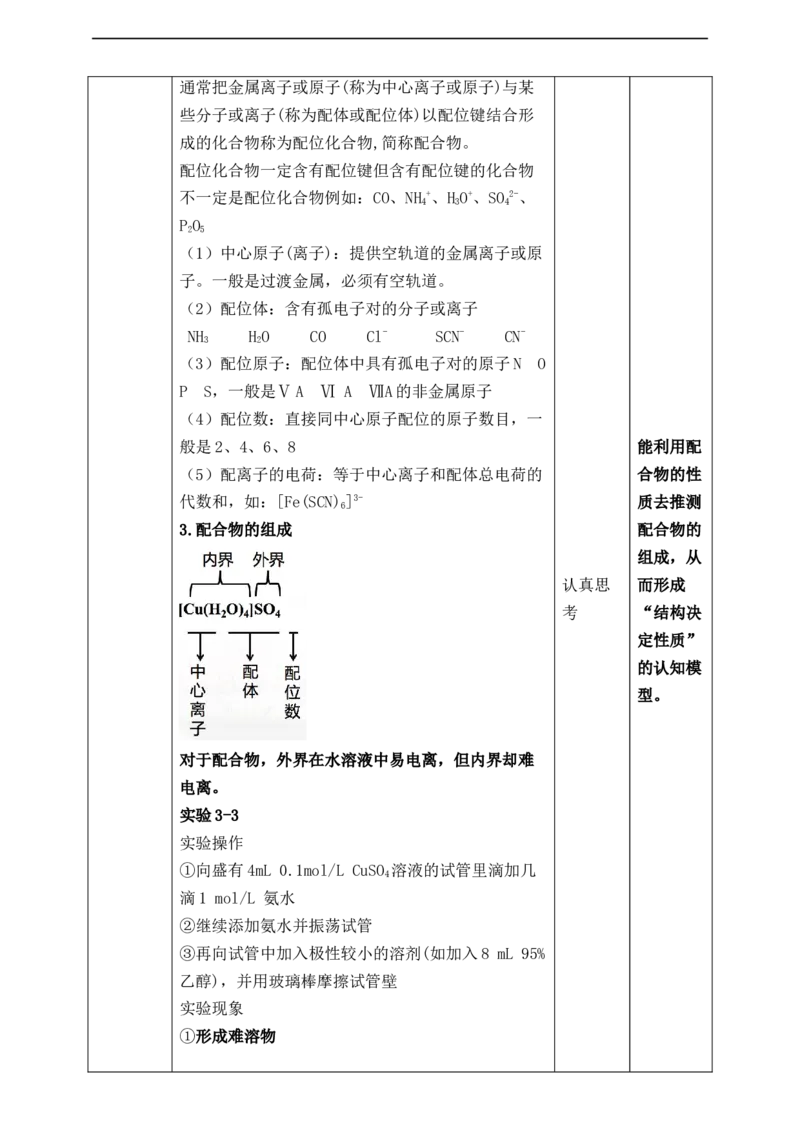
实验证明,无论在得到的深蓝色透明溶液中,还是
在析出的深蓝色的晶体中,深蓝色都是由于存在
[Cu(NH ) ]2+,它是Cu2+的另一种常见配离子,中心
3 4
离子仍然是Cu2+,而配体是NH ,配位数为4。
3
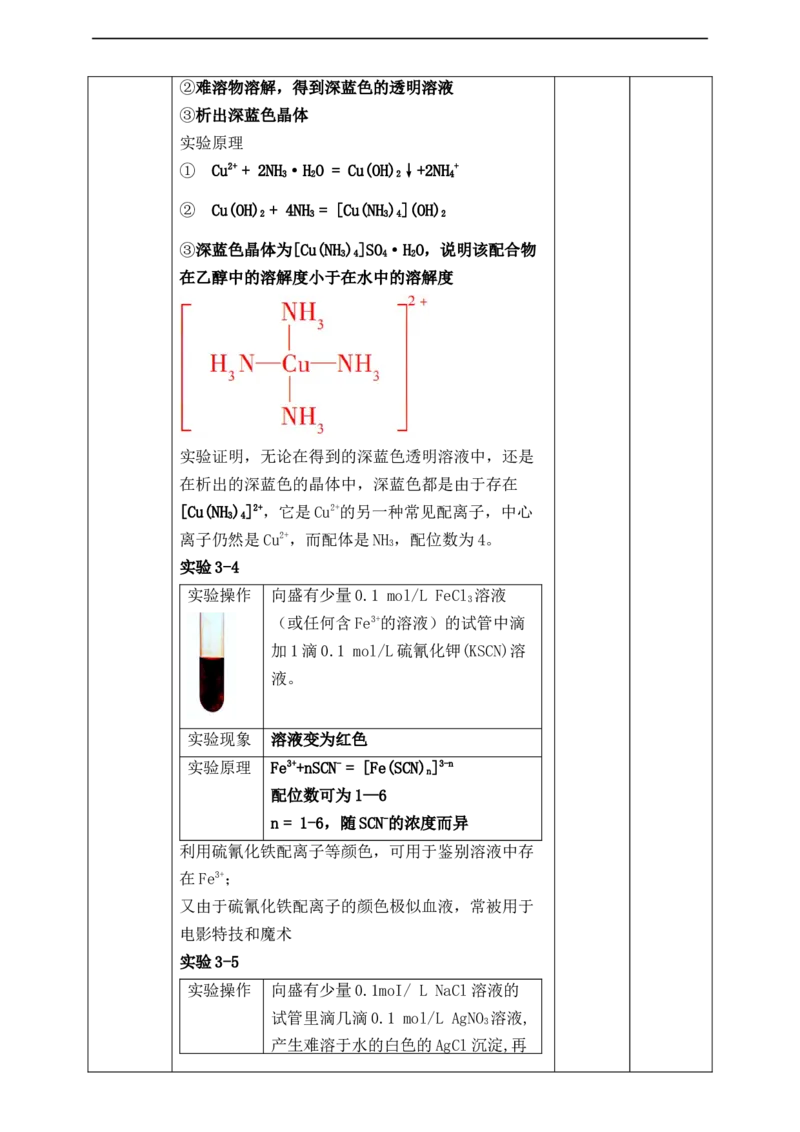
实验3-4
实验操作 向盛有少量0.1 mol/L FeCl 溶液
3
(或任何含Fe3+的溶液)的试管中滴
加1滴0.1 mol/L硫氰化钾(KSCN)溶
液。
实验现象 溶液变为红色
实验原理 Fe3++nSCN- = [Fe(SCN) ]3-n
n
配位数可为1—6
n = 1-6,随SCN-的浓度而异
利用硫氰化铁配离子等颜色,可用于鉴别溶液中存
在Fe3+;
又由于硫氰化铁配离子的颜色极似血液,常被用于
电影特技和魔术
实验3-5
实验操作 向盛有少量0.1moI/ L NaCl溶液的
试管里滴几滴0.1 mol/L AgNO 溶液,
3
产生难溶于水的白色的AgCl沉淀,再滴入1molL氨水,振荡,观察实验现
象。
实验现象 先产生白色沉淀,滴加氨水后白色沉
淀溶解
实验原理 Ag++Cl-===AgCl↓
AgCl+2NH === [Ag(NH ) ]Cl
3 3 2
4.配合物的性质
配合物具有一定的稳定性,配位键越强,配合物越
稳定。许多过渡金属元素的离子对多种配体具有很
强对结合力,因而,过渡金属配合物远比主族金属
配合物多。
5.配合物的应用
(1) 在生命体中的应用
叶绿素:Mg2+的配合物
血红素:Fe2+的配合物
酶:含锌的配合物、含锌酶有80多种
维生素B :钴配合物
12
(2)在医药中的应用
抗癌药物
(3) 配合物与生物固氮
固氮酶
(4)在生产生活中的应用
王水溶金:H[AuCl ]
4
电解氧化铝的助熔剂 Na [AlF ]
3 6
热水瓶胆镀银 [Ag(NH ) ]+
3 2
二、超分子 了解超分
1.定义 子的结构
由两种或两种以上的分子通过分子间相互作用形成 特点与性
的分子聚集体称为超分子 质。
超分子定义中的分子是广义的,包括离子。
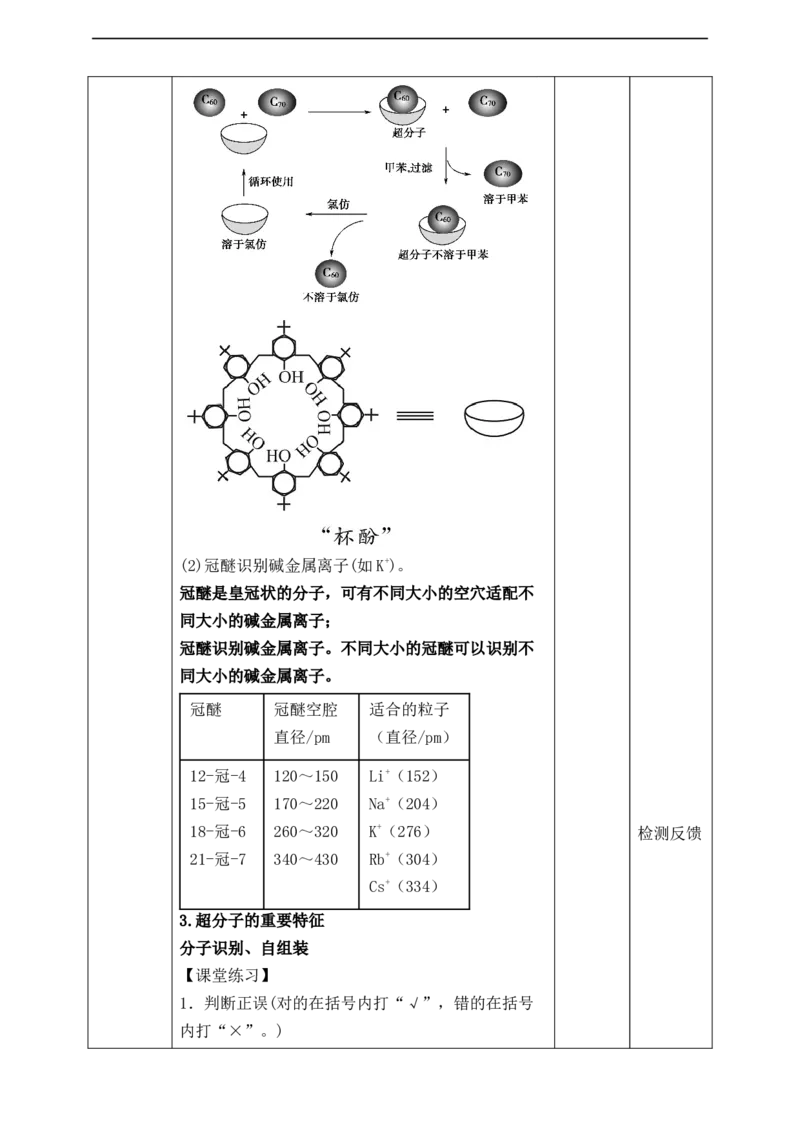
2.超分子实例(2)冠醚识别碱金属离子(如K+)。
冠醚是皇冠状的分子,可有不同大小的空穴适配不
同大小的碱金属离子;
冠醚识别碱金属离子。不同大小的冠醚可以识别不
同大小的碱金属离子。
冠醚 冠醚空腔 适合的粒子
直径/pm (直径/pm)
12-冠-4 120~150 Li+(152)
15-冠-5 170~220 Na+(204)
18-冠-6 260~320 K+(276) 检测反馈
21-冠-7 340~430 Rb+(304)
Cs+(334)
3.超分子的重要特征
分子识别、自组装
【课堂练习】
1.判断正误(对的在括号内打“√”,错的在括号
内打“×”。)(1)配位键实质上是一种特殊的共价键( )
(2)提供孤电子对的微粒既可以是分子,也可以是离
子( )
(3)有配位键的化合物就是配位化合物( )
(4)配位化合物都很稳定( )
(5)在配合物[Co(NH ) Cl]Cl 中的Cl-均可与AgNO
3 5 2 3
反应生成AgCl沉淀( )
(6)Ni(CO) 是配合物,它是由中心原子与配体构成
4
的( )
答案:(1)√(2)√(3)×(4)×(5)× (6)√
2.下列不能形成配位键的组合是( )
A.Ag+、NH B.H O、H+
3 2
C.Co3+、CO D.Ag+、H+
解析:选D. 配位键的形成条件必须是一方能提供孤
电子对,另一方能提供空轨道,A、B、C三项中,Ag
+、H+、Co3+能提供空轨道,NH 、H O、CO能提供孤
3 2
电子对,所以能形成配位键,而 D项Ag+与H+都只
能提供空轨道,而无法提供孤电子对,所以不能形
成配位键。
3.若X、Y两种粒子之间可形成配位键,则下列说法
正确的是( )
A.X、Y只能是分子
B.X、Y只能是离子
C.若X提供空轨道,则Y至少要提供一对孤电子对
D.一定是X提供空轨道,Y提供孤电子对
解析:选C。形成配位键的两种微粒可以均是分子或
者均是离子,还可以一种是分子、一种是离子,但
必须是一种微粒提供空轨道、另一种微粒提供孤电
子对,A、B项错误,C项正确。
4. 0.01 mol氯化铬(CrCl ·6H O)在水溶液中用过量
3 2
的AgNO 处理,产生0.01 mol AgCl沉淀,此氯化铬
3
最可能是( )
A.[Cr(H O) ]Cl
2 6 3
B.[Cr(H O) Cl]Cl ·H O
2 5 2 2C.[Cr(H O) Cl ]Cl·2H O
2 4 2 2
D.[Cr(H O) Cl ]·3H O
2 3 3 2
答案:C。解析 0.01 mol氯化铬(CrCl ·6H O)在水
3 2
溶液中用过量的AgNO 处理,产生0.01 mol AgCl沉
3
淀,说明1 mol氯化铬(CrCl ·6H O)中有1 mol氯
3 2
离子在外界,其余在内界,而正三价铬为六配位,
则此氯化铬最可能是[Cr(H O) Cl ]Cl·2H O,C正
2 4 2 2
确。
5. 化合物NH 与BF 可以通过配位键形成NH ·BF 。
3 3 3 3
(1)配位键的形成条件是
____________________________________。
(2)在NH ·BF 中,________原子提供孤电子对,
3 3
________原子接受电子。
解析 (1)微粒间形成配位键的条件是:一方是能
够提供孤电子对的原子或离子,另一方是具有能够
接受孤电子对的空轨道的原子或离子。
(2)在NH ·BF 中,B原子是提供空轨道的原子、N原
3 3
子提供孤对电子,B、N原子之间形成配位键。
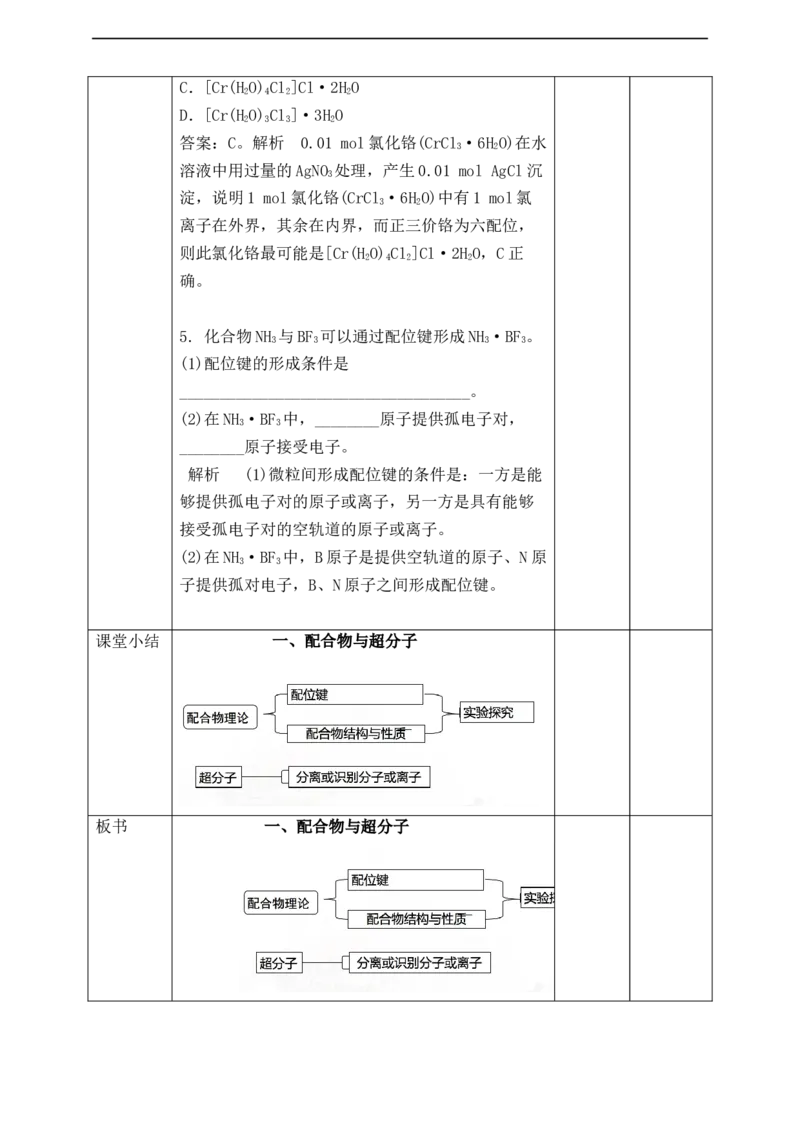
课堂小结 一、配合物与超分子
板书 一、配合物与超分子