文档内容
3.4配合物与超分子(分层作业)
1. 为阿伏加德罗常数的值。下列有关说法正确的是
A.1.8g2H16 O中含有质子的数目为N
2 A
B.0.2mol[C (NH )Cl]Cl溶于水发生电离,电离出Cl-的数目为0.6N
o 3 4 2 A
C.含4.6g钠元素的NaO和NaO 的混合物中离子数目为0.2N
2 2 2 A
D.1mol·L-1 Ca (PO ) 溶液中含有PO3- 数目一定小于2N
3 4 2 4 A
【答案】C
【解析】A.已知2H16 O的摩尔质量为20g/mol,1分子2H16 O中含有10个质子,故1.8g2H16 O中含有质子的数目
2 2 2
1.8g
为 ×10N mol-1=0.9N ,A错误;
20g/mol A A
B.已知[Co(NH )Cl]Cl=[Co(NH )Cl]++Cl-,故0.2mol[C (NH )Cl]Cl溶于水发生电离,电离出Cl-的数目为
3 4 2 3 4 2 o 3 4 2
0.2N ,B错误;
A
C.已知NaO、NaO 中阳离子和阴离子的数目比均为2:1,故含4.6g钠元素的NaO和NaO 的混合物中离子
2 2 2 2 2 2
4.6g 3
数目为 × ×N mol-1=0.3N ,C正确;
23g/mol 2 A A
D.题干未告知溶液的体积,且PO3- 会发生水解,故无法计算1mol·L-1 Ca (PO ) 溶液中含有PO3- 数目不一定小
4 3 4 2 4
于2N ,D错误;
A
故答案为:C。
2.下列说法不正确的是
A.(AlCl ) 中含有配位键
3 2
B.NH 的键角大于HO的键角
3 2
C.SiO 中的O—Si—O键角为120°
2
D.HBO 是弱酸,HBO 晶体中存在作用力为共价键、氢键和范德华力
3 3 3 3
【答案】C
【解析】A.双聚氯化铝分子中具有空轨道的铝原子与具有孤电子对的氯原子形成配位键,故A正确;
B.氨分子中氮原子的孤电子对数为1、水分子中氧原子的孤电子对数为2、孤电子对数越多,对成键电子对的
斥力越大,键角越小,所以氨分子的键角大于水分子的键角,故B正确;
C.二氧化硅晶体中硅原子与4个氧原子形成硅氧四面体,所以晶体中O—Si—O键角小于120°,为109º28',
故C错误;
D.硼酸分子能与水分子作用生成四羟基合硼离子和氢离子,所以硼酸是一元弱酸,硼酸晶体是存在作用力为共价键、氢键和范德华力的分子晶体,故D正确;
故选C。
3.下列说法错误的是
A.尿素[ ]的球棍模型:
B. 的电子式:
C. 晶体中存在离子键、 键、配位键
D.基态钛原子的价层电子排布式:
【答案】B
【解析】A.尿素结构简式为CO(NH),球棍模型为: ,故A正确;
2 2
B.NH 的电子式为 ,选项中电子式缺少了一对孤电子对,故B错误;
3
C.铵根离子与氟离子形成离子键,铵根离子存在配位键,N与H形成σ键,所以NH F中存在离子键、σ键、
4
配位键,故C正确;
D.基态钛原子的电子排布式:[Ar]3d24s2,价层电子排布式:3d24s2,故D正确。
答案选B。
4. 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元 素)的球棍模型如
图所示。下列说法错误的是( )
A.m=2
B.在Xm-中,硼原子轨道的杂化类型不同
C.1、2号原子间和4、5号原子间的化学键可能是配位键
D.若382 g硼砂晶体中含2 mol Na+,则硼砂的化学式为NaB O·10H O
2 4 7 2
【答案】 C
【解析】 根据球棍模型可知Xm-是(H B O)m-,根据元素的化合价H为+1、B为+3、O为-2,可得m=2,
4 4 9
A正确;2、4号原子均代表B原子,2号B形成3个键,该B原子为sp2杂化,4号B形成4个键,该B原子为
sp3杂化,在Xm-中,硼原子轨道的杂化类型不同,B正确;1、2号原子间不存在配位键,4号B形成4个键,
其中1个键可能是配位键,所以配位键可能存在于4号与5号原子之间,C错误;若硼砂的化学式为
NaB O·10H O,则382 g硼砂晶体中含×2=2 mol Na+,D正确。
2 4 7 2
5.下列说法错误的是
A.冠醚能识别K+形成超分子,是因为K+的直径与该冠醚空腔直径相当B.NH 与BF 形成配合物 ,是因为BF 中的B有空轨道接受NH 中N的孤电子对
3 3 3 3
C. 的酸性强于 ,是因为 的相对分子质量小于
D.自然界不存在稳定的HCl和Cl,是因为共价键具有饱和性
2 3
【答案】C
【解析】A.超分子有“分子识别”的特性,冠醚能识别K+形成超分子,就是因为K+的直径与该冠醚空腔直径
相当,A正确;
B.BF 分子中硼原子具有空轨道,能与氨分子中具有孤电子对的氮原子形成配位键,所以BF 能与NH 形成配
3 3 3
合物[NH →BF],B正确;
3 3
C.酸性的强弱与相对分子质量的大小没有关系,三氟乙酸的酸性比三氯乙酸强是因为F的电负性大于Cl,使三
氟乙酸中羟基的极性增强,更易发生电离,C错误;
D.根据共价键的饱和性,氢原子达到2电子稳定结构,氢原子只能共用1对电子对,氯原子最外层有7个电
子,只能共用一对电子满足8电子稳定结构,因此自然界不存在稳定的HCl和Cl,D正确;
2 3
故选C。
6.硫代硫酸钠(Na SO)可作定影剂,反应原理如下:AgBr+Na SO=NaBr+Na [Ag(S O)]。下列说法不正确的
2 2 3 2 2 3 3 2 3 2
是
A.SO2- 的空间结构为四面体形,中心原子S的杂化方式为sp3
2 3
B.Na[Ag(S O)]是一种配合物,其配位数为2
3 2 3 2
C.Na[Ag(S O)]是一种常见的切花保鲜液,可用NaCl标准溶液定量测定其浓度
3 2 3 2
D.已知NaBr的晶体结构与NaCl相似,则每个Br周围有6个最近且等距离的
【答案】C
【解析】A.SO2- 的结构可以看做硫酸根中的一个氧原子被硫取代,结构和硫酸根类似,中心硫原子的孤电子
2 3
对数为0,价层电子对数为4,所以空间结构为四面体形,中心原子S的杂化方式为sp3,A正确;
B.Na[Ag(S O)]是一种配合物,中心离子银离子的配位数为2,B正确;
3 2 3 2
C.Na[Ag(S O)]中银离子与SO2- 形成配位键,无单独的银离子,不能用NaCl标准溶液滴定Ag+测定其浓度,
3 2 3 2 2 3
C错误;
D.氯化钠晶体中每个Na+周围有6个Cl-,每个Cl-周围有6个Na+,NaBr的晶体结构与NaCl晶体相似,则每个
Br-周围有6个Na+,D正确;
故选C。
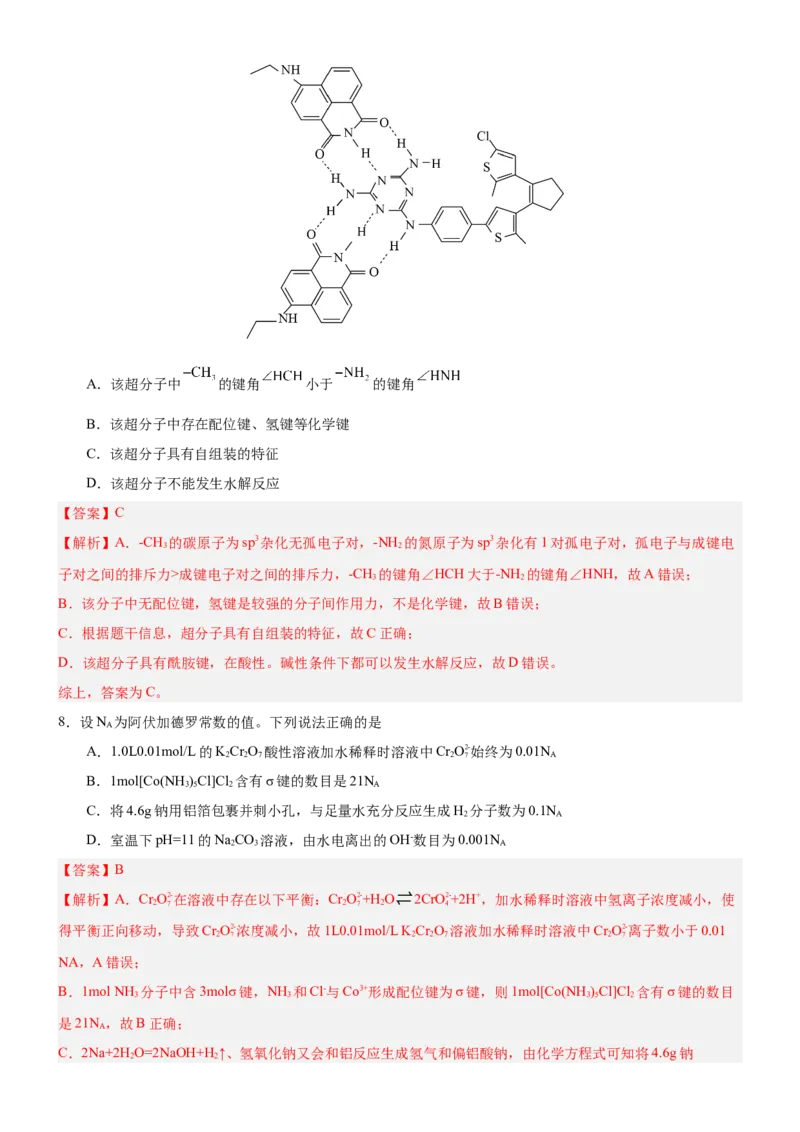
7.超分子是由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。某种超分子结构如图所示。下
列有关说法正确的是A.该超分子中 的键角 小于 的键角
B.该超分子中存在配位键、氢键等化学键
C.该超分子具有自组装的特征
D.该超分子不能发生水解反应
【答案】C
【解析】A.-CH 的碳原子为sp3杂化无孤电子对,-NH 的氮原子为sp3杂化有1对孤电子对,孤电子与成键电
3 2
子对之间的排斥力>成键电子对之间的排斥力,-CH 的键角∠HCH大于-NH 的键角∠HNH,故A错误;
3 2
B.该分子中无配位键,氢键是较强的分子间作用力,不是化学键,故B错误;
C.根据题干信息,超分子具有自组装的特征,故C正确;
D.该超分子具有酰胺键,在酸性。碱性条件下都可以发生水解反应,故D错误。
综上,答案为C。
8.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1.0L0.01mol/L的KCr O 酸性溶液加水稀释时溶液中Cr O2- 始终为0.01N
2 2 7 2 7 A
B.1mol[Co(NH)Cl]Cl 含有σ键的数目是21N
3 5 2 A
C.将4.6g钠用铝箔包裹并刺小孔,与足量水充分反应生成H 分子数为0.1N
2 A
D.室温下pH=11的NaCO 溶液,由水电离出的OH-数目为0.001N
2 3 A
【答案】B
【解析】A.Cr O2- 在溶液中存在以下平衡:Cr O2- +H O⇌2CrO2- +2H+,加水稀释时溶液中氢离子浓度减小,使
2 7 2 7 2 4
得平衡正向移动,导致Cr O2- 浓度减小,故1L0.01mol/L K Cr O 溶液加水稀释时溶液中Cr O2- 离子数小于0.01
2 7 2 2 7 2 7
NA,A错误;
B.1mol NH 分子中含3molσ键,NH 和Cl-与Co3+形成配位键为σ键,则1mol[Co(NH)Cl]Cl 含有σ键的数目
3 3 3 5 2
是21N ,故B正确;
A
C.2Na+2HO=2NaOH+H ↑、氢氧化钠又会和铝反应生成氢气和偏铝酸钠,由化学方程式可知将4.6g钠
2 2(0.2mol)用铝箔包裹并刺小孔,与足量水充分反应,生成H 的分子数为大于0.1 N ,C错误;
2 A
D.溶液体积未知,无法确定离子数目,故D错误;
故选:B。
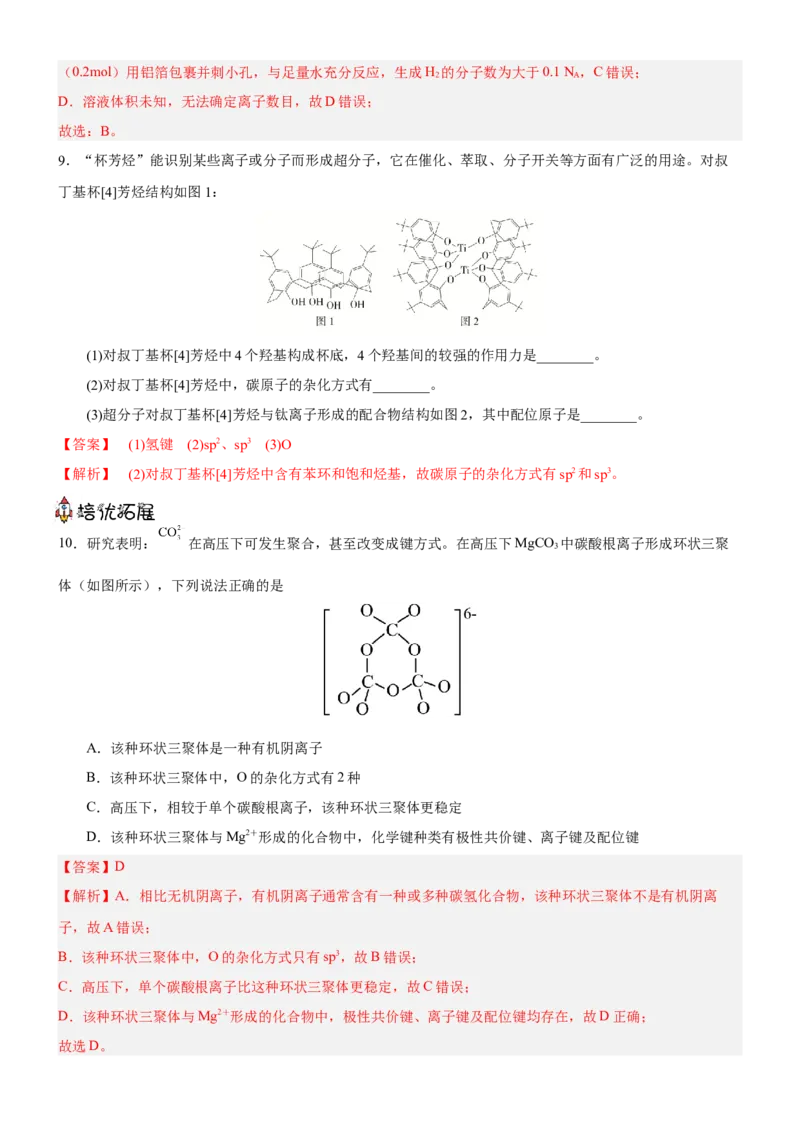
9.“杯芳烃”能识别某些离子或分子而形成超分子,它在催化、萃取、分子开关等方面有广泛的用途。对叔
丁基杯[4]芳烃结构如图1:
(1)对叔丁基杯[4]芳烃中4个羟基构成杯底,4个羟基间的较强的作用力是________。
(2)对叔丁基杯[4]芳烃中,碳原子的杂化方式有________。
(3)超分子对叔丁基杯[4]芳烃与钛离子形成的配合物结构如图2,其中配位原子是________。
【答案】 (1)氢键 (2)sp2、sp3 (3)O
【解析】 (2)对叔丁基杯[4]芳烃中含有苯环和饱和烃基,故碳原子的杂化方式有sp2和sp3。
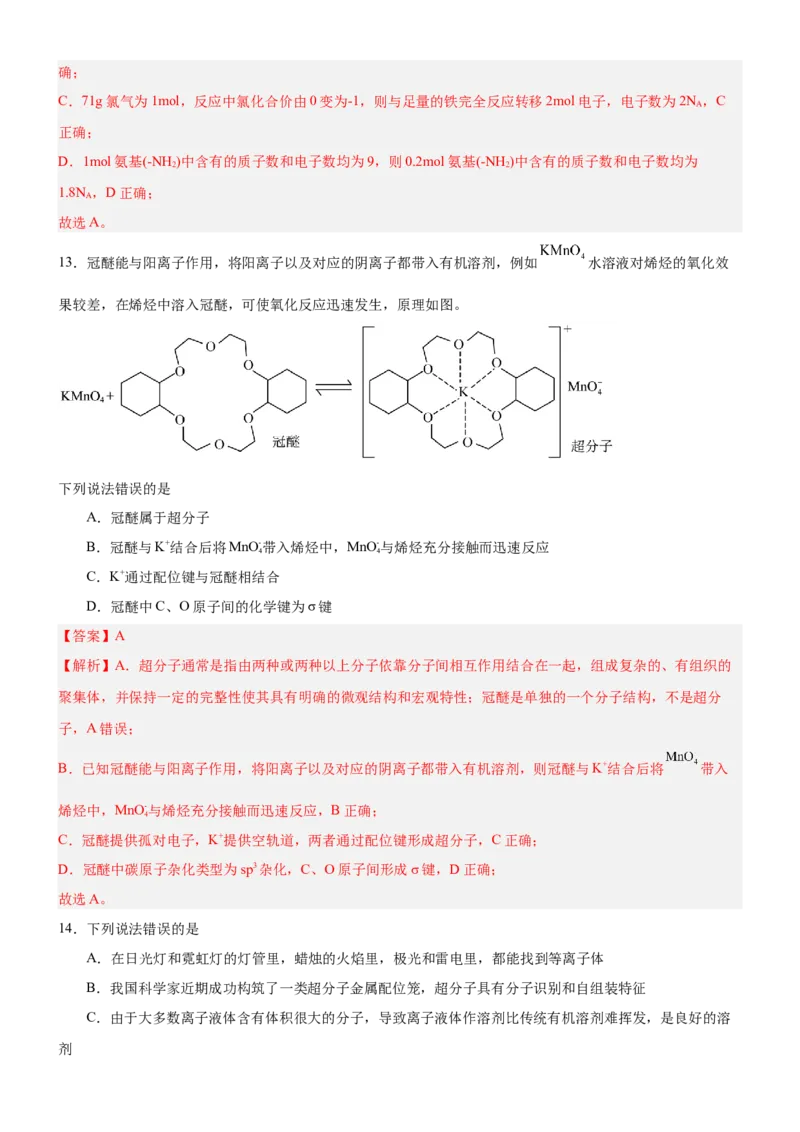
10.研究表明: 在高压下可发生聚合,甚至改变成键方式。在高压下MgCO 中碳酸根离子形成环状三聚
3
体(如图所示),下列说法正确的是
A.该种环状三聚体是一种有机阴离子
B.该种环状三聚体中,O的杂化方式有2种
C.高压下,相较于单个碳酸根离子,该种环状三聚体更稳定
D.该种环状三聚体与Mg2+形成的化合物中,化学键种类有极性共价键、离子键及配位键
【答案】D
【解析】A.相比无机阴离子,有机阴离子通常含有一种或多种碳氢化合物,该种环状三聚体不是有机阴离
子,故A错误;
B.该种环状三聚体中,O的杂化方式只有sp3,故B错误;
C.高压下,单个碳酸根离子比这种环状三聚体更稳定,故C错误;
D.该种环状三聚体与Mg2+形成的化合物中,极性共价键、离子键及配位键均存在,故D正确;
故选D。11.由C、H和与C处于同周期的X、Y四种元素组成的穴醚的键线式如图,该结构中除H外其余原子均满足8
电子稳定结构,其空腔直径大约为260~320 pm,可以适配直径与之相近的碱金属离子从而实现离子识别。下列
说法正确的是
离
直径/pm
子
204
304
A.第一电离能:X>Y
B.简单氢化物的沸点:X>Y
C.键角:C-Y-C>C-X-C
D.该穴醚可与 通过配位键形成超分子,对 进行识别
【答案】A
【分析】X、Y原子均满足8电子稳定结构,通过键连接方式X为N、Y为O
【解析】A.N电子排布式2s22p3半满比较稳定,第一电离能:N>O,A正确;
B.HO中氢键作用力更强,简单氢化物的沸点:HO>NH ,B错误;
2 2 3
C.N和O都为sp3杂化,但O中有两对孤对电子,N只有一对孤对电子,孤对电子的排斥大于成键电子排斥,
因此C-O-C键角更小,C错误;
D.Na+直径小于穴醚空腔最小值,则Li+直径小于Na+,故不适配,不能识别,D错误;
故选A。
12.设 为阿伏加德罗常数的值,下列有关说法不正确的是
A.22.4L CHCl中含有 的数目为3N
3 A
B.1mol[Cu(H O) ]2+中 键的个数为12N
2 4 A
C. 氯气与足量的铁完全反应转移的电子数为2N
A
D. 氨基 中含有的质子数和电子数均为1.8N
A
【答案】A
【解析】A.所处的状态不明确,故其物质的量无法计算,A错误;
B.1个水分子中形成2个σ键、和铜性1个σ配位键,则1mol[Cu(H O) ]2+中σ键为12mol,个数为12N ,B正
2 4 A确;
C.71g氯气为1mol,反应中氯化合价由0变为-1,则与足量的铁完全反应转移2mol电子,电子数为2N ,C
A
正确;
D.1mol氨基(-NH )中含有的质子数和电子数均为9,则0.2mol氨基(-NH )中含有的质子数和电子数均为
2 2
1.8N ,D正确;
A
故选A。
13.冠醚能与阳离子作用,将阳离子以及对应的阴离子都带入有机溶剂,例如 水溶液对烯烃的氧化效
果较差,在烯烃中溶入冠醚,可使氧化反应迅速发生,原理如图。
下列说法错误的是
A.冠醚属于超分子
B.冠醚与K+结合后将MnO- 带入烯烃中,MnO- 与烯烃充分接触而迅速反应
4 4
C.K+通过配位键与冠醚相结合
D.冠醚中C、O原子间的化学键为σ键
【答案】A
【解析】A.超分子通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的
聚集体,并保持一定的完整性使其具有明确的微观结构和宏观特性;冠醚是单独的一个分子结构,不是超分
子,A错误;
B.已知冠醚能与阳离子作用,将阳离子以及对应的阴离子都带入有机溶剂,则冠醚与K+结合后将 带入
烯烃中,MnO- 与烯烃充分接触而迅速反应,B正确;
4
C.冠醚提供孤对电子,K+提供空轨道,两者通过配位键形成超分子,C正确;
D.冠醚中碳原子杂化类型为sp3杂化,C、O原子间形成σ键,D正确;
故选A。
14.下列说法错误的是
A.在日光灯和霓虹灯的灯管里,蜡烛的火焰里,极光和雷电里,都能找到等离子体
B.我国科学家近期成功构筑了一类超分子金属配位笼,超分子具有分子识别和自组装特征
C.由于大多数离子液体含有体积很大的分子,导致离子液体作溶剂比传统有机溶剂难挥发,是良好的溶
剂D.纳米晶体是晶体颗粒尺寸为纳米量级的晶体,当晶体颗粒小至纳米级,熔点会下降
【答案】C
【解析】A.等离子体由电子、阳离子和电中性粒子组成,存在于日光灯和霓虹灯的灯管里、蜡烛火焰里、极
光和雷电里等,具有良好流动性和导电能力,故A正确;
B.超分子金属配位笼空腔可与特定的微粒紧密结合,故超分子具有分子识别和自组装特征,故B正确;
C.离子液体是指全部由离子组成的液体,大多数离子液体含有体积很大的阴、阳离子,呈液态,难挥发,但
可作为良好的溶剂是由于离子液体中含有大量的离子,因此具有强大的溶解能力,故C错误;
D.纳米晶体是晶体颗粒尺寸在纳米量级的晶体,当晶体颗粒小到纳米量级时,其熔点会下降,故D正确;
故答案选:C。
15.镍能形成多种配合物如正四面体形的 和平面正方形的 、正八面体形的
等,下列说法正确的是
A. 中的配位原子是氧原子
B. 中Ni、C、N不可能处在同一直线上
C. 中 键角比107.3°小
D. 和 中均有d轨道参与杂化
【答案】D
【解析】A.四羰基合镍分子中镍原子为中心原子,一氧化碳是配体,碳元素的电负性小于氧元素,与具有空
轨道的镍原子形成配位键时,碳原子更易给出孤电子对,则四羰基合镍分子中的配位原子是碳原子,故A错
误;
B.氰酸根离子与氮气分子的原子个数都为2、价电子数都为14,则氰酸根离子与氮气分子的空间结构相同,
都是直线形,所以四氢酸根合镍离子中镍原子、碳原子和氮原子处在同一直线上,故B错误;
C.六氨合镍离子中氮原子与具有空轨道的镍离子形成配位键,孤对电子对数为0,氨分子中氮原子的孤对电子
对数为1,孤对电子对数越多,对成键电子对的斥力越大,键角越小,则六氨合镍离子中H−N−H键角大于氨分
子的键角107.3°,故C错误;
D.由四氰酸根合镍离子的空间构型为平面正方形、六氨合镍离子的空间构型为正八面体形可知,四氰酸根合
镍离子中镍离子的杂化方式为dsp2杂化、六氨合镍离子中镍离子的杂化方式为sp3 d2杂化,均有d轨道参与杂
化,故D正确;
故选D。
16.Ni和Cu均为重要的合金元素,其单质和化合物在社会发展和国防科技等领域应用广泛。其中Cu(NH )SO
3 4 4
是一种广谱杀菌剂,下列说法正确的是A.基态Ni原子价层电子的核外电子排布式为3d84s2
B.基态Cu原子核外未成对电子的数目为2
C.基态N、S、O原子的第一电离能由大到小的顺序为N>S>O
D.Cu(NH )SO 配位数是5
3 4 4
【答案】A
【解析】A.Ni的核外电子排布式为1s22s22p63s23p63d84s2,其价电子排布式为3d84s2,故A正确;
B.Cu是29号元素,原子核外电子数为29,基态原子简化核外电子排布式为:[Ar]3d104s1,4s能级上有1个未
成对电子,故B错误;
C.同周期元素,从左到右第一电离能呈增大的趋势,同主族元素,从上往下第一电离能在减小,氮原子的2p
轨道为半充满的稳定结构,第一电离能大于相邻元素,则第一电离能由大到小的顺序为N>O>S,故C错误;
D.Cu(NH )SO 配位数是4,故D错误;
3 4 4
故答案选A。
17.乙酰乙酸乙酯存在酮式与烯醇式的互变异构,其中烯醇式可与 结合产生紫色,其结构如图所示,下列
有关该配离子的说法正确的是
A. 有23种空间运动状态的电子
B.该配离子中含有6个配体
C.该配离子中碳原子的杂化类型有 、 杂化
D.该配离子中含有的化学键有离子键、极性键、非极性键、配位键
【答案】C
【解析】A.Fe的原子序数为26,Fe原子失去4s能级上的2个电子和3d能级的1个电子形成 ,则 的
电子排布式为1s22s22p63s23p63d5,电子占有轨道数为14,有14种空间运动状态的电子,选项A错误;
B.该配离子中含有6个配位键,有3个配体,选项B错误;
C.双键上的C原子形成3个σ键且无孤电子对,采用sp2杂化,饱和C原子价层电子对数为4,采用sp3杂化,
选项C正确;
D.该配离子中含有的化学键有极性键、非极性键、配位键,不含离子键,选项D错误;答案选C。
18.铁、钴及其化合物在生活中有广泛应用。
(1)Fe2+的基态核外电子排布式为 。
(2)实验室用KSCN溶液、苯酚检验Fe3+。
①1mol苯酚分子中含有σ键的数目为 。
②类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H S C≡N)和异硫氰酸
,这两种酸中沸点较高的是 ,原因: 。
(3)氮化铁晶体的晶胞结构如图−1所示。该晶体中铁、氮的微粒个数之比为 。
(4)某铁的化合物结构简式如图−2所示:
①上述化合物中所含有的非金属元素的电负性由大到小的顺序为 (用元素符号表示)。
②上述化合物中氮原子的杂化方式为 。
(5)配合物[Co(NH )Cl]Cl 中与Co2+形成配位键的原子是 (用元素符号表示),与NH 互为等电子体的
3 5 2 3
离子是 ,区别[Co(NH )Cl]Cl 和[Co(NH )]Cl 这两种晶体的实验方案为 。
3 5 2 3 6 3
【答案】(1)1s22s22p63s23p63d6
(2) 13N 异硫氰酸 硫氰酸分子间无法形成氢键,异硫氰酸分子间可形成氢键,故异硫氰酸的沸
A
点较高
(3)4∶1
(4) O>N>C>H sp3和sp2
(5) N、Cl H O+ 称取相同质量的两种晶体分别配成溶液,向两种溶液中分别滴加足量的AgNO
3 3
溶液,静置、过滤、干燥、称量,所得AgCl固体多的原晶体为[Co(NH )]Cl ,另一种为[Co(NH )Cl]Cl
3 6 3 3 6 2
【解析】(1)Fe2+的基态核外电子排布式为:1s22s22p63s23p63d6;
(2)①1个苯酚分子中含有13个σ键和1个大π键,故1mol苯酚分子中含有σ键的数目为13N ;
A
②硫氰酸分子间无法形成氢键,异硫氰酸分子间可形成氢键,故异硫氰酸的沸点较高;1 1
(3)根据均摊法可知铁原子的个数为:8× +6× =4,N原子的个数为:1,故铁、氮的微粒个数之比为4∶1
8 2
(4)①在化合物中显负价的电负性较大,故电负性由大到小的顺序为:O>N>C>H;
②化合物中氮原子的成键方式为单键和双键,故杂化方式为:sp3和sp2;
(5)①配合物[Co(NH )Cl]Cl 内界为[Co(NH )Cl]2+,与Co2+形成配位键的原子是N、Cl;
3 5 2 3 5
②与NH 互为等电子体的离子是HO+;
3 3