文档内容
2010 年黄高优录考试选拔赛试卷 4
可能用到的相对原子质量:H-1 O-16 C-12 S-32 Na-23
一 选择题(每题有1~2个正确答案,请将正确答案的序号填入答案栏里,每小题2分,)
1.铜与浓硫酸共热的条件下可以发生化学反应 Cu + 2HSO = CuSO + SO↑ + 2HO,但是
2 4 4 2 2
在工业上制取硫酸铜不是直接利用浓硫酸与铜反应,而是将铜屑在空气中加热氧化,然后浸
入稀硫酸中反应过滤,并反复加热和浸入操作,你认为这样的优点是
A.节约能源 B.不产生污染大气的二氧化硫
C.提高硫酸的利用率 D.提高铜的利用率
2.温室时,将NaNO 和KCl两种饱和溶液混合后无晶体析出,加热蒸发过程中,首先析出的晶
3
体是
A.NaNO B.NaCl C.KCl D.KNO
3 3
3.为了除去物质中的杂质,所需药品(括号内的物质)选择不正确的是
A.NaCl中混有少量的NaSO(硝酸钡) B.CO 中含有少量的HO(浓硫酸)
2 4 2 2
C.FeCl 中含有少量CuCl(铁粉) D.CO 中含有少HCl(碳酸钠)
2 2 2
4.在已调平的天平两端各放一个等质量的烧杯,向烧杯中各注入质量相等、溶质质量分数也
相等的足量稀硫酸。在左边烧杯中投入一定质量的金属X粉末,同时在右边烧杯中投入与X
等质量的金属Y粉末。观察到天平的指针先偏向左边,当两种金属完全溶解后,天平的指针
偏向右边。则X、Y是下表组合中的
A B C D
X Mg Zn Zn Fe
Y Fe Mg Fe Zn
5.你认为下列实验方案中,可行的是
A.按溶解、过滤、蒸发的操作顺序可以分离CaCl、CaCO 的混合物
2 3
B.向某种未知溶液中加入AgNO 溶液,产生白色沉淀,证明溶液是盐酸
3
C.用磷在密闭容器中燃烧,除去密闭容器内空气中的氧气
D.将pH试纸润湿后,用玻璃棒蘸取食用白醋滴在试纸上,测定其pH
6. 18O是科学实验中常用的一种示踪原子,用仪器可以观测到它在化学变化中的行踪。在某
一饱和硫酸铜溶液(不含18O)中,加入ag带标记18O的无水硫酸铜粉末(CuSO 中的氧元素全
4
部为18O),如果保持温度不变,其结果是
A.无水硫酸铜不再溶解,ag带标记18O的无水硫酸铜粉末没有发生改变
B.溶液中可以找到带标记18O的SO2-,且白色粉末变为蓝色晶体,其质量小于ag
4
C.溶液中可以找到带标记18O的SO2-,且白色粉末变为蓝色晶体,其质量大于ag
4
D.有部分带标记18O的SO2-进入溶液中,但固体质量保持不变
4
7.1923年丹麦化学家布朗斯特提出一种理论叫酸碱质子论,人为规定凡是能够释放质子
(H+)的任何物质(包括分子或离子)都是酸,任何能接受质子的分子或离子都是碱,根据这一
理论,下列各项即属于酸又属于碱的是
A.HNO B.HSO C.OH- D.HCO-
3 2 4 3
8.已知氧化还原反应中存在如下关系:强氧化剂+强还原剂→弱氧化剂+弱还原剂,现有下
列三个能反应的式子:
2W- + X →2X- + W 2Y- + W → 2W- + Y 2X- + Z → 2Z- + X
2 2 2 2 2 2
以上反应均在同温、同压、同浓度下进行,正确结论是
A.氧化性是:Y>X B.还原性是:Y->Z-
2 2
C.2Z- + Y → 2Y- + Z 的反应能够进行
2 2D.在X-、Y-、W-、Z-中X-的还原性最强
9.在AgNO、Cu(NO)、Zn(NO) 的混合溶液中加入一些铁粉,待反应完成后再过滤,下列情况
3 3 2 3 2
中不可能存在的是
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+
B.滤纸上有Ag、Cu、Fe,滤液中有Ag+、Cu2+、Zn2+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+
D.滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+
10.已知:NaHCO + HCl = NaCl + HO + CO↑。某种混合气体中可能含有N、HCl、CO,将混
3 2 2 2
合气体依次通过NaHCO 溶液和灼热的CuO,气体体积无变化但是有红色物质生成;再通过
3
NaOH溶液,气体体积明显减小;将燃着的木条伸入装有剩余气体的集气瓶中,木条熄灭(假设
每步反应都是完全的),则下列说法中正确的是
A.一定有CO和HCl,肯定无N B.一定有CO和N,可能有HCl
2 2
C.一定有CO和HCl,可能有N D.一定有CO和N,肯定无HCl
2 2
11.向104.2g含有14.2g硫酸钠的溶液中加入45g水,从所得溶液中取出10mL,该10mL硫酸
钠溶液中Na+、SO2-、HO三种粒子个数比为
4 2
A.2∶1∶75 B.2∶1∶50 C.1∶1∶75 D.3∶5∶25
12.在20℃时,某气态碳氢化合物与氧气混合后装入密闭容器中,经充分反应后,又恢复到
20℃,此时容器内气体分子时反应前的一半。再经足量的氢氧化钠溶液吸收后,容器内几乎
成真空。此碳氢化合物可能是
A.CH B.CH C.CH D.CH
4 2 6 3 8 2 4
二 填空题(本题共35分)
13.(6分)向一盛有无色溶液的试管中加入另一种无色溶液,生成了一种白色沉淀。试根据你
学过的酸、碱、盐的知识和题目要求,推测生成的白色沉淀和对应的两种无色溶液各是什么。
(1)推测一:如果沉淀不溶于稀硝酸,沉淀可能是 ,两种无色溶液中的溶质分别是
;
(2)推测二:如果白色沉淀溶于稀硝酸且有气体产生,沉淀可能是 ,两种无色溶液
中的溶质分别是 ;
(3)推测三:如果白色沉淀溶于稀硝酸但不产生气体,沉淀可能是 ,两种无色溶液
中的溶质分别是 。
14.(4分)亚硫酸钠(NaSO)受热会分解,它在有HO存在时容易被空气中的氧气氧化为硫酸
2 3 2
钠(NaSO)。实验室贮存亚硫酸钠的试剂瓶极易炸裂,你推测其原因可能是:
2 4
① ;② ;
如果试剂瓶在冬天容易炸裂,应是原因 (填上述的序号);如果试剂瓶在夏天
容易炸裂,应是原因 。
15.(4分)腌制食品中含有亚硝酸盐,它会影响健康及诱发癌症,但维生素C对亚硝酸盐的形
成有阻挡作用。有一种设想:在含有亚硝酸盐(NaNO)的腌制食品中加入过量的化肥氯化铵
2
与其共热,生成无毒害的氮气、水、和氯化钠,过量氯化铵在持续加热的情况下分解为氨气与
氯化氢挥发,此时腌制食品便可以放心食用。
(1)写出这种设想中反应的化学方程式 ;
(2)评价这种方案,并申述理由:
(3)请提出一条减少食用腌制食品中亚硝酸盐含量的措施: 。
16.(7分)为了确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。已知氧化铁和铝
在高温下反应生成氧化铝和铁;铝和氢氧化钠的水溶液反应生成偏铝酸钠(NaAlO)和氢气。
2(1)若取ag样品,向其中加入足量的氢氧化钠溶液,测得生成的气体为bg。反应的化学方程
式为 ,样品中铝的质量为 g;
(2)若取ag样品,使其在高温下恰好完全反应,该反应的化学方程式为
,样品中氧化铁与铝的质量比为 ;
(3)待(2)中反应产物冷却后,往其中加入足量的盐酸,测得生成的气体质量为cg,则该气体
与(1)中所得的气体的质量比c∶b= 。
17.(4分)密陀僧是一氧化铅,它可与碳反应:2PbO+C 2Pb + CO↑、PbO+C Pb + CO,
2
有同学设计一简便实验以证明密陀僧中含有氧元素,在实验前后及过程中均通入氮气,试回
答:(1)为了使实验成功,混合物中碳的含量应 (填“较多”或“较少”),原因是
;
(2)该实验以干燥的氮气代替空气作为反应环境,其原因是 ;
(3)为了证明密陀僧中含有氧元素,应进行的操作是 。
三 实验题(本题共22分)
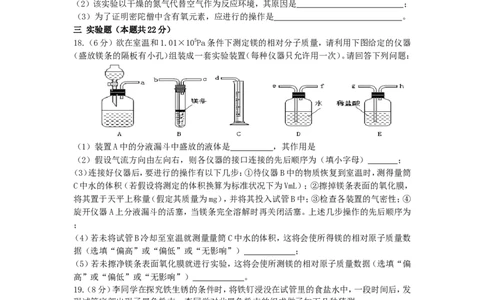
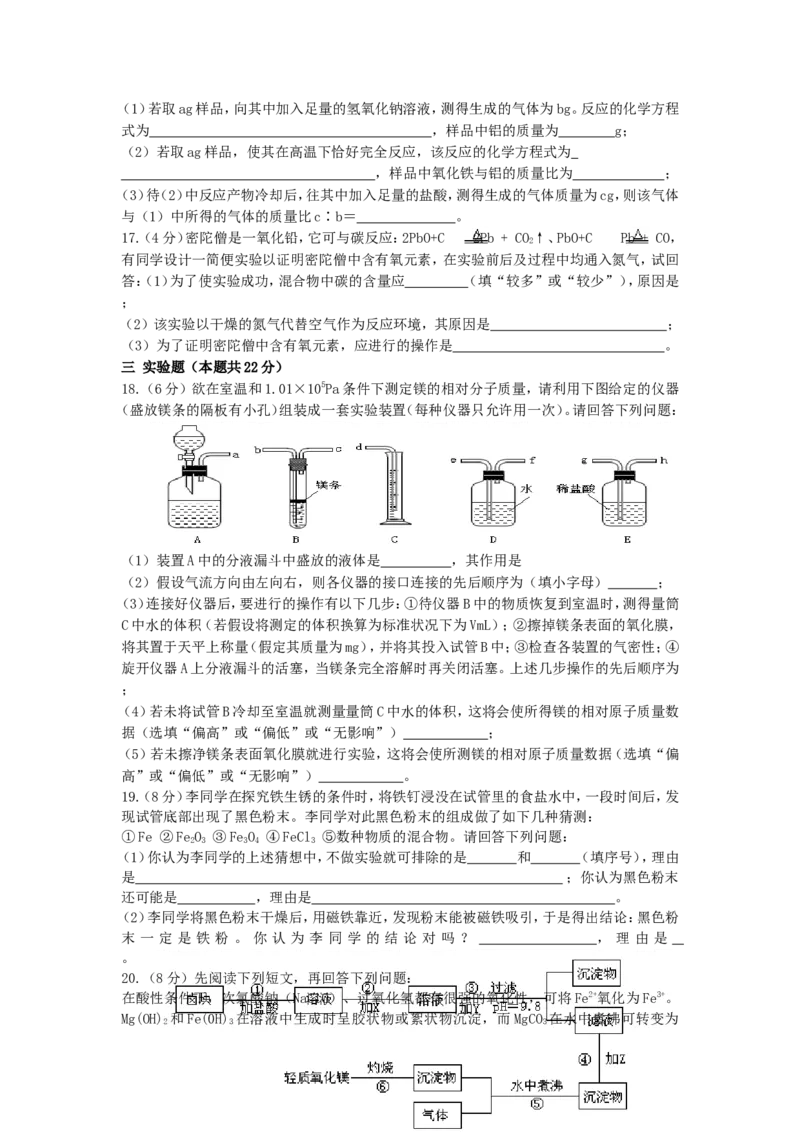
18.(6分)欲在室温和1.01×105Pa条件下测定镁的相对分子质量,请利用下图给定的仪器
(盛放镁条的隔板有小孔)组装成一套实验装置(每种仪器只允许用一次)。请回答下列问题:
(1)装置A中的分液漏斗中盛放的液体是 ,其作用是
(2)假设气流方向由左向右,则各仪器的接口连接的先后顺序为(填小字母) ;
(3)连接好仪器后,要进行的操作有以下几步:①待仪器B中的物质恢复到室温时,测得量筒
C中水的体积(若假设将测定的体积换算为标准状况下为VmL);②擦掉镁条表面的氧化膜,
将其置于天平上称量(假定其质量为mg),并将其投入试管B中;③检查各装置的气密性;④
旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞。上述几步操作的先后顺序为
;
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所得镁的相对原子质量数
据(选填“偏高”或“偏低”或“无影响”) ;
(5)若未擦净镁条表面氧化膜就进行实验,这将会使所测镁的相对原子质量数据(选填“偏
高”或“偏低”或“无影响”) 。
19.(8分)李同学在探究铁生锈的条件时,将铁钉浸没在试管里的食盐水中,一段时间后,发
现试管底部出现了黑色粉末。李同学对此黑色粉末的组成做了如下几种猜测:
①Fe ②FeO ③FeO ④FeCl ⑤数种物质的混合物。请回答下列问题:
2 3 3 4 3
(1)你认为李同学的上述猜想中,不做实验就可排除的是 和 (填序号),理由
是 ;你认为黑色粉末
还可能是 ,理由是 。
(2)李同学将黑色粉末干燥后,用磁铁靠近,发现粉末能被磁铁吸引,于是得出结论:黑色粉
末 一 定 是 铁 粉 。 你 认 为 李 同 学 的 结 论 对 吗 ? , 理 由 是
。
20.(8分)先阅读下列短文,再回答下列问题:
在酸性条件下,次氯酸钠(NaClO)、过氧化氢都有很强的氧化性,可将Fe2+氧化为Fe3+。
Mg(OH) 和Fe(0H) 在溶液中生成时呈胶状物或絮状物沉淀,而MgCO 在水中煮沸可转变为
2 3 3Mg(OH)。“卤块”的主要成分为MgCl,还含有FeCl、FeCl、MnCl 等杂质。若以它为原料,按
2 2 2 3 2
下图工艺流程即可制得“轻质氧化镁”。若要求产品不含杂质离子,而且成本较低,流程中
所用试剂或pH控制可参考表1、表2来确定。
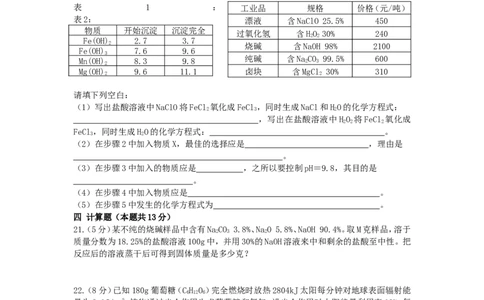
表 1 : 工业品 规格 价格(元/吨)
表2: 漂液 含NaClO 25.5% 450
物质 开始沉淀 沉淀完全
过氧化氢 含HO 30% 240
2 2
Fe(OH) 2.7 3.7
2 烧碱 含NaOH 98% 2100
Fe(OH) 7.6 9.6
3
Mn(OH) 2 8.3 9.8 纯碱 含Na 2 CO 3 99.5% 600
Mg(OH) 9.6 11.1 卤块 含MgCl 30% 310
2 2
请填下列空白:
(1)写出盐酸溶液中NaClO将FeCl 氧化成FeCl,同时生成NaCl和HO的化学方程式:
2 3 2
,写出在盐酸溶液中HO 将FeCl 氧化成
2 2 2
FeCl,同时生成HO的化学方程式: 。
3 2
(2)在步骤2中加入物质X,最佳的选择应是 ,理由是
。
(3)在步骤3中加入的物质应是 ,之所以要控制pH=9.8,其目的是
。
(4)在步骤4中加入物质应是 。
(5)在步骤5中发生的化学方程式为 。
四 计算题(本题共13分)
21.(5分)某不纯的烧碱样品中含有NaCO 3.8%、NaO 5.8%、NaOH 90.4%。取M克样品,溶于
2 3 2
质量分数为18.25%的盐酸溶液100g中,并用30%的NaOH溶液来中和剩余的盐酸至中性。把
反应后的溶液蒸干后可得到固体质量是多少克?
22.(8分)已知180g葡萄糖(CH O)完全燃烧时放热2804kJ太阳每分钟对地球表面辐射能
6 12 6
量为2.1J/cm2;植物通过光合作用生成葡萄糖和氧气。设光合作用时太阳能量利用率10%,每
片树叶面积以10cm2计算,这样的树叶100片要合成1.8g葡萄糖。问:
(1)需光照多长时间?
(2)若空气中含CO 质量分数为0.3%,需要标准状况下空气多少升?(标准状况下空气密度
2
为1.29g/L)
(3)若标准状况下氧气密度为1.429g/L,问光合作用时除生成1.8g葡萄糖,还放出氧气多少
升?
参 考 答 案
一 选择题(每题有1~2个正确答案,请将正确答案的序号填入答案栏里,每小题2分,共30分)
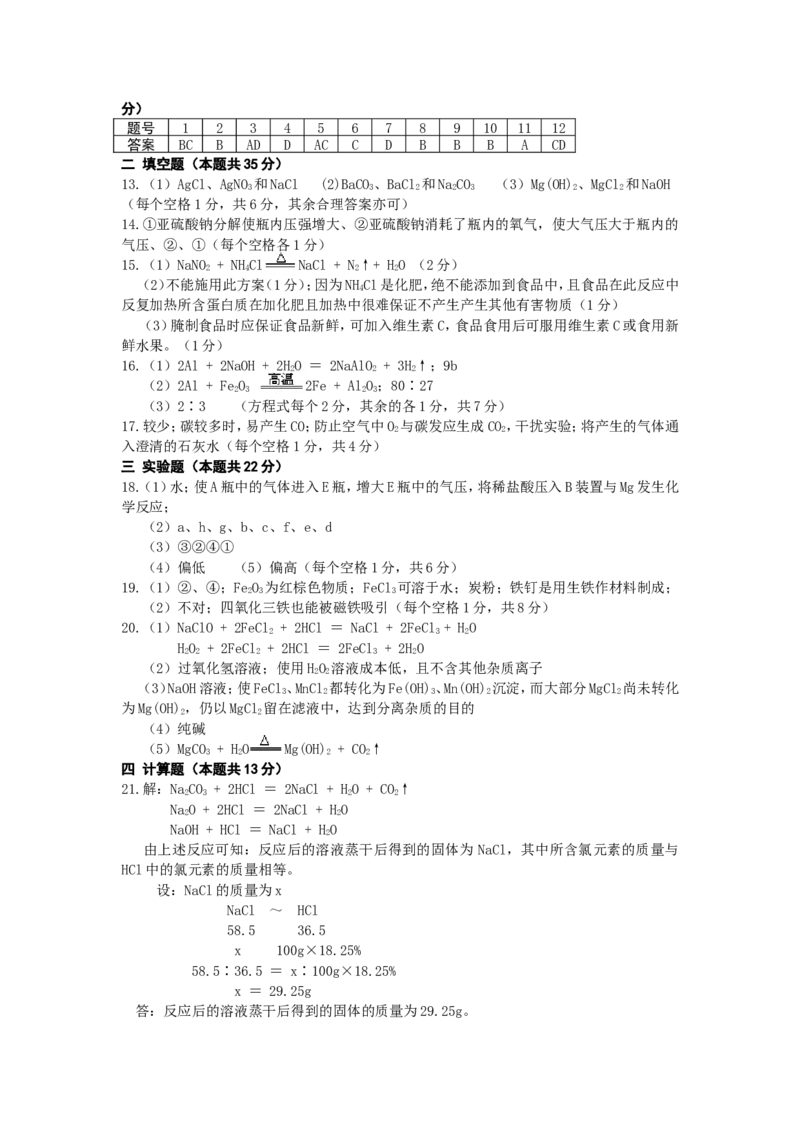
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 BC B AD D AC C D B B B A CD
二 填空题(本题共35分)
13.(1)AgCl、AgNO 和NaCl (2)BaCO、BaCl 和NaCO (3)Mg(OH)、MgCl 和NaOH
3 3 2 2 3 2 2
(每个空格1分,共6分,其余合理答案亦可)
14.①亚硫酸钠分解使瓶内压强增大、②亚硫酸钠消耗了瓶内的氧气,使大气压大于瓶内的
气压、②、①(每个空格各1分)
15.(1)NaNO + NHCl NaCl + N↑+ HO (2分)
2 4 2 2
(2)不能施用此方案(1分);因为NHCl是化肥,绝不能添加到食品中,且食品在此反应中
4
反复加热所含蛋白质在加化肥且加热中很难保证不产生产生其他有害物质(1分)
(3)腌制食品时应保证食品新鲜,可加入维生素C,食品食用后可服用维生素C或食用新
鲜水果。(1分)
16.(1)2Al + 2NaOH + 2HO = 2NaAlO + 3H↑;9b
2 2 2
(2)2Al + FeO 2Fe + AlO;80∶27
2 3 2 3
(3)2∶3 (方程式每个2分,其余的各1分,共7分)
17.较少;碳较多时,易产生CO;防止空气中O 与碳发应生成CO,干扰实验;将产生的气体通
2 2
入澄清的石灰水(每个空格1分,共4分)
三 实验题(本题共22分)
18.(1)水;使A瓶中的气体进入E瓶,增大E瓶中的气压,将稀盐酸压入B装置与Mg发生化
学反应;
(2)a、h、g、b、c、f、e、d
(3)③②④①
(4)偏低 (5)偏高(每个空格1分,共6分)
19.(1)②、④;FeO 为红棕色物质;FeCl 可溶于水;炭粉;铁钉是用生铁作材料制成;
2 3 3
(2)不对;四氧化三铁也能被磁铁吸引(每个空格1分,共8分)
20.(1)NaClO + 2FeCl + 2HCl = NaCl + 2FeCl + HO
2 3 2
HO + 2FeCl + 2HCl = 2FeCl + 2HO
2 2 2 3 2
(2)过氧化氢溶液;使用HO 溶液成本低,且不含其他杂质离子
2 2
(3)NaOH溶液;使FeCl、MnCl 都转化为Fe(OH)、Mn(OH) 沉淀,而大部分MgCl 尚未转化
3 2 3 2 2
为Mg(OH),仍以MgCl 留在滤液中,达到分离杂质的目的
2 2
(4)纯碱
(5)MgCO + HO Mg(OH) + CO↑
3 2 2 2
四 计算题(本题共13分)
21.解:NaCO + 2HCl = 2NaCl + HO + CO↑
2 3 2 2
NaO + 2HCl = 2NaCl + HO
2 2
NaOH + HCl = NaCl + HO
2
由上述反应可知:反应后的溶液蒸干后得到的固体为 NaCl,其中所含氯元素的质量与
HCl中的氯元素的质量相等。
设:NaCl的质量为x
NaCl ~ HCl
58.5 36.5
x 100g×18.25%
58.5∶36.5 = x∶100g×18.25%
x = 29.25g
答:反应后的溶液蒸干后得到的固体的质量为29.25g。22.由能量守恒可知:180gCH O 完全燃烧放热2804×103J,则生成180gCH O 需要吸热
6 12 6 6 12 6
2804×103J。
设:生成1.8g CH O 需要t分钟
6 12 6
则:2.1×10%×10×100×t = 2804×103×1/100 t = 133.5分钟
设:生成生成1.8g CH O 需要CO 质量为x,同时生成O 的质量为y
6 12 6 2 2
6CO + 6HO CH O + 6O
2 2 6 12 6 2
264 180 192
x 1.8g y
264∶x= 180∶1.8g 180∶1.8g = 192∶y
x = 2.64g y= 1.92g
故空气质量为2.64÷0.3%=880g 空气的体积为880g÷1.29g/L=682L
氧气的体积为1.92g÷1.429g/L=1.34L