文档内容
2020 年全国统一高考化学试卷(新课标Ⅰ)
参考答案与试题解析
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.(6分)国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒
剂、过氧乙酸(CH COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说
3
法错误的是( )
A.CH CH OH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
【分析】A.CH CH OH与水分子间能形成氢键,并且都是极性分子;
3 2
B.NaClO具有强氧化性;
C.过氧乙酸的结构简式为CH COOOH;
3
D.氯仿的化学名称是三氯甲烷。
【解答】解:A.CH CH OH与水分子间能形成氢键,并且都是极性分子,所以CH CH OH
3 2 3 2
能与水以任意比互溶,故A正确;
B.NaClO具有强氧化性,通过氧化能灭活病毒,故B正确;
C.过氧乙酸的结构简式为CH COOOH,相对分子质量为12×2+4+16×3=76,故C正
3
确;
D.氯仿的化学名称是三氯甲烷,不是四氯化碳,故D错误;
故选:D。
【点评】本题结合时事热点考查化学问题,平时要注意积累,题目难度不大。
2.(6分)紫花前胡醇( )可从中药材当归和白芷中提取得到,能
提高人体免疫力。有关该化合物,下列叙述错误的是( )
A.分子式为C H O
14 14 4
B.不能使酸性重铬酸钾溶液变色
第1页 | 共22页C.能够发生水解反应
D.能够发生消去反应生成双键
【分析】A、分子中14个碳原子,不饱和度为8;
B、分子中含有碳碳双键和羟基直接相连碳上有氢原子;
C、分子中含有酯基,能发生水解;
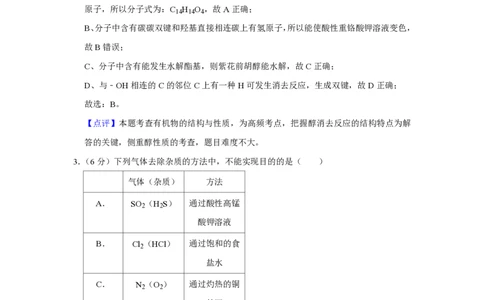
D、与﹣OH相连的C的邻位C上有一种H可发生消去反应;
【解答】解:A、分子的不饱和度为8,则氢原子个数为:14×2+2﹣8×2=14,四个氧
原子,所以分子式为:C H O ,故A正确;
14 14 4
B、分子中含有碳碳双键和羟基直接相连碳上有氢原子,所以能使酸性重铬酸钾溶液变色,
故B错误;
C、分子中含有能发生水解酯基,则紫花前胡醇能水解,故C正确;
D、与﹣OH相连的C的邻位C上有一种H可发生消去反应,生成双键,故D正确;
故选:B。
【点评】本题考查有机物的结构与性质,为高频考点,把握醇消去反应的结构特点为解
答的关键,侧重醇性质的考查,题目难度不大。
3.(6分)下列气体去除杂质的方法中,不能实现目的的是( )
气体(杂质) 方法
A. SO (H S) 通过酸性高锰
2 2
酸钾溶液
B. Cl (HCl) 通过饱和的食
2
盐水
C. N (O ) 通过灼热的铜
2 2
丝网
D. NO(NO ) 通过氢氧化钠
2
溶液
A.A B.B C.C D.D
【分析】除杂的原则是不引入新的杂质,不减少要提纯的物质,操作简单,绿色环保。
A.SO 具有还原性,易被酸性高锰酸钾溶液氧化为硫酸;
2
B.饱和食盐水可以减少氯气的溶解量;
第2页 | 共22页C.N (O )利用化学性质的差异,铜与氧气反应,;
2 2
D.2NO +2NaOH=NaNO +NaNO +H O,NO为不成盐氧化物,
2 2 3 2
【解答】解:A.SO 被酸性高锰酸钾溶液氧化为硫酸,故A错误;
2
B.Cl (HCl)利用溶解性的差异,除去HCl,故B正确;
2
C.N (O )利用化学性质的差异,铜与氧气反应,不与氮气反应,达到除杂目的,故C
2 2
正确;
D.NO 可以与NaOH发生反应:2NO +2NaOH=NaNO +NaNO +H O,NO与NaOH溶
2 2 2 3 2
液不能发生反应;尽管 NO 可以与 NO 一同跟 NaOH 发生反应:NO+NO +2NaOH═
2 2
2NaNO +H O,但由于杂质的含量一般较少,所以也不会对NO的量产生较大的影响,
3 2
故D正确;
故选:A。
【点评】本题考查了气体除杂质,要掌握各物质的性质,难度不大,注重基础。
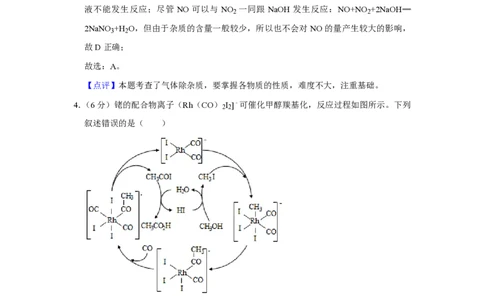
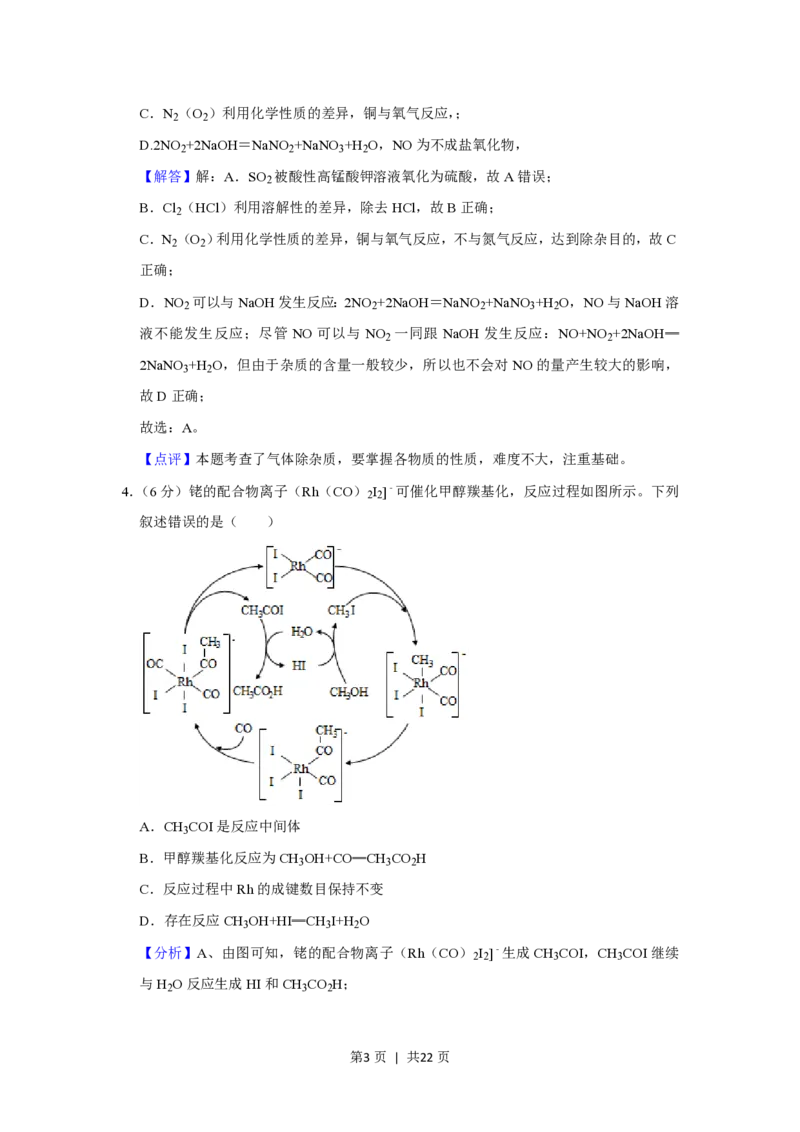
4.(6分)铑的配合物离子(Rh(CO) I ]﹣可催化甲醇羰基化,反应过程如图所示。下列
2 2
叙述错误的是( )
A.CH COI是反应中间体
3
B.甲醇羰基化反应为CH OH+CO═CH CO H
3 3 2
C.反应过程中Rh的成键数目保持不变
D.存在反应CH OH+HI═CH I+H O
3 3 2
【分析】A、由图可知,铑的配合物离子(Rh(CO) I ]﹣生成CH COI,CH COI继续
2 2 3 3
与H O反应生成HI和CH CO H;
2 3 2
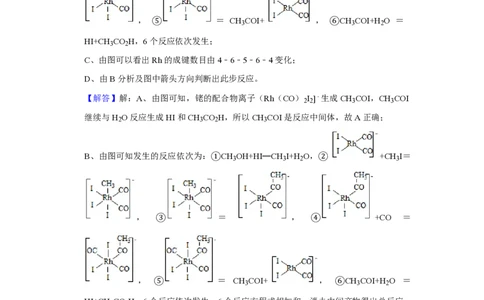
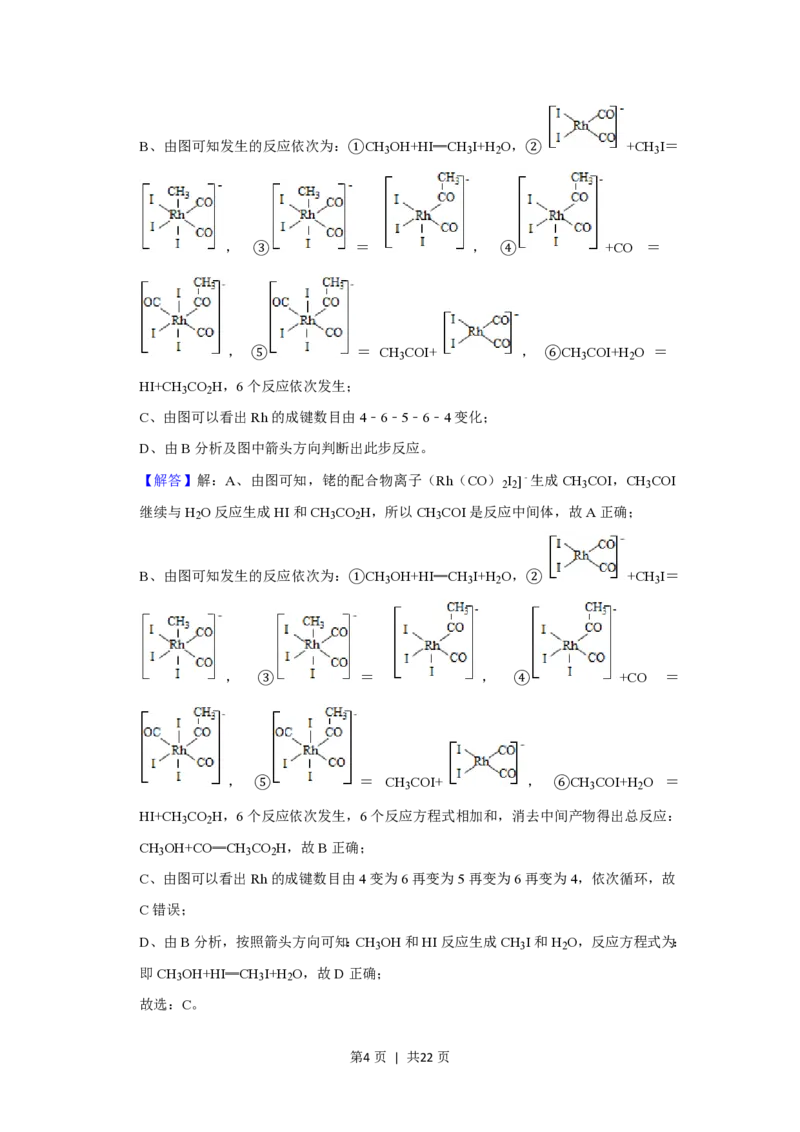
第3页 | 共22页B、由图可知发生的反应依次为:①CH OH+HI═CH I+H O,② +CH I=
3 3 2 3
, ③ = , ④ +CO =
, ⑤ = CH COI+ , ⑥CH COI+H O =
3 3 2
HI+CH CO H,6个反应依次发生;
3 2
C、由图可以看出Rh的成键数目由4﹣6﹣5﹣6﹣4变化;
D、由B分析及图中箭头方向判断出此步反应。
【解答】解:A、由图可知,铑的配合物离子(Rh(CO) I ]﹣生成CH COI,CH COI
2 2 3 3
继续与H O反应生成HI和CH CO H,所以CH COI是反应中间体,故A正确;
2 3 2 3
B、由图可知发生的反应依次为:①CH OH+HI═CH I+H O,② +CH I=
3 3 2 3
, ③ = , ④ +CO =
, ⑤ = CH COI+ , ⑥CH COI+H O =
3 3 2
HI+CH CO H,6个反应依次发生,6个反应方程式相加和,消去中间产物得出总反应:
3 2
CH OH+CO═CH CO H,故B正确;
3 3 2
C、由图可以看出Rh的成键数目由4变为6再变为5再变为6再变为4,依次循环,故
C错误;
D、由B分析,按照箭头方向可知:CH OH和HI反应生成CH I和H O,反应方程式为:
3 3 2
即CH OH+HI═CH I+H O,故D正确;
3 3 2
故选:C。
第4页 | 共22页【点评】本题考查学生对有机化学基础的理解和掌握,题目难度中等,掌握反应类型、
化学反应原理等,明确由化学反应是解题关键。同时也考查了学生阅读题目获取新信息
的能力,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力。
5.(6分)1934年约里奥﹣居里夫妇在核反应中用α粒子(即氦核 He)轰击金属原子 X,
得到核素 Y,开创了人造放射性核素的先河: X+ He→ Y+ n其中元素X、Y的
最外层电子数之和为8.下列叙述正确的是( )
A. X的相对原子质量为26
B.X、Y均可形成三氯化物
C.X的原子半径小于Y的
D.Y仅有一种含氧酸
【分析】由 X+ He→ Y+ n及质量守恒可知,W=30+1﹣4=27,X、Y的最外层电
子数之和为8,X的最外层电子数为 =3,金属原子 X的质量数为27、且位于ⅢA
族,Z=13符合题意,则X为Al;Y的最外层电子数为8﹣3=5,质子数为13+2=15,
Y为P,以此来解答。
【解答】解:由上述分析可知X为Al、Y为P,
A.W为27,X原子的相对原子质量为27,故A错误;
B.X、Y可形成三氯化物分别为AlCl 、PCl ,故B正确;
3 3
C.同周期从左向右原子半径减小,则X的原子半径大于Y的半径,故C错误;
D.Y的含氧酸有磷酸、偏磷酸等,故D错误;
故选:B。
【点评】本题考查原子结构与元素周期律,为高频考点,把握最外层电子数、质量守恒
来推断元素为解答的关键,同时侧重分析与应用能力的考查,注意规律性知识的应用,
题目难度不大。
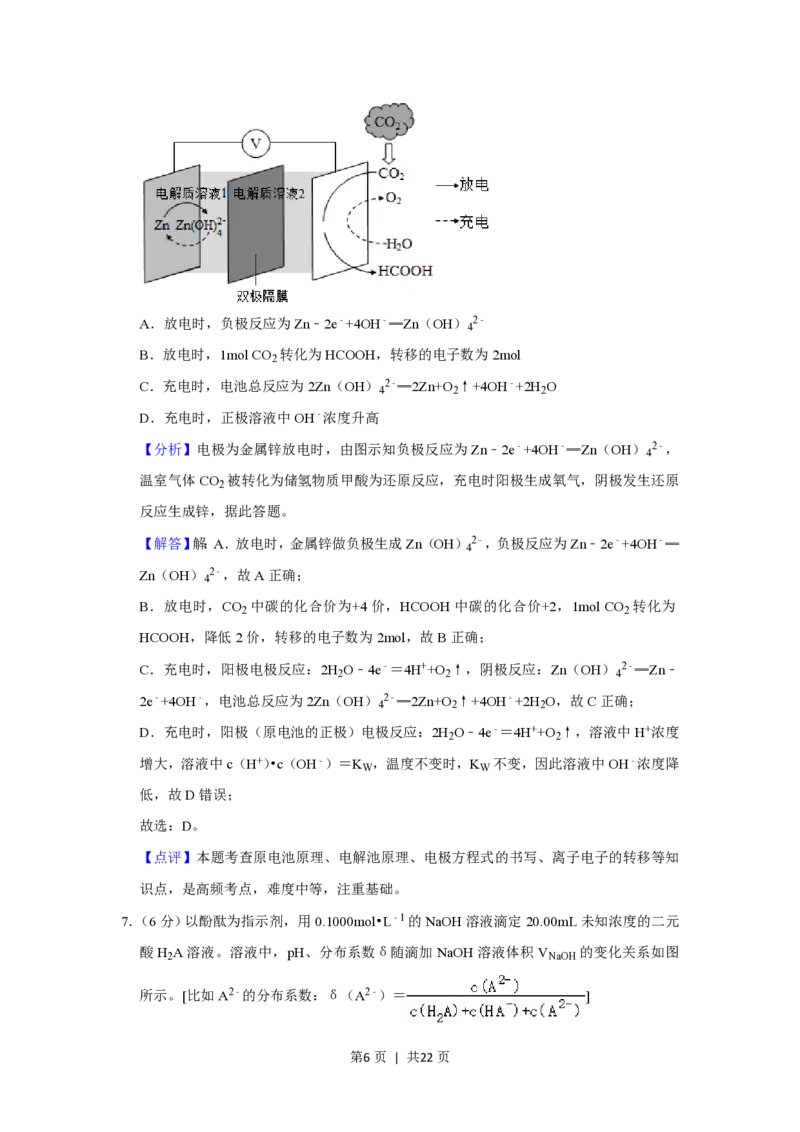
6.(6分)科学家近年发明了一种新型Zn﹣CO 水介质电池。电池示意图如图,电极为金
2
属锌和选择性催化材料。放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境
2
和能源问题提供了一种新途径。下列说法错误的是( )
第5页 | 共22页A.放电时,负极反应为Zn﹣2e﹣+4OH﹣═Zn(OH) 2﹣
4
B.放电时,1mol CO 转化为HCOOH,转移的电子数为2mol
2
C.充电时,电池总反应为2Zn(OH) 2﹣═2Zn+O ↑+4OH﹣+2H O
4 2 2
D.充电时,正极溶液中OH﹣浓度升高
【分析】电极为金属锌放电时,由图示知负极反应为Zn﹣2e﹣+4OH﹣═Zn(OH) 2﹣,
4
温室气体CO 被转化为储氢物质甲酸为还原反应,充电时阳极生成氧气,阴极发生还原
2
反应生成锌,据此答题。
【解答】解:A.放电时,金属锌做负极生成Zn(OH)2﹣,负极反应为Zn﹣2e﹣+4OH﹣═
4
Zn(OH) 2﹣,故A正确;
4
B.放电时,CO 中碳的化合价为+4价,HCOOH中碳的化合价+2,1mol CO 转化为
2 2
HCOOH,降低2价,转移的电子数为2mol,故B正确;
C.充电时,阳极电极反应:2H O﹣4e﹣=4H++O ↑,阴极反应:Zn(OH) 2﹣═Zn﹣
2 2 4
2e﹣+4OH﹣,电池总反应为2Zn(OH) 2﹣═2Zn+O ↑+4OH﹣+2H O,故C正确;
4 2 2
D.充电时,阳极(原电池的正极)电极反应:2H O﹣4e﹣=4H++O ↑,溶液中H+浓度
2 2
增大,溶液中c(H+)•c(OH﹣)=K ,温度不变时,K 不变,因此溶液中OH﹣浓度降
W W
低,故D错误;
故选:D。
【点评】本题考查原电池原理、电解池原理、电极方程式的书写、离子电子的转移等知
识点,是高频考点,难度中等,注重基础。
7.(6分)以酚酞为指示剂,用0.1000mol•L﹣1的NaOH溶液滴定20.00mL未知浓度的二元
酸H A溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关系如图
2 NaOH
所示。[比如A2﹣的分布系数:δ(A2﹣)= ]
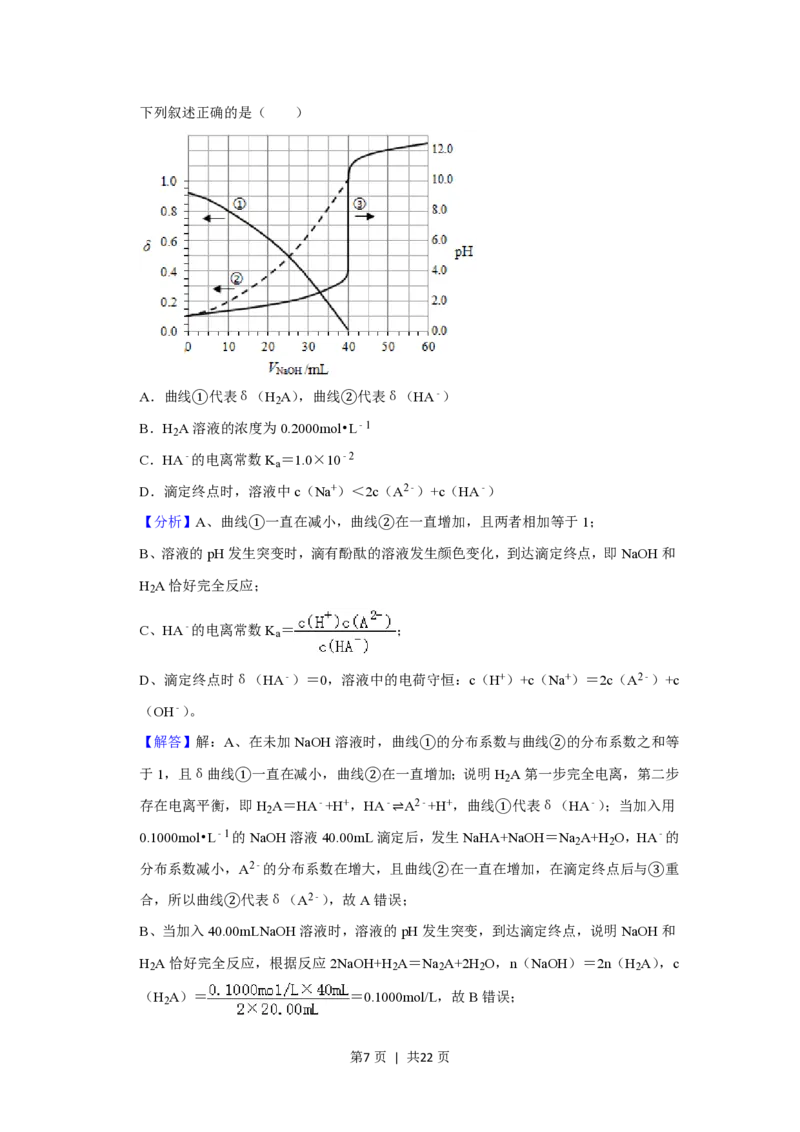
第6页 | 共22页下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA﹣)
2
B.H A溶液的浓度为0.2000mol•L﹣1
2
C.HA﹣的电离常数K =1.0×10﹣2
a
D.滴定终点时,溶液中c(Na+)<2c(A2﹣)+c(HA﹣)
【分析】A、曲线①一直在减小,曲线②在一直增加,且两者相加等于1;
B、溶液的pH发生突变时,滴有酚酞的溶液发生颜色变化,到达滴定终点,即NaOH和
H A恰好完全反应;
2
C、HA﹣的电离常数K = ;
a
D、滴定终点时δ(HA﹣)=0,溶液中的电荷守恒:c(H+)+c(Na+)=2c(A2﹣)+c
(OH﹣)。
【解答】解:A、在未加NaOH溶液时,曲线①的分布系数与曲线②的分布系数之和等
于1,且δ曲线①一直在减小,曲线②在一直增加;说明H A第一步完全电离,第二步
2
存在电离平衡,即H A=HA﹣+H+,HA﹣⇌A2﹣+H+,曲线①代表δ(HA﹣);当加入用
2
0.1000mol•L﹣1的NaOH溶液40.00mL滴定后,发生NaHA+NaOH=Na A+H O,HA﹣的
2 2
分布系数减小,A2﹣的分布系数在增大,且曲线②在一直在增加,在滴定终点后与③重
合,所以曲线②代表δ(A2﹣),故A错误;
B、当加入40.00mLNaOH溶液时,溶液的pH发生突变,到达滴定终点,说明NaOH和
H A恰好完全反应,根据反应2NaOH+H A=Na A+2H O,n(NaOH)=2n(H A),c
2 2 2 2 2
(H A)= =0.1000mol/L,故B错误;
2
第7页 | 共22页C、由于H A第一步完全电离,则HA﹣的起始浓度为0.1000mol/L,根据图象,当V =
2 NaOH
0时,HA﹣的分布系数为0.9,溶液的pH=1,A2﹣的分布系数为0.1,则HA﹣的电离平衡
常数K = = ≈1×10﹣2,故C正
a
确;
D、用酚酞作指示剂,酚酞变色的pH范围为8.2~10,终点时溶液呈碱性,c(OH﹣)>
c(H+),溶液中的电荷守恒,c(H+)+c(Na+)=2c(A2﹣)+c(OH﹣)+c(HA﹣),则
c(Na+)>2c(A2﹣)+c(HA﹣),故D错误;
故选:C。
【点评】本题考查学生对酸碱混合时的定性判断和pH的理解和掌握,以及阅读题目获取
新信息能力等,熟练掌握电离平衡、水解平衡的的影响原理等,需要学生具备扎实的基
础与综合运用知识、信息分析解决问题能力,题目难度中等。明确曲线①②③是解题关
键。
二、非选择题:共58分。第8~10题为必考题,每个试题考生都必须作答。第11~12题
为选考题,考生根据要求作答。(一)必考题:共43分。
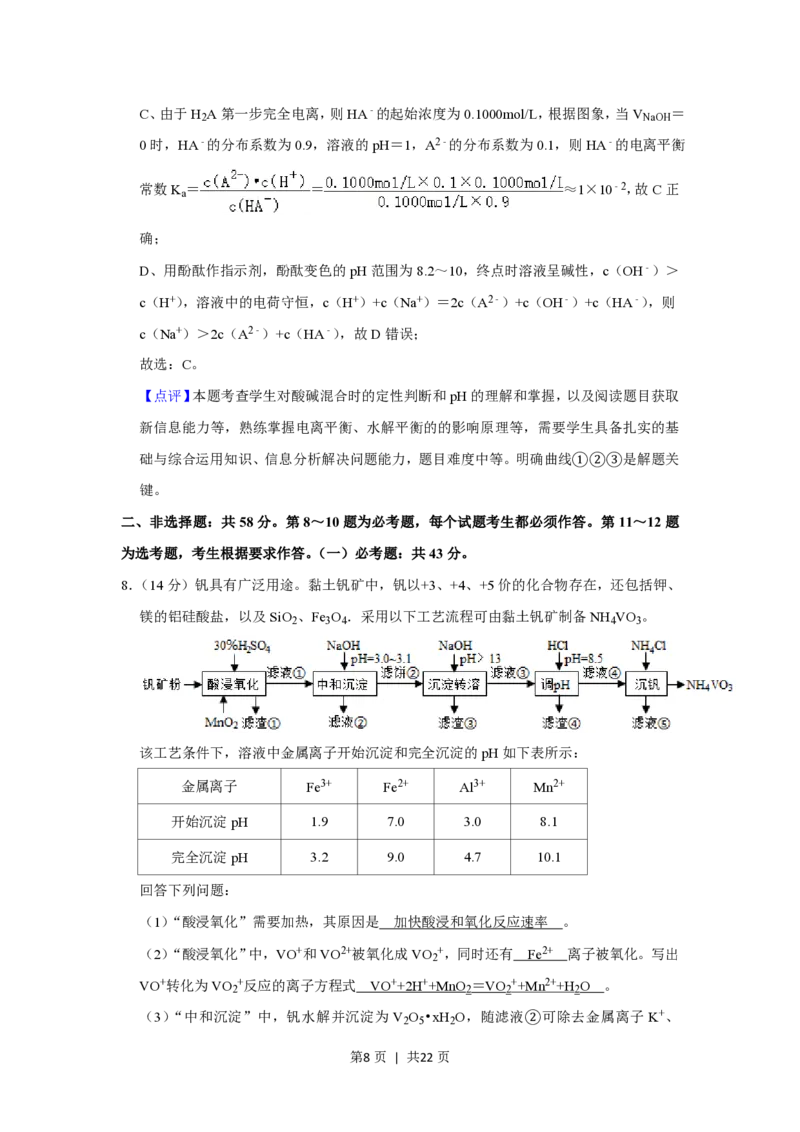
8.(14分)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、
镁的铝硅酸盐,以及SiO 、Fe O .采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是 加快酸浸和氧化反应速率 。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO +,同时还有 Fe2+ 离子被氧化。写出
2
VO+转化为VO +反应的离子方程式 VO++2H++MnO =VO ++Mn2++H O 。
2 2 2 2
(3)“中和沉淀”中,钒水解并沉淀为 V O •xH O,随滤液②可除去金属离子 K+、
2 5 2
第8页 | 共22页Mg2+、Na+、 Mn2+ ,以及部分的 Al3+和Fe3+ 。
(4)“沉淀转溶”中,V O •xH O转化为钒酸盐溶解。滤渣③的主要成分是 Fe(OH)
2 5 2
。
3
(5)“调pH”中有沉淀生成,生成沉淀反应的化学方程式是 HCl+NaAl(OH) =Al
4
(OH) ↓+NaCl+H O 。
3 2
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是 利用同离子效
4 3 4
应,促进NH VO 尽可能析出完全 。
4 3
【分析】黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以
及SiO 、Fe O ,加入稀硫酸,使Fe O 生成Fe3+和Fe2+;加入MnO 氧化还原性的Fe2+
2 3 4 3 4 2
成Fe3+;VO+和VO2+成VO +,SiO 和硅酸盐与酸生成的硅酸成为滤渣①,滤液①含有:
2 2
Fe3+、VO +、K+、Mg2+、Na+、Mn2+、Al3+;滤液①加入NaOH溶液至pH=3.0~3.1,
2
中和过量的硫酸并沉淀 Fe3+,使钒水解并沉淀为 V O •xH O,得滤饼②,除去滤液
2 5 2
②Mn2+、K+、Mg2+、Na+及部分Fe3+、Al3+;滤饼②加入过量NaOH溶液至pH>13,
沉淀转溶得滤液③,滤液③含有V O •xH O生成VO ﹣和溶于碱的Al(OH) 生成的
2 5 2 3 3
Al(OH) ﹣;滤渣③为 Fe(OH) ,滤液③加入盐酸调 pH,Al(OH) ﹣生成 Al
4 3 4
(OH)即滤渣④;滤液④含有VO ﹣,加入NH Cl沉钒的产物:NH VO ;和滤液⑤NaCl
3 3 4 4 3
溶液;
(1)升高温度,反应速率加快;
(2)加入氧化性物质可除去具有还原性的离子;依据电子转移守恒和元素守恒写出离子
方程式;
(3)根据某些离子沉淀的pH,找出相应沉淀的离子;
(4)Fe3+溶液呈强碱性时转化为Fe(OH) ;
3
(5)加入酸沉淀离子Al(OH) ﹣生成Al(OH) ;
4 3
(6)NH Cl溶于水电离出NH +,根据沉淀溶解平衡原理,利用等离子效应。
4 4
【解答】解:(1)温度升高反应速率加快;加快酸浸氧化的反应速率,
故答案为:加快酸浸和氧化反应速率;
(2)加入氧化剂MnO ,除了氧化具有还原性的VO+和VO2+,还可以氧化还原性的Fe2+
2
为Fe3+;以便后面步骤一次性的除去Fe元素;酸浸氧化VO+转化为VO +,根据电荷守
2
恒和电子转移守恒得出:在酸性条件下,+3价的矾化合价升高2生成+5价,MnO 中+4
2
价的锰化合价降低 2 生成+2 价,所以反应的离子方程式为:VO++2H++MnO =
2
第9页 | 共22页VO ++Mn2++H O,
2 2
故答案为:Fe2+;VO++2H++MnO =VO ++Mn2++H O;
2 2 2
(3)“中和沉淀”中,滤液①加入NaOH溶液至pH=3.0~3.1,中和过量的硫酸并沉淀
Fe3+和Al3+,使钒水解并沉淀为V O •xH O,得滤饼②,除去滤液②Mn2+、K+、Mg2+、
2 5 2
Na+及部分Fe3+、Al3+,
故答案为:Mn2+、Fe3+和Al3+;
(4)滤液①加入NaOH溶液至pH=3.0~3.1,中和过量的硫酸并沉淀Fe3+,使钒水解
并沉淀为V O •xH O,得滤饼②,
2 5 2
故答案为:Fe(OH) ;
3
(5)滤液③含有V O •xH O生成VO ﹣和溶于碱的Al(OH) 生成的Al(OH) ﹣;
2 5 2 3 3 4
滤液③加入盐酸调pH,Al(OH)﹣生成Al(OH) 即滤渣④;化学方程式为:HCl+NaAl
4 3
(OH) =Al(OH) ↓+NaCl+H O,
4 3 2
故答案为:HCl+NaAl(OH) =Al(OH) ↓+NaCl+H O;
4 3 2
(6)“沉钒”中析出NH VO 晶体时,NH VO 沉淀溶解平衡方程式为:NH +(aq)+VO
4 3 4 3 4 3
﹣(aq)⇌NH VO (s),需要加入过量 NH Cl,NH Cl 溶于水电离出 NH +,增大 c
4 3 4 4 4
(NH +),利用同离子效应,促进NH VO 尽可能析出完全。
4 4 3
故答案为:利用同离子效应,促进NH VO 尽可能析出完全。
4 3
【点评】本题考查学生对化学实验的理解和掌握,题目难度中等,掌握每步的除杂和分
离目的等,明确由工艺流程写出相应反应是解题关键。同时考查学生阅读题目获取新信
息的能力,需要学生具备扎实的基础与综合运用知识、信息分析解决问题能力。
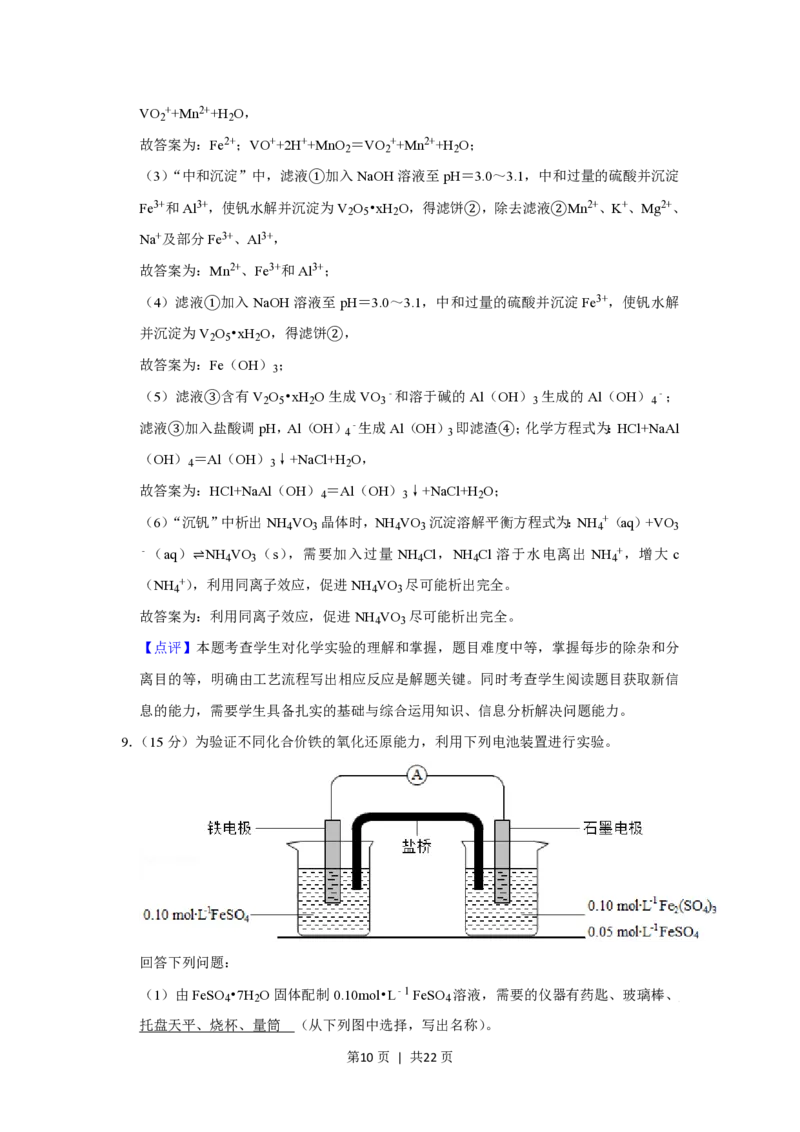
9.(15分)为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)由FeSO •7H O固体配制0.10mol•L﹣1 FeSO 溶液,需要的仪器有药匙、玻璃棒、
4 2 4
托盘天平、烧杯、量筒 (从下列图中选择,写出名称)。
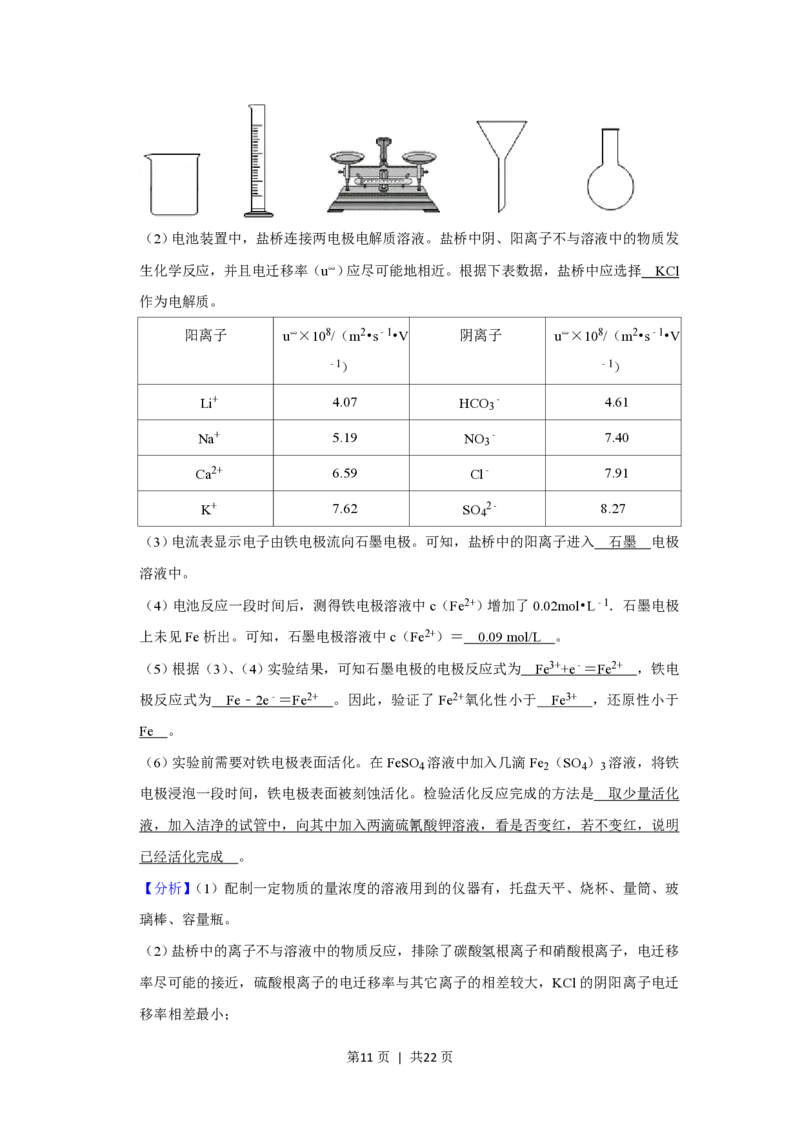
第10页 | 共22页(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发
生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择 KCl
作为电解质。
阳离子 u∞×108/(m2•s﹣1•V 阴离子 u∞×108/(m2•s﹣1•V
﹣1) ﹣1)
Li+ 4.07 HCO ﹣ 4.61
3
Na+ 5.19 NO ﹣ 7.40
3
Ca2+ 6.59 Cl﹣ 7.91
K+ 7.62 SO 2﹣ 8.27
4
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入 石墨 电极
溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol•L﹣1.石墨电极
上未见Fe析出。可知,石墨电极溶液中c(Fe2+)= 0.09 mol/L 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为 Fe3++e﹣=Fe2+ ,铁电
极反应式为 Fe﹣2e﹣=Fe2+ 。因此,验证了Fe2+氧化性小于 Fe3+ ,还原性小于
Fe 。
(6)实验前需要对铁电极表面活化。在FeSO 溶液中加入几滴Fe (SO ) 溶液,将铁
4 2 4 3
电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是 取少量活化
液,加入洁净的试管中,向其中加入两滴硫氰酸钾溶液,看是否变红,若不变红,说明
已经活化完成 。
【分析】(1)配制一定物质的量浓度的溶液用到的仪器有,托盘天平、烧杯、量筒、玻
璃棒、容量瓶。
(2)盐桥中的离子不与溶液中的物质反应,排除了碳酸氢根离子和硝酸根离子,电迁移
率尽可能的接近,硫酸根离子的电迁移率与其它离子的相差较大,KCl的阴阳离子电迁
移率相差最小;
第11页 | 共22页(3)铁电极失去电子,铁电极是负极,石墨电极是正极,原电池内部阳离子向正极移动,
所以阳离子向石墨电极移动。
(4)铁电极反应:Fe﹣2e﹣=Fe2+,铁电极增加0.02mol/L,根据电荷守恒,石墨电极反
应 Fe3++e﹣=Fe2+,则石墨电极增加 0.04 mol/L,原溶液是 0.05mol/L,现在变为 0.09
mol/L;
(5)铁电极为负极,电极反应:Fe﹣2e﹣=Fe2+,石墨电极为正极,电极反应反应:Fe3++e
﹣=Fe2+,电池的总反应式为:2Fe3++Fe=3Fe2+,根据氧化剂的氧化性大于氧化产物,所
以氧化性:Fe3+>Fe2+,同理还原性Fe>Fe2+
(6)对铁电极活化是除去表面的氧化膜,氧化膜反应完成后,铁单质把三价铁还原,所
以只要检验溶液中是否还含有三价铁离子就可以了。
【解答】解析:(1)配制一定物质的量浓度的溶液用到的仪器有:托盘天平、烧杯、量
筒、玻璃棒、容量瓶。图中给出的有托盘天平、烧杯、量筒;
故答案为:托盘天平、烧杯、量筒;
(2)盐桥中的离子不与溶液中的物质反应,排除了碳酸氢根离子和硝酸根离子,电迁移
率尽可能的接近,故选KCl;
故答案为:KCl;
(3)铁电极失去电子,铁电极是负极,石墨电极是正极,原电池内部阳离子向正极移动,
所以阳离子向石墨电极移动;
故答案为:石墨;
(4)铁电极反应:Fe﹣2e﹣=Fe2+,铁电极增加 0.02mol/L,石墨电极反应 Fe3++e﹣=
Fe2+,根据电荷守恒,则石墨电极增加0.04 mol/L,变为0.09 mol/L;
故答案为:0.09 mol/L;
(5)铁电极为负极,电极反应:Fe﹣2e﹣=Fe2+,石墨电极为正极,电极反应反应:Fe3++e
﹣=Fe2+,电池的总反应式为:2Fe3++Fe=3Fe2+;所以氧化性:Fe3+>Fe2+,还原性Fe>
Fe2+
故答案为:Fe﹣2e﹣=Fe2+;Fe3++e﹣=Fe2+;Fe3+; Fe;
(6)对铁电极活化是除去表面的氧化膜,氧化膜反应完成后,铁单质把三价铁还原,所
以只要检验溶液中是否还含有三价铁离子就可以了,取少量活化液,加入洁净的试管中,
向其中加入两滴硫氰酸钾溶液,看是否变红,若不变红,说明已经活化完成。
故答案为:取少量活化液,加入洁净的试管中,向其中加入两滴硫氰酸钾溶液,看是否
第12页 | 共22页变红,若不变红,说明已经活化完成。
【点评】本题考查了溶液的配制、原电池原理、氧化还原反应、电极方程式书写、离子
的检验等知识点,属于学科内综合,考查分析问题,解决问题的能力,难度中等。
10.(14分)硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是SO 的催
2
化氧化:SO (g)+ O (g) SO (g)△H=﹣98kJ•mol﹣1.问答下列问题:
2 2 3
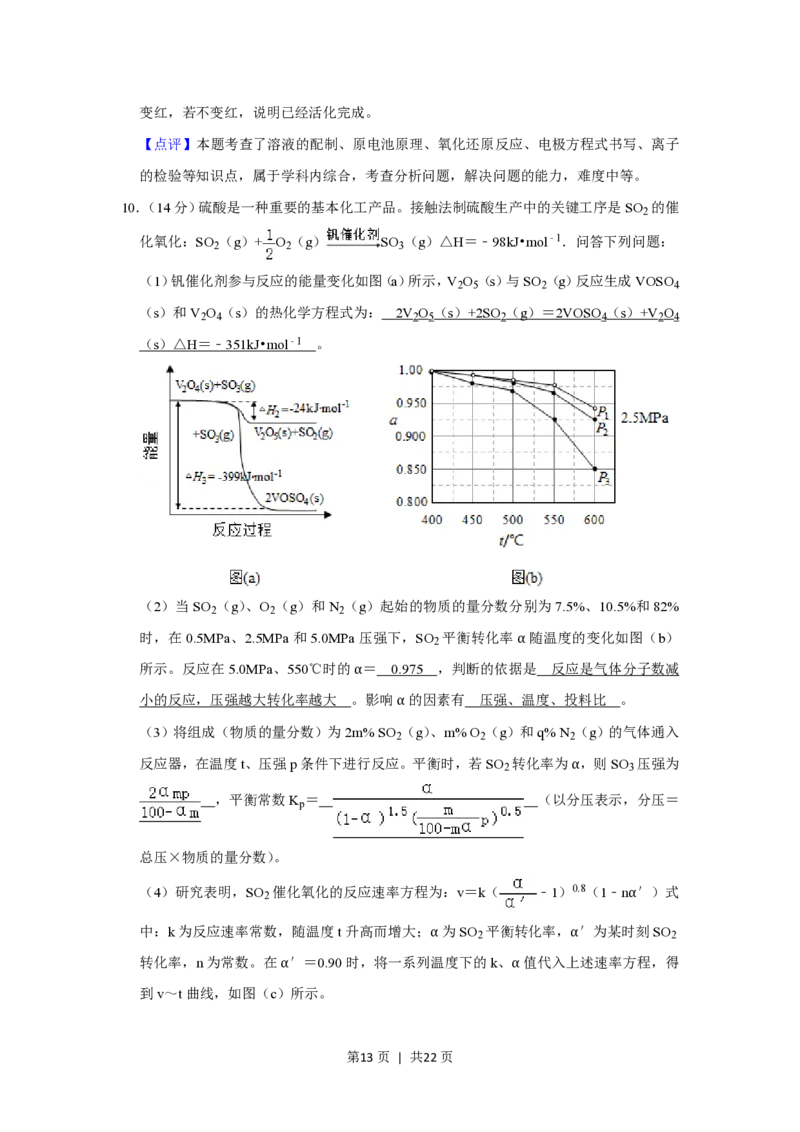
(1)钒催化剂参与反应的能量变化如图(a)所示,V O (s)与SO (g)反应生成VOSO
2 5 2 4
(s)和V O (s)的热化学方程式为: 2V O (s)+2SO (g)=2VOSO (s)+V O
2 4 2 5 2 4 2 4
(s)△H=﹣351kJ•mol﹣1 。
(2)当SO (g)、O (g)和N (g)起始的物质的量分数分别为7.5%、10.5%和82%
2 2 2
时,在0.5MPa、2.5MPa和5.0MPa压强下,SO 平衡转化率α随温度的变化如图(b)
2
所示。反应在5.0MPa、550℃时的α= 0.975 ,判断的依据是 反应是气体分子数减
小的反应,压强越大转化率越大 。影响α的因素有 压强、温度、投料比 。
(3)将组成(物质的量分数)为2m% SO (g)、m% O (g)和q% N (g)的气体通入
2 2 2
反应器,在温度t、压强p条件下进行反应。平衡时,若SO 转化率为α,则SO 压强为
2 3
,平衡常数K = (以分压表示,分压=
p
总压×物质的量分数)。
(4)研究表明,SO 催化氧化的反应速率方程为:v=k( ﹣1)0.8(1﹣nα′)式
2
中:k为反应速率常数,随温度t升高而增大;α为SO 平衡转化率,α′为某时刻SO
2 2
转化率,n为常数。在α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得
到v~t曲线,如图(c)所示。
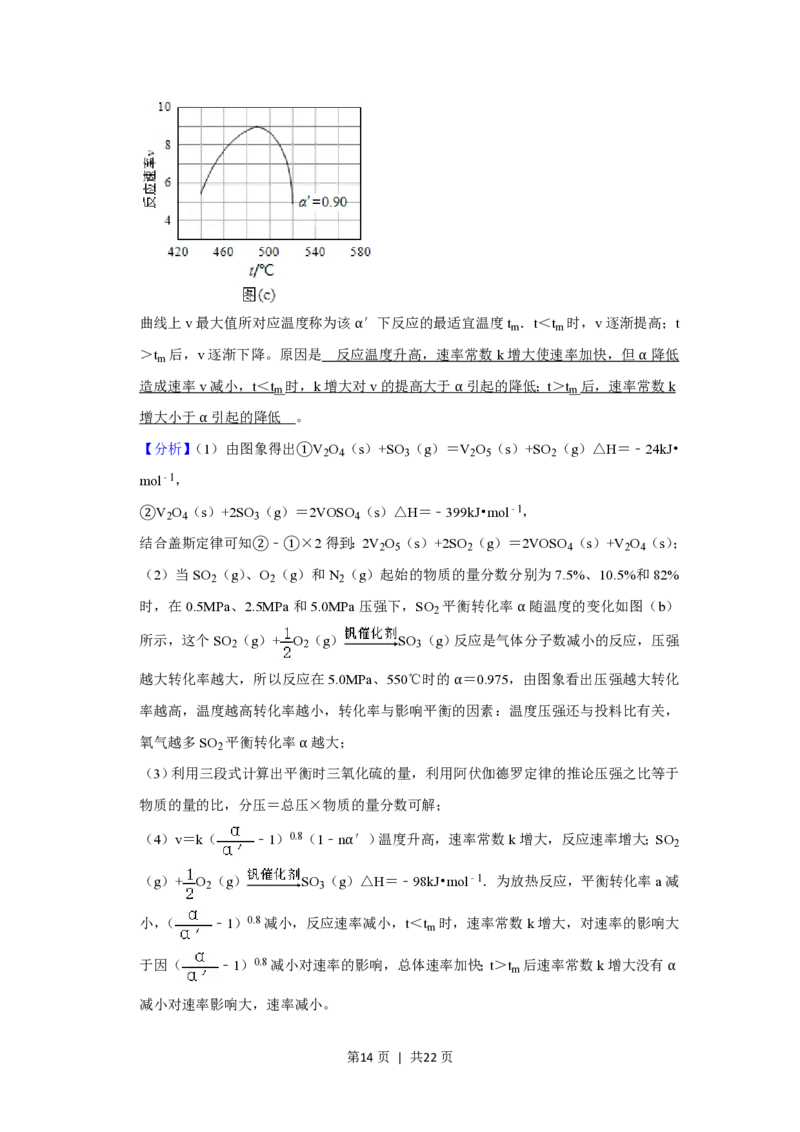
第13页 | 共22页曲线上v最大值所对应温度称为该α′下反应的最适宜温度t .t<t 时,v逐渐提高;t
m m
>t 后,v逐渐下降。原因是 反应温度升高,速率常数k增大使速率加快,但α降低
m
造成速率v减小,t<t 时,k增大对v的提高大于α引起的降低;t>t 后,速率常数k
m m
增大小于α引起的降低 。
【分析】(1)由图象得出①V O (s)+SO (g)=V O (s)+SO (g)△H=﹣24kJ•
2 4 3 2 5 2
mol﹣1,
②V O (s)+2SO (g)=2VOSO (s)△H=﹣399kJ•mol﹣1,
2 4 3 4
结合盖斯定律可知②﹣①×2得到:2V O (s)+2SO (g)=2VOSO (s)+V O (s);
2 5 2 4 2 4
(2)当SO (g)、O (g)和N (g)起始的物质的量分数分别为7.5%、10.5%和82%
2 2 2
时,在0.5MPa、2.5MPa和5.0MPa压强下,SO 平衡转化率α随温度的变化如图(b)
2
所示,这个SO (g)+ O (g) SO (g)反应是气体分子数减小的反应,压强
2 2 3
越大转化率越大,所以反应在5.0MPa、550℃时的α=0.975,由图象看出压强越大转化
率越高,温度越高转化率越小,转化率与影响平衡的因素:温度压强还与投料比有关,
氧气越多SO 平衡转化率α越大;
2
(3)利用三段式计算出平衡时三氧化硫的量,利用阿伏伽德罗定律的推论压强之比等于
物质的量的比,分压=总压×物质的量分数可解;
(4)v=k( ﹣1)0.8(1﹣nα′)温度升高,速率常数k增大,反应速率增大;SO
2
(g)+ O (g) SO (g)△H=﹣98kJ•mol﹣1.为放热反应,平衡转化率a减
2 3
小,( ﹣1)0.8减小,反应速率减小,t<t 时,速率常数k增大,对速率的影响大
m
于因( ﹣1)0.8减小对速率的影响,总体速率加快;t>t 后速率常数k增大没有α
m
减小对速率影响大,速率减小。
第14页 | 共22页【解答】解:(1)由图象得出①V O (s)+SO (g)=V O (s)+SO (g)△H=﹣24kJ
2 4 3 2 5 2
•mol﹣1,
②V O (s)+2SO (g)=2VOSO (s)△H=﹣399kJ•mol﹣1,
2 4 3 4
由盖斯定律可知②﹣①×2得到:2V O (s)+2SO (g)=2VOSO (s)+V O (s)△
2 5 2 4 2 4
H=﹣351kJ•mol﹣1;
故答案为:2V O (s)+2SO (g)=2VOSO (s)+V O (s)△H=﹣351kJ•mol﹣1;
2 5 2 4 2 4
(2)当SO (g)、O (g)和N (g)起始的物质的量分数分别为7.5%、10.5%和82%
2 2 2
时,在0.5MPa、2.5MPa和5.0MPa压强下,SO 平衡转化率α随温度的变化如图(b)
2
所示,这个SO (g)+ O (g) SO (g)反应是气体分子数减小的反应,压强
2 2 3
越大转化率越大,所以反应在5.0MPa、550℃时的α=0.975,由图象看出压强越大转化
率越高,温度越高转化率越小,转化率与影响平衡的因素:温度、压强还与投料比有关,
氧气越多SO 平衡转化率α越大;
2
故答案为:0.975;该反应是气体分子数减小的反应,压强越大转化率越大,P =
1
5.0MPa,该线550℃时的转化率为97.5%;压强、温度、投料比;
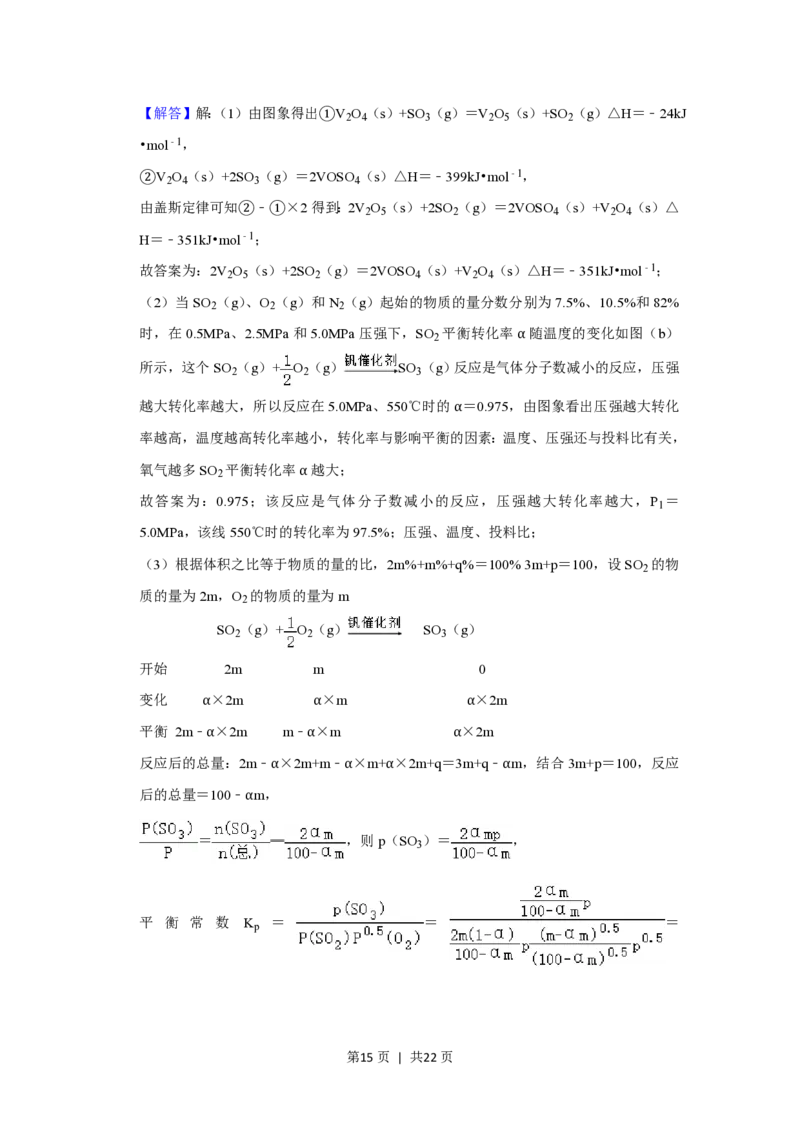
(3)根据体积之比等于物质的量的比,2m%+m%+q%=100% 3m+p=100,设SO 的物
2
质的量为2m,O 的物质的量为m
2
SO (g)+ O (g) SO (g)
2 2 3
开始 2m m 0
变化 α×2m α×m α×2m
平衡 2m﹣α×2m m﹣α×m α×2m
反应后的总量:2m﹣α×2m+m﹣α×m+α×2m+q=3m+q﹣αm,结合3m+p=100,反应
后的总量=100﹣αm,
= ═ ,则p(SO )= ,
3
平 衡 常 数 K = = =
p
第15页 | 共22页,
故答案为: ;= ;
(4)v=k( ﹣1)0.8(1﹣nα′)温度升高,表达式中速率常数k增大,反应速率
增大;SO (g)+ O (g) SO (g)△H=﹣98kJ•mol﹣1,为放热反应,平衡
2 2 3
转化率α减小,( ﹣1)0.8减小,反应速率减小,t<t 时,速率常数k增大,对速
m
率的影响大于因( ﹣1)0.8减小对速率的影响,总体速率加快;t>t 后速率常数k
m
增大没有α减小对速率影响大,速率减小。
故答案为:反应温度升高,速率常数k增大使速率加快,但α降低造成速率v减小。t<
t 时,k增大对v的提高大于α引起的降低;t>t 后,速率常数k增大小于α引起的降
m m
低。
【点评】本题考查了热化学方程式的书写,平衡转化率、压强平衡常数等知识点,情景
陌生,要好好利用图象,考查分析问题的能力,计算能力,难度较大。
(二)选考题:共15分。请考生从2道化学题中任选一题作答。如果多做,则按所做的第
一题计分。[化学--选修3:物质结构与性质](15分)
11.(15分)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的
卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为 4:5 。
(2)Li及其周期表中相邻元素的第一电离能(I )如表所示。I (Li)>I (Na),原因
1 1 1
是 Li与Na同族,Na电子层多,原子半径大,易失电子 。 I (Be)>I (B)>I
1 1 1
(Li),原因是 Li、Be、B同周期,核电荷数依次增加,Be的电子排布为:1s22s2,全
满稳定结构,第一电离能最大,与Li相比,B的核电荷数大,半径小,较难失去电子,
第一电离能较大。 。
I /(kJ•mol﹣1)
1
Li B
520 Be 801
900
第16页 | 共22页Na Al
496 Mg 578
738
(3)磷酸根离子的空间构型为 正四面体形 ,其中P的价层电子对数为 4 、杂化
轨道类型为 sp3 。
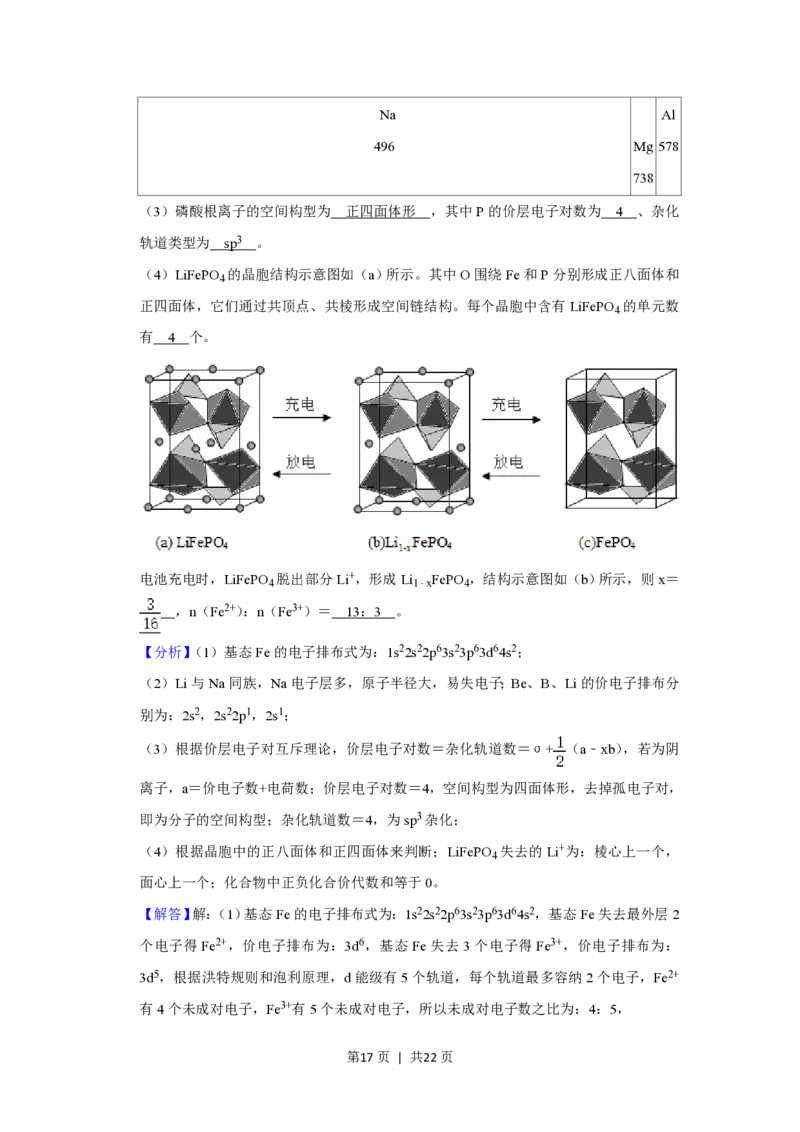
(4)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和
4
正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数
4
有 4 个。
电池充电时,LiFePO 脱出部分Li+,形成Li FePO ,结构示意图如(b)所示,则x=
4 1﹣x 4
,n(Fe2+):n(Fe3+)= 13:3 。
【分析】(1)基态Fe的电子排布式为:1s22s22p63s23p63d64s2;
(2)Li与Na同族,Na电子层多,原子半径大,易失电子;Be、B、Li的价电子排布分
别为:2s2,2s22p1,2s1;
(3)根据价层电子对互斥理论,价层电子对数=杂化轨道数=σ+ (a﹣xb),若为阴
离子,a=价电子数+电荷数;价层电子对数=4,空间构型为四面体形,去掉孤电子对,
即为分子的空间构型;杂化轨道数=4,为sp3杂化;
(4)根据晶胞中的正八面体和正四面体来判断;LiFePO 失去的Li+为:棱心上一个,
4
面心上一个;化合物中正负化合价代数和等于0。
【解答】解:(1)基态Fe的电子排布式为:1s22s22p63s23p63d64s2,基态Fe失去最外层2
个电子得 Fe2+,价电子排布为:3d6,基态 Fe 失去 3 个电子得 Fe3+,价电子排布为:
3d5,根据洪特规则和泡利原理,d能级有5个轨道,每个轨道最多容纳2个电子,Fe2+
有4个未成对电子,Fe3+有5个未成对电子,所以未成对电子数之比为:4:5,
第17页 | 共22页故答案为:4:5;
(2)Li与Na同族,Na电子层多,原子半径大,易失电子;Li、Be、B的电子排布分别
为:1s22s1,1s22s2,1s22s22p1,Li、Be、B同周期,核电荷数依次增加,Be的电子排布
为:1s22s2,全满稳定结构,第一电离能最大,与Li相比B的核电荷数大,半径小,较
难失去电子,第一电离能较大,
故答案为:Li与Na同族,Na电子层多,原子半径大,易失电子;Li、Be、B同周期,
核电荷数依次增加,Be的电子排布为:1s22s2,全满稳定结构,第一电离能最大,与Li
相比,B的核电荷数大,半径小,较难失去电子,第一电离能较大;
(3)根据价层电子对互斥理论,PO 3﹣离子的价层电子对数:4+ (5+3﹣4×2)=4+0=
4
4,VSEPR构型为:四面体形,去掉孤电子对数0,即为分子的立体构型,即正四面体形;
杂化轨道数=价层电子对数=4,中心原子P的杂化类型为:sp3杂化;
故答案为:正四面体形;4;sp3;
(4)根据晶胞中的正八面体和正四面体,可知晶体中含有4个单元LiFePO ;由图可知
4
圆球为Li+,LiFePO 失去的Li+为:棱心上一个,面心上一个;棱心上的为该晶胞的 ,
4
面心上为该晶胞的 ;因晶体中含有4个单元LiFePO ,所以x= × + × = ,
4
则1﹣x=1﹣ = ,所以化学式为Li FePO ,根据化合价代数和等于0,设Fe2+的
4
个数为x,Fe3+的的个数为y, +2x+3y+5=8,又因x+y=1,解得x= 、y= ,
所以个数比为13:3,
故答案为:4; ;13:3;
【点评】本题考查学生对原子结构和性质的理解和掌握,题目难度中等,掌握常见的基
态原子的电子排布、第一电离能、杂化方式、晶胞的计算等,明确原子杂化原理和晶胞
计算方法是解题关键。阅读题目获取新信息能力等,需要学生具备扎实的基础与综合运
用知识、信息分析解决问题能力。
[化学--选修5:有机化学基础](15分)
12.有机碱,例如二甲基胺( )、苯胺( )、吡啶( )等,在有机
合成中应用很普遍,目前“有机超强碱”的研究越来越受到关注。以下为有机超强碱F
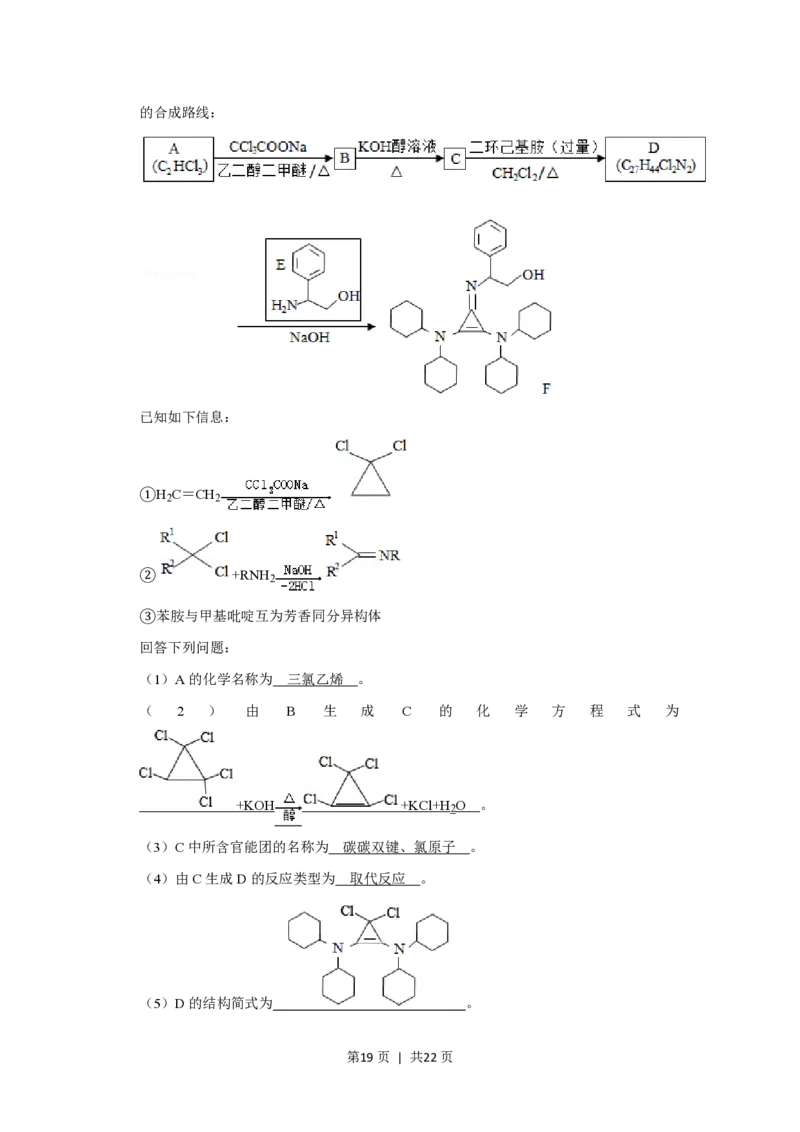
第18页 | 共22页的合成路线:
已知如下信息:
①H C=CH
2 2
② +RNH
2
③苯胺与甲基吡啶互为芳香同分异构体
回答下列问题:
(1)A的化学名称为 三氯乙烯 。
( 2 ) 由 B 生 成 C 的 化 学 方 程 式 为
+KOH +KCl+H O 。
2
(3)C中所含官能团的名称为 碳碳双键、氯原子 。
(4)由C生成D的反应类型为 取代反应 。
(5)D的结构简式为 。
第19页 | 共22页(6)E的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面
积之比为6:2:2:1的有 6 种,其中,芳香环上为二取代的结构简式为 。
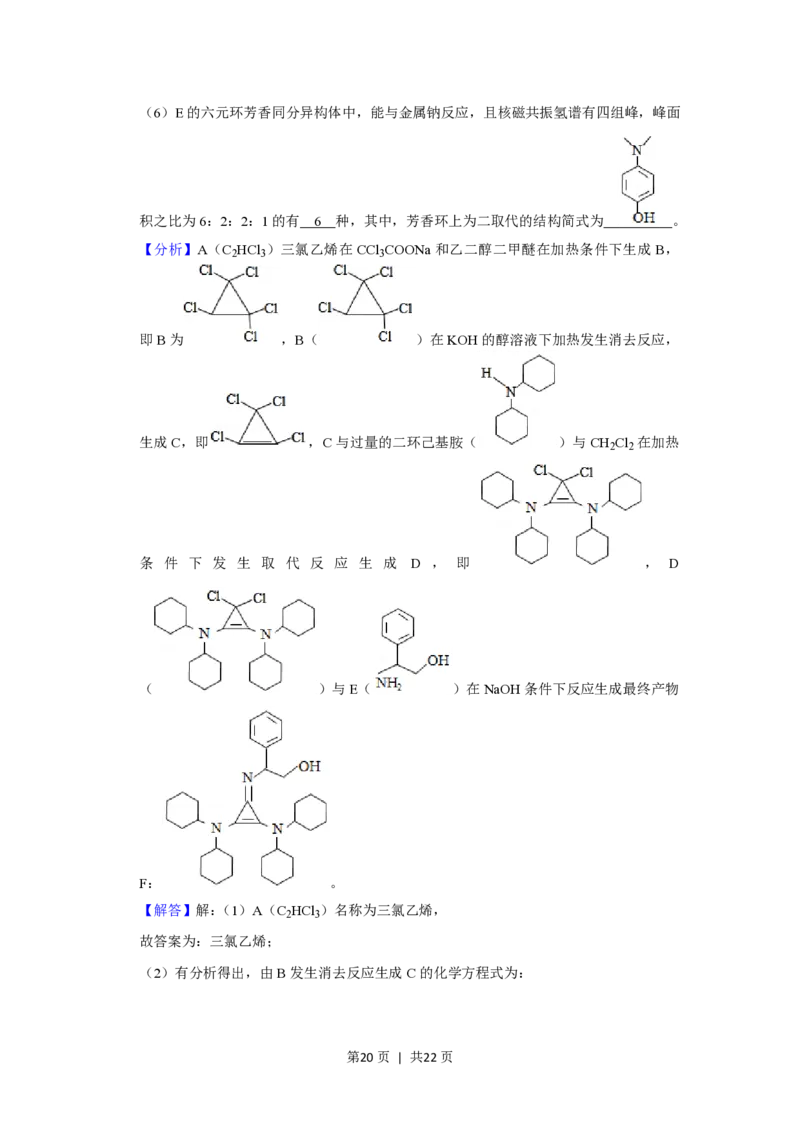
【分析】A(C HCl )三氯乙烯在CCl COONa和乙二醇二甲醚在加热条件下生成B,
2 3 3
即B为 ,B( )在KOH的醇溶液下加热发生消去反应,
生成C,即 ,C与过量的二环己基胺( )与CH Cl 在加热
2 2
条 件 下 发 生 取 代 反 应 生 成 D , 即 , D
( )与E( )在NaOH条件下反应生成最终产物
F: 。
【解答】解:(1)A(C HCl )名称为三氯乙烯,
2 3
故答案为:三氯乙烯;
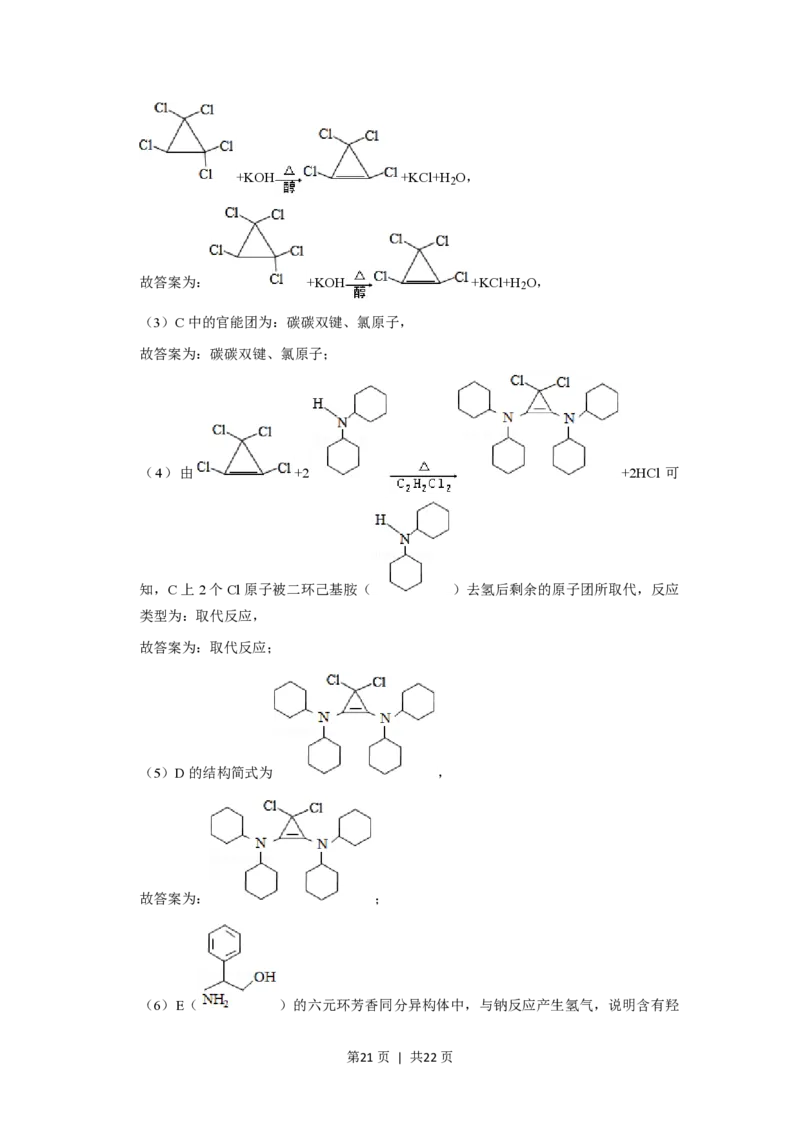
(2)有分析得出,由B发生消去反应生成C的化学方程式为:
第20页 | 共22页+KOH +KCl+H O,
2
故答案为: +KOH +KCl+H O,
2
(3)C中的官能团为:碳碳双键、氯原子,
故答案为:碳碳双键、氯原子;
(4)由 +2 +2HCl 可
知,C上2个Cl原子被二环己基胺( )去氢后剩余的原子团所取代,反应
类型为:取代反应,
故答案为:取代反应;
(5)D的结构简式为 ,
故答案为: ;
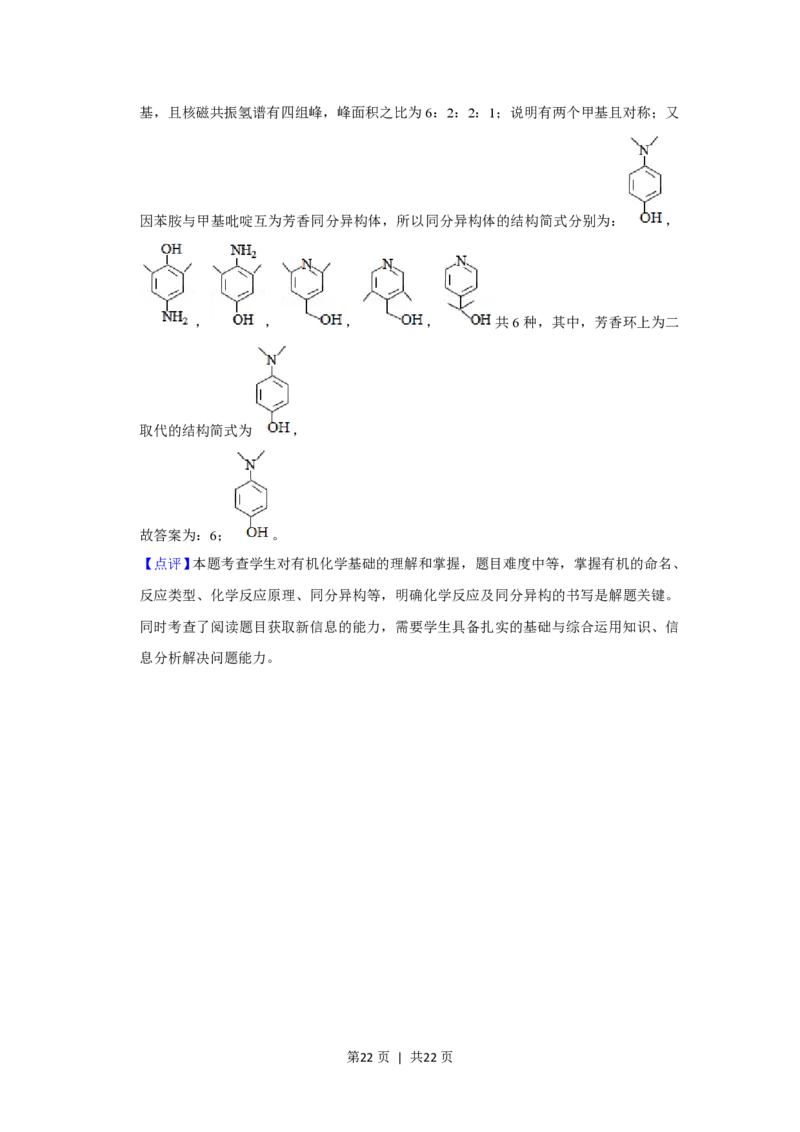
(6)E( )的六元环芳香同分异构体中,与钠反应产生氢气,说明含有羟
第21页 | 共22页基,且核磁共振氢谱有四组峰,峰面积之比为6:2:2:1;说明有两个甲基且对称;又
因苯胺与甲基吡啶互为芳香同分异构体,所以同分异构体的结构简式分别为: ,
, , , , 共6种,其中,芳香环上为二
取代的结构简式为 ,
故答案为:6; 。
【点评】本题考查学生对有机化学基础的理解和掌握,题目难度中等,掌握有机的命名、
反应类型、化学反应原理、同分异构等,明确化学反应及同分异构的书写是解题关键。
同时考查了阅读题目获取新信息的能力,需要学生具备扎实的基础与综合运用知识、信
息分析解决问题能力。
第22页 | 共22页