文档内容
2022 年普通高等学校招生全国统一考试(全国乙卷)
化学
1. 生活中处处有化学,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧
【答案】B
【解析】
【详解】A.铅笔芯的主要成分为石墨,不含二氧化铅,A错误;
B.碳酸氢钠不稳定,受热易分解产生二氧化碳,能使面团松软,可做食品膨松剂,B正确 ;
C.青铜是在纯铜(紫铜)中加入锡或铅的合金,黄铜为是由铜和锌所组成的合金,两者均属于混合物,不是
铜单质,C错误;
D.钠元素灼烧显黄色,D错误;
故选B。
2. 一种实现二氧化碳固定及再利用的反应如下:
下列叙述正确的是
A. 化合物1分子中的所有原子共平面 B. 化合物1与乙醇互为同系物
C. 化合物2分子中含有羟基和酯基 D. 化合物2可以发生开环聚合反应
【答案】D
【解析】
【详解】A.化合物1分子中还有亚甲基结构,其中心碳原子采用sp3杂化方式,所以所有原子不可能共平
面,A错误;
B.结构相似,分子上相差n个CH 的有机物互为同系物,上述化合物1为环氧乙烷,属于醚类,乙醇属
2
于醇类,与乙醇结构不相似,不是同系物,B错误;
C.根据上述化合物2的分子结构可知,分子中含酯基,不含羟基,C错误;
第1页 | 共20页D.化合物2分子可发生开环聚合形成高分子化合物 ,D正确;
答案选D。
3. 某白色粉末样品,可能含有Na SO 、Na SO 、Na S O 和Na CO 。取少量样品进行如下实验:
2 4 2 3 2 2 3 2 3
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是
A. Na SO 、Na S O B. Na SO、Na S O C. Na SO 、Na CO D. DNa SO、Na CO
2 4 2 2 3 2 3 2 2 3 2 4 2 53 2 3 2 3
【答案】A
【解析】
【详解】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向
①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在Na S O ,发生反应S O2-
2 2 3 2 3
+2H+=S↓+H O+SO ↑,离心分离,③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
2 2 2
BaSO ,说明固体中存在Na SO ,不能确定是否有Na SO 和Na CO ,Na SO 与过量盐酸反应生成二氧化
4 2 4 2 3 2 3 2 3
硫,Na CO 与过量盐酸反应生成二氧化碳,而这些现象可以被Na S O 与过量盐酸反应的现象覆盖掉,综
2 3 2 2 3
上分析,该样品中确定存在的是:Na SO 、Na S O ,
2 4 2 2 3
答案选A。
4. 由实验操作和现象,可得出相应正确结论的是
实验操作 现象 结论
氧化性:
向NaBr溶液中滴加过量氯水,再加入淀粉KI溶
A 先变橙色,后变蓝色
液 Cl >Br >I
2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制
B 无砖红色沉淀 蔗糖未发生水解
的Cu(OH) 悬浊液
2
第2页 | 共20页石蜡油加强热,将产生的气体通入Br 的CCl 溶
2 4
C 溶液红棕色变无色 气体中含有不饱和烃
液
试管口润湿的蓝色石蕊 氯乙烯加聚是可逆反
D 加热试管中的聚氯乙烯薄膜碎片
试纸变红 应
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.向NaBr溶液中滴加过量氯水,溴离子被氧化为溴单质,但氯水过量,再加入淀粉KI溶液,
过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错误;
B.向蔗糖溶液中滴加稀硫酸,水浴加热后,应加入氢氧化钠溶液使体系呈碱性,若不加氢氧化钠,未反
应的稀硫酸会和新制氢氧化铜反应,则不会产生砖红色沉淀,不能说明蔗糖没有发生水解,B错误;
C.石蜡油加强热,产生的气体能使溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,与溴发生加成反
应使溴的四氯化碳溶液褪色,C正确;
D.聚氯乙烯加强热产生能使湿润蓝色湿润试纸变红的气体,说明产生了氯化氢,不能说明氯乙烯加聚是
可逆反应,可逆反应是指在同一条件下,既能向正反应方向进行,同时又能向逆反应的方向进行的反应,
而氯乙烯加聚和聚氯乙烯加强热分解条件不同,D错误;
答案选C。
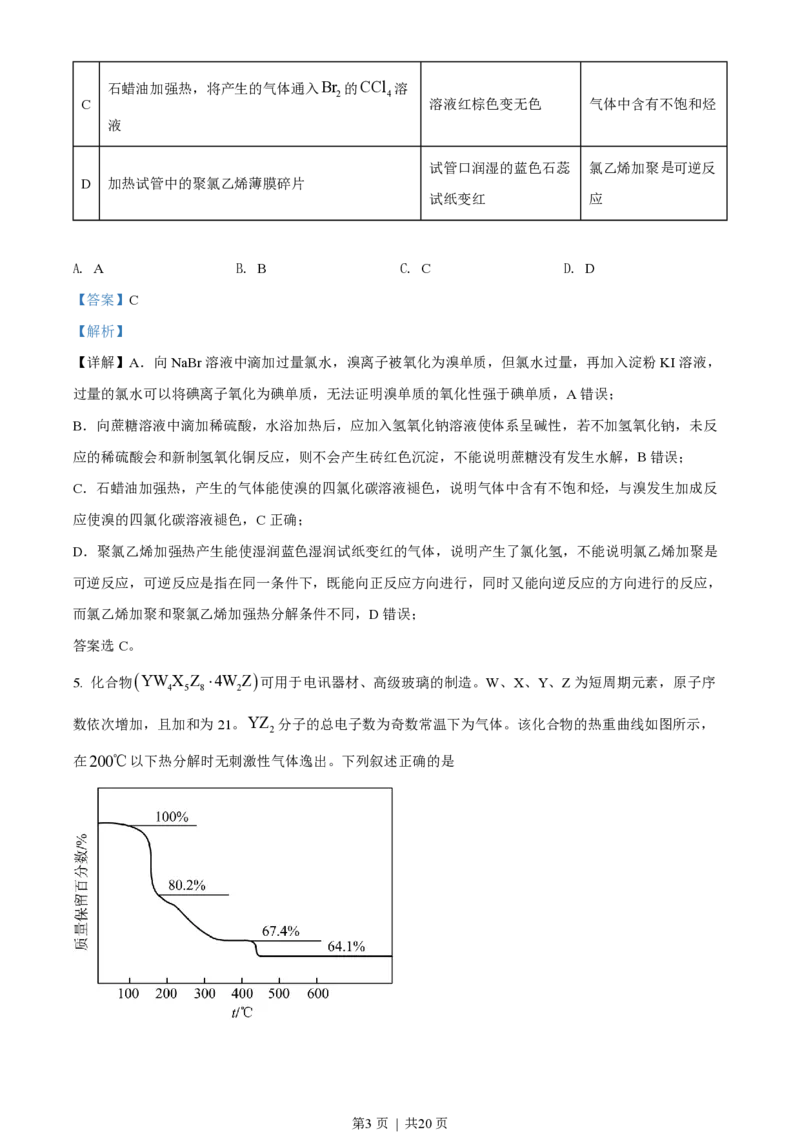
5. 化合物 YW X Z ×4W Z 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序
4 5 8 2
数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热重曲线如图所示,
2
在200℃以下热分解时无刺激性气体逸出。下列叙述正确的是
第3页 | 共20页A. W、X、Y、Z的单质常温下均为气体
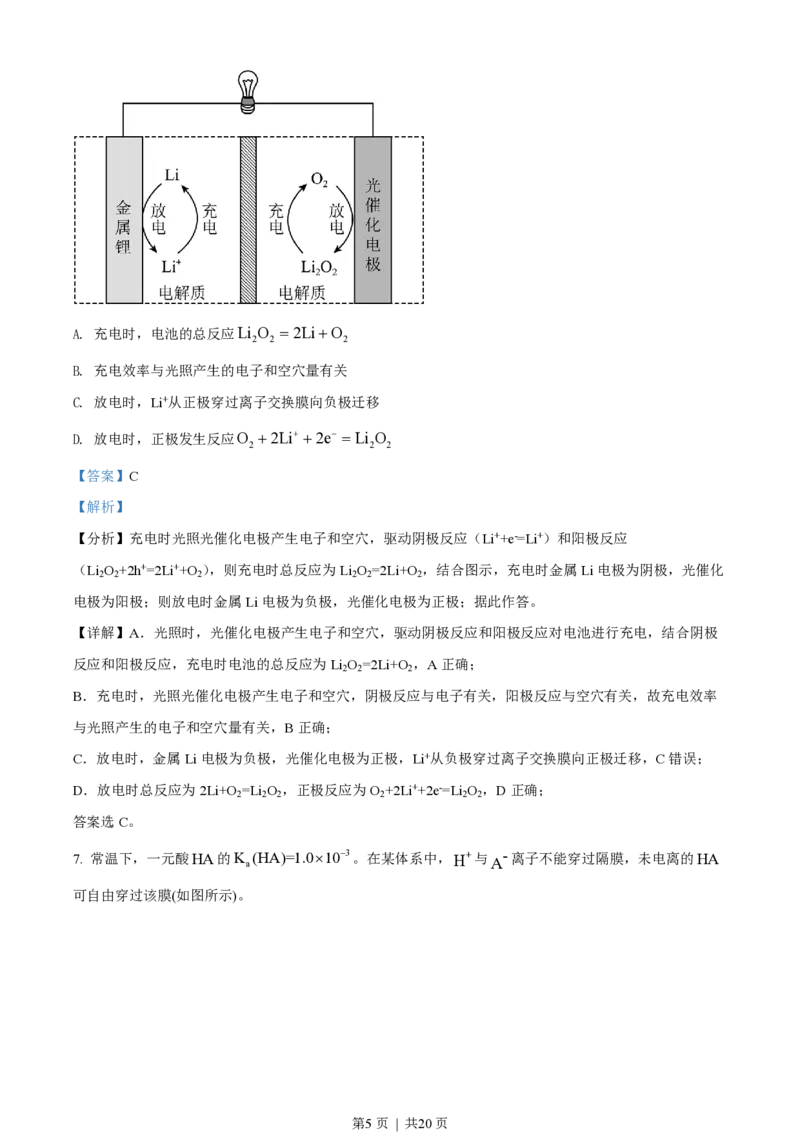
B. 最高价氧化物的水化物酸性:Y105,PbSO 可以比较彻底的转化为PbCO
3 4 c(CO2-) 4 3
3
c(SO2-)
(2)反应BaSO (s)+CO2-(aq)= BaCO (s)+SO2-(aq)的平衡常数K= 4 =0.04<<105,反应正向进行的程
4 3 3 4 c(CO2-)
3
度有限
(3) ①. Fe2+ ②. Pb+H O +2HAc=Pb(Ac) +2H O ③. 作还原剂
2 2 2 2
(4)Fe(OH) 、Al(OH)
3 3
(5)Ba2+、Na+
【解析】
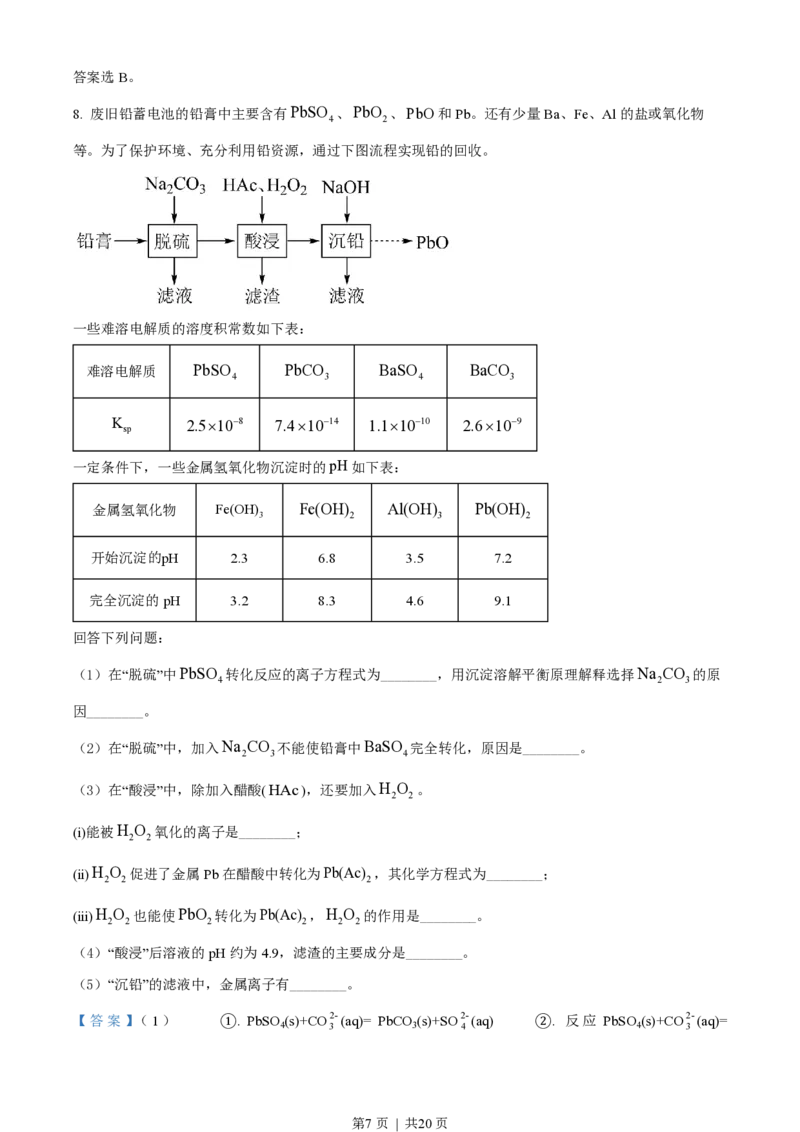
【分析】铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少量Ba、Fe、Al的盐或氧化物等,向铅膏中加
4 2
入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、过氧化氢进行酸浸,过氧
化氢可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可
知,滤渣主要成分为氢氧化铝、氢氧化铁,过滤后,向滤液中加入氢氧化钠溶液进行沉铅,得到氢氧化铅
沉淀,滤液中的金属阳离子主要为钠离子和钡离子,氢氧化铅再进行处理得到PbO。
【小问1详解】
“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO (s)+CO2-(aq)=
4 3
PbCO (s)+SO2-(aq),由一些难溶电解质的溶度积常数的数据可知,K (PbCO )=7.4´10-14,K (PbSO )=2.5
3 4 sp 3 sp 4
c(SO2-) c(Pb2+)×c(SO2-)
´10-8,反应PbSO (s)+CO2-(aq)= PbCO (s)+SO2-(aq)的平衡常数K= 4 = 4 =
4 3 3 4 c(CO2-) c(Pb2+)×c(CO2-)
3 3
K (PbSO ) 2.5´10-8
sp 4 = ≈3.4´105>105,说明可以转化的比较彻底,且转化后生成的碳酸铅可由酸浸进
K (PbCO ) 7.4´10-14
sp 3
入溶液中,减少铅的损失。
【小问2详解】
c(SO2-) c(Ba2+)×c(SO2-) K (BaSO )
反应BaSO (s)+CO2-(aq)= BaCO (s)+SO2-(aq)的平衡常数K= 4 = 4 = sp 4 =
4 3 3 4 c(CO2-) c(Ba2+)×c(CO2-) K (BaCO )
3 3 sp 3
1.1´10-10
≈0.04<<105,说明该反应正向进行的程度有限,因此加入碳酸钠不能使铅膏中的BaSO 完全转
4
2.6´10-9
化。
【小问3详解】
(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
第8页 | 共20页(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发生氧还原反应生成
2
Pb(Ac) 和H O,依据得失电子守恒和原子守恒可知,反应的化学方程式为:
2 2
Pb+H O +2HAc=Pb(Ac) +2H O。
2 2 2 2
(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,PbO 是氧化剂,则过
2 2 2
氧化氢是还原剂。
【小问4详解】
酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁。
【小问5详解】
依据分析可知,加入碳酸钠不能使铅膏中的BaSO 完全转化,铁离子、铝离子转化为了氢氧化铁、氢氧化
4
铝沉淀,铅转化为了氢氧化铅、最终变为了氧化铅,因此沉铅的滤液中,金属离子有Ba2+和加入碳酸钠、
氢氧化钠时引入的Na+。
9. 二草酸合铜(Ⅱ)酸钾(K [Cu(C O ) ])可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾
2 2 4 2
可采用如下步骤:
Ⅰ.取已知浓度的CuSO 溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,
4
过滤。
Ⅱ.向草酸(H C O )溶液中加入适量K CO 固体,制得KHC O 和K C O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分
析。
回答下列问题:
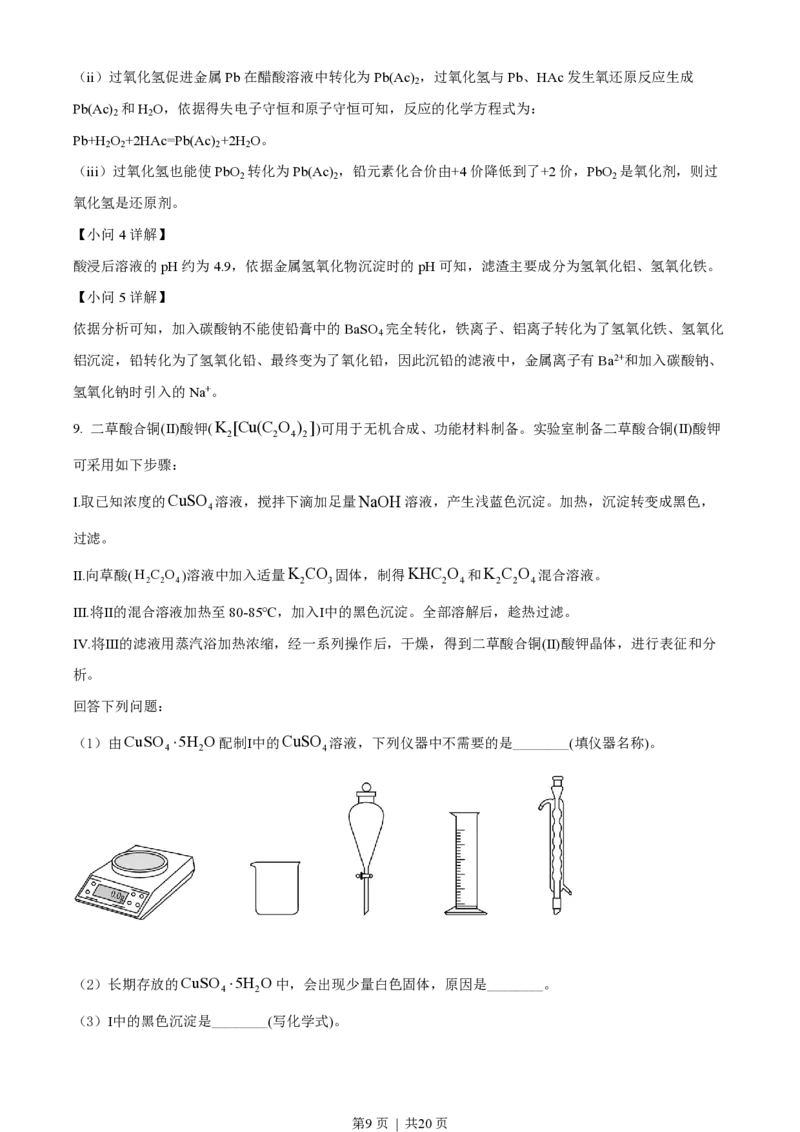
(1)由CuSO ×5H O配制Ⅰ中的CuSO 溶液,下列仪器中不需要的是________(填仪器名称)。
4 2 4
(2)长期存放的CuSO ×5H O中,会出现少量白色固体,原因是________。
4 2
(3)Ⅰ中的黑色沉淀是________(写化学式)。
第9页 | 共20页(4)Ⅱ中原料配比为n(H C O ):n(K CO )=1.5:1,写出反应的化学方程式________。
2 2 4 2 3
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入K CO 应采取________的方法。
2 3
(6)Ⅲ中应采用________进行加热。
(7)Ⅳ中“一系列操作”包括________。
【答案】(1)分液漏斗和球形冷凝管
(2)CuSO ×5H O风化失去结晶水生成无水硫酸铜
4 2
(3)CuO (4)3H C O +2K CO =2KHC O +K C O +2H O+2CO ↑
2 2 4 2 3 2 4 2 2 4 2 2
(5)分批加入并搅拌 (6)水浴
(7)冷却结晶、过滤、洗涤
【解析】
【分析】取已知浓度的CuSO 溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀氢氧化铜,加热,氢
4
氧化铜分解生成黑色的氧化铜沉淀,过滤,向草酸(H C O )溶液中加入适量K CO 固体,制得KHC O
2 2 4 2 3 2 4
和K C O 混合溶液,将KHC O 和K C O 混合溶液加热至80-85℃,加入氧化铜固体,全部溶解后,
2 2 4 2 4 2 2 4
趁热过滤,将滤液用蒸汽浴加热浓缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
【小问1详解】
由CuSO ×5H O固体配制硫酸铜溶液,需用天平称量一定质量的CuSO ×5H O固体,将称量好的固体
4 2 4 2
放入烧杯中,用量筒量取一定体积的水溶解CuSO ×5H O,因此用不到的仪器有分液漏斗和球形冷凝
4 2
管。
【小问2详解】
CuSO ×5H O含结晶水,长期放置会风化失去结晶水,生成无水硫酸铜,无水硫酸铜为白色固体。
4 2
【小问3详解】
硫酸铜溶液与氢氧化钠溶液反应生成蓝色的氢氧化铜沉淀,加热,氢氧化铜分解生成黑色的氧化铜沉淀。
【小问4详解】
草酸和碳酸钾以物质的量之比为1.5:1发生非氧化还原反应生成KHC O 、K C O 、CO 和水,依据原
2 4 2 2 4 2
子守恒可知,反应的化学方程式为:3H C O +2K CO =2KHC O +K C O +2H O+2CO ↑。
2 2 4 2 3 2 4 2 2 4 2 2
【小问5详解】
为防止草酸和碳酸钾反应时反应剧烈,造成液体喷溅,可减缓反应速率,将碳酸钾进行分批加入并搅拌。
第10页 | 共20页【小问6详解】
Ⅲ中将混合溶液加热至80-85℃,应采取水浴加热,使液体受热均匀。
【小问7详解】
从溶液获得晶体的一般方法为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,因此将Ⅲ的滤液用蒸汽浴加热浓
缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
10. 油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问
题:
(1)已知下列反应的热化学方程式:
①2H S(g)+3O (g)=2SO (g)+2H O(g) ΔH =-1036kJ×mol-1
2 2 2 2 1
②4H S(g)+2SO (g)=3S (g)+4H O(g) ΔH =94kJ×mol-1
2 2 2 2 2
③2H (g)+O (g)=2H O(g) ΔH =-484kJ×mol-1
2 2 2 3
计算H S热分解反应④2H S(g)=S (g)+2H (g)的ΔH =________kJ×mol-1。
2 2 2 2 4
(2)较普遍采用的H S处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反
2
应④高温热分解H S。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
2
(3)在1470K、100kPa反应条件下,将n(H S):n(Ar)=1:4的混合气进行H S热分解反应。平衡时混
2 2
合气中H S与H 的分压相等,H S平衡转化率为________,平衡常数K =________kPa。
2 2 2 p
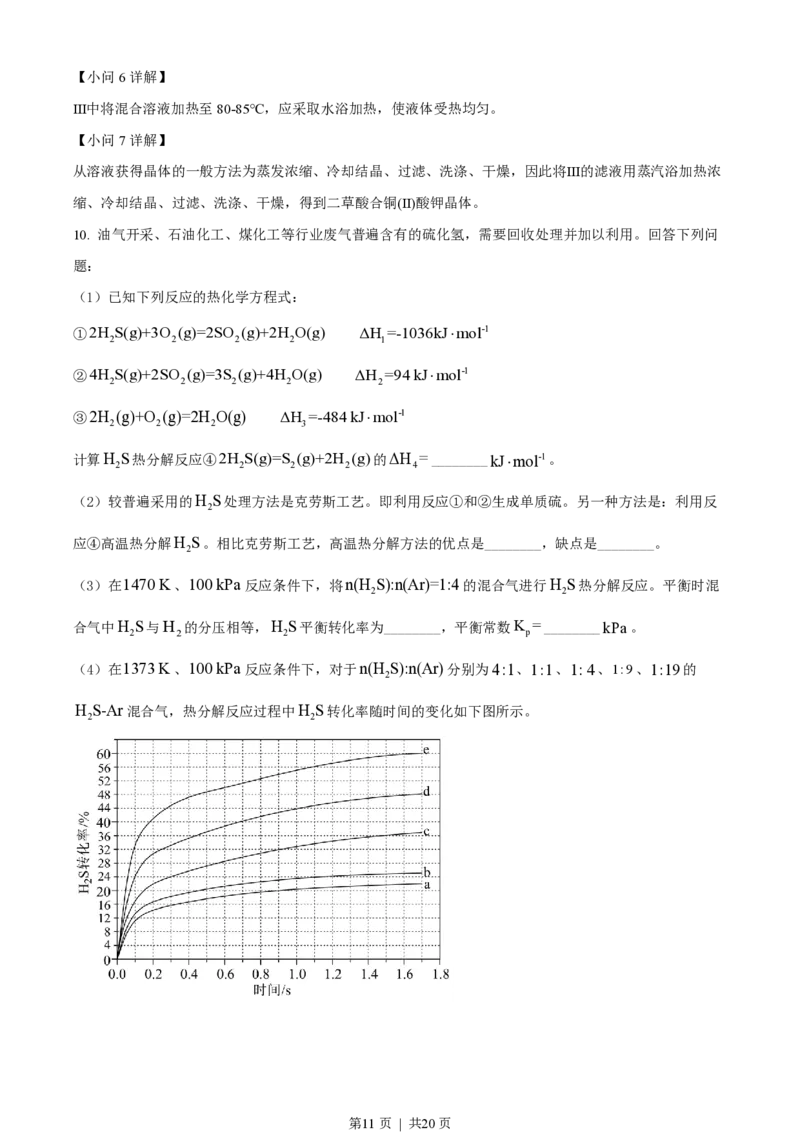
(4)在1373K、100kPa反应条件下,对于n(H S):n(Ar)分别为4:1、1:1、1:4、1:9、1:19的
2
H S-Ar混合气,热分解反应过程中H S转化率随时间的变化如下图所示。
2 2
第11页 | 共20页①n(H S):n(Ar)越小,H S平衡转化率________,理由是________。
2 2
②n(H S):n(Ar)=1:9对应图中曲线________,计算其在0-0.1s之间,H S分压的平均变化率为________
2 2
kPa×s-1。
【答案】(1)170 (2) ①. 副产物氢气可作燃料 ②. 耗能高
(3) ①. 50% ②. 4.76
(4) ①. 越高 ②. n(H S):n(Ar)越小,H S的分压越小,平衡向正反应方向进行,H S平衡转化
2 2 2
率越高 ③. d ④. 24.9
【解析】
【小问1详解】
已知:
①2H S(g)+3O (g)=2SO (g)+2H O(g) ΔH =-1036kJ/mol
2 2 2 2 1
②4H S(g)+2SO (g)=3S (g)+4H O(g) ΔH =94kJ/mol
2 2 2 2 2
③2H (g)+O (g)=2H O(g) ΔH =-484kJ/mol
2 2 2 3
1 1
根据盖斯定律(①+②)× -③即得到2H S(g)=S (g)+2H (g)的ΔH =(-1036+94)kJ/mol×
2 2 2 4
3 3
+484kJ/mol=170 kJ/mol;
【小问2详解】
1 1
根据盖斯定律(①+②)× 可得2H S(g)+O (g)=S (g)+2H O(g) ΔH=(-1036+94)kJ/mol× =-
2 2 2 2
3 3
314kJ/mol,因此,克劳斯工艺的总反应是放热反应;根据硫化氢分解的化学方程式可知,高温热分解方
法在生成单质硫的同时还有氢气生成。因此,高温热分解方法的优点是:可以获得氢气作燃料;但由于高
温分解H S会消耗大量能量,所以其缺点是耗能高;
2
【小问3详解】
假设在该条件下,硫化氢和氩的起始投料的物质的量分别为1mol和4mol,根据三段式可知:
2H S(g) S (g) + 2H (g)
2 ƒ 2 2
始/mol 1 0 0
变/mol x 0.5x x
平/mol 1-x 0.5x x
平衡时H S和H 的分压相等,则二者的物质的量相等,即1-x=x,解得x=0.5,所以H S的平衡转化
2 2 2
0.25 0.5
´100kPa´( ´100kPa)2
0.5 p(S )´ p2(H ) 5.25 5.25
率为 ´100%=50%,所以平衡常数K = 2 2 =
1 p p2(H S) 0.5
2 ( ´100kPa)2
5.25
第12页 | 共20页≈4.76kPa;
【小问4详解】
①由于正反应是体积增大的可逆反应,n(H S):n(Ar)越小,H S的分压越小,相当于降低压强,平衡向正
2 2
反应方向移动,因此H S平衡转化率越高;
2
②n(H S):n(Ar)越小,H S平衡转化率越高,所以n(H S):n(Ar)=1:9对应的曲线是d;根据图像可知
2 2 2
n(H S):n(Ar)=1:9反应进行到0.1s时H S转化率为0.24。假设在该条件下,硫化氢和氩的起始投料的
2 2
物质的量分别为1mol和9mol,则根据三段式可知
2H S(g) S (g) + 2H (g)
2 ƒ 2 2
始/mol 1 0 0
变/mol 0.24 0.12 0.24
平/mol 0.76 0.12 0.24
0.76
此时H S的压强为 ´100kPa≈7.51kPa,H S的起始压强为10kPa,所以H S分压
2 2 2
0.76+0.12+0.24+9
10kPa-7.51kPa
的平均变化率为 =24.9kPa·s-1。
0.1s
【化学—选修 3:物质结构与性质】
11. 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12ps d.1s22s22p33p2
(2)①一氯乙烯 C H Cl 分子中,C的一个_______杂化轨道与Cl的3p 轨道形成C-Cl_______键,并
2 3 x
且Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键
P4
。
x x 3
②一氯乙烷 C H Cl 、一氯乙烯 C H Cl 、一氯乙炔 C HCl 分子中,C-Cl键长的顺序是_______,
2 5 2 3 2
理由:(ⅰ)C的杂化轨道中s成分越多,形成的C-Cl键越强:(ⅱ)_______。
(3)卤化物CsICl 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X
2
的熔点比Y高的原因_______。
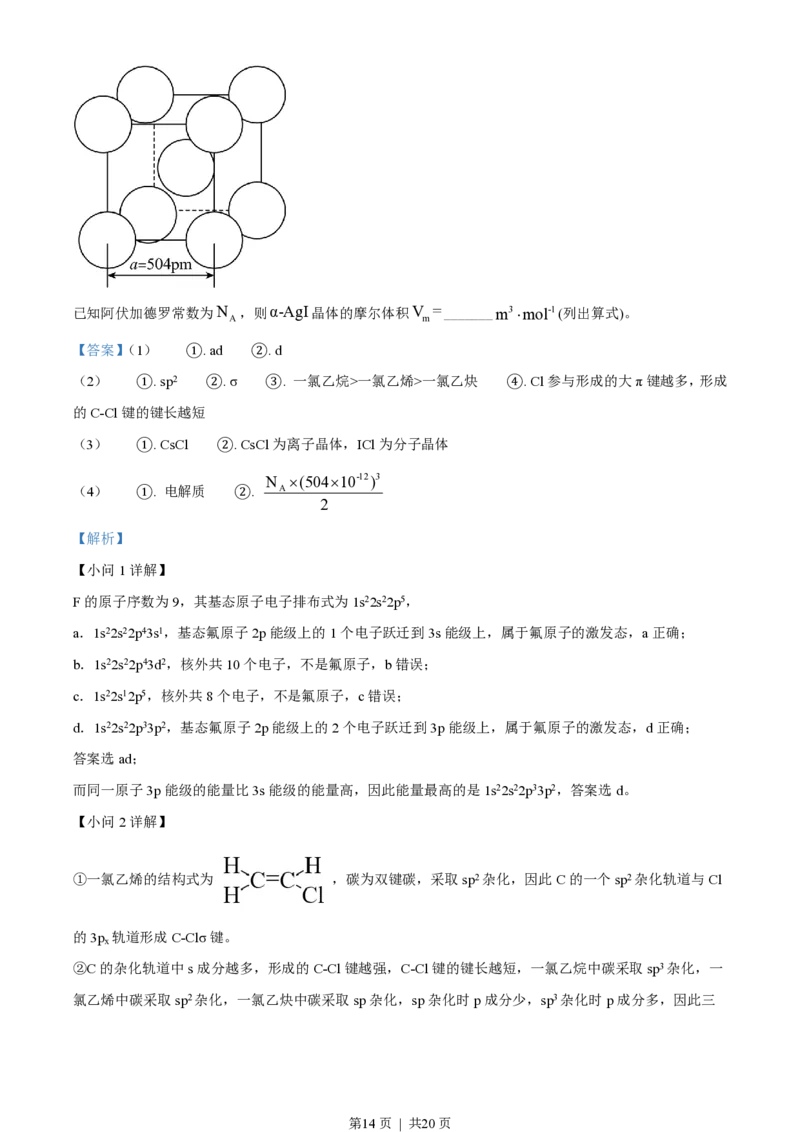
(4)α-AgI晶体中I-离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、八面体等空
隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在电池中可作为
_______。
第13页 | 共20页已知阿伏加德罗常数为N ,则α-AgI晶体的摩尔体积V =_______m3×mol-1(列出算式)。
A m
【答案】(1) ①. ad ②. d
(2) ①. sp2 ②. σ ③. 一氯乙烷>一氯乙烯>一氯乙炔 ④. Cl参与形成的大π键越多,形成
的C-Cl键的键长越短
(3) ①. CsCl ②. CsCl为离子晶体,ICl为分子晶体
N ´(504´10-12)3
(4) ①. 电解质 ②. A
2
【解析】
【小问1详解】
F的原子序数为9,其基态原子电子排布式为1s22s22p5,
a.1s22s22p43s1,基态氟原子2p能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;
b.1s22s22p43d2,核外共10个电子,不是氟原子,b错误;
c.1s22s12p5,核外共8个电子,不是氟原子,c错误;
d.1s22s22p33p2,基态氟原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,d正确;
答案选ad;
而同一原子3p能级的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,答案选d。
【小问2详解】
①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl
的3p 轨道形成C-Clσ键。
x
②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取sp3杂化,一
氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化时p成分少,sp3杂化时p成分多,因此三
第14页 | 共20页种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C-
Cl键的键长越短,一氯乙烯中Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键(Π4 ),一氯乙炔
x x 3
中Cl的3p 轨道与C的2p 轨道形成2套3中心4电子的大π键(Π4 ),因此三种物质中C-Cl键键长顺序
x x 3
为:一氯乙烷>一氯乙烯>一氯乙炔。
【小问3详解】
CsICl 发生非氧化还原反应,各元素化合价不变,生成无色晶体和红棕色液体,则无色晶体为CsCl,红棕
2
色液体为ICl,而CsCl为离子晶体,熔化时,克服的是离子键,ICl为分子晶体,熔化时,克服的是分子
间作用力,因此CsCl的熔点比ICl高。
【小问4详解】
由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良的离子导
1
体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8´ +1=2个,依据化学式AgI可知,银离子
8
N 2
个数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504´10-12)3m3,则α-AgI晶体
N N
A A
(504´10-12)3m3
V N ´(504´10-12)3
的摩尔体积V = = 2 = A m3/mol。
m n mol 2
N
A
[化学-选修5:有机化学基础]
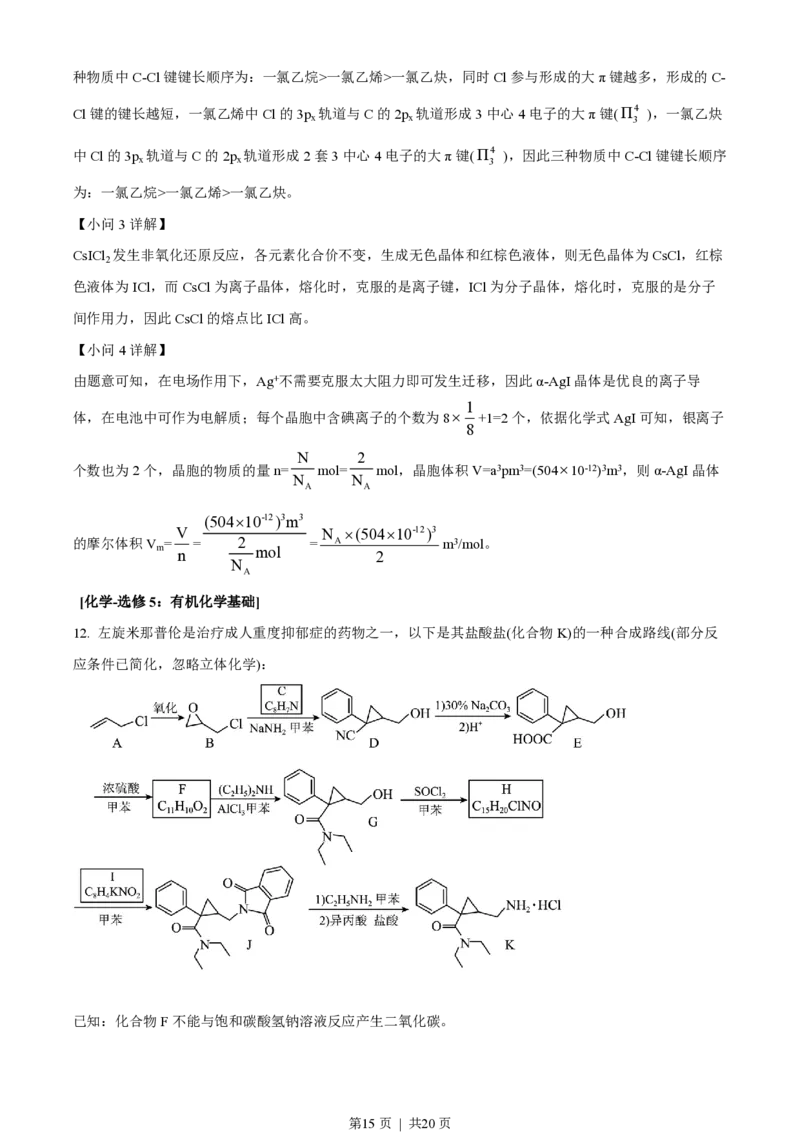
12. 左旋米那普伦是治疗成人重度抑郁症的药物之一,以下是其盐酸盐(化合物K)的一种合成路线(部分反
应条件已简化,忽略立体化学):
已知:化合物F不能与饱和碳酸氢钠溶液反应产生二氧化碳。
第15页 | 共20页回答下列问题:
(1)A的化学名称是_______。
(2)C的结构简式为_______。
(3)写出由E生成F反应的化学方程式_______。
(4)E中含氧官能团的名称为_______。
(5)由G生成H的反应类型为_______。
(6)I是一种有机物形成的盐,结构简式为_______。
(7)在E的同分异构体中,同时满足下列条件的总数为_______种。
a)含有一个苯环和三个甲基;
b)与饱和碳酸氢钠溶液反应产生二氧化碳;
c)能发生银镜反应,不能发生水解反应。
上述同分异构体经银镜反应后酸化,所得产物中,核磁共振氢谱显示有四组氢(氢原子数量比为6:3:2:
1)的结构简式为_______。
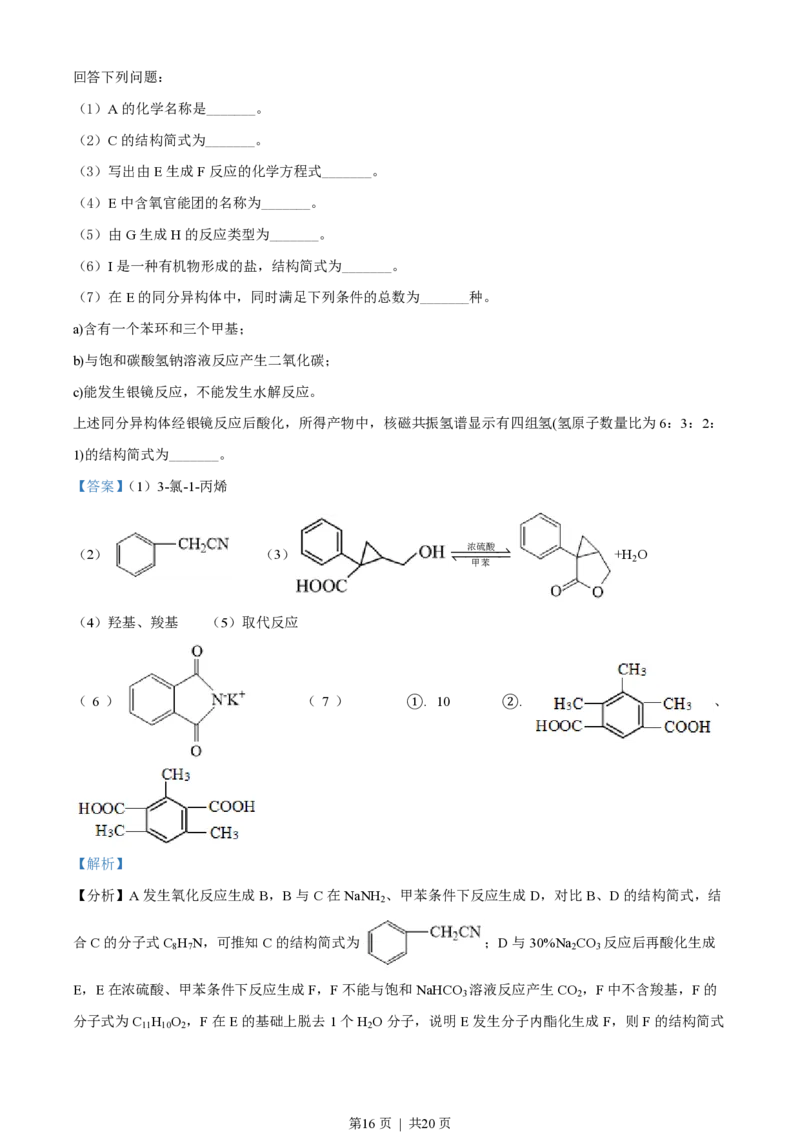
【答案】(1)3-氯-1-丙烯
浓硫酸
(2) (3) ˆˆˆˆ† +H O
‡ˆ甲ˆ苯ˆˆ 2
(4)羟基、羧基 (5)取代反应
( 6 ) ( 7 ) ①. 10 ②. 、
【解析】
【分析】A发生氧化反应生成B,B与C在NaNH 、甲苯条件下反应生成D,对比B、D的结构简式,结
2
合C的分子式C H N,可推知C的结构简式为 ;D与30%Na CO 反应后再酸化生成
8 7 2 3
E,E在浓硫酸、甲苯条件下反应生成F,F不能与饱和NaHCO 溶液反应产生CO ,F中不含羧基,F的
3 2
分子式为C H O ,F在E的基础上脱去1个H O分子,说明E发生分子内酯化生成F,则F的结构简式
11 10 2 2
第16页 | 共20页为 ;F与(C H ) NH在AlCl 、甲苯条件下反应生成G,G与SOCl 、甲苯反应生成H,H
2 5 2 3 2
的分子式为C H ClNO,H与I反应生成J,结合G、J的结构简式知,H的结构简式为
15 20
;I的分子式为C H KNO ,I是一种有机物形成的盐,则I的结构简式为
8 4 2
;据此作答。
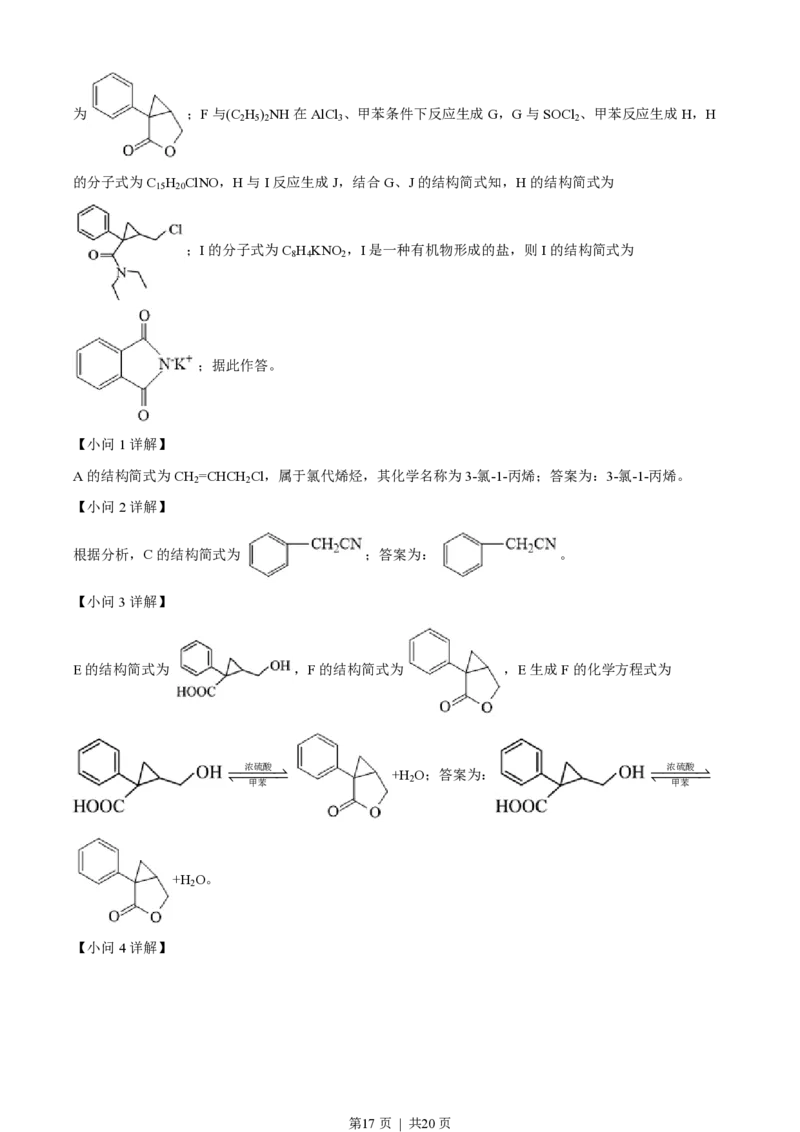
【小问1详解】
A的结构简式为CH =CHCH Cl,属于氯代烯烃,其化学名称为3-氯-1-丙烯;答案为:3-氯-1-丙烯。
2 2
【小问2详解】
根据分析,C的结构简式为 ;答案为: 。
【小问3详解】
E的结构简式为 ,F的结构简式为 ,E生成F的化学方程式为
浓硫酸 浓硫酸
ˆˆˆˆ† +H O;答案为: ˆˆˆˆ†
‡ˆ甲ˆ苯ˆˆ 2 ‡ˆ甲ˆ苯ˆˆ
+H O。
2
【小问4详解】
第17页 | 共20页E的结构简式为 ,其中含氧官能团的名称为(醇)羟基、羧基;答案为:羟基、羧
基。
【小问5详解】
G的结构简式为 ,H的结构简式为 ,G与SOCl 发生取代反应生成
2
H;答案为:取代反应。
【小问6详解】
根据分析,I的结构简式为 ;答案为: 。
【小问7详解】
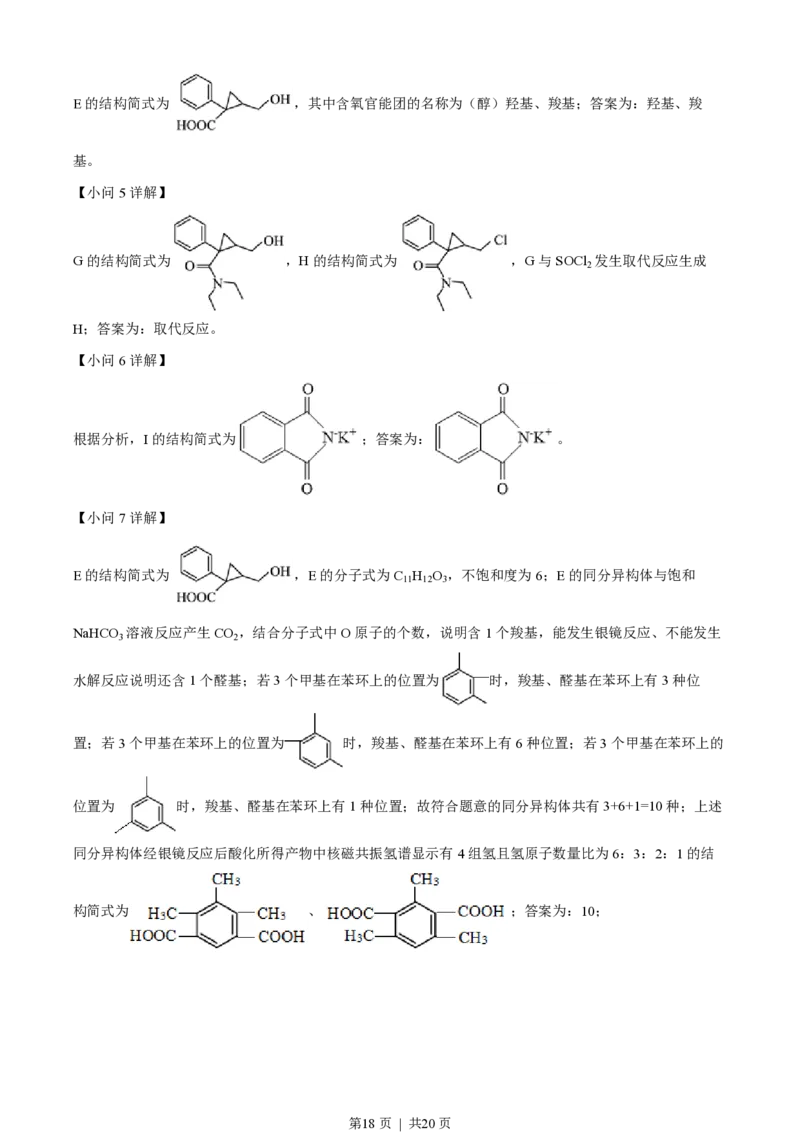
E的结构简式为 ,E的分子式为C H O ,不饱和度为6;E的同分异构体与饱和
11 12 3
NaHCO 溶液反应产生CO ,结合分子式中O原子的个数,说明含1个羧基,能发生银镜反应、不能发生
3 2
水解反应说明还含1个醛基;若3个甲基在苯环上的位置为 时,羧基、醛基在苯环上有3种位
置;若3个甲基在苯环上的位置为 时,羧基、醛基在苯环上有6种位置;若3个甲基在苯环上的
位置为 时,羧基、醛基在苯环上有1种位置;故符合题意的同分异构体共有3+6+1=10种;上述
同分异构体经银镜反应后酸化所得产物中核磁共振氢谱显示有4组氢且氢原子数量比为6:3:2:1的结
构简式为 、 ;答案为:10;
第18页 | 共20页、 。
第19页 | 共20页第20页 | 共20页