从无法建模到精准修复:线粒体碱基编辑器动物模型的新进展



线粒体疾病由线粒体DNA(mtDNA)突变引发,是基础医学与临床转化领域长期悬而未决的难题,这些突变可累及全身多个器官(如图1),导致Leber遗传性视神经病变(LHON)、 Leigh综合征、感音神经性耳聋等严重疾病。根据MITOMAP的统计,目前已验证的线粒体致病性突变有97个,其中点突变占比高达95%。然而,由于缺乏有效的点突变相关线粒体疾病小鼠模型由于缺乏有效的动物模型,尤其是携带同质性致病突变的模型,该领域的治疗策略开发长期处于瓶颈期。近年来,随着线粒体碱基编辑器(mitoBEs)的突破性发展,特别是DdCBE(CtoT)、TALED(AtoG)及新一代mitoBEs v2的问世,研究者已成功在多种动物模型中实现致病突变的精准引入与体内原位修复,标志着线粒体疾病研究正从“无法建模”迈向“精准治愈”的崭新阶段。
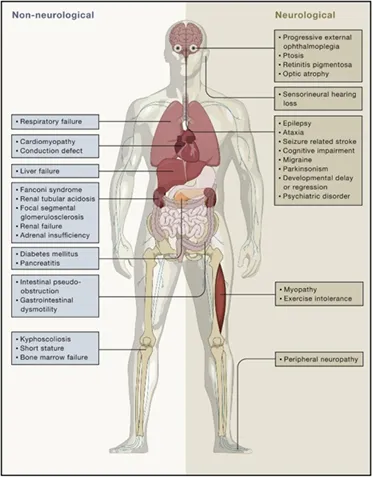
图1 线粒体疾病的受累组织器官
一、线粒体疾病动物模型构建的技术基础:碱基编辑器研究进展
2020年开发的DddA衍生胞嘧啶碱基编辑器(DdCBE)首次在无需产生双链断裂的情况下实现了mtDNA的C•G→T•A精准编辑。随后,2022年开发的TALE连接脱氨酶(TALED)补齐了A•T→G•C编辑的能力,理论上可靶向约86%的致病mtDNA点突变。然而,早期编辑器胚胎毒性高、脱靶效应广,直接应用于动物模型构建时频发胚胎发育停滞。2025年初,二代碱基编辑器问世,通过筛选低脱靶脱氨酶(TadA8e-V106W-V28F使RNA脱靶降至背景水平;CBE6d使mtDNA脱靶接近背景),同时优化胞嘧啶脱氨酶和腺嘌呤脱氨酶(通过改变脱氨酶的活性口袋结构,使其对底物的识别更加严格,从而大幅降低了其在RNA水平上的乱编辑现象)并以环状RNA形式递送(将碱基编辑器的序列头尾连接成环,这种环状结构相比线性mRNA,没有容易被降解的末端,因此在细胞内的半衰期更长,表达更持久且稳定)。这种策略使得线粒体碱基编辑效率提升至82%,且在全基因组范围未检测到脱靶效应。具体思路如下:首先利用AlphaFold2预测了TadA8e-V106W(原始编辑器中的关键脱氨酶)与RNA相互作用的3D结构。通过比对,锁定了6个可能与RNA结合有关的氨基酸残基:Arg21、Glu27、Val28、Val82、Trp106、Arg107,随后对这6个位点分别进行饱和突变(将每个氨基酸替换为其他19种氨基酸),生成大量TadA8e-V106W的突变体变体,将这些突变体构建成编辑器,转染到HEK293T细胞中,检测它们对目标DNA位点(MT-RNR2)的编辑效率,最后通过DNA靶向编辑效率和脱靶率的双重筛选,发现了V28F突变。这一突破使得构建“遗传背景干净”的疾病模型成为现实(如图2)。同时期,另有团队专注于腺嘌呤脱氨酶(TadA-8e)优化,提升A→G编辑效率,在不影响蛋白质基本折叠的前提下,对TadA-8e的关键氨基酸位点进行随机突变,创造出一个包含成千上万个变体的“编辑器库”,随后将这些变体放入哺乳动物细胞中,观察它们能否高效地将线粒体DNA中的A(腺嘌呤)变为G(鸟嘌呤),经过多轮筛选,最终分离出名为eTd-mtABE的突变体。特别是其中包含的RW/V28A等关键突变,极大地优化了酶与底物结合时的能量状态,使其催化效率指数级提升。通过定向进化TadA-8e,该团队开发出了超高效线粒体腺嘌呤碱基编辑器(eTd-mtABEs),在大鼠细胞中编辑效率提升达145倍,为后续高效建模奠定了工具基础。
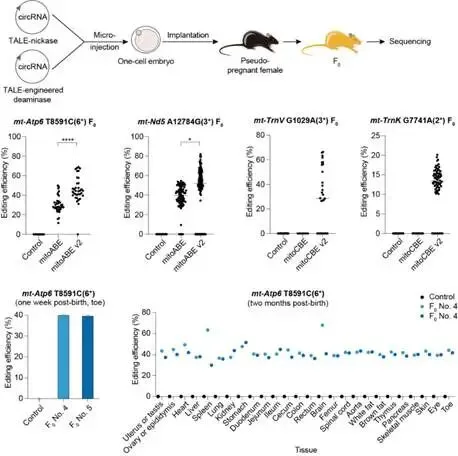
图2 mitoBEs v2实现高效线粒体疾病小鼠模型建立并且编辑结果广泛持久存在于各个组织
二、依托碱基编辑器的线粒体疾病动物模型研究进展
早期的线粒体疾病动物模型主要通过化学诱导或遗传工程构建,但这些方法操作复杂、成本高昂且对突变的精准控制较差,仅成功建立了极少数模型,如Ndufs4敲除小鼠(Leigh综合征模型)和Mfn2 T105M敲入小鼠(CMT2A神经病变模型)。Ndufs4基因编码线粒体复合物I的一个18kD亚基,其突变在人类中可导致Leigh综合征。利用CRISPR/Cas9技术建立的Ndufs4敲除小鼠,表现出与Leigh综合征患者相似的物理和行为表型。Mfn2基因编码线粒体融合蛋白Mitofusin 2,其突变是导致Charcot-Marie-Tooth病2A型(CMT2A)的主要原因。利用CRISPR/Cas9技术构建的Mfn2 Thr105Met(T105M)敲入小鼠,可以成功模拟CMT2A的临床特征。但是这些模型模拟的是“核基因突变导致的线粒体疾病”,而临床上绝大多数(约95%)线粒体疾病是由“线粒体DNA(mtDNA)点突变”引起的。
线粒体点突变动物模型的严重缺乏推动了第一代线粒体碱基编辑器技术的发展——DdCBEs和TALEDs的问世。研究者尝试将这些工具应用于小鼠模型的构建(将编码DdCBE的核酸注射到小鼠、大鼠和斑马鱼的胚胎中,或通过腺相关病毒(AAV) 递送到小鼠有丝分裂后组织中),但其编辑效率尚不足以模拟人类线粒体疾病中高突变负荷的特征。此外,DdCBEs还可能引发大量核基因组脱靶效应。(非TALE依赖性脱靶,主要源于DddA蛋白的自组装以及其与CTCF的相互作用)。
线粒体碱基编辑工具的诞生与初步应用虽然不尽完美,但是引发了科研工作者追求探索拥有低脱靶率,高编辑效率的更完美碱基编辑工具的浪潮,而更加完善的碱基编辑工具又推动了线粒体点突变动物模型的快速发展。前文所述的mitoBEs v2(二代线粒体碱基编辑器)成功构建了70种模拟人类致病突变的小鼠模型,在小鼠中的编辑效率最高可达82%,且未检测到核基因组脱靶。其中最关键的是mt-Atp6 T8591C(Leigh综合征模型)和mt-Nd5 A12784G(LHON模型)。关于Leigh综合征模型,应用一代碱基编辑器通过向小鼠胚胎注射DdCBE mRNA来建模,获得的F0代小鼠在目标位点的编辑效率通常只有5%到10% 左右,极少能超过20%。这样的低比例突变远低于线粒体疾病的致病阈值——人类Leigh综合征患者通常需要携带超过80%到90% 的突变mtDNA才会表现出明显症状。使用优化的mitoBEs v2系统和环状RNA递送策略,在F1代小鼠中实现了多个组织接近100% 的同质性突变。这些携带mt-Atp6 T8591C突变的小鼠出现了心率显著下降(人类Leigh综合征患者的核心病理特征之一:脑干受损导致心肺功能障碍),这是首次在动物模型中证明,一个mtDNA点突变能够直接导致可量化、可观测的致死性表型。关于LHON模型,线粒体疾病的母系遗传规律虽然早已在临床上确认,但在动物模型中从未被系统验证过,而第一代碱基编辑器构建的模型的突变负荷太低,在传代过程中往往因遗传漂变而丢失,无法建立稳定的遗传品系。mt-Nd5 A12784G首次在活体动物中完美复现了LHON的组织特异性(图3),验证了母系遗传的可操作性。而前文所述的二代碱基编辑器eTd-mtABEs,可以获得大鼠F0代高负荷Leigh综合征模型。注射eTd-mtABEs mRNA后,F0代大鼠的平均突变效率已达到54%,可以直接用于表型分析,无需多代筛选,建立了稳定的遗传品系,将整个建模周期从近一年缩短至两到三个月。同时,该二代编辑器的开发团队从这些患病大鼠体内分离细胞,筛选了60种DdCBE工程化变体,找到编辑窗口最窄、效率最高的变体,最后将该变体的mRNA注射回患病大鼠的受精卵中,53%的致病突变被成功恢复为野生型序列,完成了全球首例在活体动物中实现mtDNA致病突变原位纠正并逆转疾病表型的工作。
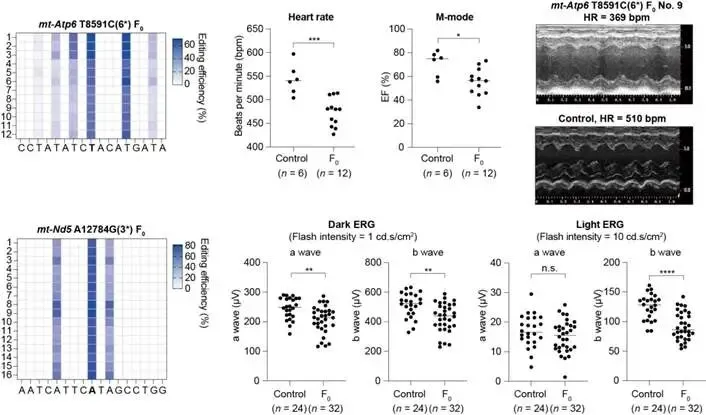
图3 mt-Nd5 A12784G小鼠表现出类似LHON的视力障碍
从DdCBE到TALED,再到2025年的二代碱基编辑器,线粒体基因编辑工具在短短几年内实现了效率和脱靶控制的双重突破。依托这些工具,研究人员已成功建立了几十种携带致病mtDNA点突变的动物模型,首次在活体动物中复现了Leigh综合征、LHON等疾病的典型表型,并实现了突变位点的原位修复。这些进展打破了长期困扰线粒体疾病研究的模型瓶颈,为后续治疗策略的开发提供了真正可用的工具和平台。
参考文献:
1.Stewart, J.B., Current progress with mammalian models of mitochondrial DNA disease. Journal of Inherited Metabolic Disease, 2021. 44(2).
2.Silva-Pinheiro, P., et al., A library of base editors for the precise ablation of all protein-coding genes in the mouse mitochondrial genome. Nature Biomedical Engineering, 2023. 7(5).
3.Zhang, X., Ren, J. et al. Precise modelling of mitochondrial diseases using optimized mitoBEs. Nature (2025).
4.Cho, S.I., et al., Targeted A-to-G base editing in human mitochondrial DNA with programmable deaminases. Cell, 2022. 185(10).
5.Mok, B.Y., et al., A bacterial cytidine deaminase toxin enables CRISPR-free mitochondrial base editing. Nature, 2020. 583(7817).

智能微生物载体
Stay Hungry, Stay Foolish


 夜雨聆风
夜雨聆风




