文档内容
专练 15 金属及其化合物的制备流程
授课提示:对应学生用书29页
一、选择题
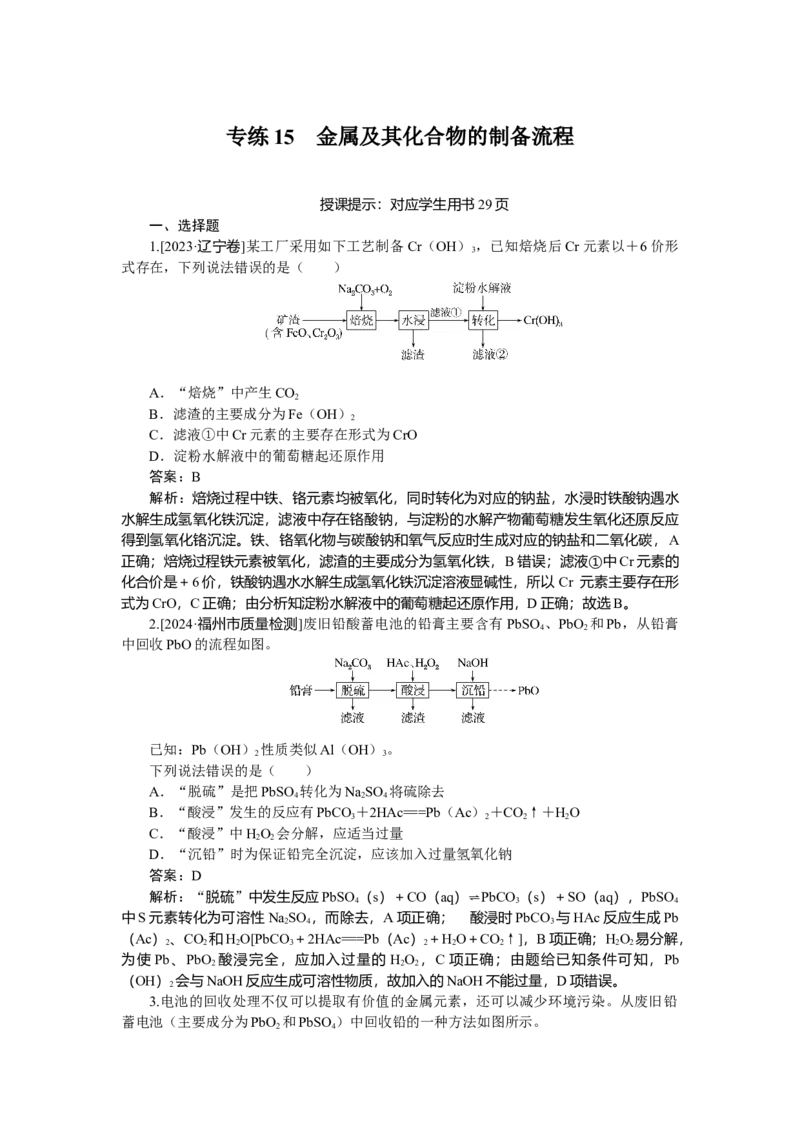
1.[2023·辽宁卷]某工厂采用如下工艺制备Cr(OH) ,已知焙烧后Cr元素以+6价形
3
式存在,下列说法错误的是( )
A.“焙烧”中产生CO
2
B.滤渣的主要成分为Fe(OH)
2
C.滤液①中Cr元素的主要存在形式为CrO
D.淀粉水解液中的葡萄糖起还原作用
答案:B
解析:焙烧过程中铁、铬元素均被氧化,同时转化为对应的钠盐,水浸时铁酸钠遇水
水解生成氢氧化铁沉淀,滤液中存在铬酸钠,与淀粉的水解产物葡萄糖发生氧化还原反应
得到氢氧化铬沉淀。铁、铬氧化物与碳酸钠和氧气反应时生成对应的钠盐和二氧化碳,A
正确;焙烧过程铁元素被氧化,滤渣的主要成分为氢氧化铁,B错误;滤液①中Cr元素的
化合价是+6价,铁酸钠遇水水解生成氢氧化铁沉淀溶液显碱性,所以 Cr 元素主要存在形
式为CrO,C正确;由分析知淀粉水解液中的葡萄糖起还原作用,D正确;故选B。
2.[2024·福州市质量检测]废旧铅酸蓄电池的铅膏主要含有 PbSO 、PbO 和Pb,从铅膏
4 2
中回收PbO的流程如图。
已知:Pb(OH) 性质类似Al(OH)。
2 3
下列说法错误的是( )
A.“脱硫”是把PbSO 转化为NaSO 将硫除去
4 2 4
B.“酸浸”发生的反应有PbCO +2HAc===Pb(Ac)+CO↑+HO
3 2 2 2
C.“酸浸”中HO 会分解,应适当过量
2 2
D.“沉铅”时为保证铅完全沉淀,应该加入过量氢氧化钠
答案:D
解析:“脱硫”中发生反应PbSO
4
(s)+CO(aq)⇌PbCO
3
(s)+SO(aq),PbSO
4
中S元素转化为可溶性NaSO ,而除去,A项正确; 酸浸时PbCO 与HAc反应生成Pb
2 4 3
(Ac)、CO 和HO[PbCO +2HAc===Pb(Ac)+HO+CO↑],B项正确;HO 易分解,
2 2 2 3 2 2 2 2 2
为使 Pb、PbO 酸浸完全,应加入过量的 HO ,C 项正确;由题给已知条件可知,Pb
2 2 2
(OH) 会与NaOH反应生成可溶性物质,故加入的NaOH不能过量,D项错误。
2
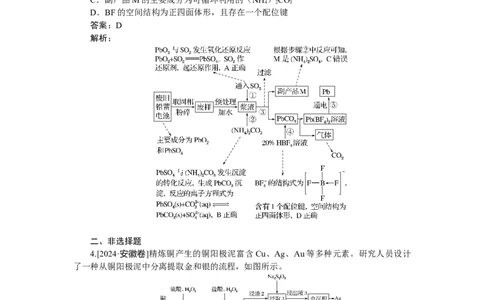
3.电池的回收处理不仅可以提取有价值的金属元素,还可以减少环境污染。从废旧铅
蓄电池(主要成分为PbO 和PbSO )中回收铅的一种方法如图所示。
2 4下列说法错误的是( )
A.步骤①中通入的二氧化硫起还原作用
B.步骤②中发生反应的离子方程式为 PbSO
4
(s)+CO(aq) ⇌PbCO
3
(s)+SO
(aq)
C.副产品M的主要成分为可循环利用的(NH )CO
4 2 3
D.BF的空间结构为正四面体形,且存在一个配位键
答案:D
解析:
二、非选择题
4.[2024·安徽卷]精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计
了一种从铜阳极泥中分离提取金和银的流程,如图所示。
回答下列问题:
(1)Cu位于元素周期表第 周期第 族。
(2)“浸出液1”中含有的金属离子主要是 。
(3)“浸取2”步骤中,单质金转化为HAuCl 的化学方程式为
4
________________________________________________________________________
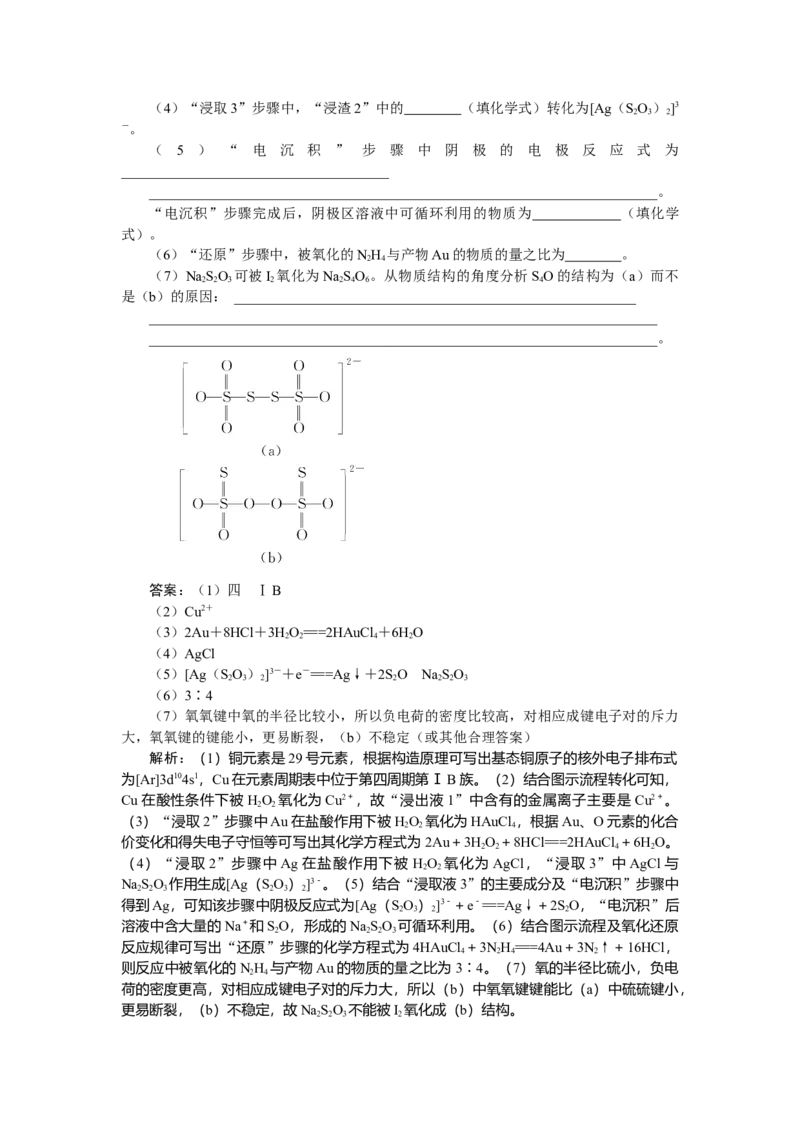
________________________________________________________________________。(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为[Ag(SO ) ]3
2 3 2
-。
( 5 ) “ 电 沉 积 ” 步 骤 中 阴 极 的 电 极 反 应 式 为
______________________________________
________________________________________________________________________。
“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为 (填化学
式)。
(6)“还原”步骤中,被氧化的NH 与产物Au的物质的量之比为 。
2 4
(7)NaSO 可被I 氧化为NaSO 。从物质结构的角度分析SO的结构为(a)而不
2 2 3 2 2 4 6 4
是(b)的原因: _________________________________________________________
________________________________________________________________________
________________________________________________________________________。
答案:(1)四 ⅠB
(2)Cu2+
(3)2Au+8HCl+3HO===2HAuCl +6HO
2 2 4 2
(4)AgCl
(5)[Ag(SO)]3-+e-===Ag↓+2SO NaSO
2 3 2 2 2 2 3
(6)3∶4
(7)氧氧键中氧的半径比较小,所以负电荷的密度比较高,对相应成键电子对的斥力
大,氧氧键的键能小,更易断裂,(b)不稳定(或其他合理答案)
解析:(1)铜元素是29号元素,根据构造原理可写出基态铜原子的核外电子排布式
为[Ar]3d104s1,Cu在元素周期表中位于第四周期第ⅠB族。(2)结合图示流程转化可知,
Cu在酸性条件下被HO 氧化为Cu2+,故“浸出液1”中含有的金属离子主要是Cu2+。
2 2
(3)“浸取2”步骤中Au在盐酸作用下被HO 氧化为HAuCl ,根据Au、O元素的化合
2 2 4
价变化和得失电子守恒等可写出其化学方程式为2Au+3HO +8HCl===2HAuCl +6HO。
2 2 4 2
(4)“浸取 2”步骤中 Ag 在盐酸作用下被 HO 氧化为 AgCl,“浸取 3”中 AgCl 与
2 2
NaSO 作用生成[Ag(SO)]3-。(5)结合“浸取液3”的主要成分及“电沉积”步骤中
2 2 3 2 3 2
得到Ag,可知该步骤中阴极反应式为[Ag(SO ) ]3-+e-===Ag↓+2SO,“电沉积”后
2 3 2 2
溶液中含大量的Na+和SO,形成的NaSO 可循环利用。(6)结合图示流程及氧化还原
2 2 2 3
反应规律可写出“还原”步骤的化学方程式为4HAuCl +3NH===4Au+3N↑+16HCl,
4 2 4 2
则反应中被氧化的NH 与产物Au的物质的量之比为3∶4。(7)氧的半径比硫小,负电
2 4
荷的密度更高,对相应成键电子对的斥力大,所以(b)中氧氧键键能比(a)中硫硫键小,
更易断裂,(b)不稳定,故NaSO 不能被I 氧化成(b)结构。
2 2 3 25.[2022·辽宁卷]某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)与软锰
2 3 2 2
矿(主要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
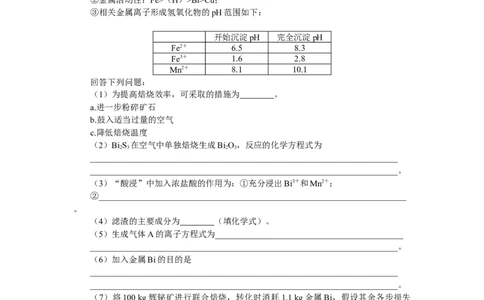
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为 。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2)BiS 在空气中单独焙烧生成BiO,反应的化学方程式为
2 3 2 3
________________________________________________________________________
________________________________________________________________________。
(3)“酸浸”中加入浓盐酸的作用为:①充分浸出Bi3+和Mn2+;
②________________________________________________________________________
。
(4)滤渣的主要成分为 (填化学式)。
(5)生成气体A的离子方程式为____________________________________________
________________________________________________________________________。
(6)加入金属Bi的目的是
________________________________________________________________________
________________________________________________________________________。
(7)将100 kg辉铋矿进行联合焙烧,转化时消耗1.1 kg金属Bi,假设其余各步损失
不计,干燥后称量BiOCl产品质量为32 kg,滴定测得产品中Bi的质量分数为78.5%。辉
铋矿中Bi元素的质量分数为 。
答案:(1)ab
(2)2BiS+9O=====2BiO+6SO
2 3 2 2 3 2
(3)抑制金属离子水解 (4)SiO
2
(5)MnO+6H++2Cl-===2Mn2++Cl↑+3HO
2 3 2 2
(6)将Fe3+转化为Fe2+
(7)24.02%
解析:(1)a项,联合焙烧时,进一步粉碎矿石,可以增大矿石与空气的接触面积,
能够提高焙烧效率;b项,鼓入适当过量的空气有利于矿石充分反应;c项,降低焙烧温度,反应速率减慢,不利于提高焙烧效率;
(2)BiS 在空气中单独焙烧生成BiO ,根据原子守恒可知还应生成SO ,结合得失
2 3 2 3 2
电子守恒,反应的化学方程式为2BiS +9O=====2BiO +6SO ;(3)加入浓盐酸后,溶
2 3 2 2 3 2
液中含有的离子主要为Bi3+、Fe3+、Mn2+、H+、Cl-,而酸浸后取滤液进行转化,故要防
止金属离子水解生成沉淀,进入滤渣,造成制得的BiOCl产率偏低;(4)滤渣主要为不溶
于浓盐酸的SiO ;(5)因MnO 有氧化性,会与浓盐酸发生氧化还原反应:MnO +6H+
2 2 3 2 3
+2Cl-===2Mn2++Cl↑+3HO;(6)由已知信息③知,调pH=2.6时,Fe3+会水解生成
2 2
Fe(OH) 沉淀,但Fe2+还没开始沉淀,故要将Fe3+转化为Fe2+,在调pH后获得含FeCl
3 2
的滤液,为了不引入新的杂质,加入Bi作还原剂。
(7)根据题目信息可知,32 kg BiOCl产品中Bi元素的质量为32 kg×78.5%=25.12
kg,转化时消耗1.1 kg金属Bi,根据Bi元素守恒可知,100 kg辉铋矿中Bi的质量分数为
×100%=24.02%。
6.草酸亚铁晶体(FeC O·2H O)是一种浅黄色固体,难溶于水,受热易分解,是生产
2 4 2
锂电池的原材料,也常用作分析试剂及显影剂等,其制备流程如下:
(1)配制硫酸亚铁铵[(NH )Fe(SO )]溶液时,需加少量硫酸,目的是
4 2 4 2
________________________________________________________________________。
(2)加热到沸腾时发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)向盛有草酸亚铁晶体的试管中滴入硫酸酸化的 KMnO 溶液,振荡,溶液变为棕
4
黄色,同时有气体生成。已知反应中MnO转化为无色的Mn2+,则该过程中被氧化的元素
是 ,若反应中消耗1 mol FeC O·2H O,则参加反应的n(KMnO )= 。
2 4 2 4
(4)称取3.80 g草酸亚铁晶体(FeC O·2H O相对分子质量是180)用热重法对其进
2 4 2
行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
①过程Ⅰ发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
②300 ℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式或
名称(请写出计算过程)。
答案:(1)抑制Fe2+水解
(2)(NH )Fe(SO )+HC O+2HO===FeC O·2H O↓+HSO +(NH )SO
4 2 4 2 2 2 4 2 2 4 2 2 4 4 2 4
(3)碳和铁 0.6(4)①FeC O·2H O=====FeC O+2HO ②Fe O
2 4 2 2 4 2 2 3
解析:(1)配制(NH )Fe(SO ) 溶液时,溶液中亚铁离子水解显酸性,加少量硫
4 2 4 2
酸的目的是抑制其水解。
(2)硫酸亚铁铵溶液中加入草酸生成草酸亚铁沉淀、硫酸和硫酸铵,反应的化学方程
式为:(NH )Fe(SO )+HC O+2HO===FeC O·2H O↓+HSO +(NH )SO 。
4 2 4 2 2 2 4 2 2 4 2 2 4 4 2 4
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的 KMnO 溶液,振荡,发现溶
4
液颜色逐渐变为棕黄色,并检测到CO 生成,说明草酸亚铁被氧化为铁离子、二氧化碳气
2
体,说明铁元素和碳元素被氧化,根据离子方程式 5FeC O +3MnO+24H+===5Fe3++
2 4
3Mn2++10CO↑+12HO可知,消耗 1 mol FeC O·2H O,则参加反应的 KMnO 为0.6
2 2 2 4 2 4
mol;
(4)①通过剩余固体的质量可知,过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶
水,反应的化学方程式为:
FeC O·2H O=====FeC O+2HO;
2 4 2 2 4 2
②3.6 g草酸亚铁晶体中的铁元素质量为:3.6 g×=1.12 g,草酸亚铁晶体中的铁元素
完全转化到氧化物中,氧化物中氧元素的质量为:1.60 g-1.12 g=0.48 g,铁元素和氧元素
的物质的量之比为:2∶3,铁的氧化物的化学式为Fe O。
2 3