文档内容
专练 47 难溶电解质的沉淀溶解平衡原理及应用
授课提示:对应学生用书93页
1.[2024·湖北卷]CO 气氛下,Pb(ClO) 溶液中含铅物种的分布如图。纵坐标(δ)为组分
2 4 2
中铅占总铅的质量分数。已知 c(Pb2+)=2.0×10-5 mol·L-1,pK (H CO)=6.4、
0 a1 2 3
pK (H CO)=10.3,pK (PbCO )=12.1。下列说法错误的是( )
a2 2 3 sp 3
A.pH=6.5时,溶液中c(CO)75%,c(Pb2+)=c(Pb2+)·δ(Pb2+)>1.5×10-5
0
mol·L-1,此时体系中还没有PbCO (s),则K (PbCO )≥c(Pb2+)·c(CO),c(CO)≤< mol·L-1
3 sp 3
=×10-7.1 mol·L-1<1.5×10-5 mol·L-1=c(Pb2+),A正确;δ(Pb2+)=δ(PbCO )时,体系中还
3
存在Pb(OH)+,因此δ(Pb2+)=δ(PbCO )<50%,则c(Pb2+)=c(Pb2+)·δ(Pb2+)<1.0×10-5
3 0
mol·L-1,B正确;体系的初始状态为Pb(ClO) 溶液和CO 气氛,由于ClO不水解,根据
4 2 2
c(Pb2+)=2.0×10-5 mol·L-1可知c(ClO)=4.0×10-5 mol·L-1,读图可知,pH=7时,δ(Pb2
0
+)<50%,δ[Pb(OH)+]<25%,则c(Pb2+)=c(Pb2+)·δ(Pb2+)<2.0×10-5 mol·L-1×50%=
0
1.0×10-5 mol·L-1,c[Pb(OH)+]=c(Pb2+)·δ[Pb(OH)+]<2.0×10-5 mol·L-1×25%=5.0×10
0
-6 mol·L-1,则 2c(Pb2+)+c[Pb(OH)+]<2×1.0×10-5 mol·L-1+5.0×10-6 mol·L-1=
2.5×10-5 mol·L-1<4.0×10-5 mol·L-1=c(ClO)<2c(CO)+c(HCO)+c(ClO),C正确;pH
=8时,含Pb物种主要以PbCO (s)形式存在,溶解PbCO 有两种方式:将其转化为Pb2+或
3 3
Pb(CO
3
),即使PbCO 3⇌Pb2++CO正向移动,或使PbCO
3
+CO⇌Pb(CO
3
)正向移动,则需要
补充CO,若由HCO电离提供CO,同时电离出的H+会降低溶液pH,与Pb(CO )存在时需
3
要较高的pH矛盾,故D错误。
2.[2024·吉林卷]25 ℃下,AgCl、AgBr和Ag CrO 的沉淀溶解平衡曲线如图所示。某
2 4
实验小组以KCrO 为指示剂,用AgNO 标准溶液分别滴定含Cl-水样、含Br-水样。
2 4 3
已知:①Ag CrO 为砖红色沉淀;
2 4
②相同条件下AgCl溶解度大于AgBr;
③25 ℃时,pK (H CrO)=0.7,pK (H CrO)=6.5。
a1 2 4 a2 2 4下列说法错误的是( )
A.曲线②为AgCl沉淀溶解平衡曲线
B.反应Ag
2
CrO
4
+H+ ⇌2Ag++HCrO的平衡常数K=10-5.2
C.滴定Cl-时,理论上混合液中指示剂浓度不宜超过10-2.0 mol·L-1
D.滴定Br-达终点时,溶液中=10-0.5
答案:D
解析:
AgCl、AgBr的阴、阳离子个数比相同,则曲线的斜
率相同,结合已知②溶解度:AgCl>AgBr,可确定③
表示AgBr,②表示AgCl,则①表示Ag CrO。
2 4
结合(6.1,6.1)可计算出K (AgBr)=10-6.1×10-6.1=10
sp
-12.2,由(2.0,7.7)可计算出K (Ag CrO)=(10-
sp 2 4
2.0)2×10-7.7=10-11.7,K (AgCl)=10-2.0×10-7.7=10-
sp
9.7。
由以上分析可知,曲线②表示AgCl沉淀溶解平衡曲线,A正确;该反应的平衡常数K
=====10-5.2,B正确;Cl-沉淀完全时,CrO才能开始沉淀,当离子浓度小于10-5
mol·L-1时可视为沉淀完全,当 Cl-沉淀完全时,溶液中 c(Ag+)=10-4.7 mol·L-1,由
K (Ag CrO)=10-11.7可知,生成Ag CrO 沉淀时c(CrO)= mol·L-1=10-0.3×10-2.0 mol·L-
sp 2 4 2 4
1<10-2.0 mol·L-1,故滴定Cl-时,理论上混合液中指示剂浓度不宜超过 10-2.0 mol·L-1,C
正确;滴定Br-达终点时,溶液中同时存在AgBr、Ag CrO 沉淀,则溶液中==10-0.5c(Ag
2 4
+),D错误。
3.[2023·全国乙卷]一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是( )
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO),K (AgCl)=K (Ag CrO)
sp sp 2 4
C.Ag
2
CrO
4
+2Cl- ⇌2AgCl+CrO的平衡常数K=107.9D.向NaCl、NaCrO 均为0.1 mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO
2 4 3 2 4
沉淀
答案:C
解析:根据图像,由(1.7,5)可得到Ag CrO 的溶度积K (Ag CrO)=c2(Ag+)·c(CrO)=
2 4 sp 2 4
(1×10-5)2×1×10-1.7=10-11.7。由(4.8,5)可得到AgCl的溶度积K (AgCl)=c(Ag+)·c(Cl-)
sp
=1×10-5×1×10-4.8=10-9.8,据此数据计算各选项结果。
假设 a 点坐标为(4,6.5),此时分别计算反应的浓度熵 Q 得,Q(AgCl)=10-10.5,
Q(Ag CrO)=10-17,二者的浓度熵均小于其对应的溶度积K ,二者不会生成沉淀,A错误;
2 4 sp
K 为难溶物的溶度积,是一种平衡常数,平衡常数只与温度有关,与浓度无关,根据分析
sp
可知,二者的溶度积不相同,B错误;该反应的平衡常数表达式为K=,将表达式转化为
与两种难溶物的溶度积有关的式子得 K=====1×107.9,C正确;向NaCl、NaCrO 均
2 4
为0.1 mol·L-1的混合溶液中滴加AgNO ,开始沉淀时所需要的c(Ag+)分别为10-8.8和10-
3
5.35,说明此时沉淀Cl-需要的银离子浓度更低,在这种情况下,先沉淀的是AgCl,D错误;
故答案选C。
4.[2024·全国甲卷]将 0.10 mmol Ag CrO 配制成 1.0 mL 悬浊液,向其中滴加 0.10
2 4
mol·L-1的NaCl溶液。lg[c /(mol·L-1)](M代表Ag+、Cl-或CrO)随加入NaCl溶液体积(V)
M
的变化关系如图所示。
下列叙述正确的是( )
A.交点a处:c(Na+)=2c(Cl-)
B.=10-2.21
C.V≤2.0 mL时不变
D.y=-7.82,y=-lg 34
1 2
答案:D
解析:Ag CrO 转化为AgCl需消耗2.0 mL NaCl溶液,结合题图知,交点 a处c(Na
2 4
+)≈ mol·L-1,c(Cl-)≈ mol·L-1,因此c(Na+)≠2c(Cl-),A错误;V(NaCl)=1.0 mL时,
溶液中存在 Ag CrO 沉淀,因此溶液中满足 K (Ag CrO)=c2(Ag+)·c(CrO),即
2 4 sp 2 4
lg[K (Ag CrO)]=2lg[c(Ag+)]+lg[c(CrO)]=2×(-5.18)+(-1.60)=-11.96,K (Ag CrO)
sp 2 4 sp 2 4
=10-11.96,则==102.21,B错误;在滴加NaCl溶液的最初阶段,滴入的Cl-的量极少,尚
不足以生成AgCl沉淀,滴入的Cl-全部以离子形式存在,其浓度随着NaCl溶液的滴入而
增大,由于Cl-未与Ag+发生作用,此时溶液仍为Ag CrO 的饱和溶液,其中c(CrO)=,
2 4
为定值,因此在此阶段,随着NaCl溶液的滴入而减小,当Ag CrO 转化为AgCl后,结合
2 4
沉淀转化反应为可逆反应知,当V(NaCl)≤2.0 mL时,体系中仍存在Ag CrO 沉淀,溶液中
2 4
满足K (Ag CrO)=c2(Ag+)·c(CrO)、K (AgCl)=c(Ag+)·c(Cl-),两式相除得=,其中c(Ag
sp 2 4 sp
+)在滴加NaCl溶液的过程中会随着c(Cl-)的增加而减少,因此会随着NaCl溶液的滴加而
增大,C错误;V(NaCl)=2.4 mL时,体系中有 AgCl沉淀,溶液中满足 lg[K (AgCl)]=
splg[c(Ag+)]+lg[c(Cl-)],代入数据-9.75=y +(-1.93),得y =-7.82,假设此时溶液中仍
1 1
存在Ag CrO ,则lg[K (Ag CrO)]=2lg[c(Ag+)]+lg[c(CrO)],代入数据-11.96=2×(-
2 4 sp 2 4
7.82)+lg[c(CrO)],得lg[c(CrO)]=3.68,即c(CrO)=103.68 mol·L-1,远超过Ag CrO 全部溶
2 4
解所得 CrO 的浓度,因此此时溶液中不存在 Ag CrO 沉淀,Ag CrO 已全部溶解,故
2 4 2 4
c(CrO)== mol·L-1,lg[c(CrO)]=lg=-lg 34,D正确。
5.[2024·浙江 1月]常温下,将等体积、浓度均为 0.40 mol·L-1 BaCl 溶液与新制
2
HSO 溶液混合,出现白色浑浊;再滴加过量的HO 溶液,振荡,出现白色沉淀。
2 3 2 2
已知:HSO K =1.4×10-2,K =6.0×10-8
2 3 a1 a2
K (BaSO)=5.0×10-10,K (BaSO)=1.1×10-10
sp 3 sp 4
下列说法不正确的是( )
A.HSO 溶液中存在c(H+)>c(HSO)>c(SO)>c(OH-)
2 3
B.将0.40 mol·L-1 HSO 溶液稀释到0.20 mol·L-1,c(SO)几乎不变
2 3
C.BaCl 溶液与HSO 溶液混合后出现的白色浑浊不含有BaSO
2 2 3 3
D.存在反应Ba2++HSO +HO===BaSO ↓+2H++HO是出现白色沉淀的主要原因
2 3 2 2 4 2
答案:C
解析:亚硫酸是二元弱酸,电离方程式为H
2
SO 3⇌H++HSO、HSO⇌H++SO,且以第
一步电离为主,则溶液中c(H+)>c(HSO)>c(SO)>c(OH-),A项正确;HSO 的第二步电离很
2 3
微弱,可近似认为溶液中c(H+)≈c(HSO),则K =≈c(SO),温度不变,平衡常数不变,故
a2
稀释时亚硫酸根离子浓度几乎不变,B项正确;两溶液等体积混合后,溶液中c(Ba2+)=
0.20 mol·L-1,根据 B 项分析知,溶液中 c(SO)≈6.0×10-8 mol·L-1,则 c(Ba2
+)·c(SO)≈1.2×10-8(mol·L-1)2>K (BaSO),故BaCl 溶液与HSO 溶液混合后出现的白色
sp 3 2 2 3
浑浊含有BaSO,C项错误;结合上述分析知,溶液中大量存在的微粒是Ba2+、HSO ,加
3 2 3
入HO 溶液后,三者发生氧化还原反应生成BaSO,故D项正确。
2 2 4
6.[2024·河北武邑中学高三月考]某温度下,向10 mL 0.1 mol·L-1 CuCl 溶液中滴加
2
0.1 mol·L-1的NaS溶液,滴加过程中溶液中-lgc(Cu2+)与NaS溶液体积(V)的关系如图所
2 2
示,下列有关说法正确的是( )
已知:lg 2=0.3,K (ZnS)=3×10-25 mol2·L-2。
sp
A.a、b、c三点中,水的电离程度最大的为b点
B.Na S溶液中:c(S2-)+c(HS-)+c(H S)=2c(Na+)
2 2
C.该温度下K (CuS)=4×10-36 mol2·L-2
sp
D.向100 mL Zn2+、Cu2+浓度均为10-5 mol·L-1的混合溶液中逐滴加入10-4 mol·L-1
的NaS溶液,Zn2+先沉淀
2
答案:C
解析:CuCl 、NaS水解促进水电离, b点是CuCl 与NaS溶液恰好完全反应的点,
2 2 2 2
溶质是氯化钠,对水的电离没有作用,水的电离程度最小, A错误;根据物料守恒,NaS
2
溶液中:2c(S2-)+2c(HS-)+2c(H S)=c(Na+),故B错误;b点是CuCl 与NaS溶液恰好完
2 2 2
全反应的点,c(Cu2+)=c(S2-),根据b点数据,c(Cu2+)=2×10-18 mol·L-1,该温度下K (CuS)=4×10-36 mol2·L-2,故C正确;K (ZnS)=3×10-25 mol2·L-2大于K (CuS),所
sp sp sp
以向100 mL Zn2+、Cu2+浓度均为10-5 mol·L-1的混合溶液中逐滴加入10-4 mol·L-1的
NaS溶液,Cu2+先沉淀, D错误。
2
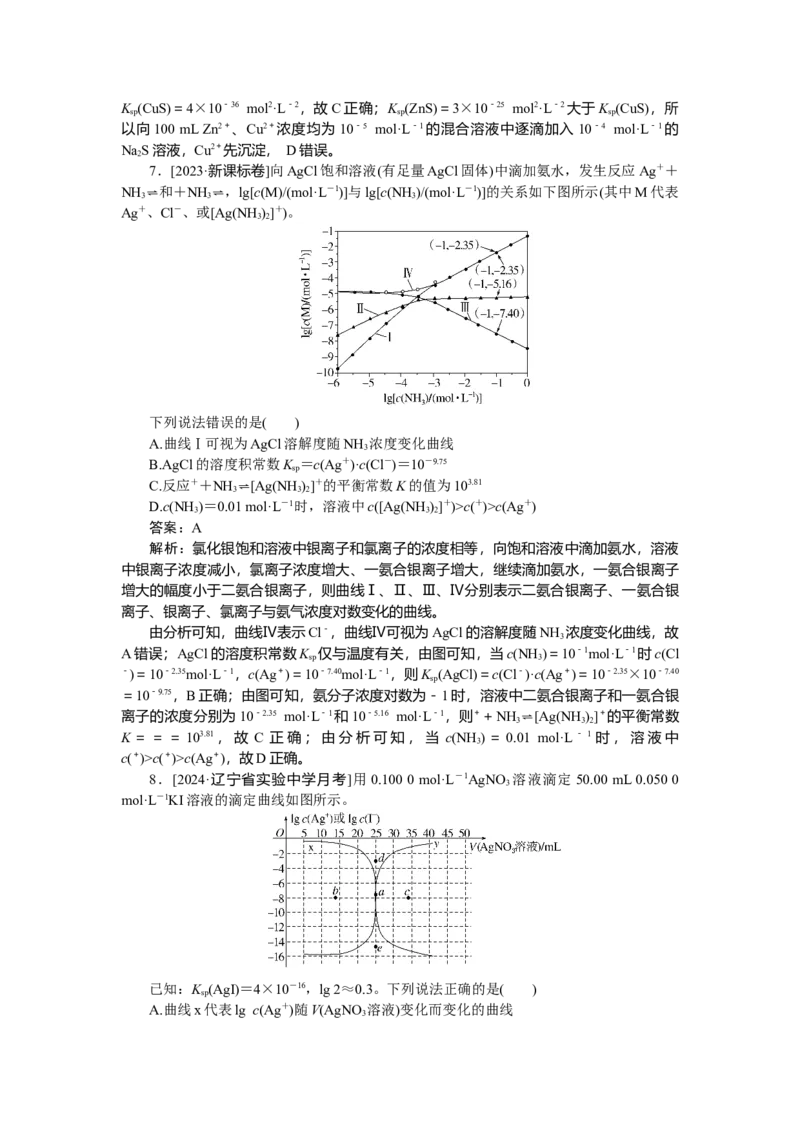
7.[2023·新课标卷]向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应Ag++
NH 3⇌ 和+NH 3⇌ ,lg[c(M)/(mol·L-1)]与lg[c(NH 3 )/(mol·L-1)]的关系如下图所示(其中M代表
Ag+、Cl-、或[Ag(NH)]+)。
3 2
下列说法错误的是( )
A.曲线Ⅰ可视为AgCl溶解度随NH 浓度变化曲线
3
B.AgCl的溶度积常数K =c(Ag+)·c(Cl-)=10-9.75
sp
C.反应++NH 3⇌[Ag(NH
3
)
2
]+的平衡常数K的值为103.81
D.c(NH )=0.01 mol·L-1时,溶液中c([Ag(NH)]+)>c(+)>c(Ag+)
3 3 2
答案:A
解析:氯化银饱和溶液中银离子和氯离子的浓度相等,向饱和溶液中滴加氨水,溶液
中银离子浓度减小,氯离子浓度增大、一氨合银离子增大,继续滴加氨水,一氨合银离子
增大的幅度小于二氨合银离子,则曲线Ⅰ、Ⅱ、Ⅲ、Ⅳ分别表示二氨合银离子、一氨合银
离子、银离子、氯离子与氨气浓度对数变化的曲线。
由分析可知,曲线Ⅳ表示Cl-,曲线Ⅳ可视为AgCl的溶解度随NH 浓度变化曲线,故
3
A错误;AgCl的溶度积常数K 仅与温度有关,由图可知,当c(NH )=10-1mol·L-1时c(Cl
sp 3
-)=10-2.35mol·L-1,c(Ag+)=10-7.40mol·L-1,则K (AgCl)=c(Cl-)·c(Ag+)=10-2.35×10-7.40
sp
=10-9.75,B正确;由图可知,氨分子浓度对数为-1时,溶液中二氨合银离子和一氨合银
离子的浓度分别为10-2.35 mol·L-1和10-5.16 mol·L-1,则++NH 3⇌[Ag(NH
3
)
2
]+的平衡常数
K===103.81,故 C 正确;由分析可知,当 c(NH )=0.01 mol·L-1 时,溶液中
3
c(+)>c(+)>c(Ag+),故D正确。
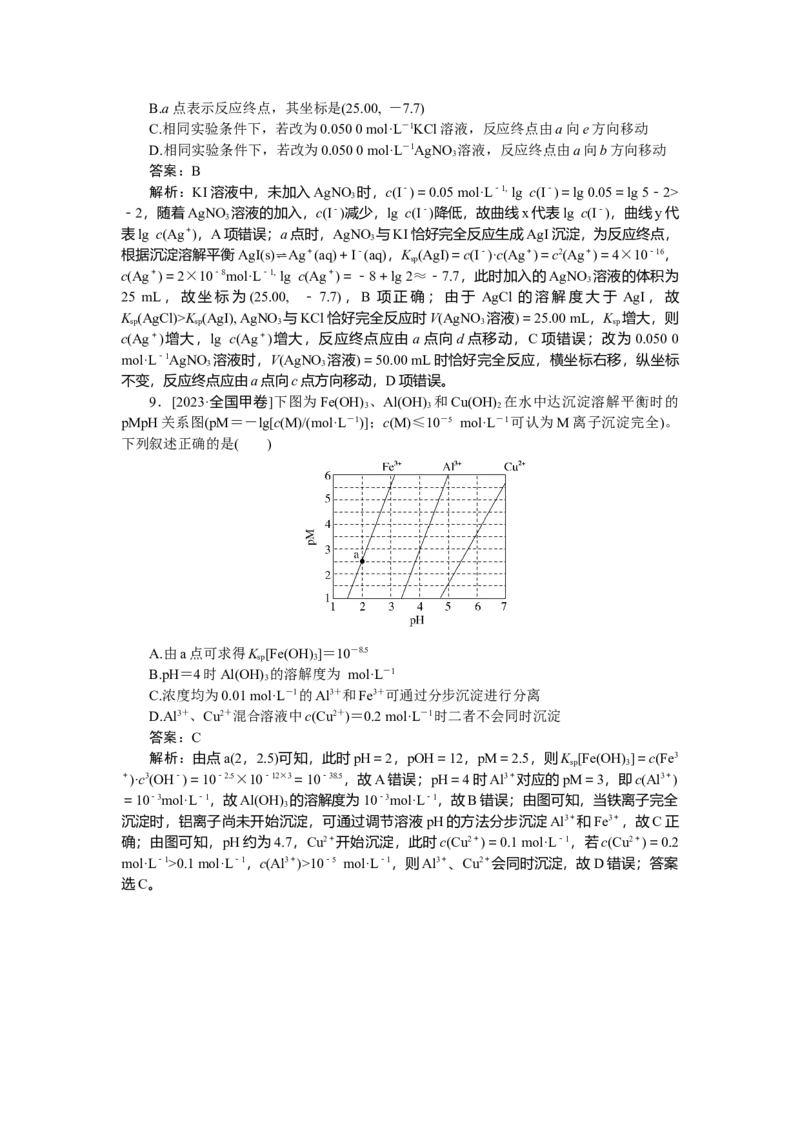
8.[2024·辽宁省实验中学月考]用0.100 0 mol·L-1AgNO 溶液滴定50.00 mL 0.050 0
3
mol·L-1KI溶液的滴定曲线如图所示。
已知:K (AgI)=4×10-16,lg 2≈0.3。下列说法正确的是( )
sp
A.曲线x代表lg c(Ag+)随V(AgNO 溶液)变化而变化的曲线
3B.a点表示反应终点,其坐标是(25.00, -7.7)
C.相同实验条件下,若改为0.050 0 mol·L-1KCl溶液,反应终点由a向e方向移动
D.相同实验条件下,若改为0.050 0 mol·L-1AgNO 溶液,反应终点由a向b方向移动
3
答案:B
解析:KI溶液中,未加入AgNO 时,c(I-)=0.05 mol·L-1, lg c(I-)=lg 0.05=lg 5-2>
3
-2,随着AgNO 溶液的加入,c(I-)减少,lg c(I-)降低,故曲线x代表lg c(I-),曲线y代
3
表lg c(Ag+),A项错误;a点时,AgNO 与KI恰好完全反应生成AgI沉淀,为反应终点,
3
根据沉淀溶解平衡AgI(s)⇌Ag+(aq)+I-(aq),K
sp
(AgI)=c(I-)·c(Ag+)=c2(Ag+)=4×10-16,
c(Ag+)=2×10-8mol·L-1, lg c(Ag+)=-8+lg 2≈-7.7,此时加入的AgNO 溶液的体积为
3
25 mL,故坐标为(25.00, -7.7),B 项正确;由于 AgCl 的溶解度大于 AgI,故
K (AgCl)>K (AgI), AgNO 与KCl恰好完全反应时V(AgNO 溶液)=25.00 mL,K 增大,则
sp sp 3 3 sp
c(Ag+)增大,lg c(Ag+)增大,反应终点应由 a点向d点移动,C项错误;改为 0.050 0
mol·L-1AgNO 溶液时,V(AgNO 溶液)=50.00 mL时恰好完全反应,横坐标右移,纵坐标
3 3
不变,反应终点应由a点向c点方向移动,D项错误。
9.[2023·全国甲卷]下图为Fe(OH) 、Al(OH) 和Cu(OH) 在水中达沉淀溶解平衡时的
3 3 2
pMpH关系图(pM=-lg[c(M)/(mol·L-1)];c(M)≤10-5 mol·L-1可认为M离子沉淀完全)。
下列叙述正确的是( )
A.由a点可求得K [Fe(OH) ]=10-8.5
sp 3
B.pH=4时Al(OH) 的溶解度为 mol·L-1
3
C.浓度均为0.01 mol·L-1的Al3+和Fe3+可通过分步沉淀进行分离
D.Al3+、Cu2+混合溶液中c(Cu2+)=0.2 mol·L-1时二者不会同时沉淀
答案:C
解析:由点a(2,2.5)可知,此时pH=2,pOH=12,pM=2.5,则K [Fe(OH) ]=c(Fe3
sp 3
+)·c3(OH-)=10-2.5×10-12×3=10-38.5,故A错误;pH=4时Al3+对应的pM=3,即c(Al3+)
=10-3mol·L-1,故Al(OH) 的溶解度为10-3mol·L-1,故B错误;由图可知,当铁离子完全
3
沉淀时,铝离子尚未开始沉淀,可通过调节溶液pH的方法分步沉淀Al3+和Fe3+,故C正
确;由图可知,pH约为4.7,Cu2+开始沉淀,此时c(Cu2+)=0.1 mol·L-1,若c(Cu2+)=0.2
mol·L-1>0.1 mol·L-1,c(Al3+)>10-5 mol·L-1,则Al3+、Cu2+会同时沉淀,故D错误;答案
选C。