文档内容
《物理》三色速记手册
第三章 热学
【考点1】分子动理论
一、分子动理论的三个观点
1.物质是由大量分子组成的
一般认为分子直径的数量级为10-10m。
1mol 任何物质都含有相同的粒子数,这个数用阿伏加德罗常数表示,即 NA=6.02×
1023mol-1。
2.分子热运动
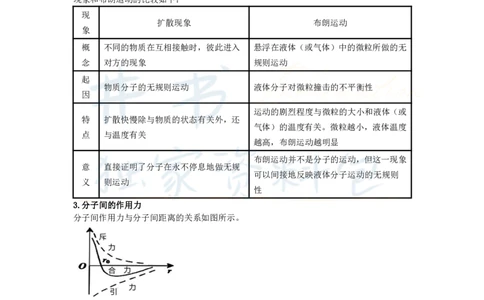
分子永不停息地做无规则运动,扩散现象和布朗运动都可以很好地证明分子的热运动。扩散
现象和布朗运动的比较如下:
现
扩散现象 布朗运动
象
概 不同的物质在互相接触时,彼此进入 悬浮在液体(或气体)中的微粒所做的无
念 对方的现象 规则运动
起
物质分子的无规则运动 液体分子对微粒撞击的不平衡性
因
运动的剧烈程度与微粒的大小和液体(或
特 扩散快慢除与物质的状态有关外,还
气体)的温度有关。微粒越小,液体温度
点 与温度有关
越高,布朗运动越明显
布朗运动并不是分子的运动,但这一现象
意 直接证明了分子在永不停息地做无规
可以间接地反映液体分子运动的无规则
义 则运动
性
3.分子间的作用力
分子间作用力与分子间距离的关系如图所示。
(1)分子之间同时存在着相互作用的引力和斥力。
(2)随着分子间距离的逐渐增大,分子间的引力与斥力都减小,但斥力减小得快;随着分
子间距的减小,分子间的引力与斥力都增大,但斥力增大得快。
二、内能
1.分子动能
做热运动的分子所具有的动能称为分子动能。物体的温度是大量分子热运动剧烈程度的标
志。温度是分子热运动平均动能的标志。温度越高,分子的平均动能越大。
2.分子势能
分子间存在相互作用力,由分子间的相互作用力和分子间的相对位置决定的能量,称为分子
势能。
34《物理》三色速记手册
分子势能的大小是由分子间的相对位置决定的。
3.物体的内能
物体中所有分子的热运动动能与分子势能的总和,叫作物体的内能。任何物体都具有内能。
物体的内能跟物体的温度和体积都有关系:温度升高时,物体内能增加;体积变化时,物
体内能变化。
机械能与整个物体的机械运动情况有关,而内能与物体内部分子的热运动和分子之间的相互
作用情况有关。内能是不同于机械能的另一种形式的能。
4.理想气体的内能
理想气体是分子间没有相互作用力的气体,是一种理想模型。理想气体分子内无分子势能,
理想气体的内能就是所有分子的动能之和。
质量为m、摩尔质量为M 的理想气体的内能为
其中,i为分子运动的自由度。单原子分子(质点)的自由度为i=3,刚性双原子分子的自
由度为i=5,刚性多原子分子的自由度为i=6。
一定量的理想气体内能完全决定于分子运动的自由度和气体的温度,而与气体的体积和压
强无关。
5.改变内能的方式
改变内能有做功和热传递两种方式。
做功时,内能与其他形式的能(如内能与机械能、内能与电能等)发生转化,而热传递只是
不同物体(或一个物体的不同部分)之间内能的转移。
做功和热传递都是过程量,内能是状态量。
6.比热容
一定质量的某种物质,在温度升高(或降低)时吸收(或放出)的热量与它的质量和升高(或
降低)的温度的乘积之比,叫作这种物质的比热容。比热容用符号c表示。
比热容是反映物质自身性质的物理量。不同的物质,比热容一般不同。
质量相同的不同物质,当吸收或放出同样热量时,比热容较大的物质温度变化较小。因此,
比热容大的物质对调节温度有很好的作用。
【考点2】气体、固体、液体
一、气体
(一)气体的状态参量
体积V:气体的体积是指气体分子所能达到的空间,也就是气体所能充满容器的容积。
温度T:表示物体的冷热程度,是分子平均动能的标志。单位K,T=t+273.15K。
压强P:单位面积上受到的正压力。气体压强是气体分子对容器频繁碰撞的结果,单位Pa。
在没有外界影响的情况下,只要经过足够长的时间,系统内各部分的状态参量能够达到稳定
状态。这种状态叫作平衡态。
当系统处于平衡态时,系统所有状态参量都不随时间变化,我们就能比较准确地描述系统
的状态。
(二)气体实验定律
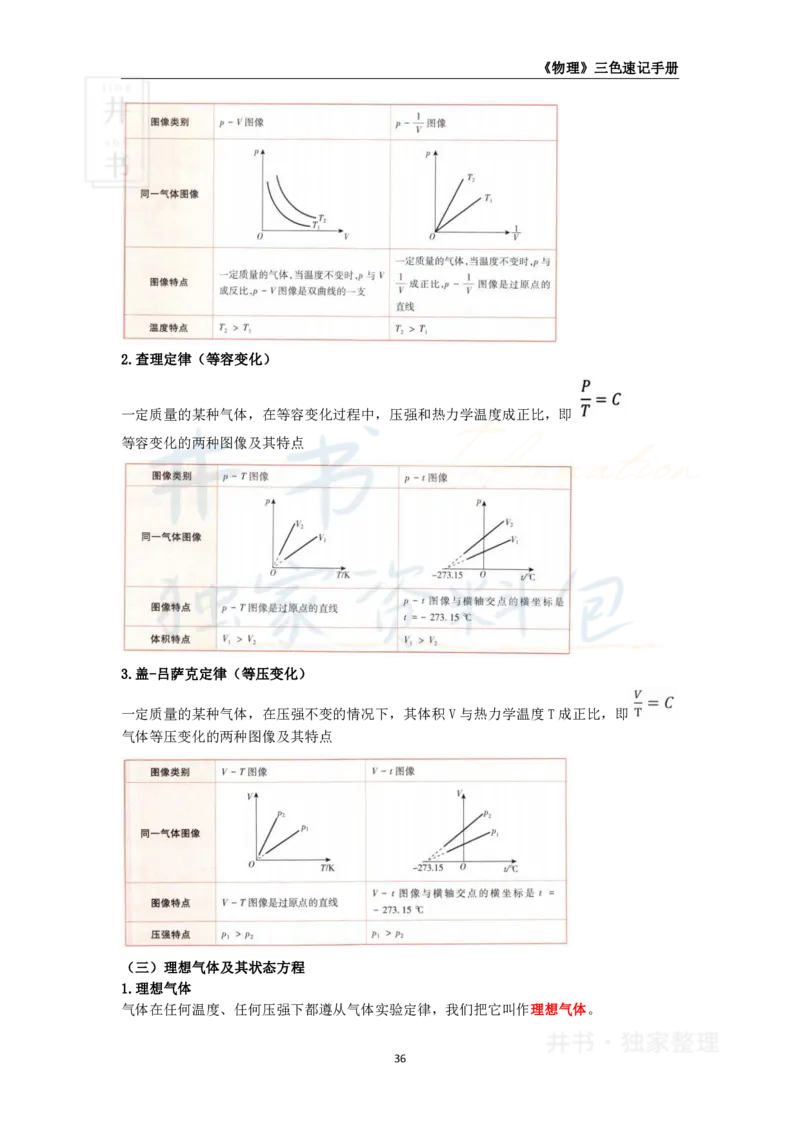
1.玻意耳定律(等温变化)
一定质量的某种气体,在温度不变的情况下,压强p与体积V成反比,即pV=C。
气体等温变化的两种图像及其特点
35《物理》三色速记手册
2.查理定律(等容变化)
一定质量的某种气体,在等容变化过程中,压强和热力学温度成正比,即
等容变化的两种图像及其特点
3.盖-吕萨克定律(等压变化)
一定质量的某种气体,在压强不变的情况下,其体积V与热力学温度T成正比,即
气体等压变化的两种图像及其特点
(三)理想气体及其状态方程
1.理想气体
气体在任何温度、任何压强下都遵从气体实验定律,我们把它叫作理想气体。
36《物理》三色速记手册
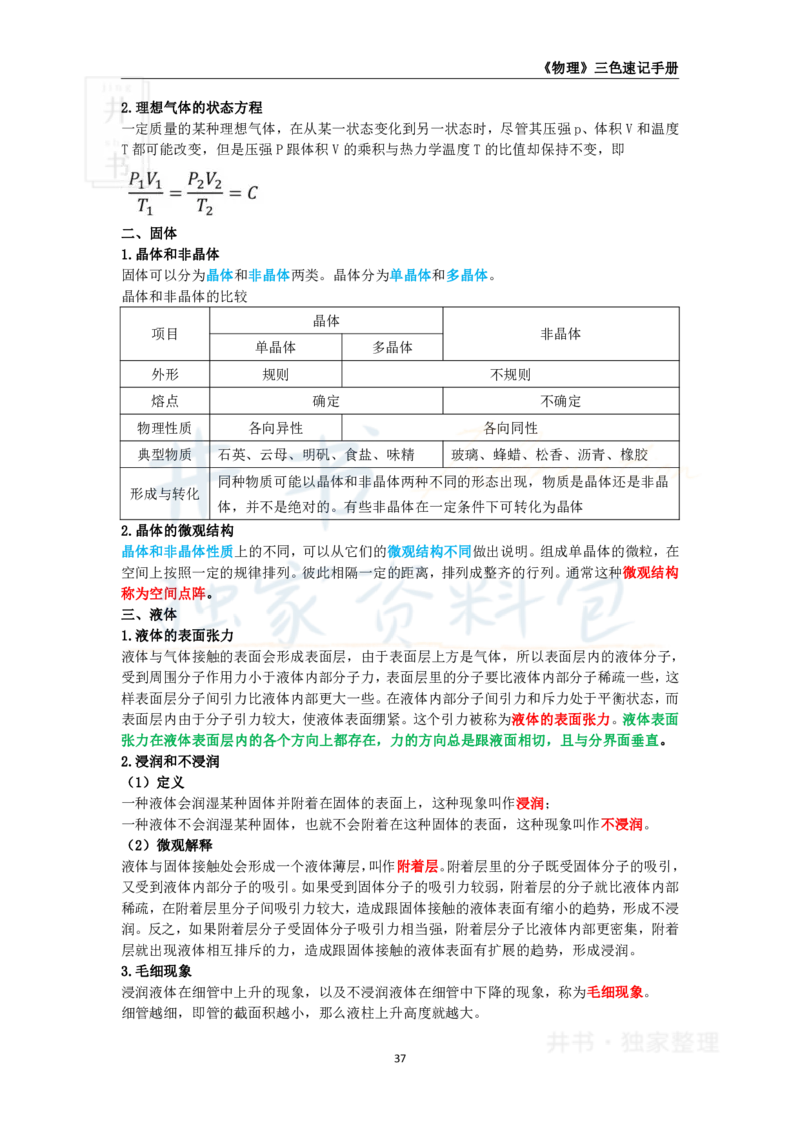
2.理想气体的状态方程
一定质量的某种理想气体,在从某一状态变化到另一状态时,尽管其压强p、体积V和温度
T都可能改变,但是压强P跟体积V的乘积与热力学温度T的比值却保持不变,即
二、固体
1.晶体和非晶体
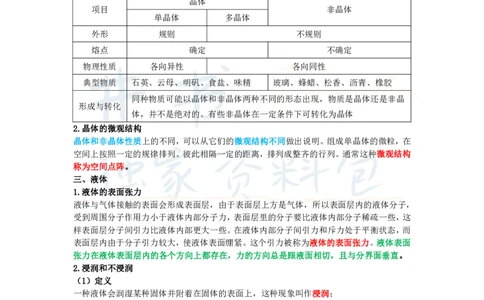
固体可以分为晶体和非晶体两类。晶体分为单晶体和多晶体。
晶体和非晶体的比较
晶体
项目 非晶体
单晶体 多晶体
外形 规则 不规则
熔点 确定 不确定
物理性质 各向异性 各向同性
典型物质 石英、云母、明矾、食盐、味精 玻璃、蜂蜡、松香、沥青、橡胶
同种物质可能以晶体和非晶体两种不同的形态出现,物质是晶体还是非晶
形成与转化
体,并不是绝对的。有些非晶体在一定条件下可转化为晶体
2.晶体的微观结构
晶体和非晶体性质上的不同,可以从它们的微观结构不同做出说明。组成单晶体的微粒,在
空间上按照一定的规律排列。彼此相隔一定的距离,排列成整齐的行列。通常这种微观结构
称为空间点阵。
三、液体
1.液体的表面张力
液体与气体接触的表面会形成表面层,由于表面层上方是气体,所以表面层内的液体分子,
受到周围分子作用力小于液体内部分子力,表面层里的分子要比液体内部分子稀疏一些,这
样表面层分子间引力比液体内部更大一些。在液体内部分子间引力和斥力处于平衡状态,而
表面层内由于分子引力较大,使液体表面绷紧。这个引力被称为液体的表面张力。液体表面
张力在液体表面层内的各个方向上都存在,力的方向总是跟液面相切,且与分界面垂直。
2.浸润和不浸润
(1)定义
一种液体会润湿某种固体并附着在固体的表面上,这种现象叫作浸润;
一种液体不会润湿某种固体,也就不会附着在这种固体的表面,这种现象叫作不浸润。
(2)微观解释
液体与固体接触处会形成一个液体薄层,叫作附着层。附着层里的分子既受固体分子的吸引,
又受到液体内部分子的吸引。如果受到固体分子的吸引力较弱,附着层的分子就比液体内部
稀疏,在附着层里分子间吸引力较大,造成跟固体接触的液体表面有缩小的趋势,形成不浸
润。反之,如果附着层分子受固体分子吸引力相当强,附着层分子比液体内部更密集,附着
层就出现液体相互排斥的力,造成跟固体接触的液体表面有扩展的趋势,形成浸润。
3.毛细现象
浸润液体在细管中上升的现象,以及不浸润液体在细管中下降的现象,称为毛细现象。
细管越细,即管的截面积越小,那么液柱上升高度就越大。
37《物理》三色速记手册
在纸张、棉花、土壤、砖块等物体内部有许多细小的孔道,这些孔道起到了毛细管的作用。
4.液晶
液晶是介于固态和液态之间的一种物质状态。液晶态既具有液体的流动性,又在一定程度
上具有晶体分子的规则排列的性质。液晶本身不能发光,主要通过电压的改变产生电场而使
液晶分子排列产生变化来显示图像。
四、物态变化
(1)熔化和凝固
熔化:物质从固态变成液态的过程叫熔化。熔化过程吸热。
凝固:物质从液态变成固态的过程叫凝固。凝固过程放热。
熔点和凝固点:晶体熔化时保持不变的温度叫熔点;晶体凝固时保持不变的温度叫凝固点。
晶体的熔点和凝固点相同。
(2)汽化和液化
汽化:物质从液态变为气态的过程叫汽化,汽化的方式有蒸发和沸腾。汽化过程要吸热。
蒸发:是在任何温度下,且只在液体表面发生的,缓慢的汽化现象。
沸腾:是在一定温度(沸点)下,在液体内部和表面同时发生的剧烈的汽化现象。液体沸腾
时要吸热,但温度保持不变,这个温度叫沸点。
影响液体蒸发快慢的因素:
液体温度;液体表面积;液面上方空气流动快慢。
液化:物质从气态变成液态的过程叫液化,液化要放热。使气体液化的方法有:降低温度和
压缩体积。(液化现象如:“白气”、雾、等)
(3)升华和凝华
升华和凝华:
物质从固态直接变成气态叫升华,要吸热;
物质从气态直接变成固态叫凝华,要放热。
【考点3】热力学定律和能量守恒定律
一、热力学定律
1.热力学第一定律
表述1:一个热力学系统的内能变化量等于外界向它传递的热量与外界对它所做的功的和。
这个关系叫作热力学第一定律。用公式表示为
外界对系统做功,W>0;系统对外界做功,W<0。
系统从外界吸收热量,Q>0;系统向外界放出热量,Q<0。
系统内能增加,△U>0;系统内能减少,△U<0。
表述2:在大学阶段,我们认为,在一般情况下,当系统状态变化时,做功与传递热量往往
是同时存在的。如果有一系统,外界对它传递的热量为Q,系统从内能为E1的初始平衡状
态改变到内能为E2的终末平衡状态,同时系统对外做功为A,那么,不论过程如何,总有
Q=E2-E1+A
这就是热力学第一定律,即外界对系统传递的热量,一部分使系统的内能增加,另一部分用
于系统对外做功。该式与中学阶段所学的热力学第一定律在本质上是一致的。
热力学第一定律的微分形式为:dQ=dE+dA
其中,dA=pdV
2.热力学第二定律
(1)热力学第二定律的一种表述
38《物理》三色速记手册
热量不会自发地从低温传到高温物体。
(2)热力学第二定律的另一种表述
不可能从单一热库吸收热量,使之完全变成功,而不产生其他影响,即第二永动机不可制成。
这两种表述是等价的,热力学第二定律指出了实际宏观过程进行的条件和方向,其实质:“一
切热现象有关的实际宏观过程都是不可逆的”,是一个能够反应过程进行的方向规律。
2.摩尔热容量
若系统物质的量是1mol,则1mol物质的热容量叫作摩尔热容量。该量用字母Cm来表示,
单位是J·mol-1·K-1。
(二)等体过程
1.等体过程的特点
等体过程的特点是气体的体积不变,即V为恒量,dV=0, 所以dA=0。
根据热力学第一定律,有dQ=dE。
在该过程中,热量:
在等体过程中,外界传给气体的热量,全部用来增加气体的内能,气体对外做功为零。
2.定容摩尔热容
由此可知,理想气体的定容摩尔热容只与分子自由度有关。
(三)等压过程
1.等压过程的特点
等压过程的特点是系统的压强保持不变,即p为恒量,dp=0。
在该过程中,热量:
2.定压摩尔热容
1mol理想气体,在等压过程中吸收的热量dQp,与温度的变化dT之比叫作定压摩尔热容,
即
39《物理》三色速记手册
(四)等温过程
等温过程的特点是系统的温度保持不变,即dT=0。由于理想气体的内能只取决于温度,所
以在等温过程中,理想气体的内能保持不变,即dE=0。
在该过程中,热量
(五)绝热过程
绝热过程是指系统始终不与外界交换热量的过程。
绝热过程中,dQ=0,则由热力学第一定律可知,dA=-dE,
绝热方程的另外两种形式: TVγ−1=C2,pγ−1T−γ=C3。
(六)卡诺热机与卡诺制冷机
卡诺循环是在两个温度恒定的热源(一个高温热源T1, 一个低温热源T2)之间工作的循
环过程。在整个循环中,工作物质只和高温热源或低温热源交换能量,没有散热漏气等因
素存在。卡诺循环是由两个准静态的等温过程和两个准静态的绝热过程组成。
卡诺制冷机:
制冷机可以制冷的原理是循环从低温热源吸热,导致低温热源(一个要使之降温的物体)的
温度降得更低。
三、能量守恒定律
能量既不会凭空产生,也不会凭空消失,它只能从一种形式转化为其他形式,或者从一个物
体转移到别的物体,在转化或转移的过程中,能量的总量保持不变。这就是能量守恒定律。
40