文档内容
2011 年广州市初中毕业生学业考试
化学试题
可能用到的相对原子质量:H-l C-l2 O-16 Mg- 24 S- 32 C1- 35. 5 Cu-64
第一部分选择题(共40分)
一、选择置(本题包括20小题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选
错、不选、多选或涂改不清的.均不给分。
1.根据《广州市城市生活垃圾分类管理暂行规定》第十一条,我市居民生活垃圾分为可回收
物、餐厨垃圾、有害垃圾、其他垃圾四类。可回收物主要有以下四种,其成分属于有机合成材
料的是( )
A.塑料 B.纸类 C.金属 D.玻璃
2.下列变化属于化学变化的是( )
A.浓盐酸挥发,形成白雾
B.冰升华,形成白雾
C.镁条在空气中燃烧.产生自烟
D.水加热到沸腾.产生蒸汽
3.下列图示实验操作中,正确的是( )
4.下列物质中属于盐的是( )
A.NaOH B.NaO C.NaSO D.Na
2 2 4
5.下列过程不是通过化学变化获得能量的是( )
A.利用炸药爆炸开山炸石 B.利用煤燃烧发电
C.利用汽油燃烧驱动汽车 D.利用水力发电
6.下列关于空气中各组成成分说法正确的是( )
A.空气中的O 只有点燃时才能发生化学反应
2
B.空气中的CO 是导致酸雨的主要原因
2C.空气中的N 可作为生产氮肥的原料
2
D.空气中的稀有气体没有任何使用价值
7核电站中可用硼酸(H BO)吸收中子,阻断核辐射。硼酸中硼元素的化合价是( )
3 3
A.+1 B.+2 C.+3 D+4
8.小烧杯中盛有含石蕊的氢氧化钠溶液.逐滴加入稀盐酸至过量,烧杯中溶液颜色变化的
顺序是( )
A.紫色——红色——蓝色
B.蓝色——紫色——红色
C.蓝色——红色——紫色
D.紫色——蓝色——红色
9.下列方法可使海水转化为饮用水的是( )
A.过滤 B.静置沉淀 C.活性炭吸附 D.蒸馏
10.下列关于O 和CO 的说法正确的是( )
2 2
A.都含有氧元素
B.都是氧化物
C.都含有氧气分子
D.都能使带有火星的木条复燃
11.下列溶液pH最大的是( )
A.10%KOH B.20%KOH C.10%HCI D.20%HCl
12.下列说法正确的是( )
A.CO 能与血液中血红蛋白结合导致中毒
2
B.CO能溶于水生成酸
C.用闻气味的方法能够区别CO 和CO
2
D.CO可以在O 中燃烧
2
13.下图是元素x的原子结构示意圈.下列说法正确的是( )
A.该原子的核外电子数为l2
B.该原子最外电子层达到了稳定结构
C.X属于非金属元素D.x与Cl形成的化台物为XCl
14.下列关于化肥的说法正确的是( )
A.过磷酸钙[Ca(HPO ) 和CaSO 的混合物]属于氮肥
2 4 2 4
B.凡施用过化肥的蔬菜都会危害健康
C.硫酸钾与熟石灰混合、研磨,能闻到刺激性的气味
D.合理施用化肥能提高农作物的产量
15下列物质能够反应,且没有明显现象的是( )
A.NaCO 溶液加入澄清石灰水中
2 3
B. Fe O 加入NaOH溶液中
2 3
C.稀HCl滴入Ba(OH) 溶液中
2
D.CO 通入澄清石灰水中
2
16.实验室用下图所示装置制取和收集O,下列操作不正确的是( )
2
A.将KClO,和MnO 混合.用纸槽装入试管中
3 2
B.将导管口伸入盛满水的集气瓶里,然后加热,立即收集O
2
C.待集气瓶充满O,盖好玻璃片后,再移出水面
2
D.收集完成后,松开橡皮塞,再熄灭酒精灯
17.向l00g10%NaOH溶液中加入12.5gNaOH固体,完全溶解后.所得溶液中溶质质量分
数为( )
A. 12. 5% B.200% C.22.5%D.25%
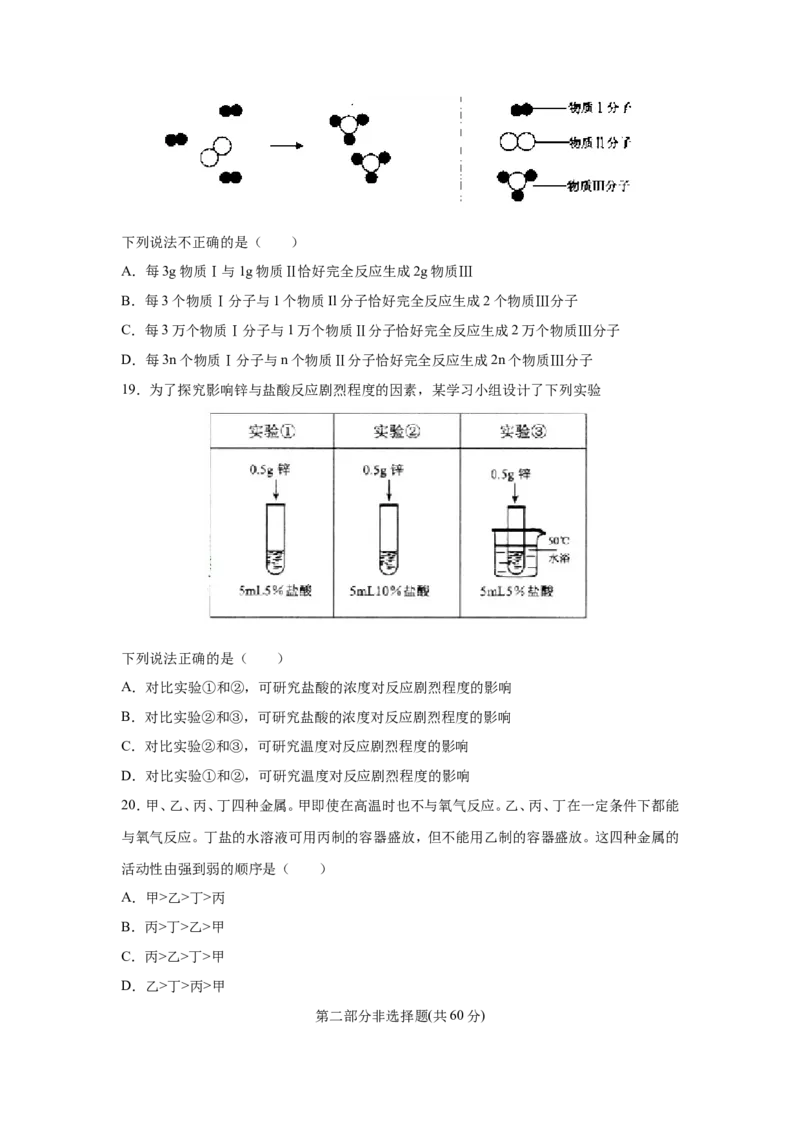
18.某化学反应的微观示意图如下,图中“ ”和“ ”分别表示不同的原子下列说法不正确的是( )
A.每3g物质Ⅰ与1g物质Ⅱ恰好完全反应生成2g物质Ⅲ
B.每3个物质Ⅰ分子与1个物质Il分子恰好完全反应生成2个物质Ⅲ分子
C.每3万个物质Ⅰ分子与1万个物质Ⅱ分子恰好完全反应生成2万个物质Ⅲ分子
D.每3n个物质Ⅰ分子与n个物质Ⅱ分子恰好完全反应生成2n个物质Ⅲ分子
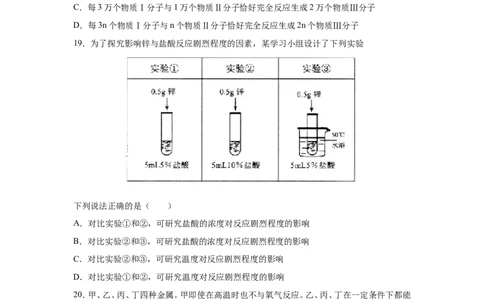
19.为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了下列实验
下列说法正确的是( )
A.对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响
B.对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响
C.对比实验②和③,可研究温度对反应剧烈程度的影响
D.对比实验①和②,可研究温度对反应剧烈程度的影响
20.甲、乙、丙、丁四种金属。甲即使在高温时也不与氧气反应。乙、丙、丁在一定条件下都能
与氧气反应。丁盐的水溶液可用丙制的容器盛放,但不能用乙制的容器盛放。这四种金属的
活动性由强到弱的顺序是( )
A.甲>乙>丁>丙
B.丙>丁>乙>甲
C.丙>乙>丁>甲
D.乙>丁>丙>甲
第二部分非选择题(共60分)二、本息包括5小题.共31分.
2l.(4分)近日,有媒体报道面条可燃,一些市民据此担心面条中加入了不安全的添加剂。
⑴仅从面条可燃就判断加入了添加剂是不科学的,因为面粉含有的主要营养素淀粉本身是
可以燃烧的,淀粉的化学式为(C H O)n,完全燃烧的产物是___________;燃烧过程中还可
6 10 5
闻到像头发烧焦似的刺鼻气味,是由于面粉中另一种营养素燃烧产生的,该营养索是-
____________。
⑵面粉不仅可以燃烧.一定条件下还会发生爆炸。2010年2月我国某大型面粉厂灌装车间发
生面粉爆炸,造成重大人员伤亡。为避免类似事件,生产过程可采取的措施有
________________。
A.密封门窗,隔绝氧气
B.严禁吸烟,杜绝货源
C.轻拿轻放,减少粉尘扬起
D.提高淀粉的着火点
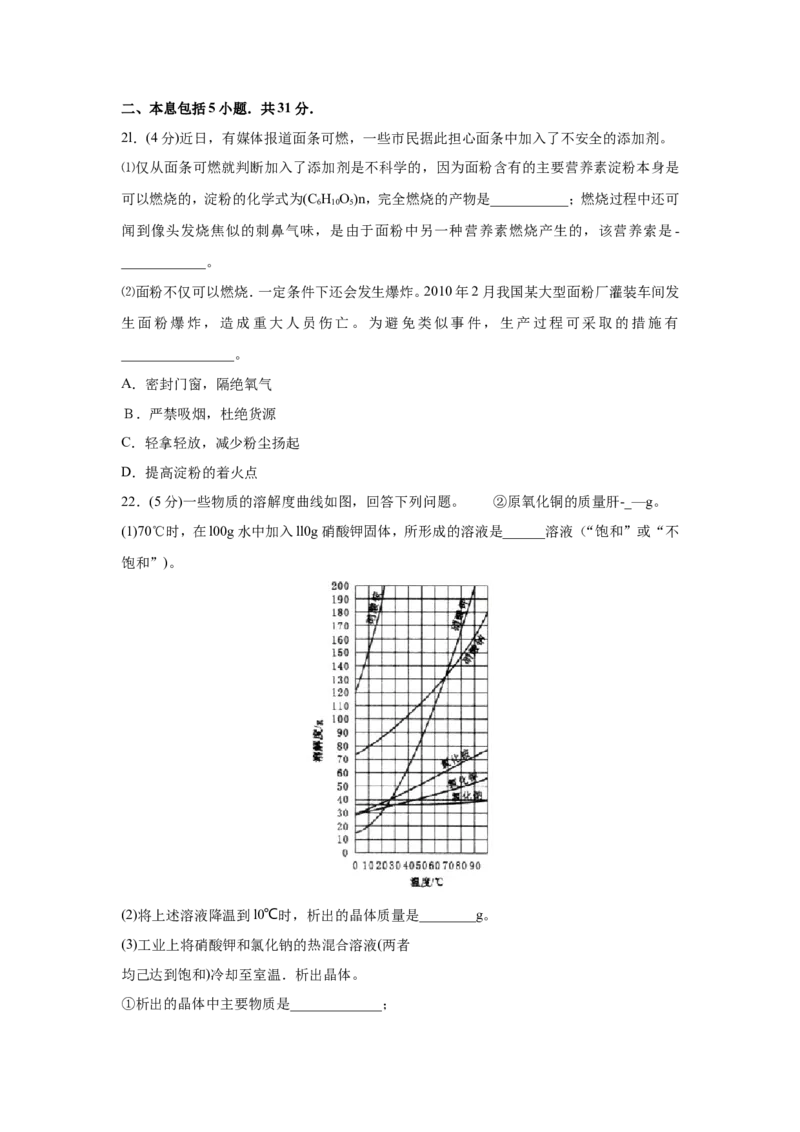
22.(5分)一些物质的溶解度曲线如图,回答下列问题。 ②原氧化铜的质量肝-_—g。
(1)70℃时,在l00g水中加入ll0g硝酸钾固体,所形成的溶液是______溶液(“饱和”或“不
饱和”)。
(2)将上述溶液降温到l0℃时,析出的晶体质量是________g。
(3)工业上将硝酸钾和氯化钠的热混合溶液(两者
均己达到饱和)冷却至室温.析出晶体。
①析出的晶体中主要物质是_____________;②关于剩余溶液.下列说法正确的是_________。
A.只含氯化钠,不含硝酸钾,且氯化钠达到饱和
B.含有氯化钠,又含有硝酸钾,且只有氯化钠达到饱和
C.含有氯化钠,叉含有硝酸钾,且两者都达到饱和
23.(7分)Cu可以形成化台价为+2和+1的化合物。其中+1价化合物称为亚铜化合物。
(1)写出下列物质的化学式:氢氧化铜________,氧化亚铜___________
(2)高温时,氧化铜可被木炭还原为铜,反应的化学方程式是__________________________
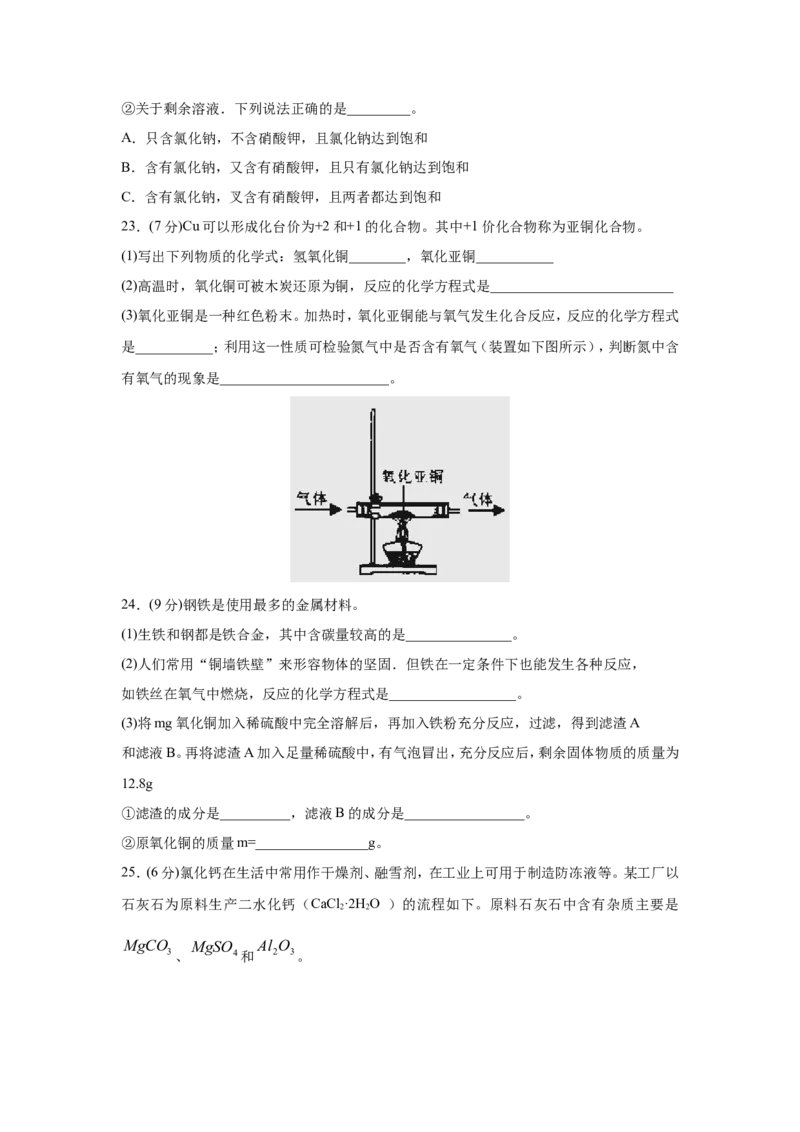
(3)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式
是___________;利用这一性质可检验氮气中是否含有氧气(装置如下图所示),判断氮中含
有氧气的现象是________________________。
24.(9分)钢铁是使用最多的金属材料。
(1)生铁和钢都是铁合金,其中含碳量较高的是_______________。
(2)人们常用“铜墙铁壁”来形容物体的坚固.但铁在一定条件下也能发生各种反应,
如铁丝在氧气中燃烧,反应的化学方程式是__________________。
(3)将mg氧化铜加入稀硫酸中完全溶解后,再加入铁粉充分反应,过滤,得到滤渣A
和滤液B。再将滤渣A加入足量稀硫酸中,有气泡冒出,充分反应后,剩余固体物质的质量为
12.8g
①滤渣的成分是__________,滤液B的成分是_________________。
②原氧化铜的质量m=________________g。
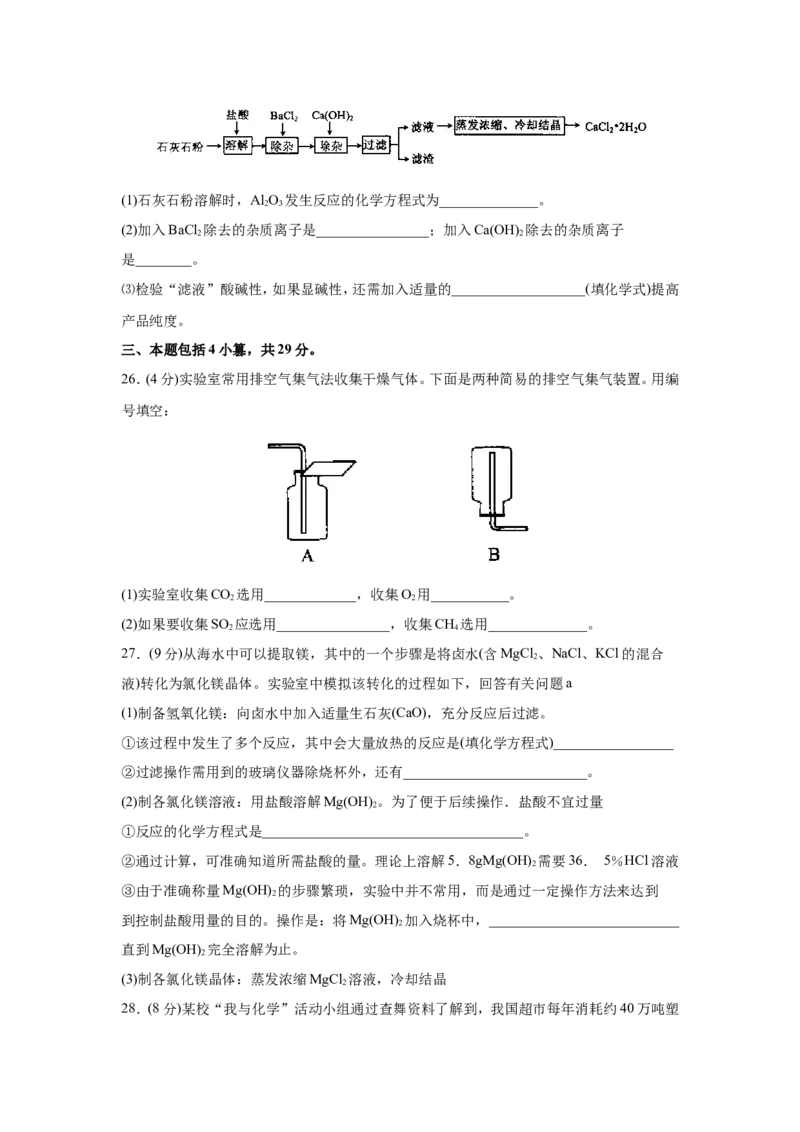
25.(6分)氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以
石灰石为原料生产二水化钙(CaCl ·2HO )的流程如下。原料石灰石中含有杂质主要是
2 2
MgCO MgSO Al O
3、 4和 2 3。(1)石灰石粉溶解时,Al O 发生反应的化学方程式为______________。
2 3
(2)加入BaCl 除去的杂质离子是________________;加入Ca(OH) 除去的杂质离子
2 2
是________。
⑶检验“滤液”酸碱性,如果显碱性,还需加入适量的___________________(填化学式)提高
产品纯度。
三、本题包括4小篡,共29分。
26.(4分)实验室常用排空气集气法收集干燥气体。下面是两种简易的排空气集气装置。用编
号填空:
(1)实验室收集CO 选用_____________,收集O 用___________。
2 2
(2)如果要收集SO 应选用________________,收集CH 选用______________。
2 4
27.(9分)从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl、NaCl、KCl的混合
2
液)转化为氯化镁晶体。实验室中模拟该转化的过程如下,回答有关问题a
(1)制备氢氧化镁:向卤水中加入适量生石灰(CaO),充分反应后过滤。
①该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)_________________
②过滤操作需用到的玻璃仪器除烧杯外,还有__________________________。
(2)制各氯化镁溶液:用盐酸溶解Mg(OH) 。为了便于后续操作.盐酸不宜过量
2
①反应的化学方程式是_____________________________________。
②通过计算,可准确知道所需盐酸的量。理论上溶解5.8gMg(OH) 需要36. 5%HCl溶液
2
③由于准确称量Mg(OH) 的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到
2
到控制盐酸用量的目的。操作是:将Mg(OH) 加入烧杯中,___________________________
2
直到Mg(OH) 完全溶解为止。
2
(3)制各氯化镁晶体:蒸发浓缩MgCl 溶液,冷却结晶
2
28.(8分)某校“我与化学”活动小组通过查舞资料了解到,我国超市每年消耗约40万吨塑料袋。假定这些使用后的废塑料袋都通过焚烧处理。将排放大量CO。该活动小组用下图所
2
示装置,测量一定质量塑料袋燃烧后产生的CO 的质量。
2
(1)为了保证测量的准确性,连接好实验装置后应检查________________________,再加入药
品进行实验。
(2)装置Ⅰ的小烧杯中加入足量HO 和催化剂.可持续产生O 供塑料袋充分燃烧,产
2 2 2
生O 的化学方程式是__________________________。
2
(3)塑料袋燃尽,装置Ⅰ逐渐冷却时,装置Ⅱ中液体也不易倒吸进入装置Ⅰ中.原因是
___________________
(4)根据实验目的,需要称量的是_________。
A.实验前塑料袋的质量
B.实验前和实验后装置Ⅱ的质量
C.实验前和实验后装置Ⅲ的质量
29.(8分)有三种白色粉末.分别是碳酸钡、硫酸钡和碳酸钠。请设计一个实验方案.把这
三种粉末区分开来。叙述实验操作、预期现象和结论。
(实验室仅提供了稀HCl、NaSO 溶液、蒸馏水以及常用的实验仪器。)
2 4
实验操作 预期现象与结论
参考答案
1.A 2.C 3.B 4.C 5.D 6.C 7.C 8.B 9.D 10.A 11.B 12.D 13.A 14.D 15.C16.B 17.B 18.A 19.A 20.D
21.水和二氧化碳 蛋白质 BC
22.
⑴不饱和
⑵90
⑶①硝酸钾 ②C
23.
Cu(OH) CuO
⑴ 2
C 2CuO高温2CuCO
⑵ 2
2Cu OO 4CuO
⑶ 2 2 红色粉末变成黑色
24.
⑴生铁
3Fe2O 点燃Fe O
⑵ 2 3 4
⑶①Cu、Fe FeSO4、H2O ②16g
25.
Al O 6HCl 2AlCl 3H O
⑴ 2 3 3 2
Mg2
⑵硫酸根离子 镁离子
⑶HCl
26.
⑴A A
⑵A B
27.
CaO H O Ca(OH)
⑴① 2 2 ②漏斗、玻璃棒
Mg(OH) 2HCl MgCl 2H O
⑵① 2 2 2
②20
③用胶头滴管逐滴加入稀盐酸溶液28.
⑴装置气密性
2H O MnO 2H OO
⑵ 2 2 2 2 2
⑶装置Ⅰ中生成氧气,使Ⅰ内压强增大
⑷A C
29.
实验操作 预期现象与结论
分别取三种粉末样品于试管中加入蒸馏水 一支试管粉末溶液,该粉末为碳酸钠,另两
支试管无明显现象
分别往剩下的两支试管中加入稀盐酸 有气泡产生的是碳酸钡,无明显现象的硫酸
钡