文档内容
滨州市二〇一一年初中学生学业考试
化 学 试 题
可能用到的相对原子质量:
H 1 C 12 N 14 O 16 Na 23
第Ⅰ卷(选择题 共48分)
一、选择题(本题包括l6小题,每小题只有一个选项符合题意。每小题3分,共48分)
1.下列说法正确的是
A.空气中氧气的质量分数为21%
B. 空气中各成分所占的比例是永恒不变的
C.空气是由多种物质组成的混合物
D. 空气质量级别数目越大,空气的质量越好
2. 为预防自行车生锈,下列做法中不合理的是
A.车架表面喷涂油漆 B.钢圈表面镀防护金属
C.链条表面涂机油 D.露天放置,日晒雨淋
3.下列做法不会损害人体健康的是
A.用含小苏打的发酵粉焙制糕点 B.用三聚氰胺假冒牛奶中的蛋白质
C.用甲醛的水溶液浸泡水产品 D.用霉变花生制成的花生油烹调食品
4.下图所示的实验操作中正确的是
A.闻气体气味 B.滴加液体 C.取用块状固体 D.稀释浓硫酸
5.下列叙述错误的是
A.分子、原子和离子都能直接构成物质
B.原子中原子核与核外电子的电量相等,电性相反,所以整个原子不显电性
C.决定原子质量大小的主要是质子和电子
D.原子如果得到或失去电子就变成离子
6.日常生活中的下列物品:①“飞火流星”足球 ②铝合金门窗 ③橡皮塞 ④大理石板
⑤羊毛衫 ⑥铅笔芯 ⑦保鲜膜,主要是由有机高分子材料制成的是
A.①②③⑤ B.①③⑤⑦ C.②③④⑤⑦ D.①③⑥⑦
7.森林着火时,救火员开辟防火隔离带的目的是
A.隔绝空气 B.开辟道路以利于运水灭火
C.隔离可燃物 D.使可燃物温度降低到着火点以下
8.乙醇的分子结构模型如图所示,则下列叙述正确的是A.乙醇是由三种元素组成的无机物 B.一个乙醇分子中含有28个质子
C.乙醇中碳、氧元素的质量比为3:2 D.乙醇中氧元素的质量分数最大
9.下列实验数据合理的是
A.用pH试纸测得某地雨水的pH为5
B.用10 mL量筒量取了6.53 mL水
C.用20g 氯化钠和l00g 水配制的l20g 食盐水,其溶质质量分数为20%
D.用托盘天平称得某纯碱样品的质量为10.57g
10. 下列关于海水晒盐原理的分析正确的是
A.利用阳光照射,使海水升温得到食盐
B.利用海风降温析出食盐晶体
C.利用海水在阳光下发生分解反应制得食盐
D.利用阳光和风力使水分蒸发得到食盐
11. 下列关于某些营养物质的化学性质描述错误的是
A.淀粉遇碘水会变蓝
B. 蛋白质遇可溶性重金属盐会失去生理活性
C.油脂能在人体内氧化分解,释放出热量
D.葡萄糖在人体内可转化为蔗糖、淀粉和纤维素
12.下图中“ ”和“ ”分别表示两种元素的原子,能用该图表示的化学反应是
A.C+O
2
C
b
o
i
m
n
CO
2
B.C+ CO
2
C
b
o
i
m
n
2CO
C.H + Cl Com 2HCl D.2H + O Com 2HO
2 2 bin 2 2 bin 2
13.以下推理正确的是
A. 酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B. 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性
C. 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D. 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
14.下列说法正确的是
A.盐酸能使紫色石蕊试液变蓝
B. 浓硫酸露置于空气中,溶质的质量质量分数变大C. 长期露置于空气中的固体氢氧化钠,其成分不会发生变化
D.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
15. 除去下列物质中的少量杂质,所用试剂或方法不正确的是
选项 物质 杂质 试剂或方法
A NaCl 固体 泥沙 加水溶解、过滤、蒸发
B NaCl 溶液 NaC0 滴加硫酸溶液至不再产生气泡
2 3
C KNO 溶液 Ba(N0 ) 滴加适量KSO 溶液、过滤
3 3 2 2 4
D N 0 通过红热的铜丝
2 2
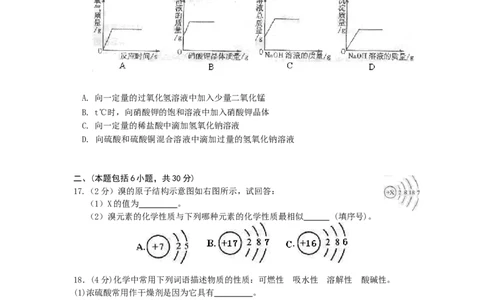
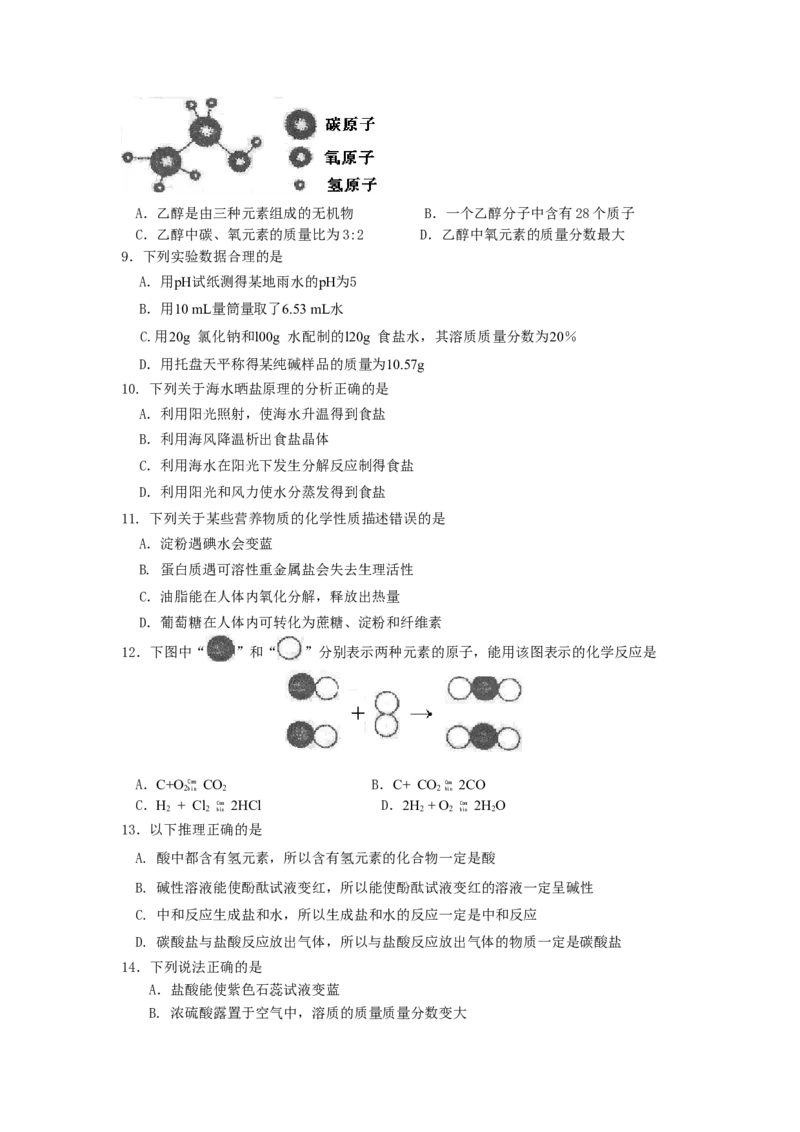
16. 下列图像能正确反映其对应操作中各量变化关系的是
A. 向一定量的过氧化氢溶液中加入少量二氧化锰
B. t℃时,向硝酸钾的饱和溶液中加入硝酸钾晶体
C. 向一定量的稀盐酸中滴加氢氧化钠溶液
D. 向硫酸和硫酸铜混合溶液中滴加过量的氢氧化钠溶液
二、(本题包括6小题,共30分)
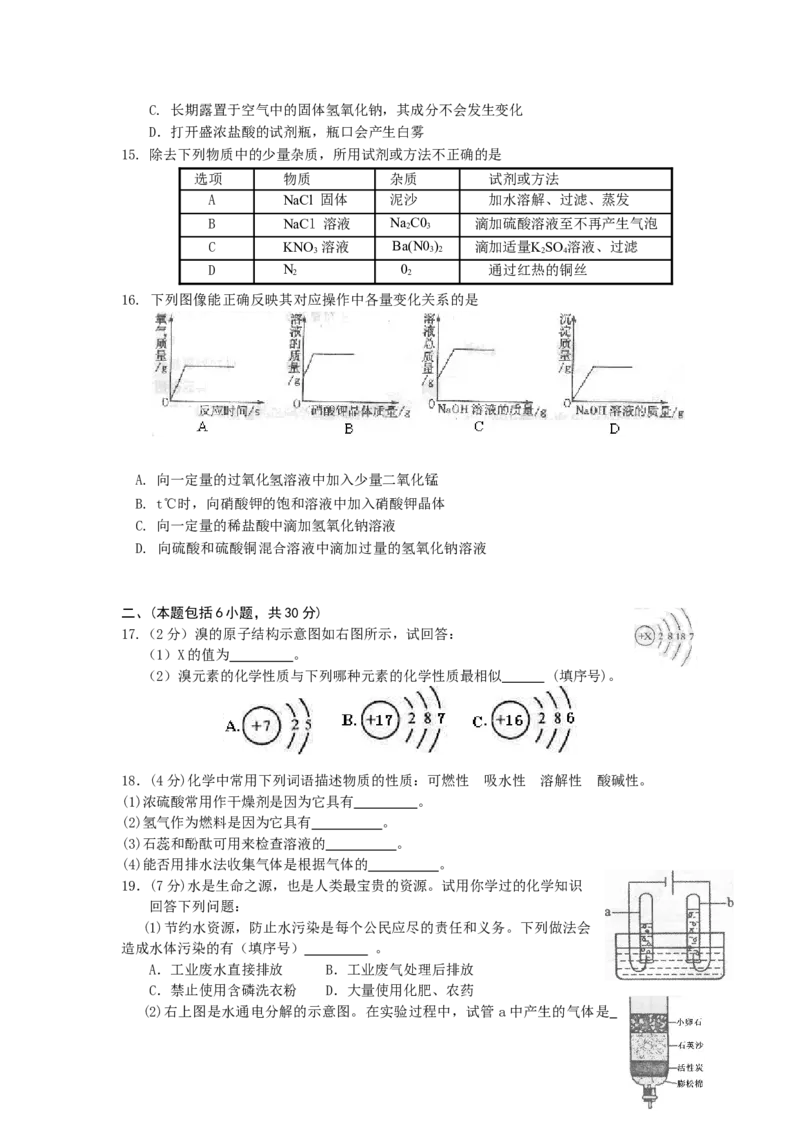
17.(2分)溴的原子结构示意图如右图所示,试回答:
(1)X的值为 。
(2)溴元素的化学性质与下列哪种元素的化学性质最相似 (填序号)。
18.(4分)化学中常用下列词语描述物质的性质:可燃性 吸水性 溶解性 酸碱性。
(1)浓硫酸常用作干燥剂是因为它具有 。
(2)氢气作为燃料是因为它具有 。
(3)石蕊和酚酞可用来检查溶液的 。
(4)能否用排水法收集气体是根据气体的 。
19.(7分)水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识
回答下列问题:
(1)节约水资源,防止水污染是每个公民应尽的责任和义务。下列做法会
造成水体污染的有(填序号) 。
A.工业废水直接排放 B.工业废气处理后排放
C.禁止使用含磷洗衣粉 D.大量使用化肥、农药
(2)右上图是水通电分解的示意图。在实验过程中,试管 a中产生的气体是,写出该反应的化学方程式: 。
(3)为除去水中的不溶性杂质,某同学制作了右图所示的简易净水器,其中活性炭的主要
作用是 。
(4)某些地方的饮用水中含有少量的Ca(HCO ) 等可溶性盐。烧水时,Ca(HCO ) 发生分解
3 2 3 2
反应,生成难溶性的CaCO 。试写出Ca(HCO ) 受热分解的化学方程式 。
3 3 2
20.(7分)科学是一把双刃剑。2011年3月11日,日本大地震引发的福岛核电站核泄漏事故
使我们对碘有了新的认识:
(1)自然界中的碘(127)是人体必需的一种元素,该元素在人体中为一种 (填
“常 量”或“微量”)元素,如果人体缺乏碘元素就会导致 。
(2)我们食用的加碘盐中的碘主要以KIO 的形式存在,KIO 中碘的化合价是 ,KIO
3 3 3
受热易分解,因此做菜时应注意 。
(3)日本福岛核电站反应堆内发生的核裂变可产生放射性碘l31和铯l37,其中碘131原
子中含有53个质子和 个中子。科学证明,每人日服用含碘100 mg的碘片能有效
阻止碘131的辐射。曾一度被抢购的加碘盐每500 g中含碘20 mg,按上述标准,即使这些
碘都转化成能防止辐射的碘,每人每天应吃 g加碘盐才起作用,这远远超出了人体
正常摄入食盐量,显然是不科学的!
(4)这次核泄漏事故,使新能源的开发和安全使用再次成为人们谈论的话题。除了开发和
利用核能之外,人类还可以利用的新能源有 等。
21.(3分)右图为硝酸钾和氯化钠的溶解度曲线。由图可知:
(1)当温度为30℃时,硝酸钾的溶解度 (填“>”、
“<”或“=”)氯化钠的溶解度。
(2)当硝酸钾中含有少量氯化钠时,可用 法提纯
硝酸钾。
(3)硝酸钾、氯化钠都属于 (填“易溶”、“可
溶”、“微溶”或“难溶”)物质。
22.(7分)化学用语是学习和研究化学的工具,试按要求完成下
列各题:
(1)写出化学符号或化学符号所表示的意义:
①2个硫酸根离子 ;
②3O 。
2
(2)用化学式填空:
①最简单的有机物 ;
②侯氏制碱法制得的纯碱 。
(3)右图是物质基本分类和基本转化关系图,
试
按下列要求填空:
物质类别:① ,② ;
变化类型:③ (填“物理变化”或“化学变化”)。
三、(本题包括2小题,共l2分)
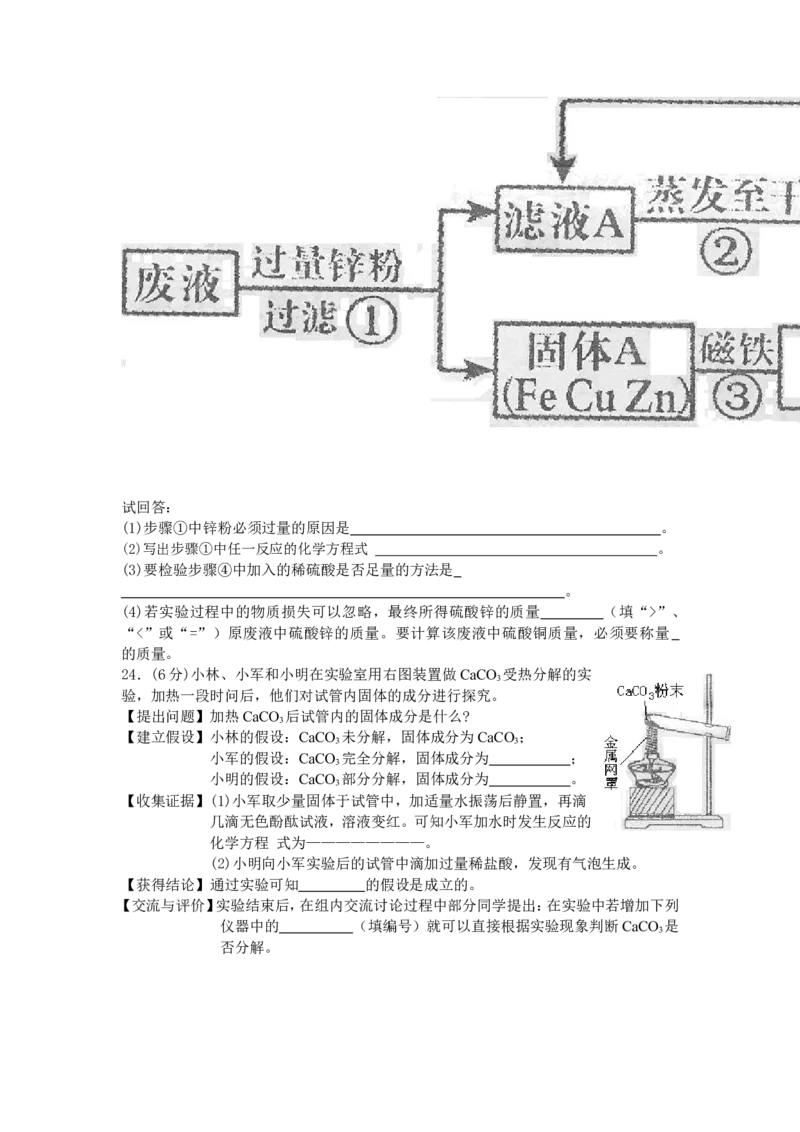
23. (6分)某化学实验小组实验结束时,将含有CuSO 、ZnSO、FeSO 的废液倒在废液缸里,
4 4 4
为回收有关金属和盐,同学们设计了如下实验方案:试回答:
(1)步骤①中锌粉必须过量的原因是 。
(2)写出步骤①中任一反应的化学方程式 。
(3)要检验步骤④中加入的稀硫酸是否足量的方法是
。
(4)若实验过程中的物质损失可以忽略,最终所得硫酸锌的质量 (填“>”、
“<”或“=”)原废液中硫酸锌的质量。要计算该废液中硫酸铜质量,必须要称量
的质量。
24.(6分)小林、小军和小明在实验室用右图装置做CaCO 受热分解的实
3
验,加热一段时问后,他们对试管内固体的成分进行探究。
【提出问题】加热CaCO 后试管内的固体成分是什么?
3
【建立假设】小林的假设:CaCO 未分解,固体成分为CaCO ;
3 3
小军的假设:CaCO 完全分解,固体成分为 ;
3
小明的假设:CaCO 部分分解,固体成分为 。
3
【收集证据】(1)小军取少量固体于试管中,加适量水振荡后静置,再滴
几滴无色酚酞试液,溶液变红。可知小军加水时发生反应的
化学方程 式为————————。
(2)小明向小军实验后的试管中滴加过量稀盐酸,发现有气泡生成。
【获得结论】通过实验可知 的假设是成立的。
【交流与评价】实验结束后,在组内交流讨论过程中部分同学提出:在实验中若增加下列
仪器中的 (填编号)就可以直接根据实验现象判断CaCO 是
3
否分解。四、(本题包括l小题,共l0分)
25.为测定某碳酸氢铵化肥中的含氮量,小滨在实验室里取用8.5 g该化肥样品与20g NaOH
溶液共热,恰好完全反应,测得残留物为 26.8 g (提示:反应的化学方程式为
NH HCO+2NaOH== Na CO+2H O+NH↑,生成的氨气全部逸出,其他成分不含氮,也不参
4 3 2 3 2 3
加反应)。试求:
(1)生成氨气的质量。
(2)该化肥中氮元素的质量分数(计算结果精确到0.1%)。
(3)所用溶液的溶质质量分数。
化学试题(A)答案及评分说明
一、选择题(本题包括l6小,每小题3分,共48分)
1.C 2.D 3.A 4.B 5.C 6.B 7.C 8.C
9.A l0.D ll.D l2.A l3.B l4.D l5.B l6.A
二、(本题包括6小题,每个化学方程式2分,其余每空l分,共30分)
17.(2分) (1)35 (2)B
18.(4分)(1)吸水性 (2)可燃性 (3)酸碱性 (4)溶解性
19. (7分)(1)A、D (2)氢气(或H 2 ) 2H 2 O C b o i m n 2H 2 ↑+ O 2 ↑
△
(3)吸附 (4) Ca(HCO ) CaCO ↓+ CO↑+ HO
3 2 == 3 2 2
20.(7分)
(1)微量 甲状腺肿(或大脖子病)
(2)+5 菜快要出锅时再加盐 ’
(3)78 2500
(4)太阳能、地热能、风能、氢能、潮汐能(答任一合理答案即可)
21.(3分) (1)> (2)降温结晶(或冷却热饱和溶液) (3)易溶
22.(7分)
(1)①2SO 2— ②三个氧分子 (2)①CH ②NaCO
4 4 2 3
(3)①纯净物 ②单质 ③化学变化
三、(本题包括2小题,每个化学方程式2分,其余每空l分,共12分)
23. (6分)
(1)将废液中的Cu2+和Fe2+全部置换出来
(2)Zn+ CuSO = ZnSO +Cu (或Fe+CuSO===Cu+FeSO )
4 4 4 4
(3)取步骤④的滤渣于试管中,加入少量稀硫酸,若有气泡产生,则酸不足量(或若无气泡产生,则酸已足量)
(4)> 固体D(或铜)
24. (6分)
【建立假设】CaO CaO、CaCO
3
【收集证据】(1)CaO+ HO == Ca(OH)
2 2
【获得结论】小明
【交流与评价】①③
四、(本题包括1小题,共10分)
25. 解:(1)生成氨气的质量为:8.5g + 20g ==1.7g
(2)设参加反应的碳酸氢铵的质量为 x,参加反应的氢氧化钠的质量为 y
NH HCO + 2NaOH == NaCO + NH ↑+ 2HO
4 3 2 3 3 2
79 80 17
x y 1.7g
79:17==x:1.7g x==7.9g
7.9g碳酸氢铵中韩氮元素的质量为:7.9g × == 1.4g
碳铵化肥中氮元素的质量分数为:
(3)80:17 == y:1.7g y==8g
溶质质量分数为
答:(1)生成氨气的质量为1.7g;
(2)该化肥中氮元素的质量分数为16.5%;
(3)所用溶液的溶质质量分数为40%。