文档内容
化学保温训练(二)
命题人:欧光太、谢凡、彭海洋、左传鹏、申卫波、陈巧玲
审题人:左传鹏、彭海洋
一、单项选择题
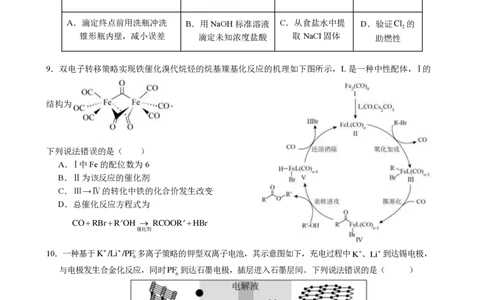
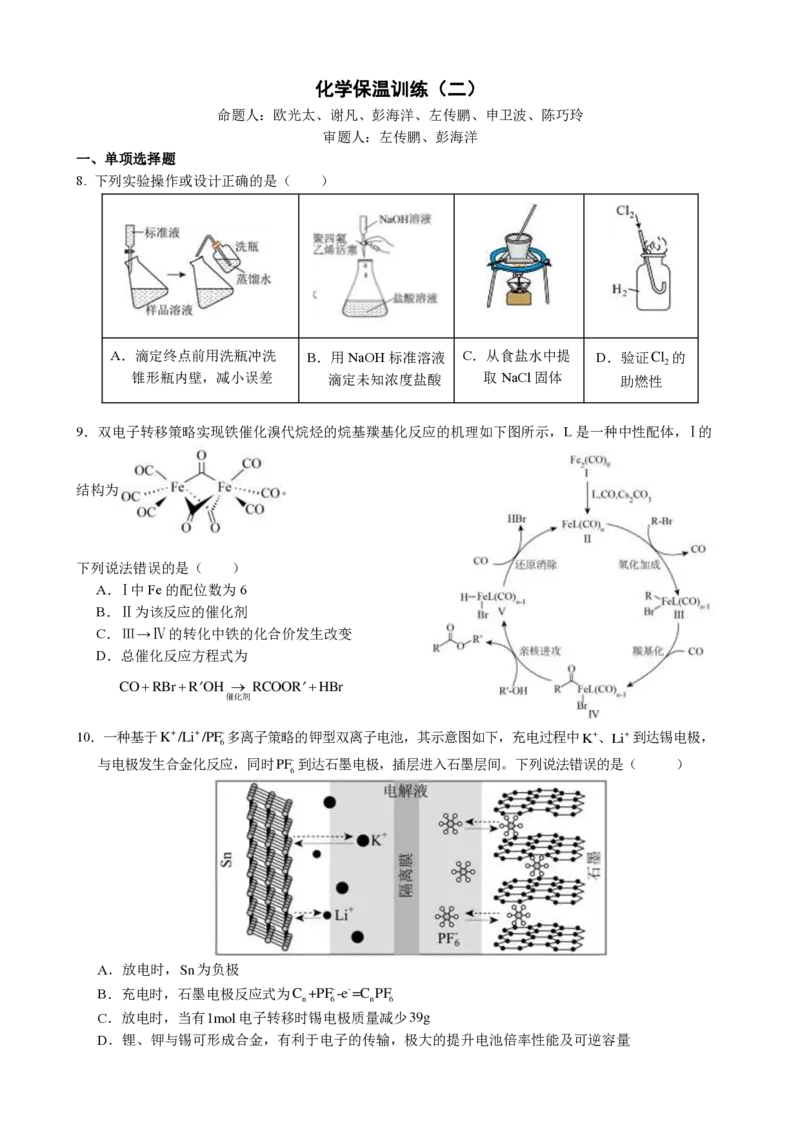
8. 下列实验操作或设计正确的是( )
A.滴定终点前用洗瓶冲洗 B.用NaOH标准溶液 C.从食盐水中提 D.验证Cl 的
2
锥形瓶内壁,减小误差 滴定未知浓度盐酸 取NaCl固体 助燃性
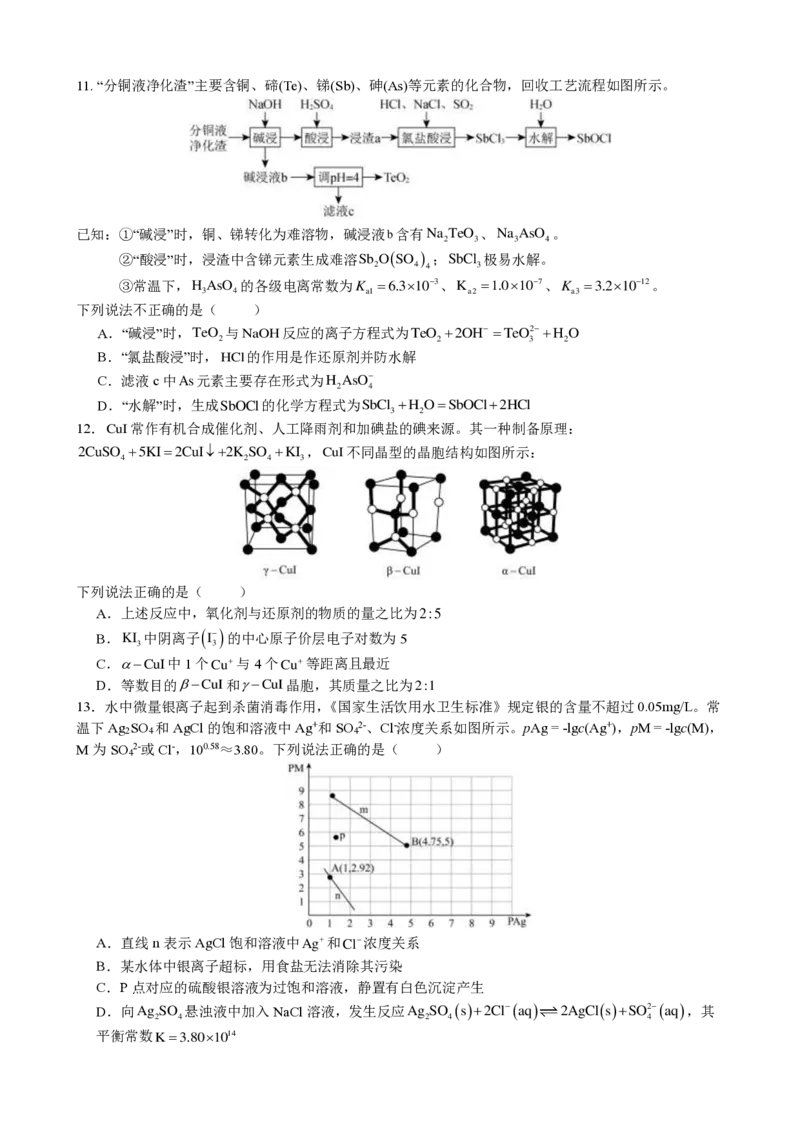
9.双电子转移策略实现铁催化溴代烷烃的烷基羰基化反应的机理如下图所示,L是一种中性配体,Ⅰ的
结构为 。
下列说法错误的是( )
A.Ⅰ中Fe的配位数为6
B.Ⅱ为该反应的催化剂
C.Ⅲ→Ⅳ的转化中铁的化合价发生改变
D.总催化反应方程式为
CO+RBr+ROH → RCOOR+HBr
催化剂
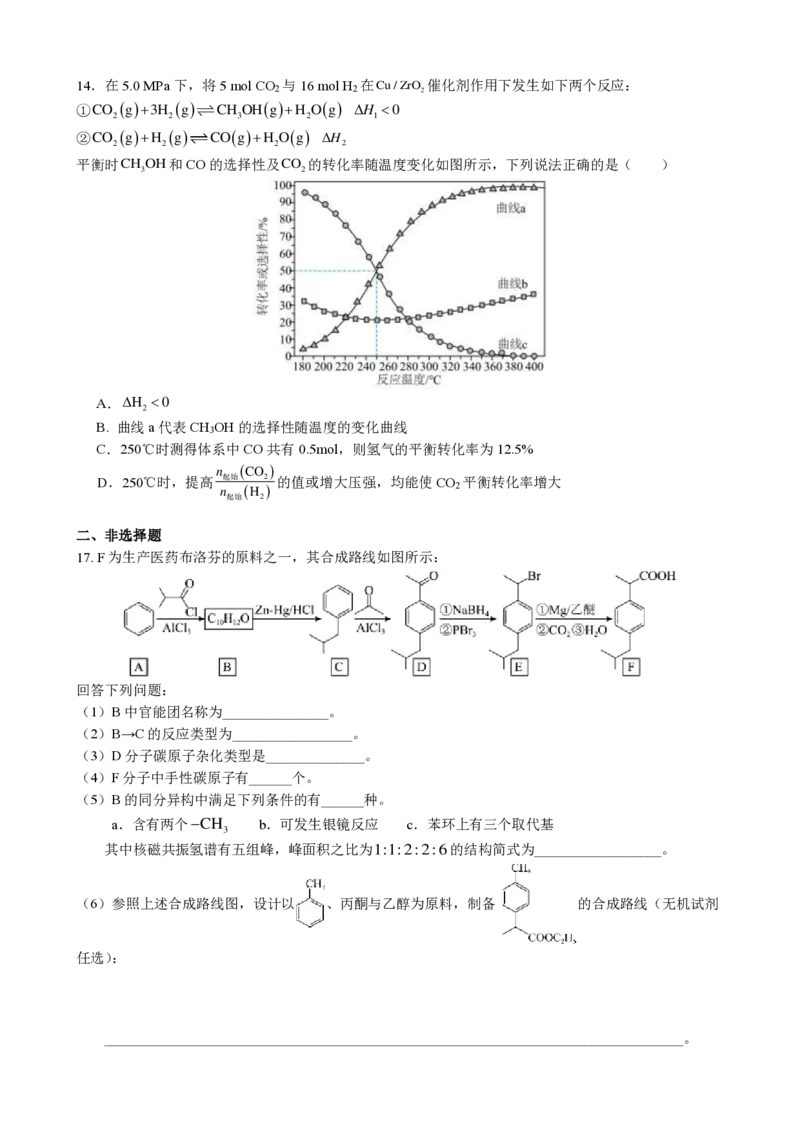
10.一种基于K+/Li+/PF-多离子策略的钾型双离子电池,其示意图如下,充电过程中K+、Li+到达锡电极,
6
与电极发生合金化反应,同时PF-到达石墨电极,插层进入石墨层间。下列说法错误的是( )
6
A.放电时,Sn为负极
B.充电时,石墨电极反应式为C +PF--e-=C PF
n 6 n 6
C.放电时,当有1mol电子转移时锡电极质量减少39g
D.锂、钾与锡可形成合金,有利于电子的传输,极大的提升电池倍率性能及可逆容量
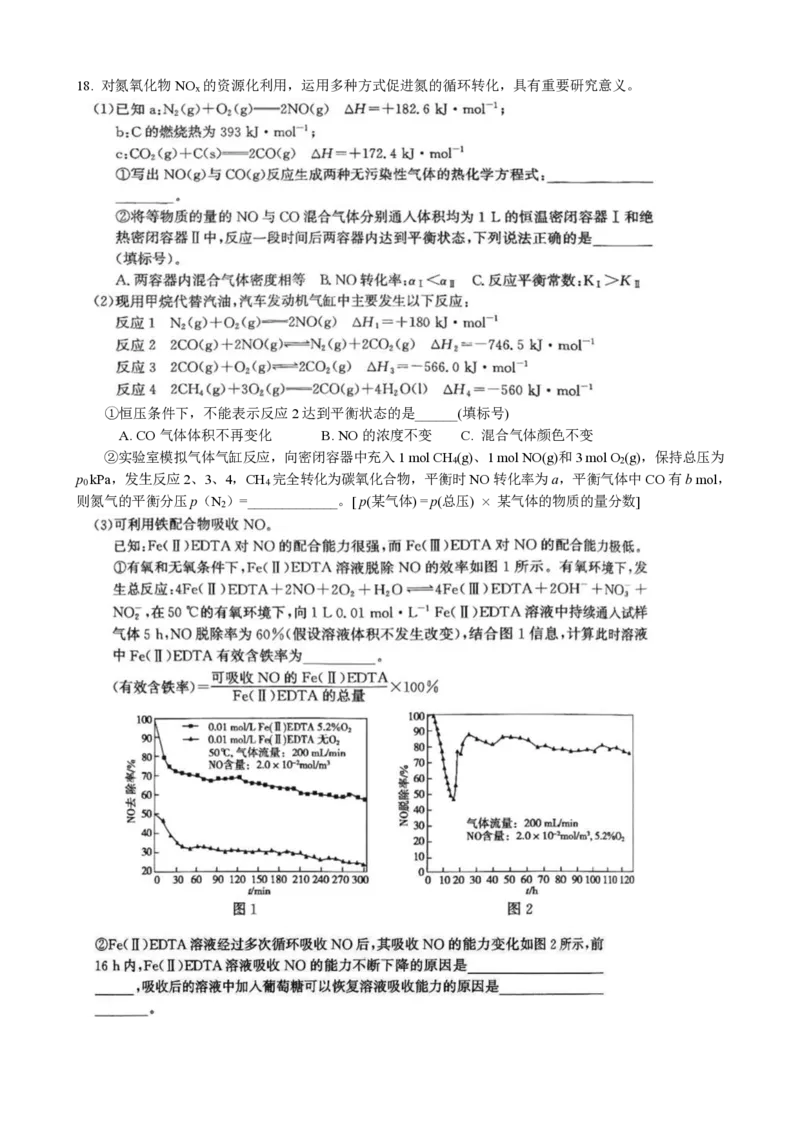
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}11. “分铜液净化渣”主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,回收工艺流程如图所示。
已知:①“碱浸”时,铜、锑转化为难溶物,碱浸液b含有Na TeO 、Na AsO 。
2 3 3 4
②“酸浸”时,浸渣中含锑元素生成难溶Sb O(SO ) ;SbCl 极易水解。
2 4 4 3
③常温下,H AsO 的各级电离常数为K =6.310−3、K =1.010−7、K =3.210−12。
3 4 a1 a2 a3
下列说法不正确的是( )
A.“碱浸”时,TeO 与NaOH反应的离子方程式为TeO +2OH− =TeO2−+H O
2 2 3 2
B.“氯盐酸浸”时,HCl的作用是作还原剂并防水解
C.滤液c中As元素主要存在形式为H AsO−
2 4
D.“水解”时,生成SbOCl的化学方程式为SbCl +H O=SbOCl+2HCl
3 2
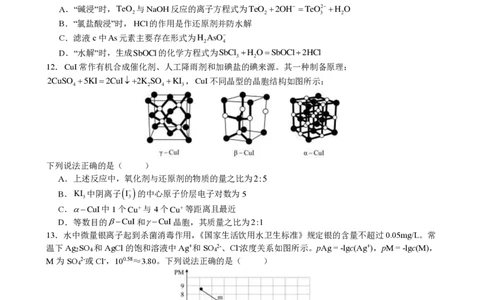
12.CuI常作有机合成催化剂、人工降雨剂和加碘盐的碘来源。其一种制备原理:
2CuSO +5KI=2CuI+2K SO +KI ,CuI不同晶型的晶胞结构如图所示:
4 2 4 3
下列说法正确的是( )
A.上述反应中,氧化剂与还原剂的物质的量之比为2:5
B.KI 中阴离子
( I−)
的中心原子价层电子对数为5
3 3
C.−CuI中1个Cu+与4个Cu+等距离且最近
D.等数目的−CuI和−CuI晶胞,其质量之比为2:1
13.水中微量银离子起到杀菌消毒作用,《国家生活饮用水卫生标准》规定银的含量不超过0.05mg/L。常
温下Ag SO 和AgCl的饱和溶液中Ag+和SO 2-、Cl-浓度关系如图所示。pAg = -lgc(Ag+),pM = -lgc(M),
2 4 4
M为SO 2-或Cl-,100.58≈3.80。下列说法正确的是( )
4
A.直线n表示AgCl饱和溶液中Ag+和Cl−浓度关系
B.某水体中银离子超标,用食盐无法消除其污染
C.P点对应的硫酸银溶液为过饱和溶液,静置有白色沉淀产生
D.向Ag SO 悬浊液中加入NaCl溶液,发生反应Ag SO (s)+2Cl−(aq) 2AgCl(s)+SO2−(aq),其
2 4 2 4 4
平衡常数K=3.801014
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}14.在5.0 MPa下,将5 mol CO 与16 mol H 在Cu/ZrO 催化剂作用下发生如下两个反应:
2 2 2
①CO (g)+3H (g) CH OH(g)+H O(g) ΔH 0
2 2 3 2 1
②CO (g)+H (g) CO(g)+H O(g) ΔH
2 2 2 2
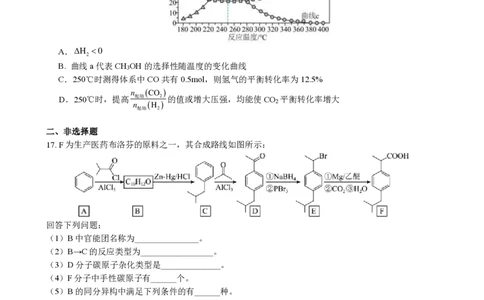
平衡时CH OH和CO的选择性及CO 的转化率随温度变化如图所示,下列说法正确的是( )
3 2
A.H 0
2
B. 曲线a代表CH OH的选择性随温度的变化曲线
3
C.250℃时测得体系中CO共有0.5mol,则氢气的平衡转化率为12.5%
n (CO )
D.250℃时,提高 起始 2 的值或增大压强,均能使CO 平衡转化率增大
n (H ) 2
起始 2
二、非选择题
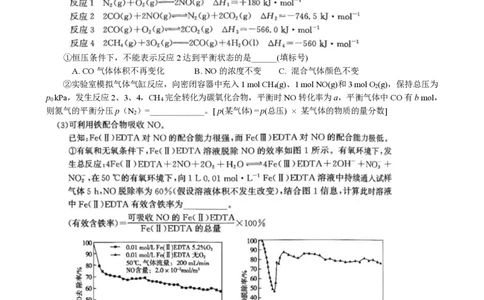
17. F为生产医药布洛芬的原料之一,其合成路线如图所示:
回答下列问题:
(1)B中官能团名称为_______________。
(2)B→C的反应类型为_________________。
(3)D分子碳原子杂化类型是______________。
(4)F分子中手性碳原子有______个。
(5)B的同分异构中满足下列条件的有______种。
a.含有两个−CH b.可发生银镜反应 c.苯环上有三个取代基
3
其中核磁共振氢谱有五组峰,峰面积之比为1:1:2:2:6的结构简式为__________________。
(6)参照上述合成路线图,设计以 、丙酮与乙醇为原料,制备 的合成路线(无机试剂
任选):
__________________________________________________________________________________。
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}18. 对氮氧化物NO 的资源化利用,运用多种方式促进氮的循环转化,具有重要研究意义。
x
①恒压条件下,不能表示反应2达到平衡状态的是______(填标号)
A. CO气体体积不再变化 B. NO的浓度不变 C. 混合气体颜色不变
②实验室模拟气体气缸反应,向密闭容器中充入1 mol CH (g)、1 mol NO(g)和3 mol O (g),保持总压为
4 2
p kPa,发生反应2、3、4,CH 完全转化为碳氧化合物,平衡时NO转化率为a,平衡气体中CO有b mol,
0 4
则氮气的平衡分压p(N 2 )=_____________。[ p(某气体) = p(总压) × 某气体的物质的量分数]
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}化学保温训练(二)参考答案
8.【答案】A
解析:中和滴定达终点前,滴入半滴标准液,用洗瓶冲洗锥形瓶内壁,使标准液流入锥形瓶与待测液反应,
减小误差,A正确;滴定操作时,左手无名指和小手指向手心弯曲,用其余三指控制活塞的转动,故B错
误;用蒸发法从食盐水中提取NaCl固体,应该用蒸发皿,故C错误;验证Cl 的助燃性,应该把燃着的氢
2
气放入纯净的氯气中,氢气能继续燃烧,D错误。
9.【答案】C
【分析】起始物质Fe (CO) (Ⅰ),在配体L、CO和Cs CO 作用下,转化为FeL(CO) ,这是催化剂的活
2 9 2 3 n
化过程,使催化剂具备催化活性。FeL(CO) (Ⅱ)与溴代烷烃R - Br反应,生成 (Ⅲ),
n
在这个过程中,R - Br的C - Br键断裂,R基团和Br原子分别与Fe原子成键。 (Ⅲ)与
CO发生羰基化反应,CO插入到Fe - R键之间,生成 (Ⅳ)。醇R'-OH作为亲核试剂,进
攻 (Ⅳ)中羰基的碳原子,形成 和 (Ⅴ) 。
(Ⅴ)与CO发生还原消除反应,生成HBr,同时FeL(CO) (Ⅱ)再生,从而完成催化循环,使反应能
n
够持续进行。
【详解】A.在配合物中,配位数是指与中心原子直接相连的配位原子的总数。观察Ⅰ的结构,Fe 与6
个CO 配体相连,所以Fe的配位数为6,A正确;
B. 催化剂在反应前后质量和化学性质不变。从反应机理图可以看出,Ⅱ参与反应后又在反应过程中再
生,符合催化剂的特征,所以Ⅱ为该反应的催化剂,B正确;
C.Ⅲ→Ⅳ,插入中性分子CO,且Fe的电负性小于C,Ⅲ→Ⅳ的转化中铁的化合价没有发生改变,C错
误;
D.从反应机理图中可以看出,反应物为CO、RBr、R'OH,生成物为RCOOR'和HBr,所以总催化反
应方程式为 催化剂 ,D正确;综上,答案C。
CO+RBr+ROH → RCOOR+HBr
10. 【答案】C
【分析】充电时阳离子移向阴极,由题干可知,锡电极为阴极,钾离子、锂离子在阴极得电子与锡发生
合金化形成合金;石墨为阳极,PF-到达石墨电极,插层进入石墨层间;则放电时,锡电极为负极,石墨
6
电极为正极。
【解析】A.由分析可知,放电时,锡电极为负极,A正确;
B.充电时,石墨电极为阳极,发生氧化反应,电极反应式为:C +PF--e-=C PF,B正确;
n 6 n 6
C.放电时,当有1mol电子转移时,合金在电极上失电子形成离子脱离电极,锡电极质量减少量无法计算,
C错误;
D.锂、钾与锡可形成合金,增强导电性和电容量,有利于电子的传输,极大的提升电池倍率性能及可逆
容量,D正确;故选C。
11.【答案】B
【分析】分铜液净化渣碱浸后,碱浸液中含Na TeO 、Na AsO ,铜元素和锑元素转化为氧化物或氢氧
2 3 3 4
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}化物,硫酸酸浸后得到Sb O(SO ) 沉淀,经过氯盐酸浸后得到SbCl ,水解后得到SbOCl,碱浸液中含
2 4 4 3
Na TeO 、Na AsO ,调节pH值后得到TeO 沉淀,据此解答。
2 3 3 4 2
【详解】A.碱浸液b含有Na TeO ,因此“碱浸”时,TeO 与NaOH反应的离子方程式为
2 3 2
TeO +2OH− =TeO2−+H O,A正确;
2 3 2
B.“氯盐酸浸”时,HCl的作用不是还原剂,其中作还原剂的是SO ,B错误;
2
c ( H+) c ( H AsO−) 10−4c ( H AsO−)
C.pH=4时,溶液为酸性,根据各级电离平衡常数分析,K = 2 4 = 2 4
a1 c(H AsO ) c(H AsO )
3 4 3 4
c
(
H
AsO−)
6.310−3
=6.3×10-3, 2 4 = =63,故滤液中As元素最主要的存在形式为H AsO−,C正确;
c(H AsO ) 10−4 2 4
3 4
D.“水解”时依据元素守恒可知还有氯化氢生成,生成SbOCl的化学方程式为
SbCl +H O=SbOCl+2HCl,D正确;
3 2
答案选C。
12.【答案】B
【详解】A.2CuSO (氧化剂)+3KI(还原剂)+2KI =2CuI+2K SO +KI 中,氧化剂与还原剂的物质的
4 2 4 3
量之比为2:3,A错误;
7+1−21
B.I−中I为中心原子,中心原子价层电子对数为2+ =5,B正确;
3 2
C.由图,−CuI中顶点Cu+与面心的12个Cu+等距离且最近,C错误;
D.−CuI中,8个Cu位于顶点、1个Cu位于体内,4个I位于棱上、1个I位于体内,据“均摊法”,
1 1
晶胞中含8 +1=2个Cu、4 +1=2个I,即1个晶胞含2个“CuI”;同理,−CuI晶胞中8个Cu位
8 4
于顶点、6个Cu位于面心,4个I位于晶胞内,含4个“CuI”;相等数目晶胞中,−CuI,−CuI晶胞
质量之比为1:2,D错误;
故选B。
13. 【答案】D
【详解】A.据斜率分析,直线n表示Ag SO 饱和溶液中Ag+和SO2−浓度关系,A错误;
2 4 4
B.直线m表示AgCl饱和溶液中c
( Ag+)
和c
( Cl−)
关系;要消除银污染,银的含量要0.05mg/L,即
c(Ag+)小于等于4.610−7molL−1,当c ( Ag+) 4.610−7molL−1时,
10−9.75
c ( Cl−) molL−1=2.210−3.75molL−1,因此,水体中银离子超标,可以用食盐消除其污染,B错
4.610−7
误;
C.P点位于直线n上方,对应的离子浓度小,为不饱和溶液,静置无沉淀产生,C错误;
D.由图像可以求得:K (Ag SO )=c2( Ag+) c ( SO2−) =0.1210−2.92 =10−4.92,
sp 2 4 4
K (AgCl)=c ( Ag+) c ( Cl−) =10−4.7510−5 =10−9.75,反应Ag SO (s)+2Cl−(aq) 2AgCl(s)+SO2−(aq),
sp 2 4 4
c ( SO2−) K (Ag SO ) 10−4.92
其平衡常数K= 4 = sp 2 4 = =1014.58 3.801014,D正确;
c2( Cl−) K2 (AgCl) 10−9.7510−9.75
sp
14.【答案】C
【详解】A.CH OH和CO的选择性之和应为100%,故曲线b代表CO 的转化率随温度的变化曲线。温
3 2
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}H 0
度升高,反应①平衡逆向移动,如果转化率增大,则反应②平衡必然要正向移动, 2 ,A错误;B.
曲线a代表CO的选择性,曲线b代表CH OH的选择性。B错误;C.250℃时测得体系中CO共有0.5mol,
3
2
根据图像知
n(CH
3
OH)=0.5mol
,故两个反应共消耗 2molH 2,故氢气的平衡转化率为16
100%=12.5%
,
n (CO )
起始 2
n (H )
C正确;D.提高 起始 2 的值,二氧化碳的平衡转化率减小;增大压强反应I平衡正向移动,可提高二
氧化碳的平衡转化率,D错误;故选C。
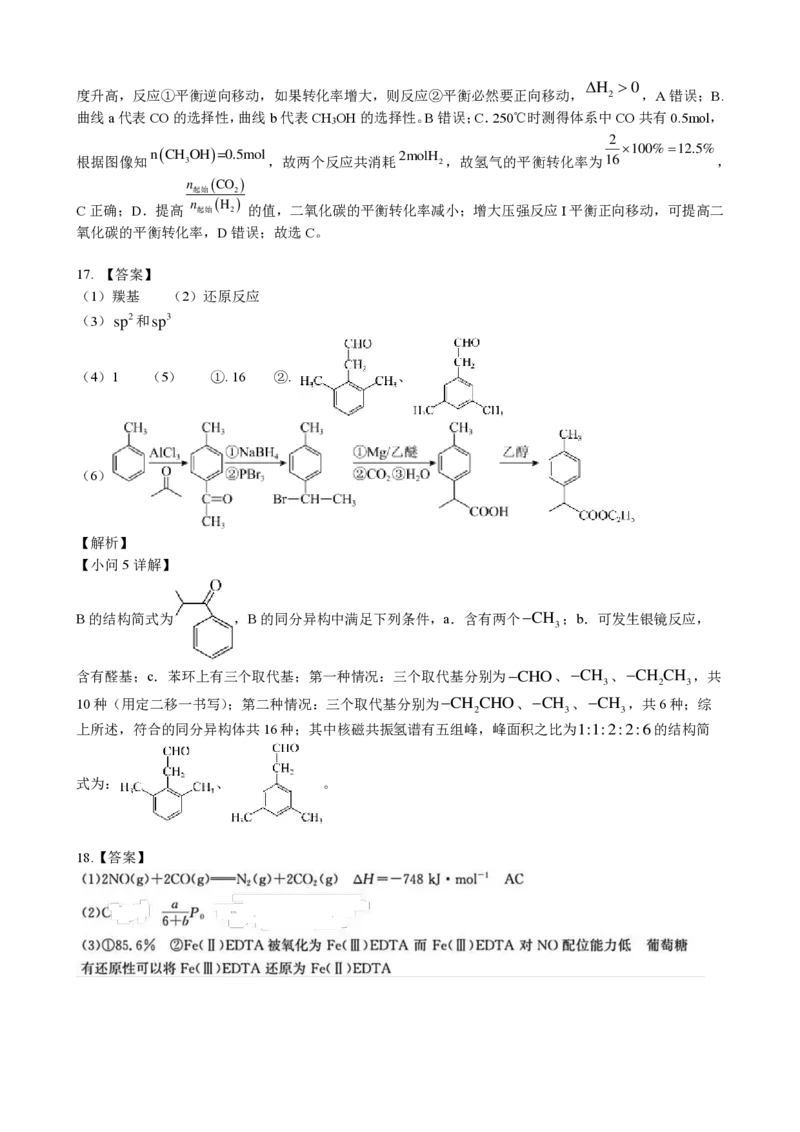
17. 【答案】
(1)羰基 (2)还原反应
(3)sp2和sp3
(4)1 (5) ①. 16 ②. 、
(6)
【解析】
【小问5详解】
B的结构简式为 ,B的同分异构中满足下列条件,a.含有两个−CH ;b.可发生银镜反应,
3
含有醛基;c.苯环上有三个取代基;第一种情况:三个取代基分别为−CHO、−CH 、−CH CH ,共
3 2 3
10种(用定二移一书写);第二种情况:三个取代基分别为−CH CHO、−CH 、−CH ,共6种;综
2 3 3
上所述,符合的同分异构体共16种;其中核磁共振氢谱有五组峰,峰面积之比为1:1:2:2:6的结构简
式为: 、 。
18.【答案】
{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}{#{QQABJYCoxgi4kBTACB4LEQF+CkoQkICjJWoMBQCZOAxLQIFABIA=}#}