文档内容
2015年厦门市初中毕业及高中阶段各类学校招生考试
化 学
(试卷满分:100分 考试时间:60分钟)
准考证号__________________姓名__________________座位号__________________
注意事项:
1.试卷分为Ⅰ、Ⅱ两卷,共18题,共5页,另有答题卡。
2.答案一律写在答题卡上,否则不能得分。
3.可能用到的相对原子质量:H-1 C-12 O-16 Mg-24 Cl-35.5 Zn-65
第Ⅰ卷 选择题(共10题,25分)
本卷第1~5题各2分,第6~10题各3分。每题只有一个选项符合题意,在答题卡选择题
栏内用2B铅笔将该选项涂黑。
1.夏天防雷电,远离金属。这是因为金属具有
A.导电性 B.导热性 C.延展性 D.光泽
2.下列物质属于氮肥的是
A.熟石灰 B.硫酸钾 C.过磷酸钙 D.氯化铵
3.下列过程仅发生物理变化的是
A.白磷自燃 B.蜡烛燃烧 C.干冰升华 D.呼吸作用
4.某同学体内缺少维生素,该同学饮食中需适量增加的食物是
A.米饭、面条 B.蔬菜、水果 C.瘦肉、鸡蛋 D.奶油、花生油
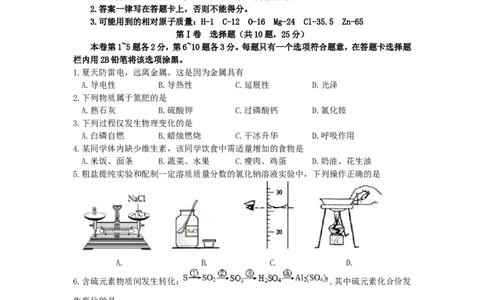
5.粗盐提纯实验和配制一定溶质质量分数的氯化钠溶液实验中,下列操作正确的是
A. B. C. D.
6.含硫元素物质间发生转化: ,其中硫元素化合价发
生变化的是
A.①② B.③④ C.①③ D.②④
7.新装修房室内存在甲醛(CHO)、苯(CH)等有害物质。下列叙述正确的是
2 6 6
A.甲醛分子中含有水分子 B.甲醛中碳元素质量分数为40%
C.苯中碳元素与氢元素的质量比为1:1 D.甲醛和苯都属于无机化合物
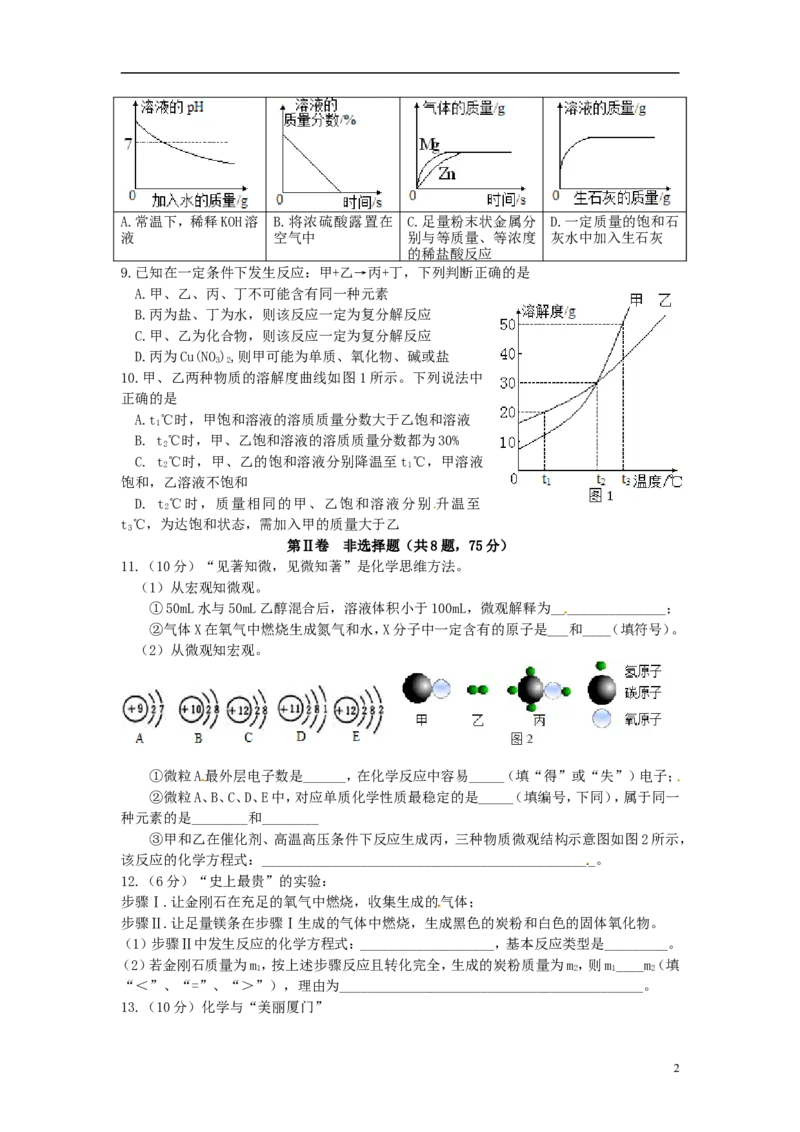
8.下列图像能正确反映对应变化关系的是
1A.常温下,稀释KOH溶 B.将浓硫酸露置在 C.足量粉末状金属分 D.一定质量的饱和石
液 空气中 别与等质量、等浓度 灰水中加入生石灰
的稀盐酸反应
9.已知在一定条件下发生反应:甲+乙→丙+丁,下列判断正确的是
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为盐、丁为水,则该反应一定为复分解反应
C.甲、乙为化合物,则该反应一定为复分解反应
D.丙为Cu(NO),则甲可能为单质、氧化物、碱或盐
3 2
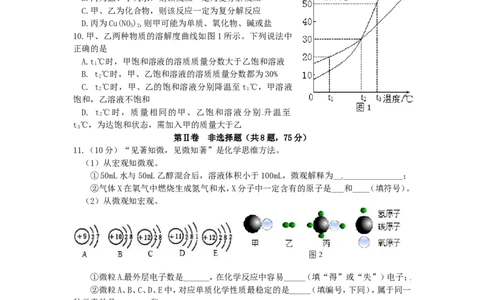
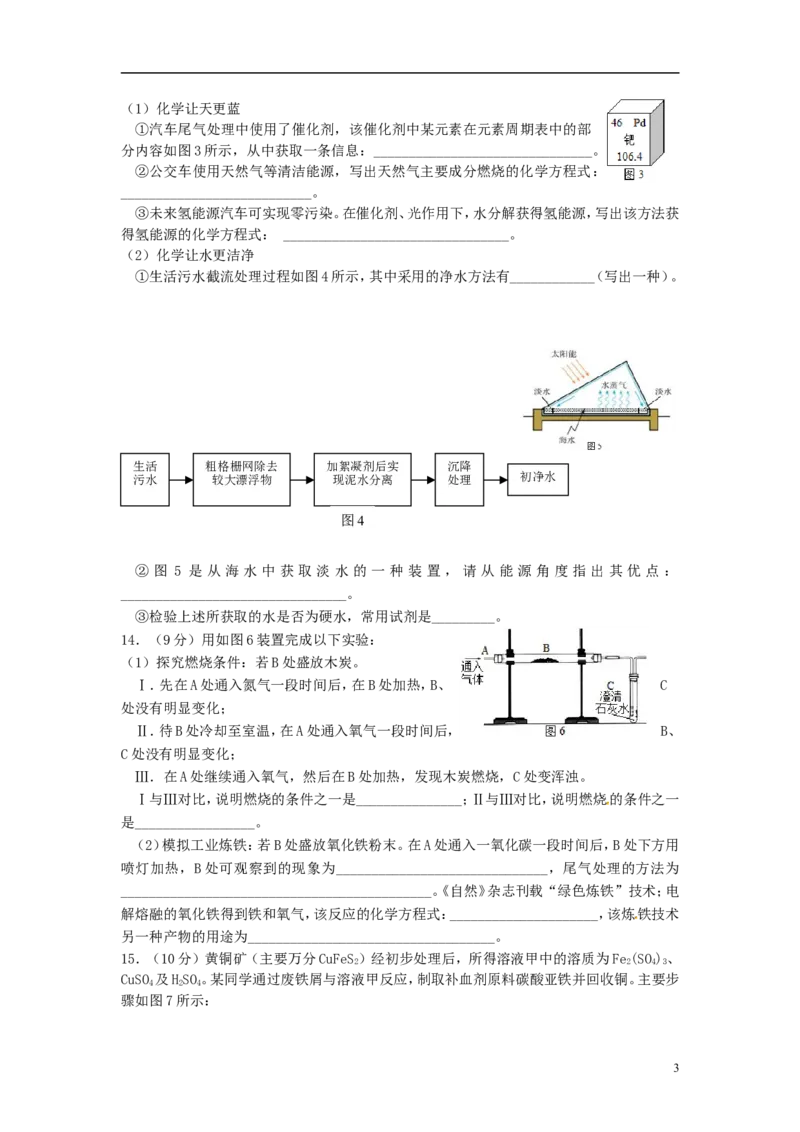
10.甲、乙两种物质的溶解度曲线如图1所示。下列说法中
正确的是
A.t℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
1
B. t℃时,甲、乙饱和溶液的溶质质量分数都为30%
2
C. t℃时,甲、乙的饱和溶液分别降温至t℃,甲溶液
2 1
饱和,乙溶液不饱和
D. t℃时,质量相同的甲、乙饱和溶液分别 升温至
2
t℃,为达饱和状态,需加入甲的质量大于乙
3
第Ⅱ卷 非选择题(共8题,75分)
11.(10分)“见著知微,见微知著”是化学思维方法。
(1)从宏观知微观。
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为________________;
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是___和____(填符号)。
(2)从微观知宏观。
①微粒A最外层电子数是______,在化学反应中容易_____(填“得”或“失”)电子;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是_____(填编号,下同),属于同一
种元素的是________和________
③甲和乙在催化剂、高温高压条件下反应生成丙,三种物质微观结构示意图如图2所示,
该反应的化学方程式:_______________________________________________。
12.(6分)“史上最贵”的实验:
步骤Ⅰ.让金刚石在充足的氧气中燃烧,收集生成的气体;
步骤Ⅱ.让足量镁条在步骤Ⅰ生成的气体中燃烧,生成黑色的炭粉和白色的固体氧化物。
(1)步骤Ⅱ中发生反应的化学方程式:___________________,基本反应类型是_________。
(2)若金刚石质量为m,按上述步骤反应且转化完全,生成的炭粉质量为m,则m____m(填
1 2 1 2
“<”、“=”、“>”),理由为___________________________________________。
13.(10分)化学与“美丽厦门”
2(1)化学让天更蓝
①汽车尾气处理中使用了催化剂,该催化剂中某元素在元素周期表中的部
分内容如图3所示,从中获取一条信息:_______________________________。
②公交车使用天然气等清洁能源,写出天然气主要成分燃烧的化学方程式:
___________________________。
③未来氢能源汽车可实现零污染。在催化剂、光作用下,水分解获得氢能源,写出该方法获
得氢能源的化学方程式: ________________________________。
(2)化学让水更洁净
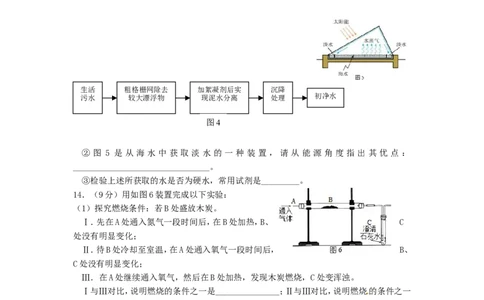
①生活污水截流处理过程如图4所示,其中采用的净水方法有____________(写出一种)。
生活 粗格栅网除去 加絮凝剂后实 沉降
污水 较大漂浮物 现泥水分离 处理 初净水
图4
② 图 5 是 从 海 水 中 获 取 淡 水 的 一 种 装 置 , 请 从 能 源 角 度 指 出 其 优 点 :
________________________________。
③检验上述所获取的水是否为硬水,常用试剂是_________。
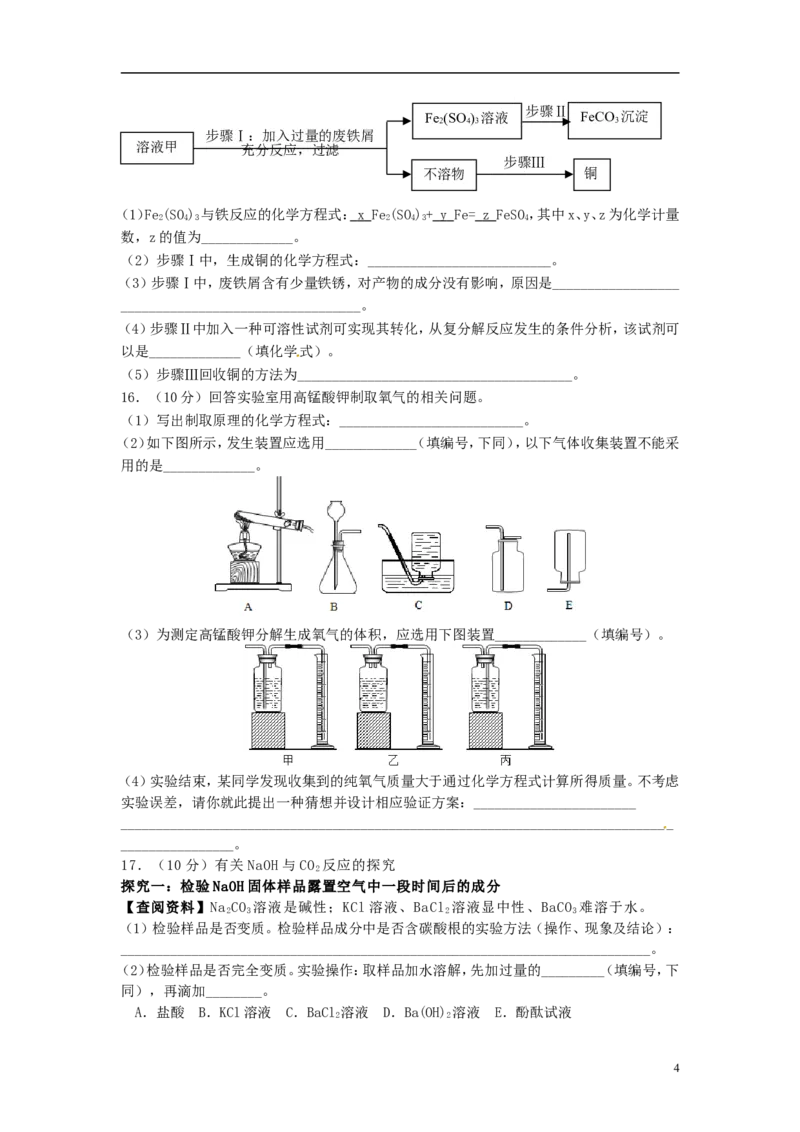
14.(9分)用如图6装置完成以下实验:
(1)探究燃烧条件:若B处盛放木炭。
Ⅰ.先在A处通入氮气一段时间后,在B处加热,B、 C
处没有明显变化;
Ⅱ.待B处冷却至室温,在A处通入氧气一段时间后, B、
C处没有明显变化;
Ⅲ.在A处继续通入氧气,然后在B处加热,发现木炭燃烧,C处变浑浊。
Ⅰ与Ⅲ对比,说明燃烧的条件之一是_______________;Ⅱ与Ⅲ对比,说明燃烧的条件之一
是_________________。
(2)模拟工业炼铁:若B处盛放氧化铁粉末。在A处通入一氧化碳一段时间后,B处下方用
喷灯加热,B处可观察到的现象为______________________________,尾气处理的方法为
____________________________________________。《自然》杂志刊载“绿色炼铁”技术;电
解熔融的氧化铁得到铁和氧气,该反应的化学方程式:_____________________,该炼铁技术
另一种产物的用途为___________________________________。
15.(10分)黄铜矿(主要万分CuFeS)经初步处理后,所得溶液甲中的溶质为Fe(SO)、
2 2 4 3
CuSO 及HSO。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步
4 2 4
骤如图7所示:
3步骤Ⅱ
Fe (SO ) 溶液 FeCO 沉淀
2 4 3 3
步骤Ⅰ:加入过量的废铁屑
溶液甲 充分反应,过滤
步骤Ⅲ
不溶物 铜
(1)Fe(SO) 与铁反应的化学方程式: x Fe(SO)+ y Fe= z FeSO,其中x、y、z为化学计量
2 4 3 2 4 3 4
数,z的值为_____________。
(2)步骤Ⅰ中,生成铜的化学方程式:__________________________。
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是__________________
__________________________________。
(4)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可
以是_____________(填化学式)。
(5)步骤Ⅲ回收铜的方法为_______________________________________。
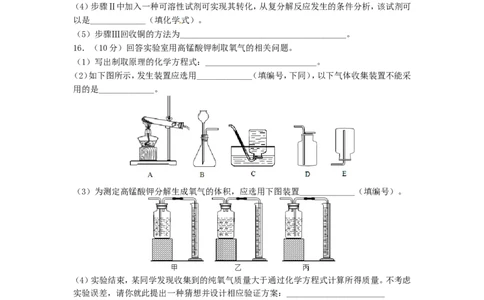
16.(10分)回答实验室用高锰酸钾制取氧气的相关问题。
(1)写出制取原理的化学方程式:__________________________。
(2)如下图所示,发生装置应选用_____________(填编号,下同),以下气体收集装置不能采
用的是_____________。
(3)为测定高锰酸钾分解生成氧气的体积,应选用下图装置_____________(填编号)。
(4)实验结束,某同学发现收集到的纯氧气质量大于通过化学方程式计算所得质量。不考虑
实验误差,请你就此提出一种猜想并设计相应验证方案:_______________________
______________________________________________________________________________
________________。
17.(10分)有关NaOH与CO 反应的探究
2
探究一:检验NaOH固体样品露置空气中一段时间后的成分
【查阅资料】Na CO 溶液是碱性;KCl溶液、BaCl 溶液显中性、BaCO 难溶于水。
2 3 2 3
(1)检验样品是否变质。检验样品成分中是否含碳酸根的实验方法(操作、现象及结论):
___________________________________________________________________________。
(2)检验样品是否完全变质。实验操作:取样品加水溶解,先加过量的_________(填编号,下
同),再滴加________。
A.盐酸 B.KCl溶液 C.BaCl 溶液 D.Ba(OH) 溶液 E.酚酞试液
2 2
4探究二:用NaOH溶液测定空气中酸性气体(CO、SO)的体积分数
2 2
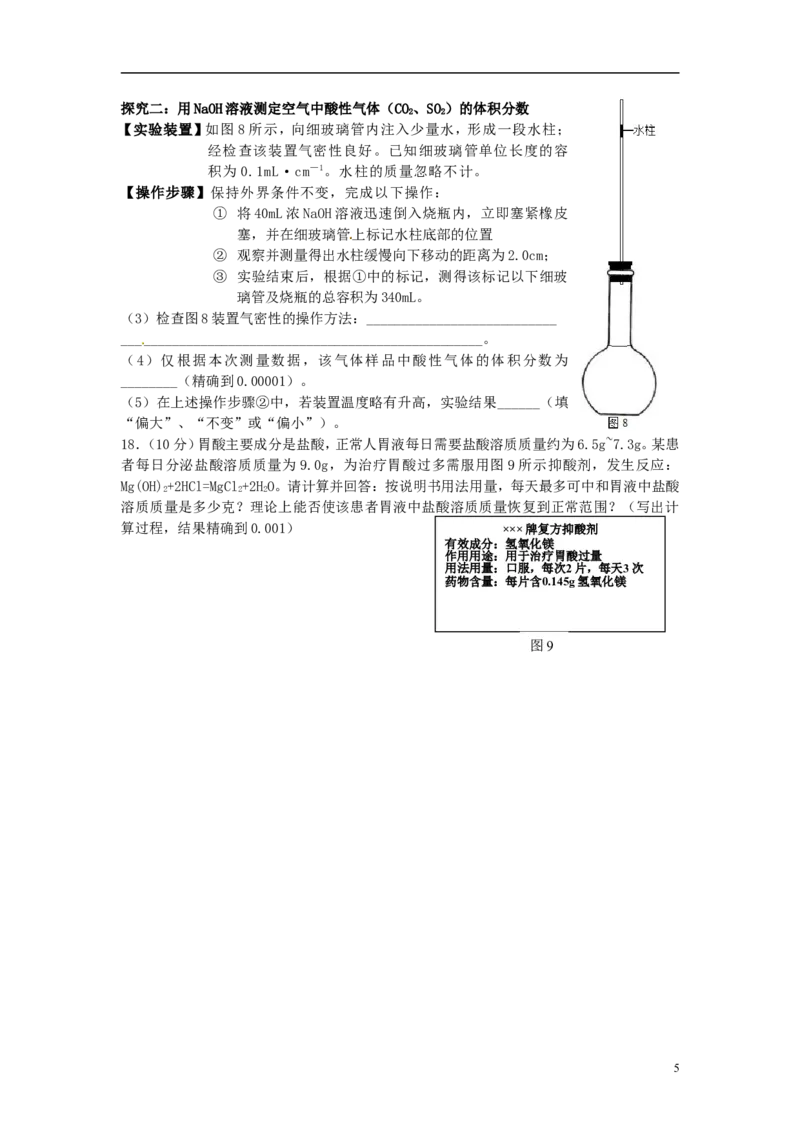
【实验装置】如图8所示,向细玻璃管内注入少量水,形成一段水柱;
经检查该装置气密性良好。已知细玻璃管单位长度的容
积为0.1mL·cm—1。水柱的质量忽略不计。
【操作步骤】保持外界条件不变,完成以下操作:
① 将40mL浓NaOH溶液迅速倒入烧瓶内,立即塞紧橡皮
塞,并在细玻璃管上标记水柱底部的位置
② 观察并测量得出水柱缓慢向下移动的距离为2.0cm;
③ 实验结束后,根据①中的标记,测得该标记以下细玻
璃管及烧瓶的总容积为340mL。
(3)检查图8装置气密性的操作方法:___________________________
___________________________________________________。
(4)仅根据本次测量数据,该气体样品中酸性气体的体积分数为
________(精确到0.00001)。
(5)在上述操作步骤②中,若装置温度略有升高,实验结果______(填
“偏大”、“不变”或“偏小”)。
18.(10分)胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g。某患
者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图9所示抑酸剂,发生反应:
Mg(OH)+2HCl=MgCl+2HO。请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸
2 2 2
溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计
算过程,结果精确到0.001) ×××牌复方抑酸剂
有效成分:氢氧化镁
作用用途:用于治疗胃酸过量
用法用量:口服,每次2片,每天3次
药物含量:每片含0.145g氢氧化镁
图9
52015年厦门市初中毕业及高中阶段各类学校招生考试化学
试题参考答案及评分标准
说明:1.化学方程式评分要求:每个化学方程式3分,所有化学式都正确1分,配平正确1分,
其他都正确1分。
2.开放性试题评分要求:只要学生的答案符合题意就按要求给分。
3.非选择题除化学方程式3分及特别注明外,其他每空各1分。
第Ⅰ卷选择题(共10题,25分)
本卷第1~5题各2分,第6~10题各3分。每题只有一个选项符合题意,在答题卡选择题
栏内用2B铅笔将该选项涂黑。
题号 1 2 3 4 5 6 7 8 9 10
答案 A D C B C A B C D D
第Ⅱ卷非选择题(共8题,75分)
11.(10分)(1)①分子间有间隔 ②N H
(2)①7 得 ②B C和E(两空全对共1分) ③CO+2H 催化剂 CHOH
2高温、高压 3
12.(6分)(1)2Mg+CO 点燃 2MgO+C 置换反应
2
(2)= 物质转化过程中元素质量守恒(或其他合理答案,两空全对给2分)
13.(10分)(1)①该元素原子序数为46(或其他合理答案)
②CH+2O 点燃 2HO+CO ③2HO催化剂 2H↑+O↑
4 2 2 2 2 光 2 2
(2)①过滤(或其他合理答案) ②节能 ③肥皂水
14.(9分)(1)氧气 温度达到着火点
(2)固体由红色变为黑色(2分)
将酒精灯放于导管口点燃尾气(或其他合理答案)
2FeO 通电4Fe+3O↑
2 3熔融 2
15.(10分)(1)3
(2)Fe+CuSO=Cu+FeSO
4 4
(3)铁锈与硫酸反应生成硫酸铁(2分)
(4)NaCO(或其他合理答案,2分)
2 3
(5)加入过量的稀硫酸,过滤、洗涤、干燥(或其他合理答案,2分)
16.(10分)(1)2KMnO △ KMnO+MnO+O↑
4 2 4 2 2
(2)A E (3)丙(2分)
(4)可能是产物KMnO 受热生成氧气;取KMnO 固体加热,用带火星的木条检验
2 4 2 4
是否生成氧气(或其他合理答案,3分)
17.(10分)
探究一:(1)取少量该样品,加入足量的稀盐酸,若有气体生成,把生成的气体通入澄清的石
灰水,石灰水变浑浊,说明该样品成分中含碳酸根。(3分)
(2)C E
探究二:(3)将图中装置直立于桌面一段时间后,如果水柱位置不发生移动,则说明装置气密
性良好。(或其他合理答案,2分)
(4)0.067%(2分)
(5)偏小
18.(10分)
解:设可消耗胃液中盐酸溶质质量为m
Mg(OH) + 2HCl = MgCl + 2HO
2 2 2
58 2×36.5
0.145×2×3 m
658 =2×36.5
0.145×2×3 m
m=1.095g
服药一天后胃液中剩余盐酸溶质质量=9.0g—1.095g=7.905g
7.905g>7.3g,不能恢复到正常范围。
答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是1.095g,理论上不能使该患
者胃液中盐酸溶质质量恢复到正常范围。
(说明:其他解法参考以上解题过程给分)
7