文档内容
微信公众号:文采学社
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
主讲老师 岳筱涵
粉笔教师教育 粉笔教师微信公众号:文采学社
说在课前
01 学习方法
课 前 课 中 课 后
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
提前预习 重在微理解,笔记次之 及时梳理
02 课堂要求
♣
我有问题要问老师,老师能马上回答吗?
♣ 声音小,网络卡怎么办?目
录
content
微信公众号:文采学社
1 化学计量
2 物质的组成、分类及变化
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微 3 离子反应
4 氧化还原反应微信公众号:文采学社
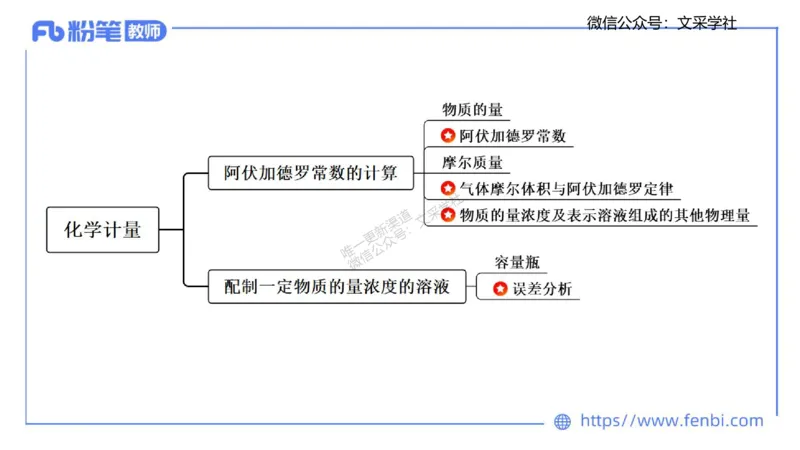
化学计量
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P3
一、物质的量与阿伏加德罗常数
(一)物质的量
物质的量是一个物理量,它表示含有一定数目粒子的集合体,符号是 n。
单位是摩尔,简称摩,符号是 mol。
社
学
作为物质的量的单位,mol 可以用来道计量采所有微观粒子,如分子、原子、
文
渠
:
新
号
更
众
一
离子、质子、中子、电子以及他们 唯 的特公定组合。如1 mol Fe、1 mol O 、1 mol
信 2
微
Na+、1 mol SO 2-等。
4微信公众号:文采学社
P4
【粉笔提示】
1.使用物质的量时,一定要指出物质的名称或写出物质的化学式,
它用来描述的是确切的物质。
如应写为1 mol H ,1 mol H+,而不能写成“1 mol氢”。
2
社
学
2.考生做题时要看好所问微粒的种类。 采
道
文
渠
:
新
号
更
众
如“2g 氢气所含氢原子的物质一的 公 量为 2 mol 而不是 1 mol ”。
唯
信
微
3. 物质的量与物质的质量有关而与物质所处的状态无关。微信公众号:文采学社
P4
(二)阿伏加德罗常数(N )
A
国际上规定,1mol 粒子集合体所含的粒子数约为 6.02×1023。
1mol 任何粒子的粒子数叫作阿伏加德罗常数,符号为 N ,通常用
A
6.02×1023mol–1 表示。
社N
n、N 、N(粒子数)之间的关系为:n
学
采
A 道 文
渠 : N
新 A
号
更
众
一
公
唯
信
微微信公众号:文采学社
P4
【粉笔提示】
1.阿伏加德罗常数的标准是人为规定的。 如果改变了它的标准,则
摩尔质量、气体摩尔体积、物质的量浓度等均发生改变。
而质量、粒子数、一定质量的气体体积、气体密度等客观存在因素
社
学
并不会因此而改变。 采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P4
2.关于阿伏加德罗常数的判断:
(1)计算微粒数目
①注意惰性气体为单原子分子;
②注意气体单质不一定是双原子分子;
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P4
③混合气体中某原子物质的量的计算:分别计算两种气体原子的最简整数
比(即实验式),若最简整数比相同,则混合气体质量与 M (实验式 / 最简式)
之比即为混合气体的最简式的物质的量。
(例:求 84g 乙烯和丙烯混合气体中 C 原子的物质的量)
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P4
④注意物质变化,气体单独存在或混合时可能发生某些反应,
如 NO 气体中存在 2NO N O 的反应,HCl 和 NH 混合会发生
2 2 2 4 3
反应,导致粒子数目发生变化。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P4
(2)计算转移电子数
⑤注意反应物量的多少,如 Cl 与 FeI 反应时,Cl 的量不同,生成物不同,
2 2 2
转移电子的数目也不同。
社
Cl 少量:2I- + Cl ===I + 2Cl- 学
2 2 2 道 采
文
渠
:
新
号
更
众
一
公
唯
信
2I- + Cl ===I + 2Cl- 微
2 2
Cl 过量:2Fe2+ + Cl ===2Cl- + 2Fe3+
2 2
总:4I- + 2Fe2+ + 3Cl ===6Cl- + 2Fe3+ + 2I
2 2微信公众号:文采学社
P5
(3)物质结构
⑥物质结构:
P :1 mol P 中存在6 mol P-P键
4 4
SiO :1 mol SiO 中存在4 mol Si-O键
2 2
社
金刚石:1mol金刚石中存在2 mol C-C键 学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P5
(4)溶液中粒子数目
⑦电离:先判断物质属于强电解质还是弱电解质,强电解质完全电离,
弱电解质不能完全电离,存在电离平衡,注意离子数目的变化。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
⑧水解:由于离子发生水解反应,导致自身离子数目减少。
微微信公众号:文采学社
讲义无
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P11
3. 已知 N 是阿伏加德罗常数的值。下列说法不正确的是( )。
A
A. 3g 3He 含有的中子数目为 N
A
B. 1mol K Cr O 被还原为 Cr3+ 时得到的电子数为 6N
2 2 7 A
社
C. 48g 正丁烷和 10g 异丁烷的混合物中共价学键数目为 13N
采
道 A
文
渠
:
新
号
更
众
一
D. 1L 0.1mol·L −1磷酸钠溶液中含有公的 Na+ 数目为 0.1N
唯
信 A
微微信公众号:文采学社
P5
二、摩尔质量
单位物质的量的物质所具有的质量叫作摩尔质量。
符号为 M,常用的单位为 g·mol-1。
1mol 任何粒子集合体都约含有 6.02×10 23 个粒子;而 1mol 任何粒子或物
社
学
质的质量以 g 为单位时,其数值与该粒子的相采对原子质量(Ar)或相对分子质
道
文
渠
:
新
号
更
众
量(Mr)相等。 一
公
唯
信
微
m
n,M,m 之间的关系为:n
M微信公众号:文采学社
P5
【粉笔提示】
相对原子质量、相对分子质量
相对原子质量(Ar):以一种碳原子质量的1/12作为标准,其他
原子的质量跟它相比较所得的比,就是这种原子的相对原子质量。单
社
学
位是“1”,一般不写出。 道 采
文
渠
:
新
号
更
众
一
某元素
唯
一公个原子的质量
信
相对原子质量 微
1
(一个12
C
原子的质量)
12
相对原子质量 ≈ 质子数(Z)+中子数(N)
相对分子质量(M ):化学式中各原子的相对原子质量的总和。
r微信公众号:文采学社
P11
1. 设 N 表示阿伏加德罗常数的值。下列叙述正确的是( )。
A
A. 0.1mol SiO 晶体中含有的 Si—O 键的数目为 0.2N
2 A
B. 3.6g CaO 晶体中阴离子的数目为 0.1N
2 A
社
学
采
道
文
渠
:
C. Cu 与浓硝酸反应生成 4.6g NO新 和 N O 混合气体时,转移的电子数
号
更
2 众 2 4
一
公
唯
信
微
为 0.1N
A
D. 18g H O 和 D O 的混合物中,所含电子的数目为 9N
2 2 A微信公众号:文采学社
P5
三、气体摩尔体积与阿伏加德罗定律
(一)气体摩尔体积
单位物质的量的气体所占的体积叫作气体摩尔体积,符号为V ,
m
常用单位为 L·mol-1。
V 社
学
V 、V、n之间的关系为:n 道 采
文
m 渠
:
V新
号
更
一
m众
公
唯
信
微微信公众号:文采学社
P6
粉笔提示
物质体积的大小主要由三个因素决定:
①构成物质微粒的多少;
②粒子之间的距离;
社
学
③粒子本身的大小。 采
道
文
渠
:
新
号
更
一
众
公
唯
信
微微信公众号:文采学社
P6
气体摩尔体积的数值不是固定不变的,它取决于气体所处的温度和压强。
只要温度、压强一定,气体分子间的平均距离就一定,气体摩尔体积就是一
个定值。
标准状况,即在 0℃和101 kPa的条件下,V 约为22.4 L·mol-1。
m社
学
采
道
文
常温常压下(25℃和101 kPa),气体渠分:子间的平均距离变大,则 V >
新
号 m
更
众
一
公
唯
信
22.4 L·mol-1。
微微信公众号:文采学社
P6
【粉笔提示】
1.气体摩尔体积为 22.4L/mol 的使用条件:
①标准状况;
②物质在标准状况下是气体。
社
学
不在标准状况下或物质在标准状况下不是采气体都不适用。固体和
道
文
渠
:
新
号
更
众
液体也有摩尔体积,但数值一般不相一同。
公
唯
信
微
例如:a.标准状况下,新戊烷、环己烷、辛烷、苯、四氯化碳、
溴、水、SO 均不是气体,以上均不适用。
3
b.“1 mol水蒸气在标准状况下所占的体积是22.4 L”这种表述不
正确。微信公众号:文采学社
P6
2.气体摩尔体积研究的对象是气体(包括混合气体),但概念中的
“任何气体”不包括一些易挥发性物质的蒸气,如水蒸气、溴蒸气、碘
蒸气等。
3.并非只有在标准状况下,1 mol气体的体积才约是22.4 L。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P11
4. 设 N 为阿伏加德罗常数的值。下列说法正确的是( )。
A
A. 2g D O 中含有的质子数、中子数、电子数均为 N
2 A
B. 0.1mol 氯酸钾与足量浓盐酸反应生成氯气时转移电子数为 0.6N
A
社
C. 1L 0.1mol·L–1 NaHSO 溶液中含有的阳离学子数目为 0.1N
采
4 道 A
文
渠
:
新
号
更
众
一
D. 标准状况下,2.24L SO 与足量氧公气充分反应,生成 SO 的分子数
唯
2 信 3
微
为 0.1N
A微信公众号:文采学社
P11
6. 设N 为阿伏加德罗常数的值,下列说法正确的是( )。
A
A. 1mol 乙酸和 1mol 乙醇充分反应生成的水分子数为N
A
B. 常温常压下,3.0g 含甲醛的冰醋酸中含有的原子总数为 0.4N
A
社
学
采
道
文
渠
C. 标准状况下,1.12L 甲醇中碳原子的:数目为 0.05N
新
更 号 A
众
一
公
唯
信
微
D. 1L1mol/L 的 NaClO 溶液中含有 ClO-的数目为N
A微信公众号:文采学社
P6
(二)阿伏加德罗定律及其推论
1.阿伏加德罗定律
同温、同压下,相同体积的任何气体都含有相同数目的分子。
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
P7
2.阿伏加德罗定律的推论
结论
条件
公式 语言叙述
社
学
T、p 相同 同温、同压下,气体采的体积与其物质的量成正比
道
文
渠
:
新
号
更
众
一
公
唯
信
T、V 相同 温度、体微积相同的气体,其压强与其物质的量成正比
T、p 相同 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比微信公众号:文采学社
P7
【粉笔提示】
对阿伏加德罗定律的理解要明确三点:
1.适用范围:气体;
2.同温、同压、同体积、同分子数(同物质的量),即四同。四
社
学
同相互制约,只要三同成立,则第四同也成立采;只要两同成立,则另
道
文
渠
:
新
号
更
众
两项一定成比例,即可概括为:三同一定一同,二同成比例。
公
唯
信
微
3. 标准状况下的气体摩尔体积是阿伏加德罗定律的一个特例。微信公众号:文采学社
P7
四、物质的量浓度
(一)表示方法
物质的量浓度表示单位体积的溶液里所含溶质 B 的物质的量,也
称为 B 的物质的量浓度,符号为 c 。单位是 mol/L。物质的量浓度是
B
社
学
表示溶液组成的物理量。 道 采
文
渠
:
新
号
更
n 一 众
计算公式:
唯
公
c B 信
微
B
V
n :溶质 B 的物质的量,单位为 mol;
B
V:溶液的体积,单位为 L。微信公众号:文采学社
P8
【粉笔提示】
1.物质的量浓度的概念中,体积是溶液的体积而不是溶剂的体积;
一般来说单位是 L 而不是 mL;溶质的量是物质的量而不是质量。
2. 正确判断溶液中溶质的化学成分,溶质可以是化合物,也可以
社
学
是离子或其他特定组合,但溶于水后溶质可能采会发生变化:如 SO
道
渠 文 3
:
新
号
更
众
H SO ,CuSO ·5H O CuSO ,一 N公a、Na O、Na O NaOH 等。
唯
2 4 4 2 4 信 2 2 2
微
再比如 NH 溶于水得 NH ·H O,但习惯上认为氨水的溶质是 NH 。
3 3 2 3
3.同一溶液,无论取出多大体积,其各种浓度(物质的量浓度、
溶质的质量分数、离子浓度)均不变。微信公众号:文采学社
P11
5.用 N 表示阿伏加德罗常数的值,下列说法正确的是( )。
A
A. 18g 14CH 中所含中子数为 10N
4 A
B. 1mol Na O 与水完全反应,转移的电子数为 N
2 2 A
社
学
采
道
文
渠
C. 2mol SO 与 1mol O 在一定条件下充:分反应生成 SO 的分子数为 2N
新
2 2 更 号 3 A
众
一
公
唯
信
微
D. 10mL pH=11 的 KOH 溶液中,水电离出的 OH– 的数目为 1.0×10–5 N
A微信公众号:文采学社
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微微信公众号:文采学社
社
学
采
道
文
渠
:
新
号
更
众
一
公
唯
信
微
粉笔教师教育 粉笔教师