文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
鄂州市2023年初中学业水平考试
化学
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40
第Ⅰ卷 选择题(共44分)
一、选择题(每小题只有一个选项符合题意,本大题共22小题,每小题2分,共44分)
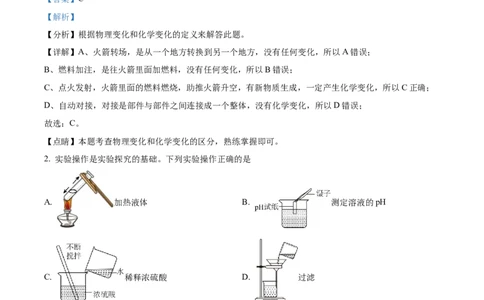
1. 2021年5月30日5时01分,我国天舟二号货运飞船与天和核心舱完成自主快速交会对接,引起世界关
注,下列过程中一定发生化学变化的是
A. 火箭转场 B. 燃料加注 C. 点火发射 D. 自动对接
【答案】C
【解析】
【分析】根据物理变化和化学变化的定义来解答此题。
【详解】A、火箭转场,是从一个地方转换到另一个地方,没有任何变化,所以A错误;
B、燃料加注,是往火箭里面加燃料,没有任何变化,所以B错误;
C、点火发射,火箭里面的燃料燃烧,助推火箭升空,有新物质生成,一定产生化学变化,所以C正确;
D、自动对接,对接是部件与部件之间连接成一个整体,没有化学变化,所以D错误;
故选:C。
【点睛】本题考查物理变化和化学变化的区分,熟练掌握即可。
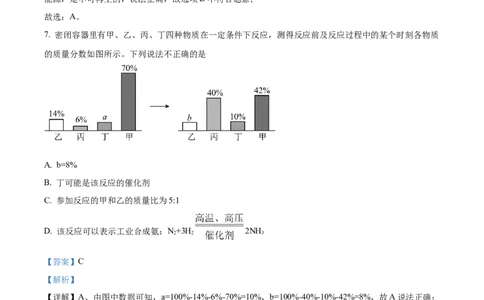
2. 实验操作是实验探究的基础。下列实验操作正确的是
A. 加热液体 B. 测定溶液的pH
C. 稀释浓硫酸 D. 过滤
【答案】A
【解析】
【详解】A、加热试管中的液体时,用外焰加热,液体不超过试管容积的三分之一,试管夹夹在中上部,
试管口斜向上,与水平方向大约成45°夹角,图示操作正确;
B、用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸
取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH,不能将pH试纸伸入待测液中,
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
以免污染待测液,图示操作错误;
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散,
一定不能把水注入浓硫酸中,以防止酸液飞溅,图示操作错误;
D、过滤时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,图示操作错误;
故选:A。
3. 下列物质中,属于纯净物的是
A. 水泥砂浆 B. 液态氧 C. 洁净的空气 D. 汽水
【答案】B
【解析】
【详解】A、水泥砂浆中含有水泥、水、沙等物质,属于混合物,故A错误;
B、液态氧中只含有氧气分子,属于纯净物,故B正确;
C、空气中含有氮气、氧气等物质,属于混合物,故C错误;
D、汽水中含有水、糖等物质,属于混合物,故D错误;
故选B。
4. “端午时节粽飘香。”据研究,粽子的香味来源于粽叶中含有的对乙烯基苯酚(化学式为C HO)。下
8 8
列有关对乙烯基苯酚的说法正确的是
A. 对乙烯基苯酚属于有机物
B. 对乙烯基苯酚中含有4个氢分子
C. 对乙烯基苯酚中氢元素的质量分数最大
D. 对乙烯基苯酚中碳元素和氧元素的质量比为8:1
【答案】A
【解析】
【详解】A、对乙烯基苯酚是含碳元素的化合物,属于有机物,故选项说法正确;
B、对乙烯基苯酚是由对乙烯基苯酚分子构成的,不含有氢分子,故选项说法错误;
C、对乙烯基苯酚中碳元素、氢元素和氧元素的质量比为(12×8):(1×8):(16×1)=12:1:2,其中
碳元素的质量分数最大,故选项说法错误;
D、对乙烯基苯酚中碳元素和氧元素的质量比为(12×8):(16×1)=6:1,故选项说法错误;
故选:A。
5. 铷是一种重要的化学元素,可应用于原子钟、卫星导航、计算机通信等。铷原子的结构示意图及其在元
素周期表中的信息如图所示。下列说法正确的是
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 铷原子在化学反应中易得到电子
B. 铷原子的中子数是37
C. 铷的相对原子质量是85.47g
D. 铷位于元素周期表第5周期
【答案】D
【解析】
【详解】A、在原子中,质子数=核外电子数,则37=2+8+18+8+x,x=1,最外层电子数是1,小于4,在化
学反应中易失去1个电子而形成阳离子,故选项说法错误;
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为37,汉字下方的数
字表示相对原子质量,该元素的相对原子质量为85.47;根据原子中原子序数=核电荷数=质子数,则该原
子的核内质子数为37;根据在原子中,质子数+中子数=相对原子质量,铷的相对原子质量为85.47,不是
质子数的两倍,则原子核内中子数不等于37,故选项说法错误;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为85.47,
相对原子质量单位是“1”,不是“g”,通常省略,故选项说法错误;
D、周期数=原子核外电子层数,铷元素的原子核外有5个电子层,则在元素周期表中,铷元素位于第五周
期,故选项说法正确;
故选:D
6. 归纳与总结是学习化学的基本方法。下列知识点归纳与总结完全正确的一组是
A. 化学与生活 B. 化学与安全
①生活中用煮沸的方法给水杀菌消毒 ①在煤炉上放一盆水不能防止一氧化碳中毒
②用活性炭吸附冰箱中的异味 ②室内起火,立即开窗通风
C. 化学与健康 D. 化学与社会
①人体缺乏维生素A会患夜盲症
①合成纤维、合成橡胶、合金属于合成材料
②霉变的大米经淘洗干净煮熟后就可以食
②煤、石油、天然气属于化石能源,是不可再生的
用
A. A B. B C. C D. D
【答案】A
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【解析】
【详解】A、①生活中用煮沸的方法给水杀菌消毒,说法正确;②活性炭具有吸附性,可用活性炭吸附冰
箱中的异味,说法正确,故选项A符合题意;
B、①一氧化碳难溶于水,在煤炉上放一盆水不能防止一氧化碳中毒,说法正确;②室内起火,不能立即
开窗通风,以防空气流通造成火势蔓延,说法错误,故选项B不符合题意;
C、①人体缺乏维生素A会患夜盲症,说法正确;②霉变的大米经淘洗干净煮熟后也不可以食用,以防危
害人体健康,说法错误,故选项C不符合题意;
D、 ①合成纤维、合成橡胶属于合成材料,合金属于金属材料,说法错误;②煤、石油、天然气属于化石
能源,是不可再生的,说法正确,故选项D不符合题意;
故选:A。
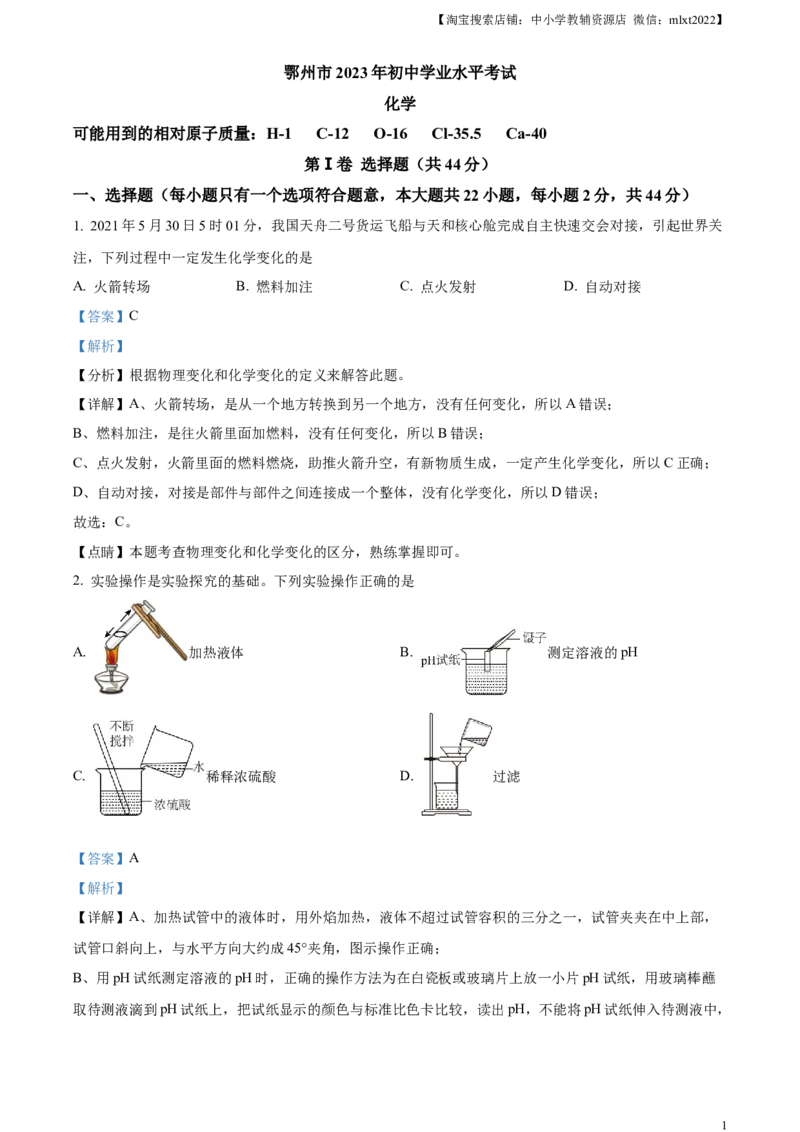
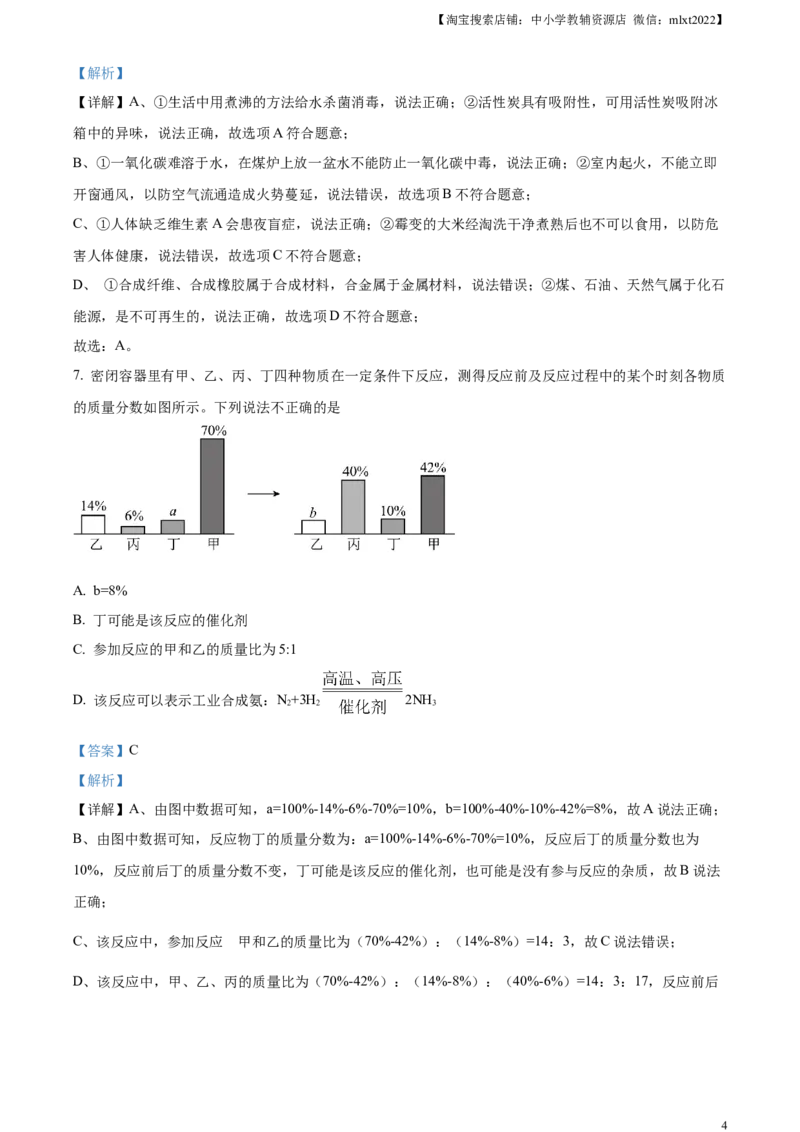
7. 密闭容器里有甲、乙、丙、丁四种物质在一定条件下反应,测得反应前及反应过程中的某个时刻各物质
的质量分数如图所示。下列说法不正确的是
A. b=8%
B. 丁可能是该反应的催化剂
C. 参加反应的甲和乙的质量比为5:1
D. 该反应可以表示工业合成氨:N+3H 2NH
2 2 3
【答案】C
【解析】
【详解】A、由图中数据可知,a=100%-14%-6%-70%=10%,b=100%-40%-10%-42%=8%,故A说法正确;
B、由图中数据可知,反应物丁的质量分数为:a=100%-14%-6%-70%=10%,反应后丁的质量分数也为
10%,反应前后丁的质量分数不变,丁可能是该反应的催化剂,也可能是没有参与反应的杂质,故B说法
正确;
的
C、该反应中,参加反应 甲和乙的质量比为(70%-42%):(14%-8%)=14:3,故C说法错误;
D、该反应中,甲、乙、丙的质量比为(70%-42%):(14%-8%):(40%-6%)=14:3:17,反应前后
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
丁的质量分数不变,可能是该反应的催化剂,工业合成氨为: ,合成氨的反
应中N、H、NH 的质量比为28:6:34=14:3:17,所以该反应可以表示工业合成氨,故D说法正确;
2 2 3
故选:C。
8. 鉴别、检验、除杂和分离是认识和研究物质的常用方法。下列实验方案不能达到目的的是
选项 实验目的 实验方案
A 鉴别酒精和水 闻气味
B 检验CO中是否含有CO 将气体通入澄清石灰水,观察是否变浑浊
2
C 除去MnO 中混有的少量KCl固体 加足量水溶解、过滤、洗涤、干燥
2
D 分离锌粉和铜粉 加足量的稀硫酸,过滤
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、闻气味,可以鉴别酒精和水,有酒的芳香气味的是酒精,无明显气味的是水,故选项实验方
案能达到目的;
B、二氧化碳能使澄清石灰水变浑浊,将气体通入澄清石灰水,观察是否变浑浊,可检验CO中是否含有
CO,故选项实验方案能达到目的;
2
C、KCl易溶于水,MnO 难溶于水,可用加足量水溶解、过滤、洗涤、干燥分离得到二氧化锰,故选项实
2
验方案能达到目的;
D、加足量的稀硫酸,锌能与稀硫酸反应生成硫酸锌和氢气,铜不与稀硫酸反应,过滤,能分离出铜,但
无法分离出锌,故选项实验方案不能达到目的;
故选:D。
9. 下列各组物质在NaOH溶液中能大量共存且溶液为无色的是
A. NaNO 、NH Cl 、KMnO 、Ba(NO )
3 4 4 3 2
B. KSO 、KOH 、NaNO 、NaCl
2 4 3
C. NaSO 、Ca(NO ) 、BaCl KCl
2 4 3 2 2 、
D. KNO 、 NaCO 、MgCl 、HSO
3 2 3 2 2 4
【答案】B
【解析】
【详解】A、氢氧化钠与氯化铵反应,生成氯化钠、氨气、水,高锰酸钾溶液呈紫红色,A错误;
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
B、氢氧化钠、硫酸钾、氢氧化钾、硝酸钠、氯化钠几种物质间不发生反应,且溶液均为无色,B正确;
C、硫酸钠与氯化钡反应,生成硫酸钡沉淀、氯化钠,两种物质不能大量共存,C错误;
D、碳酸钠与硫酸发生反应,生成硫酸钠、水、二氧化碳,两种物质不能大量共存,D错误。
故选B。
10. 图像能直观表达各种变化关系,加深对知识的理解。下列对有关图像的描述正确的是
A. ①表示向一定量的Ba(OH) 溶液中加水
2
B. ②表示一定的温度时,向NaCl饱和溶液中加入NaCl固体并搅拌
C. ③表示电解水
D. ④表示加热分解一定质量的氯酸钾和二氧化锰固体混合物
【答案】C
【解析】
【详解】A、Ba(OH) 溶液呈碱性,溶液的pH大于7,向一定量的Ba(OH) 溶液中加水时,溶液的碱
2 2
性减弱,pH变小,但溶液始终呈碱性,其pH始终大于7,不可能小于等于7,故A图像错误;
的
B、一定 温度时,向NaCl饱和溶液中加入NaCl固体并搅拌,氯化钠固体并不能继续溶解,因此溶液中
溶质的质量分数不变,故B图像错误;
C、电解水实验中,根据正氧负氢,氧一氢二,即生成氢气与氧气的体积比约为2:1,故C图像正确;
D、氯酸钾在二氧化锰的催化作用下,加热分解为氯化钾和氧气,在此反应中,二氧化锰作为催化剂,其
质量保持不变,因此固体中锰元素的质量保持不变,故D图像错误;
故选C。
二、非选择题(本大题共7小题,35—40题每空1分,第41题6分,共30分)
11. 化学用语是简明扼要、信息丰富、国际通用的语言。请用化学用语填空:
(1)氦气________。
(2)人体中含量最多的金属元素_________。
(3)标出氧化铝中铝元素的化合价________。
(4)两个硫离子________。
【答案】(1)He (2)Ca
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(3)
(4)2S2-
【解析】
【小问1详解】
氦气属于稀有气体,氦气是由氦原子直接构成的,化学式直接用元素符号表示为He;
【小问2详解】
书写元素符号时应注意:由一个字母表示的元素符号要大写;由两个字母表示的元素符号,第一个字母大
写,第二个字母小写。人体中含量最多的金属元素是钙元素,表示为Ca;
【小问3详解】
氧化铝中氧元素显示-2价,根据在化合物中元素正负化合价代数和为0,设铝元素的化合价为x,则有2x+
(-2)×3=0,解得x=+3,根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在
其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,数值为1时,不能省略;氧化铝中
铝元素显+3价表示为: ;
【小问4详解】
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号
在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字。2个硫离子表示
为2S2-。
12. 鄂州花湖机场是客运和货运两用机场,年内将开通40条国内货运航线、6条国际货运航线,正向国际
一流航空货运枢纽目标迈进。“五一”期间,小琳随父母乘车到花湖机场游玩。
(1)途经花马湖,她见湖水清澈透明,想知道湖水是硬水还是软水,可向湖水的水样中加入______进行
检验。
(2)到达机场入口,一股浓郁的花香扑鼻而来,请从分子的角度解释原因__________。
(3)抵达航站楼,她看到一棵植株矮小、叶色发黄的树苗,你认为应施加下列化肥中的 (填字
母序号)。
A. NH HCO B. Ca (PO ) C. KSO
4 3 3 4 2 2 4
(4)进入候机厅,她看到消防柜里存放的二氧化碳灭火器,请写出用二氧化碳灭火器灭火的原理
________。
【答案】(1)肥皂水 (2)分子在不断运动 (3)A
(4)隔绝空气(或氧气)和降低温度至可燃物的着火点以下
【解析】
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【小问1详解】
用肥皂水可以鉴别硬水和软水,加入肥皂水,振荡,产生泡沫较多的是软水,产生泡沫较少、浮渣较多的
是硬水;
【小问2详解】
一股浓郁 的花香扑鼻而来,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香;
【小问3详解】
氮肥能使农作物枝叶繁茂、叶色浓绿、提高产量;某农民种植的小麦植株矮小,叶色发黄,说明土壤中缺
乏氮元素,因此选氮肥;
A、NH HCO 中只含有氮、磷、钾三种元素中的氮元素,属于氮肥,符合题意;
4 3
B、Ca (PO ) 中只含有氮、磷、钾三种元素中的磷元素,属于磷肥,不符合题意;
3 4 2
C、KSO 中只含有氮、磷、钾三种元素中的钾元素,属于钾肥,不符合题意;
2 4
故选A;
【小问4详解】
二氧化碳灭火器的灭火原理是液体二氧化碳汽化时吸收大量的热,降低温度至可燃物的着火点以下,同时
二氧化碳气体覆盖在可燃物表面,隔绝氧气,达到灭火效果。
13. 如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线图,请回答下列问题:
(1)P点的含义是________。
(2)O 的溶解度随温度变化的趋势与图中________物质相似。
2
(3)t℃时,将60gA物质加到50g水中,充分溶解后,所得到溶液的质量为_____g。
3
(4)t℃ 时,等质量的A、B、C三种物质的饱和溶液分别降温到t℃,对所得溶液的分析不正确的是
3 1
_____(填序号)。
①溶解度:B>A>C
②溶剂质量:C>B>A
③溶液质量:B>A>C
④溶质质量分数:B>A>C
【答案】(1)t℃时,A、B两种物质的溶解度相等
2
(2)C (3)80
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(4)①③##③①
【解析】
【小问1详解】
P点的含义是:t℃时,A、B两种物质的溶解度相等;
2
【小问2详解】
气压一定的条件下,气体的溶解度随温度的升高而减小,所以O 的溶解度随温度变化的趋势与C相似;
2
【小问3详解】
设t℃时,A物质的溶解度是x,则 , ,所以将60gA物质加到50g水中充分溶解后,
3
只能溶解30g的A物质,所以所得溶液的质量为30g+50g=80g;
【小问4详解】
①由溶解度曲线可知,t℃时,溶解度:B>A=C,①错误;
1
②根据溶液质量=溶质质量+溶剂质量可知,溶液质量一定,溶质质量越大,溶剂质量越小,t℃时,A物
3
质的溶解度最大,C物质的溶解度最小,因此等质量的A、B、C三种物质的饱和溶液中溶剂质量C>B>
A,分别降温到t℃,不会影响溶剂质量的变化,②正确;
1
③降低温度,C物质的溶解度增大,不会析出晶体,A物质的溶解度受温度变化影响较大,B物质的溶解
度受温度变化影响较小,等质量的饱和溶液,降温后,A物质析出的晶体较多,所以溶液质量:C>B>
A,③错误;
④降温后,A、B溶解度减小,析出晶体,还是饱和溶液,降温之后溶解度B大于A,溶质质量分数B大
于A;降温之后C溶解度变大,变为不饱和溶液,溶质质量分数不变,降温之前C溶解度最小,故降温后
溶质质量分数B>A>C,④正确;
故选①③。
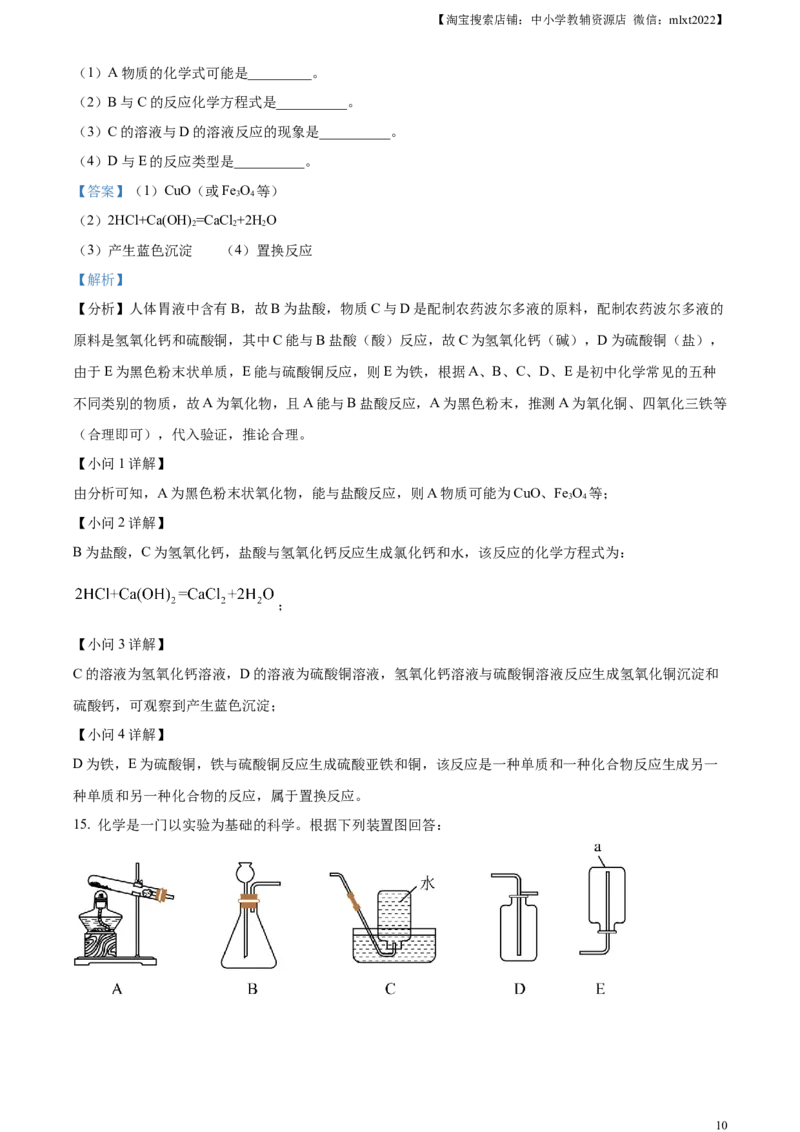
14. 如图,A、B、C、D、E是初中化学常见的五种不同类别的物质,其中E是单质,且A、E均为黑色粉
末,人体胃液中含有B,物质C与D是配制农药波尔多液的原料,图中两圆相交表示圆中的物质间能发生
化学反应。请回答:
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(1)A物质的化学式可能是_________。
(2)B与C的反应化学方程式是__________。
(3)C的溶液与D的溶液反应的现象是__________。
(4)D与E的反应类型是__________。
【答案】(1)CuO(或Fe O 等)
3 4
(2)2HCl+Ca(OH)=CaCl +2H O
2 2 2
(3)产生蓝色沉淀 (4)置换反应
【解析】
【分析】人体胃液中含有B,故B为盐酸,物质C与D是配制农药波尔多液的原料,配制农药波尔多液的
原料是氢氧化钙和硫酸铜,其中C能与B盐酸(酸)反应,故C为氢氧化钙(碱),D为硫酸铜(盐),
由于E为黑色粉末状单质,E能与硫酸铜反应,则E为铁,根据A、B、C、D、E是初中化学常见的五种
不同类别的物质,故A为氧化物,且A能与B盐酸反应,A为黑色粉末,推测A为氧化铜、四氧化三铁等
(合理即可),代入验证,推论合理。
【小问1详解】
由分析可知,A为黑色粉末状氧化物,能与盐酸反应,则A物质可能为CuO、Fe O 等;
3 4
【小问2详解】
B为盐酸,C为氢氧化钙,盐酸与氢氧化钙反应生成氯化钙和水,该反应的化学方程式为:
;
【小问3详解】
C的溶液为氢氧化钙溶液,D的溶液为硫酸铜溶液,氢氧化钙溶液与硫酸铜溶液反应生成氢氧化铜沉淀和
硫酸钙,可观察到产生蓝色沉淀;
【小问4详解】
D为铁,E为硫酸铜,铁与硫酸铜反应生成硫酸亚铁和铜,该反应是一种单质和一种化合物反应生成另一
种单质和另一种化合物的反应,属于置换反应。
15. 化学是一门以实验为基础的科学。根据下列装置图回答:
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(1)写出仪器a的名称________。
(2)实验室制取氧气和二氧化碳均可选用的发生装置是________(填字母序号),用该装置制取氧气的
化学方程式为_________。
(3)实验室用高锰酸钾制取并收集纯净的氧气,应选用的装置是________(填字母序号)。
【答案】(1)集气瓶 (2) ①. B ②.
(3)AC
【解析】
【
小问1详解】
由图可知,仪器a的名称为:集气瓶;
【小问2详解】
实验室用石灰石或大理石与稀盐酸反应制取二氧化碳,该反应是固液常温型,发生装置选B,过氧化氢溶
液和二氧化锰混合制取氧气,反应是固液常温型,发生装置也选B;过氧化氢在二氧化锰的催化作用下生
成水和氧气,反应的化学方程式为: ;
【小问3详解】
高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,该反应属于固体加热型,选择装置A作为发生
装置,氧气不易溶于水,可采用排水法收集较为纯净的氧气,所以应选用的装置为:AC。
16. 某化学兴趣小组的同学发现,上个月做实验用的氢氧化钠溶液忘了盖上瓶盖。对于该瓶溶液是否变质,
同学们提出了如下假设:
假设一:该溶液没有变质;
假设二:该溶液部分变质;
假设三:该溶液全部变质。
为了验证假设,同学们共同设计了实验方案并进行实验,请你帮他们完善该探究过程。
查阅资料发现,Ba(NO ) 溶液呈中性。
3 2
实验过程 实验现象 实验结论
步骤一:取少量该瓶溶液于试管中,滴加过量的Ba(NO ) 溶液,振
3 2 ______
荡 原溶液中一定含有碳酸
钠
步骤二:取步骤一试管中的少量上层清液于另一支试管中,滴加酚 溶液变红 原溶液中一定含有
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
酞溶液 色 ______
结论:假设二成立
反思一:氢氧化钠溶液露置于空气中易变质,写出反应的化学方程式________。
反思二:步骤一中,滴加Ba(NO ) 溶液过量的目的是 _______。
3 2
【答案】 ①. 产生白色沉淀 ②. 氢氧化钠##NaOH ③. CO+2NaOH=Na CO+H O ④. 检验
2 2 3 2
和除尽溶液中的碳酸钠
【解析】
【详解】步骤一:根据实验结论原溶液中一定含有碳酸钠反推现象,硝酸钡与碳酸钠反应,生成硝酸钠、
碳酸钡沉淀,可观察到,有白色沉淀生成;
步骤二:由于硝酸钡过量,将溶液中的碳酸钠完全消耗,此时溶液中无碳酸钠,因为硝酸钡呈中性,不能
使酚酞变红,故使酚酞变红的是氢氧化钠,由此得出结论原溶液中一定含有氢氧化钠;
反思一:氢氧化钠与二氧化碳反应,生成碳酸钠、水,反应的化学方程式为:CO+2NaOH=Na CO+H O;
2 2 3 2
反思二:碳酸钠溶液也呈碱性,也能使酚酞变红,为了排除碳酸钠对步骤二的干扰,需加入过量硝酸钡,
检验和除尽碳酸钠。
17. 为测定某瓶稀盐酸的溶质质量分数,取4.0g石灰石样品于烧杯中,将该稀盐酸40.0g分4次加入烧杯
中,充分反应后经过滤、洗涤、干燥、称重,得实验数据如下:
第一 第三
第二次 第四次
次 次
加入稀盐酸的质量/g 10.0 10.0 10.0 10.0
剩余固体的质量/g 3.0 2.0 1.0 0.6
已知:石灰石样品中的杂质既不与盐酸反应,也不溶于水。请计算:
(1)4.0g石灰石中碳酸钙的质量是_____g。
(2)求该瓶稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
【答案】(1)3.4 (2)解:通过数据比较可知:10.0g稀盐酸完全反应可以消耗碳酸钙的质量为
1.0g,
设10.0g稀盐酸中溶质质量为x
12【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
x=0.73 g
则该瓶稀盐酸的溶质质量分数为: ,
答:该瓶稀盐酸的溶质质量分数为7.3%。
【解析】
【
小问1详解】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,杂质不与稀盐酸反应,由表格数据分析可知,第一次加
入的10.0g稀盐酸能与4.0g-3.0g=1.0g碳酸钙完全反应;第二次加入的10.0g稀盐酸能与3.0g-2.0g=1.0g碳酸
钙完全反应;第三次加入的10.0g稀盐酸能与2.0g-1.0g=1.0g碳酸钙完全反应;第四次加入的10.0g稀盐酸
只能与1.0g-0.6g=0.4g碳酸钙反应,说明此时碳酸钙已经完全反应,最终剩余的0.6g为石灰石样品中的杂
质,故4.0g石灰石中碳酸钙的质量是4.0g-0.6g=3.4g;
【小问2详解】
见答案。
13