文档内容
2025 年重庆市普通高中学业水平选择性考试
高三第一次联合诊断检测 化学
化学测试卷共4页,满分100分。考试时间75分钟。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 李子坝单轨列车穿楼而过,成为重庆的热门景点。下列与单轨列车有关的材料属于新型无机非金属材料的是
A.铺设单轨轨道所用的锰钢
B.单轨列车车厢内的聚乙烯手扶拉环
C.单轨列车车窗所用的钢化玻璃
D.单轨列车信息传输系统中用到的光导纤维
2. 下列物质中所有碳原子都是sp3杂化,且具有碱性的是
A.CH COONa B. OH C.CH CH NH D.CH≡CCH NH
3 3 2 2 2 2
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.溶有CO 的水溶液中:Al3+、Ba2+、Cl-、I-
2
B.铁氰化钾溶液中:Fe2+、Ca2+、NO -、Cl-
3
C.遇紫色石蕊溶液显红色的溶液中:Na+、K+、[Al(OH) ]-、CO2-
4 3
D.水电离出的c(H+)=1×10-13 mol·L-1的溶液中:K+、NH +、HCO -、SO2-
4 3 4
点燃
4. 黑火药是中国古代四大发明之一,其爆炸反应为S+2KNO +3C K S+3CO ↑+N ↑。下列说法正确的是
3 2 2 2
A.电负性:N>O>H B.基态原子核外未成对电子数:N>S>K
C.第一电离能:O>N>C D.K、C、N、O都位于元素周期表的p区
5. 下列实验装置或操作能达到实验目的的是
NH
3
苯
水 饱和NaCO 溶液
2 3
A.提纯乙酸乙酯 B.吸收氨气 C.除去CO 中的少量HCl D.制取少量CO
2 2
6. 有机物Ⅱ是由我国科学家合成的一种可循环的高分子材料(R为饱和烃基),Ⅰ和Ⅱ可互相转化。下列说法错误的是
A.可用溴的四氯化碳溶液鉴别Ⅰ和Ⅱ
O 催化剂
[ ]
B.有机物Ⅰ不存在顺反异构 n
O O
C.图中Ⅰ→Ⅱ反应的原子利用率为100% O
R △ R
D.有机物Ⅱ不溶于水,也不与酸和碱反应 Ⅰ Ⅱ
7. 单质X的转化如右图所示,下列说法错误的是
盐酸 加热蒸干灼烧
A.单质a具有漂白性 b的水溶液 红
棕
B.X对应的元素是人体必需的微量元素 单 单 色
单质X 质 质
粉
C.单质X可以与水蒸气反应
单质a
X a
加热蒸干灼烧
末
D.苯酚与c的水溶液作用显紫色 c的水溶液 d
8. X、Y、Z、W、M、G是原子序数依次增大的前四周期元素,X的一种同位素没有中子,基态Y原子核外的s能
级电子数是p能级电子数的两倍,W、M位于同一主族,W元素的某种单质可用于自来水消毒,G的单质可用作
食品抗氧化剂。下列说法错误的是
A.键角:MW >X M>X W B.原子半径:M>Z>W
3 2 2
C.简单氢化物的沸点:W>Z D.Y、Z、M组成的一种离子可用于检验G3+
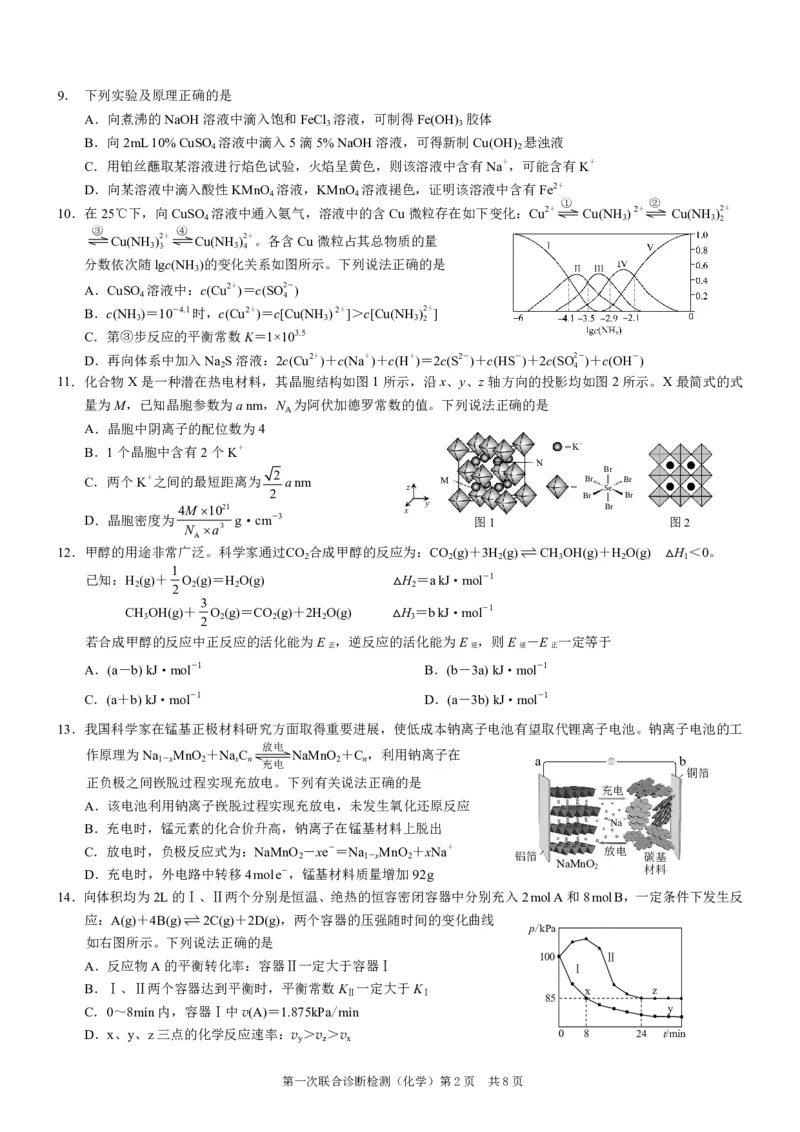
第一次联合诊断检测(化学)第1页 共8页9. 下列实验及原理正确的是
A.向煮沸的NaOH溶液中滴入饱和FeCl 溶液,可制得Fe(OH) 胶体
3 3
B.向2mL10% CuSO 溶液中滴入5滴5% NaOH溶液,可得新制Cu(OH) 悬浊液
4 2
C.用铂丝蘸取某溶液进行焰色试验,火焰呈黄色,则该溶液中含有Na+,可能含有K+
D.向某溶液中滴入酸性KMnO 溶液,KMnO 溶液褪色,证明该溶液中含有Fe2+
4 4
① ②
10.在25℃下,向CuSO 溶液中通入氨气,溶液中的含Cu微粒存在如下变化:Cu2+ Cu(NH ) 2+ Cu(NH )2+
4 3 3 2
③ ④
Cu(NH
)2+
Cu(NH
)2+。各含Cu微粒占其总物质的量
3 3 3 4
分数依次随lgc(NH )的变化关系如图所示。下列说法正确的是
3
A.CuSO 溶液中:c(Cu2+)=c(SO2- )
4 4
B.c(NH )=10-4.1时,c(Cu2+)=c[Cu(NH ) 2+]>c[Cu(NH )2+ ]
3 3 3 2
C.第③步反应的平衡常数K=1×103.5
D.再向体系中加入Na S溶液:2c(Cu2+)+c(Na+)+c(H+)=2c(S2-)+c(HS-)+2c(SO2- )+c(OH-)
2 4
11.化合物X是一种潜在热电材料,其晶胞结构如图1所示,沿x、y、z轴方向的投影均如图2所示。X最简式的式
量为M,已知晶胞参数为anm,N 为阿伏加德罗常数的值。下列说法正确的是
A
A.晶胞中阴离子的配位数为4
B.1个晶胞中含有2个K+ =K+
N
C.两个K+之间的最短距离为 2 anm M Br Br Br
z = Se
2 Br Br
4M1021 x y Br
D.晶胞密度为 g·cm-3 图1 图2
N a3
A
12.甲醇的用途非常广泛。科学家通过CO 合成甲醇的反应为:CO (g)+3H (g)CH OH(g)+H O(g) H <0。
2 2 2 3 2 1
1
已知:H (g)+ O (g)=H O(g) H =akJ·mol-1 △
2 2 2 2 2
3
CH OH(g)+ O (g)=CO (g)+2H O(g) △H =bkJ·mol-1
3 2 2 2 2 3
若合成甲醇的反应中正反应的活化能为E ,逆反应的△活化能为E ,则E -E 一定等于
正 逆 逆 正
A.(a-b) kJ·mol-1 B.(b-3a) kJ·mol-1
C.(a+b) kJ·mol-1 D.(a-3b) kJ·mol-1
13.我国科学家在锰基正极材料研究方面取得重要进展,使低成本钠离子电池有望取代锂离子电池。钠离子电池的工
放电
作原理为Na MnO +NaC NaMnO +C ,利用钠离子在
1-x 2 x n 充电 2 n a b
铜箔
正负极之间嵌脱过程实现充放电。下列有关说法正确的是
充电
A.该电池利用钠离子嵌脱过程实现充放电,未发生氧化还原反应
B.充电时,锰元素的化合价升高,钠离子在锰基材料上脱出
Na+
C.放电时,负极反应式为:NaMnO 2 -xe-=Na 1-x MnO 2 +xNa+ 铝箔 放电 碳基
D.充电时,外电路中转移4mole-,锰基材料质量增加92g NaMnO 2 材料
14.向体积均为2L的Ⅰ、Ⅱ两个分别是恒温、绝热的恒容密闭容器中分别充入2molA和8molB,一定条件下发生反
应:A(g)+4B(g)2C(g)+2D(g),两个容器的压强随时间的变化曲线
p/kPa
如右图所示。下列说法正确的是
100 Ⅱ
A.反应物A的平衡转化率:容器Ⅱ一定大于容器Ⅰ
Ⅰ
B.Ⅰ、Ⅱ两个容器达到平衡时,平衡常数KⅡ 一定大于KⅠ
x z
85
C.0~8min内,容器Ⅰ中v(A)=1.875kPa/min y
D.x、y、z三点的化学反应速率:v >v >v 0 8 24 t/min
y z x
第一次联合诊断检测(化学)第2页 共8页二、非选择题:本题共4小题,共58分。
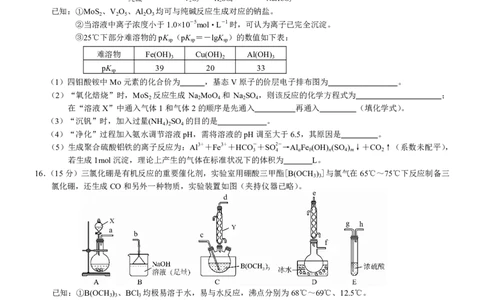
15.(14分)四钼酸铵的用途非常广泛,可用作催化剂、防腐剂、阻燃剂、电化学应用等。下图是用辉钼矿(含
MoS 、V O 、CuS 、Fe O 、Al O 等)制备四钼酸铵和一些副产品的工艺流程图:
2 2 5 2 3 4 2 3
HSO、
2 4
纯碱、氧气 (NH 4 ) 2 SO 4 氨水 H 2 SO 4
四钼酸铵
辉钼矿 氧化焙烧 沉钒 净化 沉钼
(NH)Mo O ·2HO
4 2 4 13 2
NHVO 滤渣1
滤液1
4 3
气体1
溶液X 气体2 煅烧 酸溶 … 聚合 聚合硫酸铝铁
一系列操作
纯碱 V
2
O
5
H
2
SO
4
NaHCO
3
已知:①MoS 、V O 、Al O 均可与纯碱反应生成对应的钠盐。
2 2 5 2 3
②当溶液中离子浓度小于1.0×10-5mol·L-1时,可认为离子已完全沉淀。
③25℃下部分难溶物的pK (pK =-lgK )的数值如下表:
sp sp sp
难溶物 Fe(OH) Cu(OH) Al(OH)
3 2 3
pK 39 20 33
sp
(1) 四钼酸铵中Mo元素的化合价为 ,基态V原子的价层电子排布图为 。
(2)“氧化焙烧”时,MoS 反应生成 Na MoO 和 Na SO ,则该反应的化学方程式为 ;
2 2 4 2 4
在“溶液X”中通入气体1和气体2的顺序是先通入 再通入 (填化学式)。
(3)“沉钒”时,加入过量(NH ) SO 的目的是 。
4 2 4
(4)“净化”过程加入氨水调节溶液pH,需将溶液的pH调至大于6.5,其原因是 。
(5)生成聚合硫酸铝铁的离子反应为:Al3++Fe3++HCO -+SO2-→Al Fe (OH) (SO ) ↓+CO ↑(系数未配平),
3 4 a b n 4 m 2
若生成1mol沉淀,理论上产生的气体在标准状况下的体积为 L。
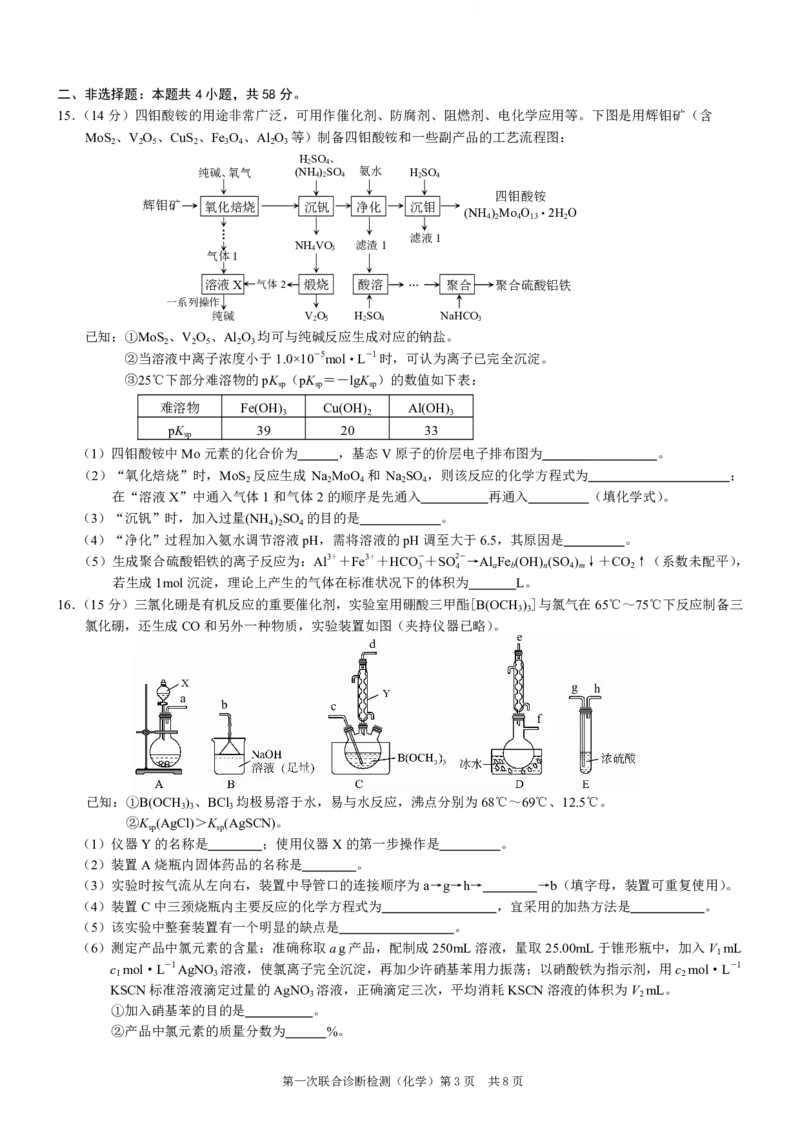
16.(15分)三氯化硼是有机反应的重要催化剂,实验室用硼酸三甲酯[B(OCH ) ]与氯气在65℃~75℃下反应制备三
3 3
氯化硼,还生成CO和另外一种物质,实验装置如图(夹持仪器已略)。
e
d
YX
g h
a Y
b c
f
已知:①B(OCH ) 、BCl 均极易溶于水,易与水反应,沸点分别为68℃~69℃、12.5℃。
3 3 3
②K (AgCl)>K (AgSCN)。
sp sp
(1)仪器Y的名称是 ;使用仪器X的第一步操作是 。
(2)装置A烧瓶内固体药品的名称是 。
(3)实验时按气流从左向右,装置中导管口的连接顺序为a→g→h→ →b(填字母,装置可重复使用)。
(4)装置C中三颈烧瓶内主要反应的化学方程式为 ,宜采用的加热方法是 。
(5)该实验中整套装置有一个明显的缺点是 。
(6)测定产品中氯元素的含量:准确称取ag产品,配制成250mL溶液,量取25.00mL于锥形瓶中,加入V mL
1
c mol·L-1 AgNO 溶液,使氯离子完全沉淀,再加少许硝基苯用力振荡;以硝酸铁为指示剂,用c mol·L-1
1 3 2
KSCN标准溶液滴定过量的AgNO 溶液,正确滴定三次,平均消耗KSCN溶液的体积为V mL。
3 2
①加入硝基苯的目的是 。
②产品中氯元素的质量分数为 %。
第一次联合诊断检测(化学)第3页 共8页17.(14分)甲醇是一种关键的化学原料,用CO和CO 都可合成甲醇。 2
(1)CO 加氢制取甲醇的过程含有以下三个反应。
2
Ⅰ.CO (g)+3H (g)CH OH(g)+H O(g) K 2 2 3 2 1
Ⅱ.CO (g)+H (g)CO(g)+H O(g) K 2 2 2 2
Ⅲ.CO(g)+2H (g)CH OH(g) ΔH= 91.0 kJ·mol-1 K
2 3 3
①T℃时,已知K =1.0,K =2.5,求K 的值 (写出推断过程)。
2 3 1
②反应Ⅲ反应历程如右图所示,写出生成CH OH决速步骤的化学方
3
程式 ;图中m的值约为 (保留到小数点后2位,已知1eV=1.6×10-22 kJ)。
(2)甲醇与水蒸气在催化剂作用下可制取H ,一定温度下,在恒容体系中加入2mol CH OH(g)和2 molH O(g),
2 3 2
发生反应:Ⅳ.CH OH(g)2H (g)+CO(g);Ⅴ.CO(g)+H O(g)H (g)+CO (g)。
3 2 2 2 2
①下列能说明体系一定达到平衡状态的是 (填字母)。
a.v(CH OH)=v(CO) b.体系的压强保持不变
3
c.混合气体的平均摩尔质量保持不变 d.混合气体的密度保持不变
②测得体系的初始压强为p kPa,达到平衡时,甲醇的转化率为90%,H O(g)的分压为0.25p kPa,则反应Ⅴ
0 2 0
的压强平衡常数K = (以平衡分压代替物质的量浓度计算,分压=总压×物质的量分数)。
p
(3)电解CO 可以制取CH OH,其电解原理如右图所示。双极膜内为水, A B
2 3
电解时双极膜内的水解离成H+和OH-,分别向两侧发生迁移。 双极膜
①电源的负极是 (填“A”或“B”)。 石
墨 O2 CO2
催
化
②
③
催
当
化
催
电
化
极
电
的
极
电
生
极
成
反
48
应
gC
式
H
为
O H 时 , 阳 极 室 溶 液
。
增 加的质量为 g。
电
极
K
溶
O
液
H
酸
CH
性
3O
溶
H
液
电
极
3
a膜 b膜
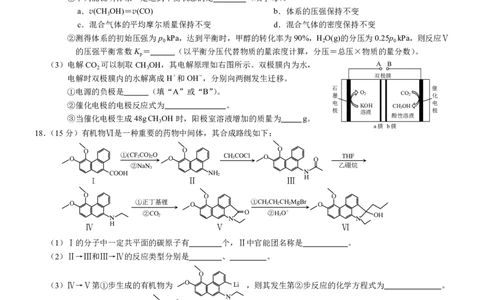
18.(15分)有机物Ⅵ是一种重要的药物中间体,其合成路线如下:
O O O
O ①(CF 3 CO) 2 O O CH 3 COCl O O THF
②NaN 乙硼烷
3
I COOH Ⅱ NH 2 Ⅲ N H
O O O
O ①正丁基锂 O ①CH 3 CH 2 CH 2 MgBr O
N
②CO
2 N
O ②H
3
O+
N OH
Ⅳ H Ⅴ Ⅵ
(1)Ⅰ的分子中一定共平面的碳原子有 个,Ⅱ中官能团名称是 。
(2)Ⅱ→Ⅲ和Ⅲ→Ⅳ的反应类型分别是 、 。
O
(3)Ⅳ→Ⅴ第①步生成的有机物为 O L i ,则其发生第②步反应的化学方程式为 。
N
O H
O
(4)原料Ⅰ中混有杂质 ,则Ⅴ中混有与Ⅴ互为同分异构体的副产物Y,Y也含有1个含氮五元
COOH
环。该副产物Y的结构简式为 。
(5)有机物W的分子比Ⅱ少1个碳原子,符合下列条件的W的同分异构体有 种(不考虑立体异构)。
①分子中含有-NH ,含1个手性碳原子;②酸性条件下能水解生成两种芳香族化合物,水解生成的羧基直
2
接连在苯环上,且水解产物遇FeCl 溶液均不显色。
3
O
(6)以CH 3 MgBr和 为原料制备 H 2 N 的部分合成路线如下,请将流程补充完整(无机试剂和
有机溶剂任用,合成路线示例见本题题干)。 O CH 3 MgBr OH KMnO 4 。
HO+
3
第一次联合诊断检测(化学)第4页 共8页
)g(2H2+)g(OC
)g(2H2+)g(*OC
0.7
0 -0.1 0 -0.2 -0.3
-0.6
-0.5
-0.9
-1.3 -1.4
反应历程
Ve/量能对相
-m
3
)g(2H
2
+)g(*OCH
)g(2H
+)g(*OC2H
)g(*HO3HC
)g(
HO3HC