文档内容
7.【答案】A
【详解】A.液晶分子中沿分子长轴方向有序排列,从而表现出类似晶体的各向异性,A正确;
B.较高压力、温度和引发剂作用下,乙烯加聚成密度较小的聚乙烯,即低密度聚乙烯,B错误;
C.碳纤维是碳元素的一种单质,是新型无机非金属材料,C错误;
D.暖宝宝放热是利用原电池原理,铁作负极,最终将化学能转化为热能,D错误。
8.【答案】D
【详解】A.根据反应过程知,A与B反应是成肽反应,生成C和水,是取代反应,A正确;
B.合成E时,E中含有两段由物质D形成的链节,每段需要m个D,所以合成E时,参加反应的D和C
的物质的量之比为2m∶1,B正确;
C.E中的含氧官能团有4种,即酰胺基、醚键、羟基和酯基,C正确;
D.E在酸性条件下充分水解后可以转化得到A,但不能得到碱性物质B,D错误。
9. 【答案】C
【详解】A.浓度相同的CF COOH和CCl COOH两种溶液,,F的电负性强于Cl,F对电子的吸引能力更
3 3
强,导致羧基上的H更容易电离,因此现象应为CF COOH的pH更小,A错误;
3
B.麦芽糖自身有还原性,也能和新制CuOH 反应生成砖红色沉淀,则该实验不能说明麦芽糖发生了水解,
2
B错误;
C.Ba2与CrO2
4
形成难溶的BaCrO
4
沉淀,使反应Cr
2
O
7
2H
2
O2CrO2
4
2H的平衡正向移动,c H 增
大,C正确;
D.盐酸也能与酸性高锰酸钾溶液反应使溶液褪色,则将铁锈溶于浓盐酸,滴入高锰酸钾溶液,紫色褪去不
能说明铁锈中含有二价铁,故D错误;
10.【答案】D
【分析】四种原子序数依次递增的短周期元素W、X、Y、Z,W、X、Z分别位于不同周期,分别位于第
一、第二、第三周期,则W为H元素;X形成4个共价键,则X为C元素;Z为Na元素;Y形成2个
共价键,原子序数比C大,比Na小,说明Y原子核外有2个电子层,最外层有6个电子,则Y是O元
素,以此分析解答。
【详解】A.体现超分子分子识别的特征,A错误;
B.CH 与H O均为分子晶体,H O可形成分子间氢键,为非密堆积,CH 为密堆积。
4 2 2 4
C.H、O、Na三种元素中组成的二元化合物有H O 、H O、Na O、Na O 、NaH等,至少有三种离子化合
2 2 2 2 2 2
物,C错误;
D.水分子间存在氢键,X与W组成的简单化合物的沸点一定比Y与W组成的简单化合物的沸点低,即
CH <H O,其它化合物不一定,如C H 沸点高于100度,故D正确。
4 2 10 22
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}11.【答案】D
【分析】NO- 在亚硝酸盐还原酶的作用下转化为X,NO- 中氮元素化合价为+3价,X中氮元素化合价比
2 2
+3价低,X可能为NO或N O,X在X还原酶的作用下转化为Y,Y中氮元素化合价比X中低,X、Y均
2
为氮氧化物,则Y为N O、X为NO,据此分析;
2
【详解】A.分子构型N-N-O,中心的N形成2个σ键,无孤电子对,N原子采取sp杂化,N O的分子是
2
直线形的,A正确;
B.9gNO物质的量为0.3mol,转移电子0.6mol,B正确;
C.pH越小,阳离子水解程度越大,根据越弱越水解,碱性NH ·H O>NH OH,C正确;
3 2 2
D.⑥氮化合价上升,D错误。
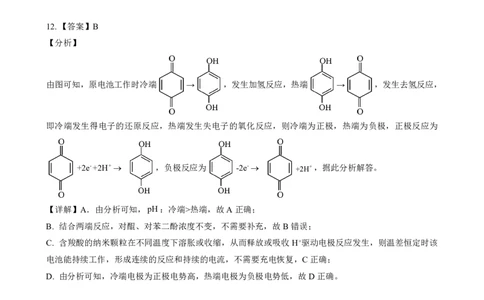
12.【答案】B
【分析】
由图可知,原电池工作时冷端 → ,发生加氢反应,热端 → ,发生去氢反应,
即冷端发生得电子的还原反应,热端发生失电子的氧化反应,则冷端为正极,热端为负极,正极反应为
+2e-+2H+ ,负极反应为 -2e- +2H+,据此分析解答。
【详解】A.由分析可知,pH:冷端>热端,故A正确;
B. 结合两端反应,对醌、对苯二酚浓度不变,不需要补充,故B错误;
C. 含羧酸的纳米颗粒在不同温度下溶胀或收缩,从而释放或吸收H+驱动电极反应发生,则温差恒定时该
电池能持续工作,形成连续的反应和持续的电流,不需要充电恢复,C正确;
D. 由分析可知,冷端电极为正极电势高,热端电极为负极电势低,故D正确。
13.【答案】C
【分析】由题意可知,随着c Cl的增加,c Ag 逐渐减小,故线l 对应于pc Ag ,随着c Cl的增加,
1
逐渐出现AgClAgCl AgCl2 AgCl3的转化,故AgCl、AgCl2、AgCl3依次出现,即线l 、l 、
2 3 4 2 3 4 2 3
l 分别对应于pc AgCl 、pc AgCl2 、pc AgCl3。
4 2 3 4
【详解】A.由线l 知,c Cl 107mol/L时,pc Ag 3,即c Ag 103mol/L,故K 1010,A正
1 sp
确;
B.由题干知①+②+③得Ag+(aq)+3Cl-(aq) AgCl 2-(aq),K=c(AgCl 2-)/[c(Ag+)c3(Cl-)],由多重平衡
3 3
的复合平衡常数规则知,K=K K K ,B正确;
1 2 3
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}C.由N点坐标知,K =10-c,由M点坐标知,K =10-a,③+④得到反应式为
3 4
AgClaq2ClaqAgCl3aq,其平衡常数K=K K =10-a+c ,P点c AgCl- =c AgCl3- ,故P点的
2 4 3 4 2 4
c
Cl-
=
K=10-a+c/2,即lgc Cl-
=
a+c
,C错误;
2
D.P点溶液中有Na,根据电荷守恒应满足关系:
c
Ag+
+c
H+
+c
Na+
=c
Cl-
+c
OH-
+c
AgCl-
+2c
AgCl2-
+3c
AgCl3-
+c(NO -),因为
2 3 4 3
c(AgCl -)=c(AgCl -),所以有c(Ag+)+c(H+)+c(Na+)=c(Cl-)+c(OH-)+c(NO -)+3c(AgCl -)+3c(AgCl 3-),D正确。
2 3 3 2 4
【分析】含铅烟灰(主要化学成分为PbO、Fe O 、In O 和In S )加入MnO 、H SO 氧化酸浸后,PbO
2 3 2 3 2 3 2 2 4
转变为PbSO 沉淀,Fe O 和In O 分别溶于硫酸,In S 、MnO 、H SO 发生氧化还原反应,滤液中含Fe3、
4 2 3 2 3 2 3 2 2 4
In3、SO2、Mn2,滤渣A为过量的MnO 和PbSO ,向滤液中加入有机萃取剂除去Mn2、SO2,在有
4 2 4 4
机相中加入盐酸,反萃取除去Fe3,在HInCl 溶液中加入Zn,得到粗铟,电解精炼得到铟。
4
【详解】(1)基态铟原子的电子排布式为 Kr 4d105s25p1;
(2) 由分析可知,PbO转变为PbSO 沉淀,即PbO+H SO =PbSO H O,滤渣A除了过量的MnO 还有
4 2 4 4 2 2
PbSO ;
4
(3)由分析可知,In S 、MnO 、H SO 发生氧化还原反应,S由-2价变为+6价,Mn由+4价变为+2价,则
2 3 2 2 4
In S 化合价升高24价,MnO 降低2,根据化合价升降守恒得到物质的量之比为1:12;
2 3 2
(4)P204的酸性强于P507的酸性,其原因是:-R是推电子基团,使含氧酸的酸性减弱(或-OR是吸电子基
团,使含氧酸的酸性增强),因此P204的酸性强于P507的酸性;
(5)H+也可与金属Zn反应,故方程式为:
(6)反萃取时,Fe3尽可能留在有机相,In3尽可能反萃取到水相,则由题中图示可知,当盐酸的浓度在
2~3mol/L之间时,In3的反萃取率较高,而Fe3的反萃取率很小,所以盐酸的最佳浓度范围为2~3mol/L;
(7)Fe
3
O
4
中n Fe3:n Fe2:n O22:1:4,晶胞含有8个正四面体空隙,即有2个Fe3和1个Fe2,1
个三价铁离子放入正四面体空隙;晶胞中由3、6、7、9、8、12处的原子形成一个正八面体空隙,剩余
1
的空间以每条棱分析:如4、7、9、13或1、3、4、7等处的原子形成的四面体空隙为正八面体空隙的 ,
4
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}1
共12条棱,则正八面体空隙有112 4个,其中已经有一个放Fe3,另外一个Fe2占据一个正八面体
4
空隙,所以有2个正八面体空隙没有被填充,故答案为:7:2;
根据分析可知晶胞中Fe3 2个,Fe2 1个,O四个, 。
232
N(a1010)3
A
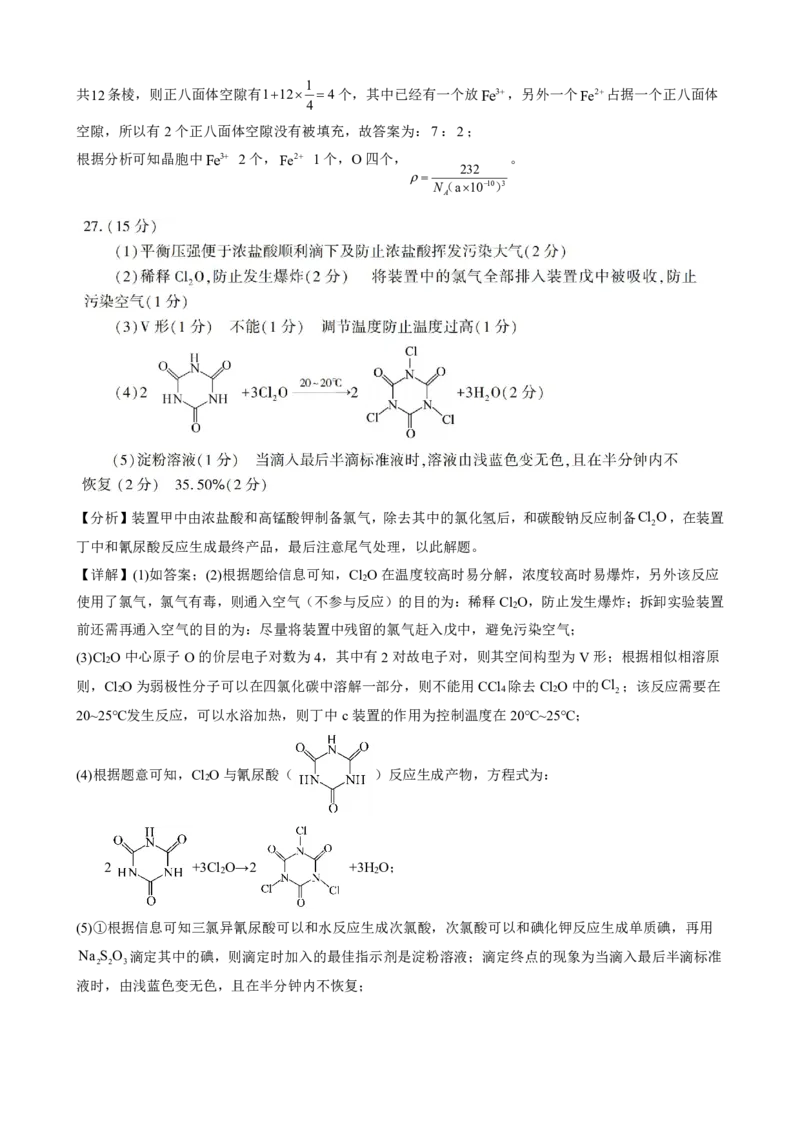
【分析】装置甲中由浓盐酸和高锰酸钾制备氯气,除去其中的氯化氢后,和碳酸钠反应制备Cl O,在装置
2
丁中和氰尿酸反应生成最终产品,最后注意尾气处理,以此解题。
【详解】(1)如答案;(2)根据题给信息可知,Cl O在温度较高时易分解,浓度较高时易爆炸,另外该反应
2
使用了氯气,氯气有毒,则通入空气(不参与反应)的目的为:稀释Cl O,防止发生爆炸;拆卸实验装置
2
前还需再通入空气的目的为:尽量将装置中残留的氯气赶入戊中,避免污染空气;
(3)Cl O中心原子O的价层电子对数为4,其中有2对故电子对,则其空间构型为V形;根据相似相溶原
2
则,Cl O为弱极性分子可以在四氯化碳中溶解一部分,则不能用CCl 除去Cl O中的Cl ;该反应需要在
2 4 2 2
20~25℃发生反应,可以水浴加热,则丁中c装置的作用为控制温度在20℃~25℃;
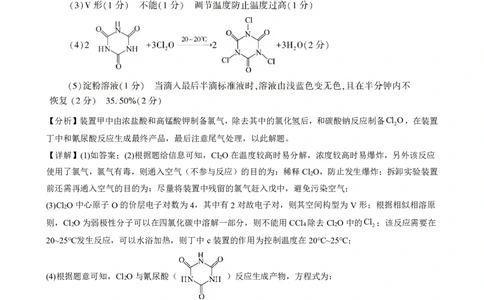
(4)根据题意可知,Cl O与氰尿酸( )反应生成产物,方程式为:
2
2 +3Cl O→2 +3H O;
2 2
(5)①根据信息可知三氯异氰尿酸可以和水反应生成次氯酸,次氯酸可以和碘化钾反应生成单质碘,再用
Na S O 滴定其中的碘,则滴定时加入的最佳指示剂是淀粉溶液;滴定终点的现象为当滴入最后半滴标准
2 2 3
液时,由浅蓝色变无色,且在半分钟内不恢复;
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}②根据得失电子守恒可知,关系式为: ~3HClO~3I ~6Na S O ,则
2 2 2 3
n( )= ,样品有效氯为
1 1
0.2000mol/L0.03L 0.006mol
6 6
1
0.006mol335.5g/mol
6
100%35.50%
0.3g
H 2H 2H
【详解】(1)反应B×2反应A×2可得反应:2H 2 (g)+O 2 (g)=2H 2 O(g),则由盖斯定律可得: 2 1,
1 1
则反应B的H H H 124kJ /mol (484kJ /mol)118kJ /mol ;
2 1 2 2
(2)反应B为放热反应、气体体积增大的反应,升温平衡逆移,产率下降,故a错误;加压平衡逆移,故b
错误;充入氧气平衡正向移动,反应速率增大,c正确;及时分离水蒸气,反应速率减小,d不正确;加
催化剂不改变平衡产率,e不正确,故选c;
(3)从能量变化图可知,路径中由c生成d的活化能最高,为决速步骤,其反应式为:
CH CHCH*H*CH CHCH* 2H*或CH CHCH*CH CHCH* H*;
3 3 3 2 3 3 3 2
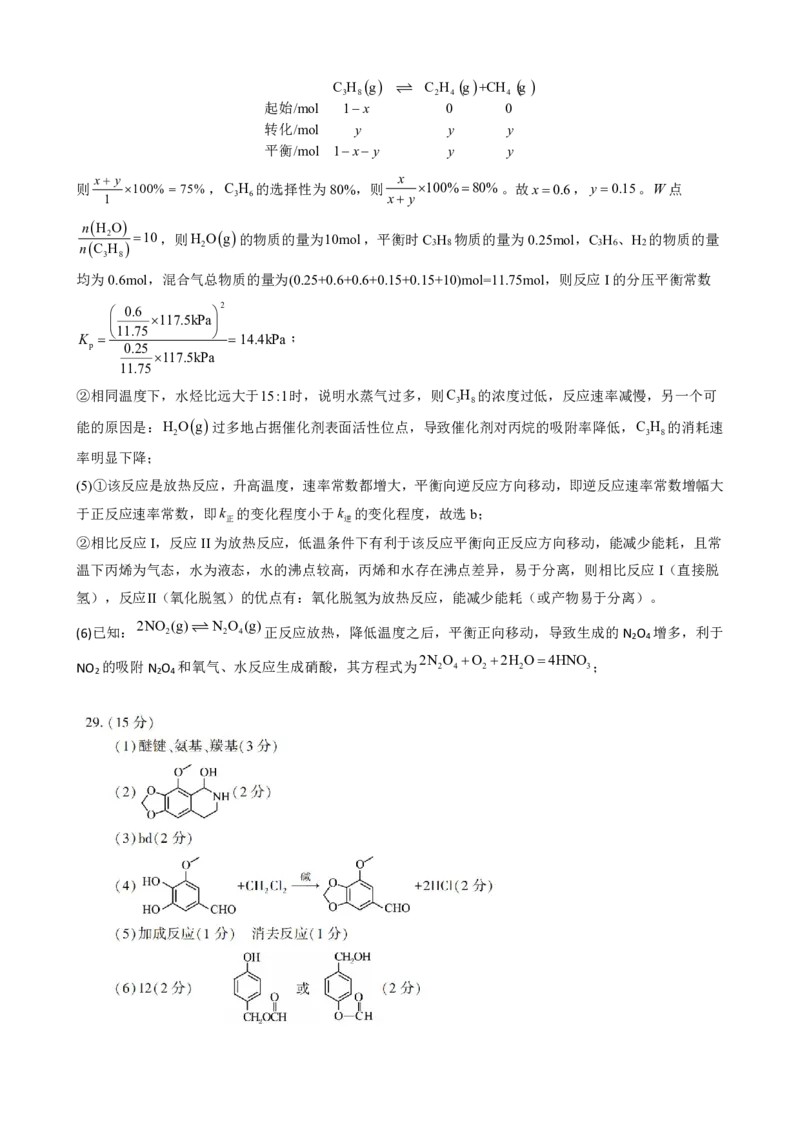
(4)①W点C H 的平衡转化率为75%,设C H 通过反应I和副反应转化的物质的量分别为xmol、ymol,
3 8 3 8
且起始n(C H )=1mol,根据已知条件列出“三段式”:
3 8
C H g C H g H g
3 8 3 6 2
起始/mol 1 0 0
转化/mol x x x
平衡/mol 1x x x
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}C H g C H gCH g
3 8 2 4 4
起始/mol 1x 0 0
转化/mol y y y
平衡/mol 1xy y y
x y x
则 100% 75%,C H 的选择性为80%,则 100%80%。故x0.6,y0.15。W点
1 3 6 xy
nH O
2 10,则H Og的物质的量为10mol,平衡时C H 物质的量为0.25mol,C H 、H 的物质的量
nC H 2 3 8 3 6 2
3 8
均为0.6mol,混合气总物质的量为(0.25+0.6+0.6+0.15+0.15+10)mol=11.75mol,则反应I的分压平衡常数
2
0.6
117.5kPa
K 11.75 14.4kPa ;
p 0.25
117.5kPa
11.75
②相同温度下,水烃比远大于15:1时,说明水蒸气过多,则C H 的浓度过低,反应速率减慢,另一个可
3 8
能的原因是:H Og过多地占据催化剂表面活性位点,导致催化剂对丙烷的吸附率降低,C H 的消耗速
2 3 8
率明显下降;
(5)①该反应是放热反应,升高温度,速率常数都增大,平衡向逆反应方向移动,即逆反应速率常数增幅大
于正反应速率常数,即k 的变化程度小于k 的变化程度,故选b;
正 逆
②相比反应I,反应II为放热反应,低温条件下有利于该反应平衡向正反应方向移动,能减少能耗,且常
温下丙烯为气态,水为液态,水的沸点较高,丙烯和水存在沸点差异,易于分离,则相比反应I(直接脱
氢),反应Ⅱ(氧化脱氢)的优点有:氧化脱氢为放热反应,能减少能耗(或产物易于分离)。
(6)已知:
2NO
2
(g)N
2
O
4
(g)
正反应放热,降低温度之后,平衡正向移动,导致生成的N O 增多,利于
2 4
2N O O 2H O4HNO
NO 的吸附N O 和氧气、水反应生成硝酸,其方程式为 2 4 2 2 3;
2 2 4
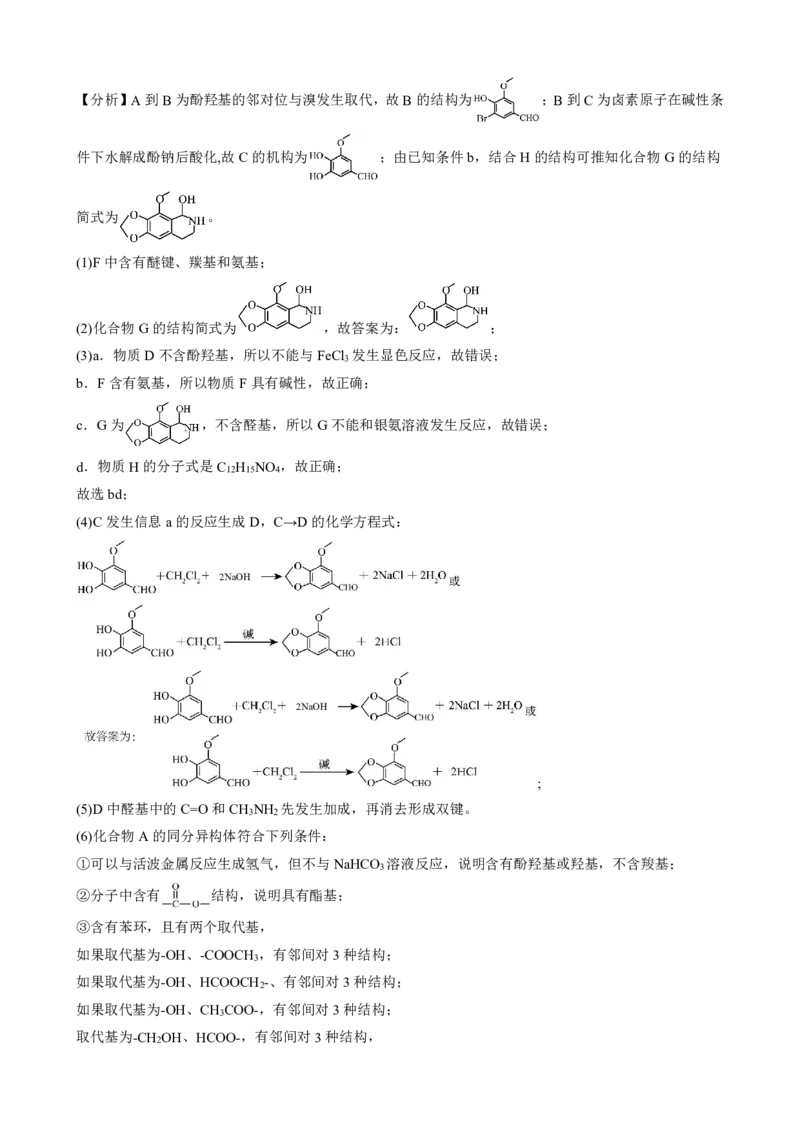
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}【分析】A到B为酚羟基的邻对位与溴发生取代,故B的结构为 ;B到C为卤素原子在碱性条
件下水解成酚钠后酸化,故C的机构为 ;由已知条件b,结合H的结构可推知化合物G的结构
简式为 。
(1)F中含有醚键、羰基和氨基;
(2)化合物G的结构简式为 ,故答案为: ;
(3)a.物质D不含酚羟基,所以不能与FeCl 发生显色反应,故错误;
3
b.F含有氨基,所以物质F具有碱性,故正确;
c.G为 ,不含醛基,所以G不能和银氨溶液发生反应,故错误;
d.物质H的分子式是C H NO ,故正确;
12 15 4
故选bd;
(4)C发生信息a的反应生成D,C→D的化学方程式:
2NaOH
2NaOH
;
(5)D中醛基中的C=O和CH NH 先发生加成,再消去形成双键。
3 2
(6)化合物A的同分异构体符合下列条件:
①可以与活波金属反应生成氢气,但不与NaHCO 溶液反应,说明含有酚羟基或羟基,不含羧基;
3
②分子中含有 结构,说明具有酯基;
③含有苯环,且有两个取代基,
如果取代基为-OH、-COOCH ,有邻间对3种结构;
3
如果取代基为-OH、HCOOCH -、有邻间对3种结构;
2
如果取代基为-OH、CH COO-,有邻间对3种结构;
3
取代基为-CH OH、HCOO-,有邻间对3种结构,
2
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}所以符合条件的有12种;峰面积之比符合题意的有
故答案为:12;
{#{QQABLYyEogAgAAAAAAgCQwEgCgKQkAACAQoORBAQIAABwBFABAA=}#}