文档内容
秘密 启用前
★
年高考考前适应性测试
2025
化学参考答案详解及评分说明
评分说明:
考生如按其他方法或步骤解答,正确的,同样给分;有错的,根据错误的性质,参照评分参考中相应的规定评分。
一、选择题:本题共14小题,每小题3分,共42分。
1.B
【解析】高级脂肪酸不属于有机高分子,选项不合理。
B
2.D
Cl
【解析】基态 原子价电子排布式是 , 选项错误;四氯化碳的电子式为 ,选项错误;基态 原子的
10 2
Zn 3d 4s A ClC Cl B K
Cl
最高能层符号为 ,选项错误; 的结构为 [ ],所以含有离子键、非极性共价键、键和 键, 选项
2+ 2-
N C CaC2 Ca C≡C σ π D
正确。
3.A
【解析】容量瓶、分液漏斗和酸式滴定管使用前需要检查是否漏水, 选项正确;氯水中的 有漂白性,能使
A HClO
试纸褪色,不能用 试纸检测氯水的 , 选项错误;锥形瓶不需要润洗,否则实验结果有误差, 选项错
pH pH pH B C
误; 制取 时,棉花的作用是防止 颗粒被 的气流吹入到导气管中,避免堵塞导气管,而制取
KMnO4 O2 KMnO4 O2 NH3
时棉花的作用是减缓空气的对流,防止 逸出污染空气, 选项错误。
NH3 D
4.D
【解析】浓 具有脱水性,能脱去糖类化合物中的水分并使其炭化, 选项错误;加热 与浓 混合物制
H2SO4 A NaI H3PO4
备 ,利用了 的难挥发性, 选项错误; 溶液蒸发时, 发生水解,蒸发结晶后得不到无水 ,
2+
HI H3PO4 B MgCl2 Mg MgCl2 C
选项错误; 和氢氟酸反应生成 和 , 不属于盐,是共价化合物, 选项正确。
SiO2 SiF4 H2O SiF4 D
5.C
【解析】该物质的分子式为 , 选项错误;该分子中C原子有 、 、 种杂化类型, 选项错误;和
2 3
C19H15NO3 A sp sp sp3 B H2
反应既是加成反应又是还原反应,碳碳三键能被 氧化,羧基酯化反应,酰胺基的水解反应都属于取代反
KMnO4
应,选项正确; 只和羧基反应, 和羧基、酰胺基都反应,消耗 、 的物质的量不相同, 选项错误。
C Na NaOH Na NaOH D
6.B
【解析】若有 参加反应, 原子共得到 电子,根据得失电子相等可知被 氧化的 的
2molKNO3 N 10mol 2molKNO3 C
物质的量为 ,数目为 N , 选项错误;依据电荷守恒以及物料守恒,可得到 溶液中c( ) c( )
- +
2.5mol 2.5 A B K2S OH = H
c( ) c( ), 选项正确。
-
+ HS +2 H2S D
7.C
【解析】盐酸中的 也能使 溶液褪色, 选项错误;由于醋酸、盐酸的浓度未知,虽然盐酸的 小于醋酸,
-
Cl KMnO4 A pH
但不能证明 是弱电解质,选项错误;溶液变红褐色,说明 水解的 和 反应,使水解平衡正向
3+ + 2-
CH3COOH B Fe H SO3
移动,产生了 ( )胶体;产生蓝色沉淀,说明 发生还原反应生成了 ,选项正确;玻璃中有 ,灼
3+ 2+
Fe OH 3 Fe Fe C Na2SiO3
烧也能出现黄色, 选项错误。
D
8.B
【解析】 和 中, 原子的配位数都是 , 选项错误; 生成 、生成 有 — 键生成,生成 、生成
LAlH2 a Al 4 A LAlH2 a b c Al O d e f g
有 — 键断裂,选项正确;该反应有两种产物 和甲醛,选项错误;反应过程中有部分 元素由 价变为
Al O B g C H -1 +1
价,例如 生成 时, 选项错误。
LAlH2 a D
化学试题答案 第 页(共 页)
1 49.B
【解析】电负性 , , 选项错误; ·中 原子的价层电子对数为 (可看作 ),其价层电子对互斥模型
N>P H>Al A CH3 C 3.5 4
为四面体,选项正确;元素的氢化物的状态有固态、液态或气态,而 元素的氢化物为气态和液态,选项错误;
B C N C
基态 原子的电子排布式为[ ] ,电子的空间运动状态数及原子轨道数为 , 选项错误。
10 2 4
Se Ar 3d 4s 4p 18 D
10.D
【解析】 是弱酸,不能拆开,选项错误;电解 溶液生成的 ( )难溶,不能拆开,选项错误;苯酚的电离
HClO A MgCl2 Mg OH 2 B
常数比碳酸的一级电离常数小,比二级电离常数大,只能生成 ,选项错误。 ( )== ,
+ 3+ 2-
NaHCO3 C KAl SO4 2 K +Al +2SO4
氢氧化钡溶液少量 只能生成 ( ),沉淀 份 需要 份 、同时 份 只能沉淀 份 ,所
3+ 3+ - 2+ 2-
Al Al OH 3 1 Al 3 OH 1.5 Ba 1.5 SO4
以n( )∶n( ) ∶, 选项正确。
3+ 2-
Al SO4 =2 3 D
11.B
【解析】温度一定时,投料比越大, 的平衡转化率越小,所以x x, 选项错误;b、c两点的温度相同,平衡常
CH4 1< 2 A
数也相同,b点时
() () () ()
CH4 g + H2O g CO g + 3H2 g
c( )
0 mol/L 1 1 0 0
c( )
Δ mol/L 0.7 0.7 0.7 2.1
c ( )
平 mol/L 0.3 0.3 0.7 2.1
3
K 0.7 × 2.1
=
2
0.3
选项正确;由图可知温度升高 的平衡转化率增大,可推测 H ,选项错误;温度b a, 的平衡转化
B CH4 Δ > 0 C > CH4
率b a,则生成物浓度b a,所以v () v (), 选项错误。
> > 逆 b > 逆 a D
12.A
【解析】观察晶胞结构,利用均摊法可以数出该晶胞中有 个 、个 和 个 ,所以 选项正确; 原子填充
2 Fe 4 Sb 12 O A Sb
在 原子形成的八面体空隙中, 原子的配位数为 , 选项错误; 点 原子和原点 原子间的距离为
O Sb 6 B W Sb Fe
c x c x
- ,所以其原子分数坐标为( ,, - ),选项错误;该晶体密度为 792 21 -3 , 选项错误。
0 0 c C a cN × 10 g ⋅ cm D
2
2 2 A
13.D
【解析】观察反应原理,电极上发生氧化反应 ·,选项正确,所以 电极为阳极,为电源的正极,为负
- -
C I -e =I B C a b
极, 选项正确。 在 电极上生成·,又在反应 和 生成,所以 是催化剂,选项正确。反应 的另一种产物
- -
A I C I d f I C d
是 , 选项错误。
+
H D
14.D
【解析】 增大,c( )减小、c( )增大, c( )增大、 c( )减小,所以曲线 代表 与 c( )变化
2- 2-
pH H2A A -lg H2A -lg A M pH -lg H2A
c( ) K c( ) c( )
2- 2- 2-
关系; A a2 、 A K , 增大, A 减小,且呈线性关系,所以曲线 代表
c( - ) = c( + ) -lgc( - ) = -lg a2 - pH pH -lgc( - ) Q pH
HA H HA HA
c( ) c( )
2- 2-
与 A 变化关系,而且当 A 时,K ,K ,、选项错误。 点时c( ) c( ),
-lgc(
-
) -lgc(
-
) =0 lg a2=-pH a2=10 -4.3 A B a H2A = A 2-
HA HA
电荷守恒式为c( ) ( ) c( ) c( ) ( ),c( ) c( ) c( ) c( ) c( ),
+ + - - 2- + + - -
K + c H = OH + HA + 2c A K + H = OH + HA + 2 H2A
c( K + ) - c( OH - ) = c( HA - ) + 2 c ( H2A ) - c( H + ), C 选项错误。 b 点时 c (H c + ( )· c (
-
A ) 2- ) = 10 -4.3 ,c( H + ) = 10 -4.3 ,所以
HA
c( ) c ,D选项正确。
- 2-
HA = (A )
化学试题答案 第 页(共 页)
2 4二、非选择题:本题共 小题,共 分。
4 58
( 分,每空2分)
15. 14
()第四周期 族
1 ⅢA
() ==
+ 3+
2 2Ga2S3+3O2+12H 4Ga +6S+6H2O
() ( )
3 Fe OH 3
() 进入无机相,使 和 分离,除去 ( ) == ( )
2+ 3+ 2+ 2+
4 Zn Ga Zn Zn 2Ga HA2 R2+3H2SO4 Ga2 SO4 3+4RH+2H2A2
()
5 ac
()[ ( )] ==
- - -
6 Ga OH 4 +3e Ga+4OH
【解析】() 和 位于同一主族,所以 位于第四周期 族。()在酸性条件下, 可氧化 价的 和 ,
2+
1 Ga Al Ga ⅢA 2 O2 -2 S Fe
所以离子方程式为 == 。()根据已知条件中沉淀的 和流程图可知,中
+ 3+
2Ga2S3+ 3O2+ 12H 4Ga + 6S+ 6H2O 3 pH
和除杂时生成 ( )沉淀。()根据 、 协同萃取体系对金属离子的优先萃取顺序为
3+ 3+
Fe OH 3 4 P204 YW100 :Fe > Ga >
, 进入无机相, 进入有机相,使 和 分离,除去 ;反萃取时,加入 ,平衡逆向移
2+ 2+ 2+ 3+ 3+ 2+ 2+
Fe > Zn Zn Ga Ga Zn Zn H2SO4
动,“反萃取”加入稀硫酸的化学方程式为 ( ) == ( ) 。()[ ( )]的
-
2Ga HA2 R2+3H2SO4 Ga2 SO4 3+4RH+2H2A2 5 Ga OH 4
结构和[ ( )]相似,含有极性共价键和配位键。()由[ ( )]制备 发生还原反应,所以阴极电极反
- -
Al OH 4 6 Ga OH 4 Ga
应为[ ( )] == 。
- - -
Ga OH 4 +3e Ga+4OH
( 分,除标注外每空2分)
16. 14
() ======N==i======
1 H2 + O2 乙基蒽醌 H2O2
() ( 或 或 )
2 hmde hmed mhde mhed
() 、 、
3 Ⅰ Ⅱ Ⅲ Ⅳ
()防止 和 混合气体在加热时发生爆炸( 分)
4 H2 O2 1
()除去 中的混有的 、 ( 分)
5 H2 HCl H2O 1
() 滴入最后半滴酸性 标准溶液,溶液由无色变为浅紫色,且半分钟内不褪色
6 ① KMnO4 ②54.4%
【解析】()总反应是 和 在乙基蒽醌和 的催化作用下生成 。()根据反应原理,乙基蒽醌先和 反
1 H2 O2 Ni H2O2 2 H2
应,所以先打开活塞 和 ,等第一步反应完成后,抽出剩余的 ,关闭活塞 和 ,打开活塞 和 ,发生第
Ⅰ Ⅱ H2 Ⅰ Ⅱ Ⅲ Ⅳ
二步反应,根据反应的原理,接口的连接顺序为 或 或 或 。()抽出剩余 的目的是
hmde hmed mhde mhed 4 H2
防止剩余的 和 混合气体在加热时发生爆炸。()除去 中混有的 、 防止催化剂中毒。()滴定时发
H2 O2 5 H2 HCl H2O 6
生氧化还原反应的方程式为 == 。由于第三次滴定消耗标准液的体
- + 2+
2MnO4 +5H2O2+6H 2Mn +5O2↑ +8H2O
积误差较大,所以该数据舍去,第一次滴定可求出 待测液中n( )
-1 -3
500mL H2O2 =0.0500mol·L ×32.02×10 L×
;第二次滴定可求出 待测液中n( ) ;综合
-1 -3
2.5×500/50 500mL H2O2 =0.0500mol·L ×31.98×10 L×2.5×500/50
两次求平均值为n( ) ,m( ) ,所以产品中 质量分数为 。
H2O2 =0.04mol H2O2 =1.36g H2O2 1.36/2.5×100%=54.4%
( 分,除标注外每空 分)
17. 15 2
() () ()
1 < 2 +43 3 BC
() 温度升高,催化剂对反应 的催化活性降低,乙烯的选择性降低
4 ①N ② Ⅱ ③0.77%
() 立方体(或正方体)( 分) 2a
5 ① 1 ②
2
化学试题答案 第 页(共 页)
3 4【解析】()反应物的气体分子总数大于生成物。() 。() 催化剂 对应的
1 2 803×2+436-1071-464×2=43 4 ① N
乙烯平衡选择性高, 平衡转化率也高。 温度升高,催化剂对反应 的催化活性降低,乙烯的选择性降低。
CO2 ② Ⅱ
() () () ()
③ CO2 g +H2 g CO g +H2O g
n( )
mol 1 3 0 0
n( )
Δ mol 0.08 0.08 0.08 0.08
n( ) x x x
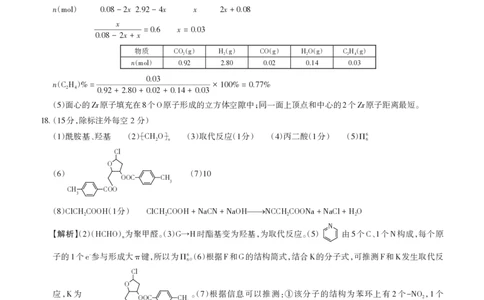
mol 0.92 2.92-4 0.08-2 2 +0.08
() () () ()
2CO g +4H2 g C2H4 g +2H2O g
n( )
mol 0.08 2.92 0 0.08
n( ) x x x x
Δ mol 2 4 2
n( ) x x x x
mol 0.08-2 2.92-4 2 +0.08
x
x
x x =0.6 = 0.03
0.08 − 2 +
物质 () () () () ()
CO2 g H2 g CO g H2O g C2H4 g
n( )
mol 0.92 2.80 0.02 0.14 0.03
n( ) 0.03
C2H4 %= × 100% = 0.77%
0.92 + 2.80 + 0.02 + 0.14 + 0.03
()面心的 原子填充在 个 原子形成的立方体空隙中;同一面上顶点和中心的 个 原子距离最短。
5 Zr 8 O 2 Zr
( 分,除标注外每空2分)
18. 15
()酰胺基、羟基 ()[ ] ()取代反应( 分) ()丙二酸( 分) ()
1 2 CH2O n 3 1 4 1 5 Π 6 6
Cl
O
() ()
6 7 10
OOC CH
3
CH COO
3
() ( 分) ¾¾¾®
8 ClCH2COOH 1 ClCH2COOH+NaCN+NaOH NCCH2COONa+NaCl+H2O
【解析】()( )为聚甲醛。() 时酯基变为羟基,为取代反应。() N 由 个 、个 构成,每个原
2 HCHO n 3 G→H 5 5 C 1 N
子的 个 参与形成大 键,所以为 。()根据 和 的结构简式,结合 的分子式,可推测 和 发生取代反
- 6
1 e π Π6 6 F G K F K
Cl
O
应, 为 。( )根据信息可以推测: 该分子的结构为苯环上有 个 ,个
K
OOC CH
7 ① 2 -NO2 1
3
CH COO
3
,共有 种同分异构体; 该分子的结构为苯环上有 个 ,个 ,共有 种同分异构体; 该分
-CH3 6 ② 1 -NO2 1 -CH2NO2 3 ③
子的结构为苯环上有 个 ( ),有 种同分异构体。()由 酸性水解得 可推测是 水
1 -CH NO2 2 1 8 N HOOCCH2COOH -CN
解得 ,且 是 在碱性条件下生成的,所以 为 ,M和 发生取代反应得 ,可推M为
-COOH N M N NCCH2COONa NaCN N
, 生成 的化学方程式 ¾¾¾® 。
ClCH2COOH M N ClCH2COOH+NaCN+NaOH NCCH2COONa+NaCl+H2O
化学试题答案 第 页(共 页)
4 4