文档内容
宜宾三中高2023级高三第一次模拟考试
化学试题
注意事项:
1. 答卷前,考生务必将自己的班级、姓名、考号填写在答题卡上。
2. 回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其它答案标号。回答非选择题时,用黑色字迹的笔将答案写在答题卡上。写在本试卷
上无效。
可能用到的相对原子质量:H-1 Li-7 Be-9 C-12 N-14 O-16 Cl-35.5
一、选择题(本题包括 15个小题,每小题 3分,共 45分,每小题只有一个选项符合题意)
1.2024年12月,中国申报的“春节——中国人庆祝传统新年的社会实践”正式列入《人类非
物质文化遗产代表作名录》。下列有关春节习俗中的化学知识说法错误的是
A.“剪窗花”纸张的主要成分是纤维素,纤维素与淀粉互为同分异构体
B.“放烟花”利用某些金属元素的焰色试验,焰色试验属于物理变化
C.“蒸馒头”使用的发酵粉中小苏打属于盐类物质
D.“做豆腐”一系列过程中涉及胶体的性质,胶体是一种分散系
2. 下列化学用语的表达正确的是
A. HClO的空间填充模型: B. CH COOH中的C-C键为:sp3-sp2σ键
3
C. 的名称:二乙酸乙二酯 D. 丙烷中碳原子杂化轨道示意图:
3. 常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:
B.由水电离出 为 的溶液:NO -、Fe2+、NH +、Cl-
3 4
C.使甲基橙变红色的溶液:
D.通入足量 的溶液:
4.根据下列实验操作和现象所得结论错误的是
选项 实验操作和现象 结论
A 用激光笔照射某有色玻璃,看到一条光亮的“通路” 该有色玻璃是胶体
B 用铂丝蘸取溶液在酒精灯外焰上灼烧,观察到黄色 溶液中有钠盐
用惰性电极电解CuCl 溶液,将湿润的淀粉KI试纸靠
2
C 阳极有Cl 生成
2
近阳极,试纸变蓝
D 向FeCl 溶液中滴加KSCN溶液,一段时间后溶液变红 Fe2+被氧化为Fe3+
2
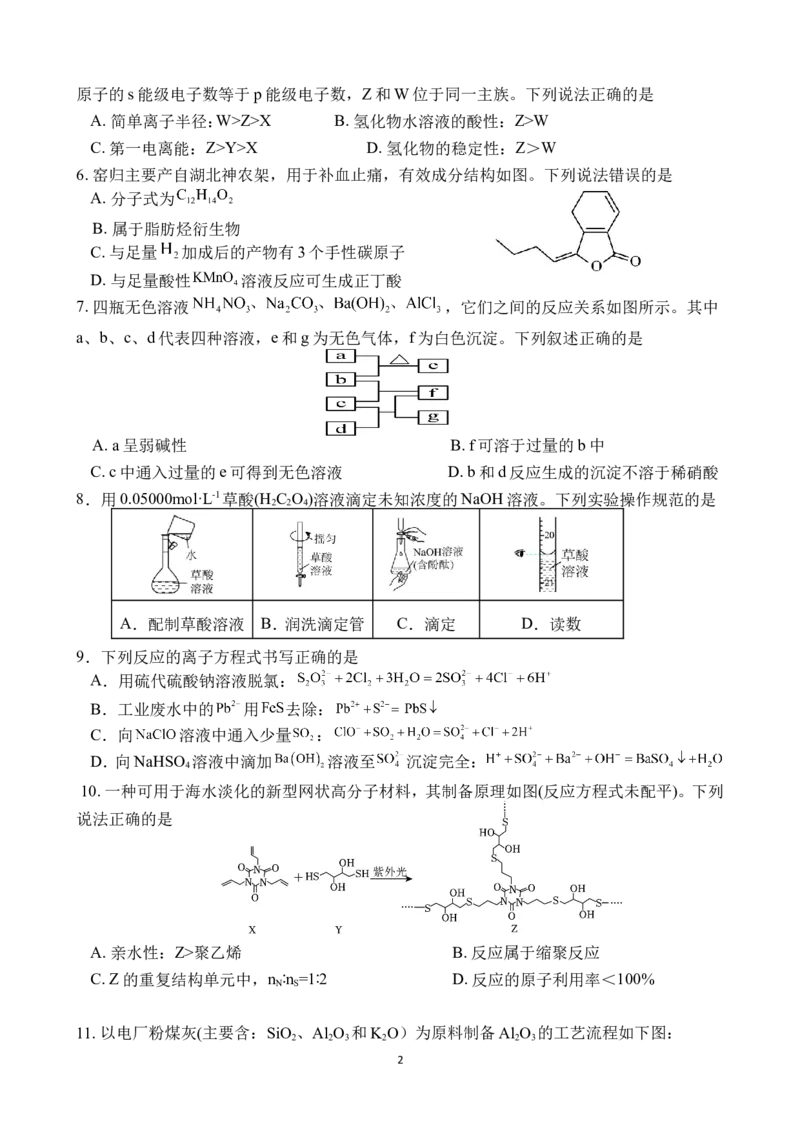
5.短周期主族元素X、Y、Z、W的原子序数依次增大,X的简单氢化物常用作制冷剂,基态Y
1原子的s能级电子数等于p能级电子数,Z和W位于同一主族。下列说法正确的是
A. 简单离子半径:W>Z>X B. 氢化物水溶液的酸性:Z>W
C. 第一电离能:Z>Y>X D. 氢化物的稳定性:Z>W
6. 窑归主要产自湖北神农架,用于补血止痛,有效成分结构如图。下列说法错误的是
A. 分子式为
B. 属于脂肪烃衍生物
C. 与足量 加成后的产物有3个手性碳原子
D. 与足量酸性 溶液反应可生成正丁酸
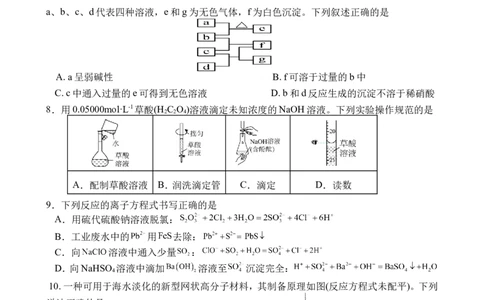
7. 四瓶无色溶液 ,它们之间的反应关系如图所示。其中
a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列叙述正确的是
A. a呈弱碱性 B. f可溶于过量的b中
C. c中通入过量的e可得到无色溶液 D. b和d反应生成的沉淀不溶于稀硝酸
8.用0.05000mol·L-1草酸(H C O )溶液滴定未知浓度的NaOH溶液。下列实验操作规范的是
2 2 4
A.配制草酸溶液 B.润洗滴定管 C.滴定 D.读数
9.下列反应的离子方程式书写正确的是
A.用硫代硫酸钠溶液脱氯:
B.工业废水中的 用 去除:
C.向 溶液中通入少量 :
D.向NaHSO 溶液中滴加 溶液至 沉淀完全:
4
10. 一种可用于海水淡化的新型网状高分子材料,其制备原理如图(反应方程式未配平)。下列
说法正确的是
A. 亲水性:Z>聚乙烯 B. 反应属于缩聚反应
C. Z的重复结构单元中,n ∶n =1∶2 D. 反应的原子利用率<100%
N S
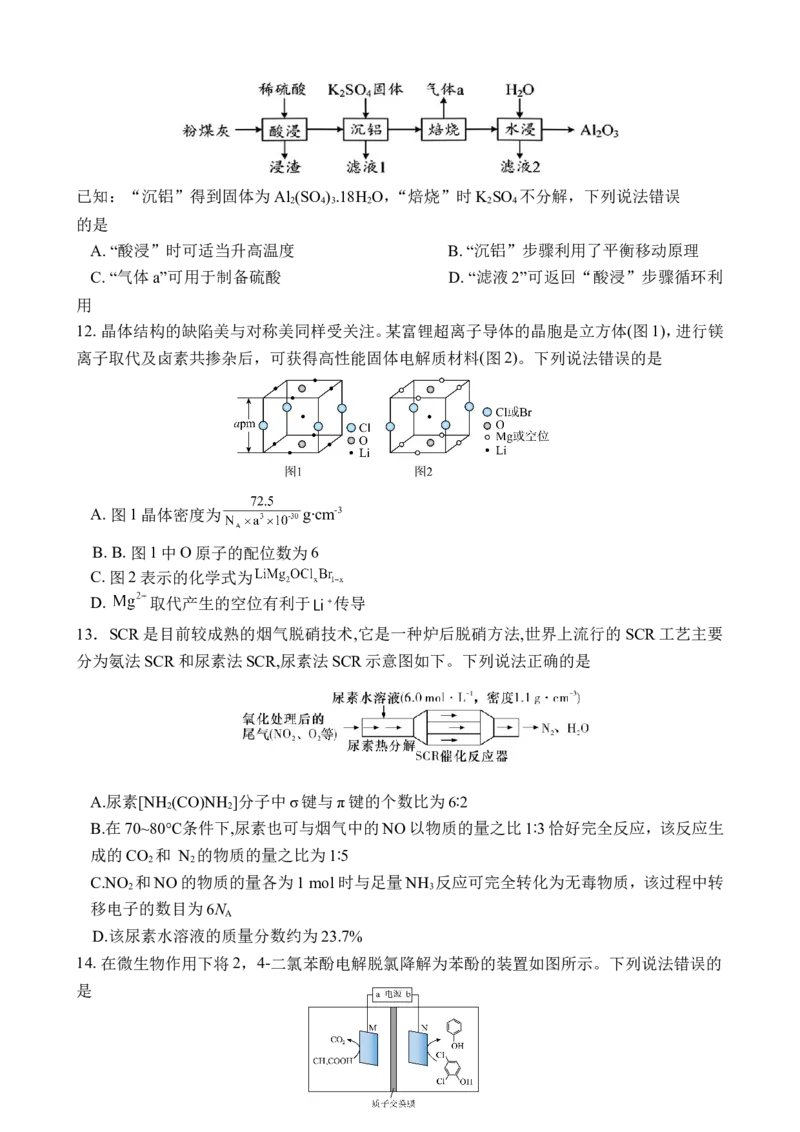
11. 以电厂粉煤灰(主要含:SiO 、Al O 和K O)为原料制备Al O 的工艺流程如下图:
2 2 3 2 2 3
2已知:“沉铝”得到固体为Al (SO ) .18H O,“焙烧”时K SO 不分解,下列说法错误
2 4 3 2 2 4
的是
A. “酸浸”时可适当升高温度 B. “沉铝”步骤利用了平衡移动原理
C. “气体a”可用于制备硫酸 D. “滤液2”可返回“酸浸”步骤循环利
用
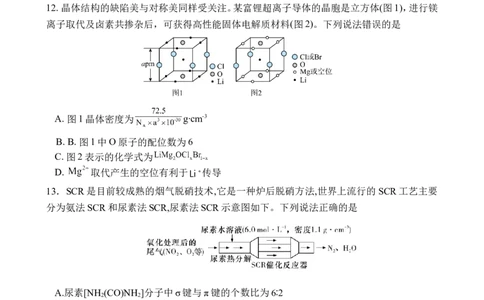
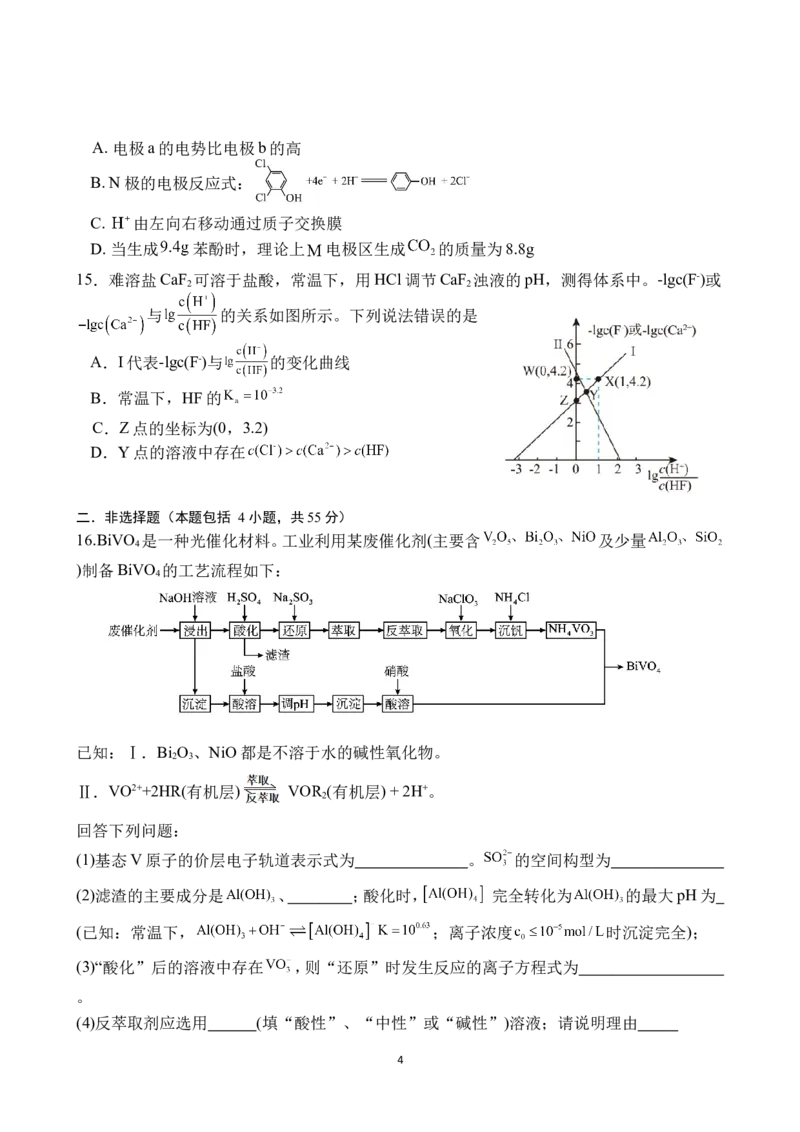
12. 晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁
离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A. 图1晶体密度为 g∙cm-3
B. B. 图1中O原子的配位数为6
C. 图2表示的化学式为
D. 取代产生的空位有利于 传导
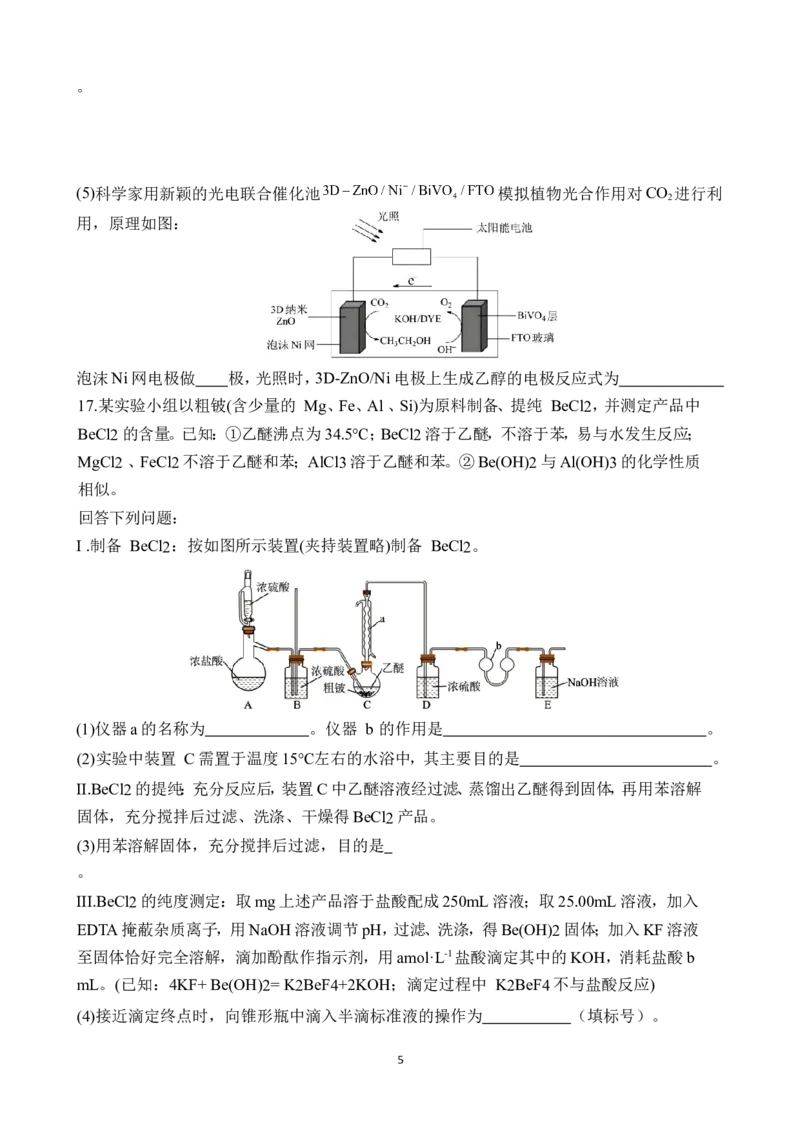
13.SCR是目前较成熟的烟气脱硝技术,它是一种炉后脱硝方法,世界上流行的SCR工艺主要
分为氨法SCR和尿素法SCR,尿素法SCR示意图如下。下列说法正确的是
A.尿素[NH (CO)NH ]分子中σ键与π键的个数比为6∶2
2 2
B.在70~80℃条件下,尿素也可与烟气中的NO以物质的量之比1∶3恰好完全反应,该反应生
成的CO 和 N 的物质的量之比为1∶5
2 2
C.NO 和NO的物质的量各为1 mol 时与足量NH 反应可完全转化为无毒物质,该过程中转
2 3
移电子的数目为6N
A
D.该尿素水溶液的质量分数约为23.7%
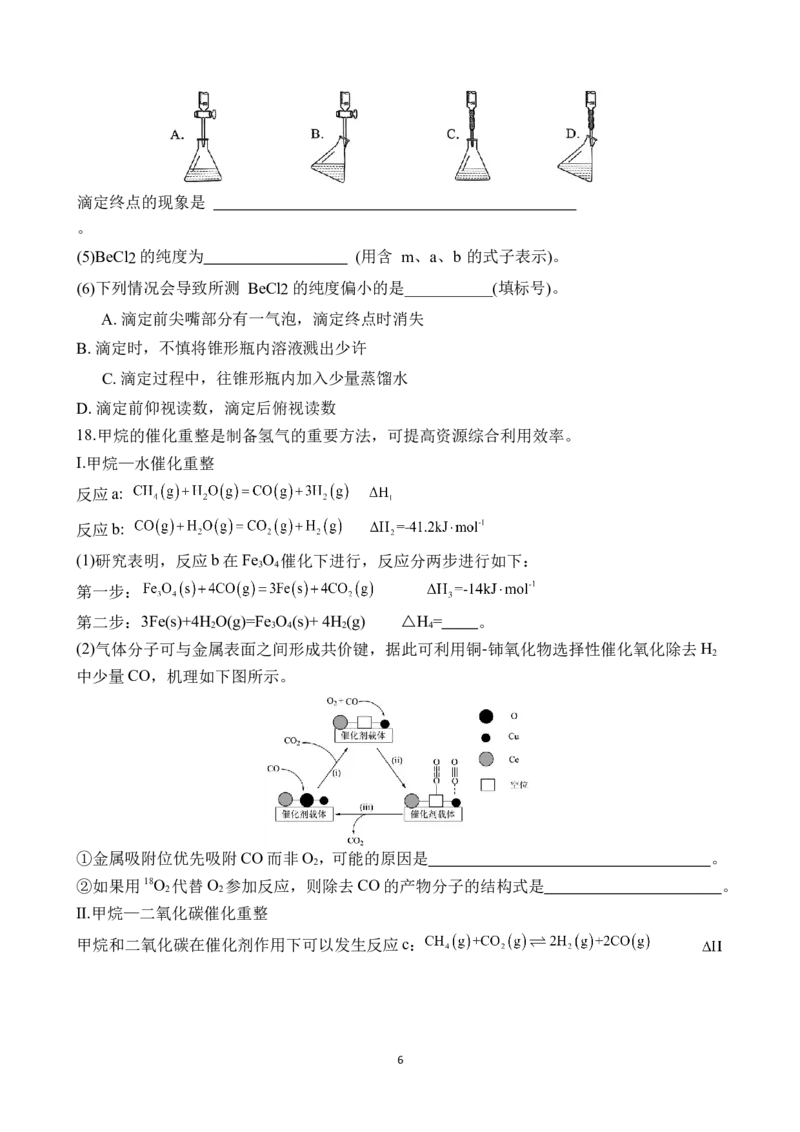
14. 在微生物作用下将2,4-二氯苯酚电解脱氯降解为苯酚的装置如图所示。下列说法错误的
是
3A. 电极a的电势比电极b的高
B. N极的电极反应式:
C. 由左向右移动通过质子交换膜
D. 当生成 苯酚时,理论上 电极区生成 的质量为8.8g
15.难溶盐CaF 可溶于盐酸,常温下,用HCl调节CaF 浊液的pH,测得体系中。-lgc(F-)或
2 2
与 的关系如图所示。下列说法错误的是
A.I代表-lgc(F-)与 的变化曲线
B.常温下,HF的
C.Z点的坐标为(0,3.2)
D.Y点的溶液中存在
二.非选择题(本题包括 4 小题,共55分)
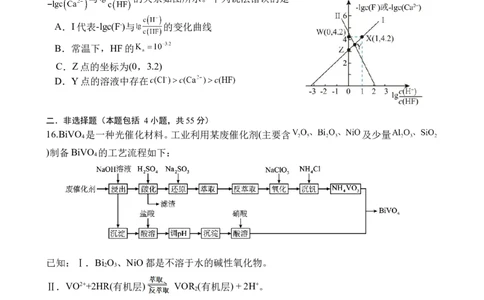
16.BiVO 是一种光催化材料。工业利用某废催化剂(主要含 及少量
4
)制备BiVO 的工艺流程如下:
4
已知:Ⅰ.Bi O 、NiO都是不溶于水的碱性氧化物。
2 3
Ⅱ.VO2++2HR(有机层) VOR (有机层) + 2H+。
2
回答下列问题:
(1)基态V原子的价层电子轨道表示式为 。 的空间构型为
(2)滤渣的主要成分是 、 ;酸化时, 完全转化为 的最大pH为
(已知:常温下, ;离子浓度 时沉淀完全);
(3)“酸化”后的溶液中存在 ,则“还原”时发生反应的离子方程式为
。
(4)反萃取剂应选用 (填“酸性”、“中性”或“碱性”)溶液;请说明理由
4。
(5)科学家用新颖的光电联合催化池 模拟植物光合作用对CO 进行利
2
用,原理如图:
泡沫Ni网电极做 极,光照时,3D-ZnO/Ni电极上生成乙醇的电极反应式为
17.某实验小组以粗铍(含少量的 Mg、Fe、Al 、Si)为原料制备、提纯 BeCl2,并测定产品中
BeCl2 的含量。已知:①乙醚沸点为34.5℃;BeCl2溶于乙醚,不溶于苯,易与水发生反应;
MgCl2 、FeCl2不溶于乙醚和苯;AlCl3溶于乙醚和苯。②Be(OH)2与Al(OH)3的化学性质
相似。
回答下列问题:
I .制备 BeCl2:按如图所示装置(夹持装置略)制备 BeCl2。
(1)仪器a的名称为 。仪器 b 的作用是 。
(2)实验中装置 C需置于温度15℃左右的水浴中,其主要目的是 。
II.BeCl2的提纯:充分反应后,装置C中乙醚溶液经过滤、蒸馏出乙醚得到固体,再用苯溶解
固体,充分搅拌后过滤、洗涤、干燥得BeCl2产品。
(3)用苯溶解固体,充分搅拌后过滤,目的是
。
III.BeCl2的纯度测定:取mg上述产品溶于盐酸配成250mL溶液;取25.00mL溶液,加入
EDTA掩蔽杂质离子,用NaOH溶液调节pH,过滤、洗涤,得Be(OH)2固体;加入KF溶液
至固体恰好完全溶解,滴加酚酞作指示剂,用amol·L-1盐酸滴定其中的KOH,消耗盐酸b
mL。(已知:4KF+ Be(OH)2= K2BeF4+2KOH;滴定过程中 K2BeF4不与盐酸反应)
(4)接近滴定终点时,向锥形瓶中滴入半滴标准液的操作为 (填标号)。
5滴定终点的现象是
。
(5)BeCl2的纯度为 (用含 m、a、b 的式子表示)。
(6)下列情况会导致所测 BeCl2的纯度偏小的是___________(填标号)。
A. 滴定前尖嘴部分有一气泡,滴定终点时消失
B. 滴定时,不慎将锥形瓶内溶液溅出少许
C. 滴定过程中,往锥形瓶内加入少量蒸馏水
D. 滴定前仰视读数,滴定后俯视读数
18.甲烷的催化重整是制备氢气的重要方法,可提高资源综合利用效率。
I.甲烷—水催化重整
反应a:
反应b:
(1)研究表明,反应b在Fe O 催化下进行,反应分两步进行如下:
3 4
第一步:
第二步:3Fe(s)+4H O(g)=Fe O (s)+ 4H (g) △H = 。
2 3 4 2 4
(2)气体分子可与金属表面之间形成共价键,据此可利用铜-铈氧化物选择性催化氧化除去H
2
中少量CO,机理如下图所示。
①金属吸附位优先吸附CO而非O ,可能的原因是 。
2
②如果用18O 代替O 参加反应,则除去CO的产物分子的结构式是 。
2 2
Ⅱ.甲烷—二氧化碳催化重整
甲烷和二氧化碳在催化剂作用下可以发生反应c:
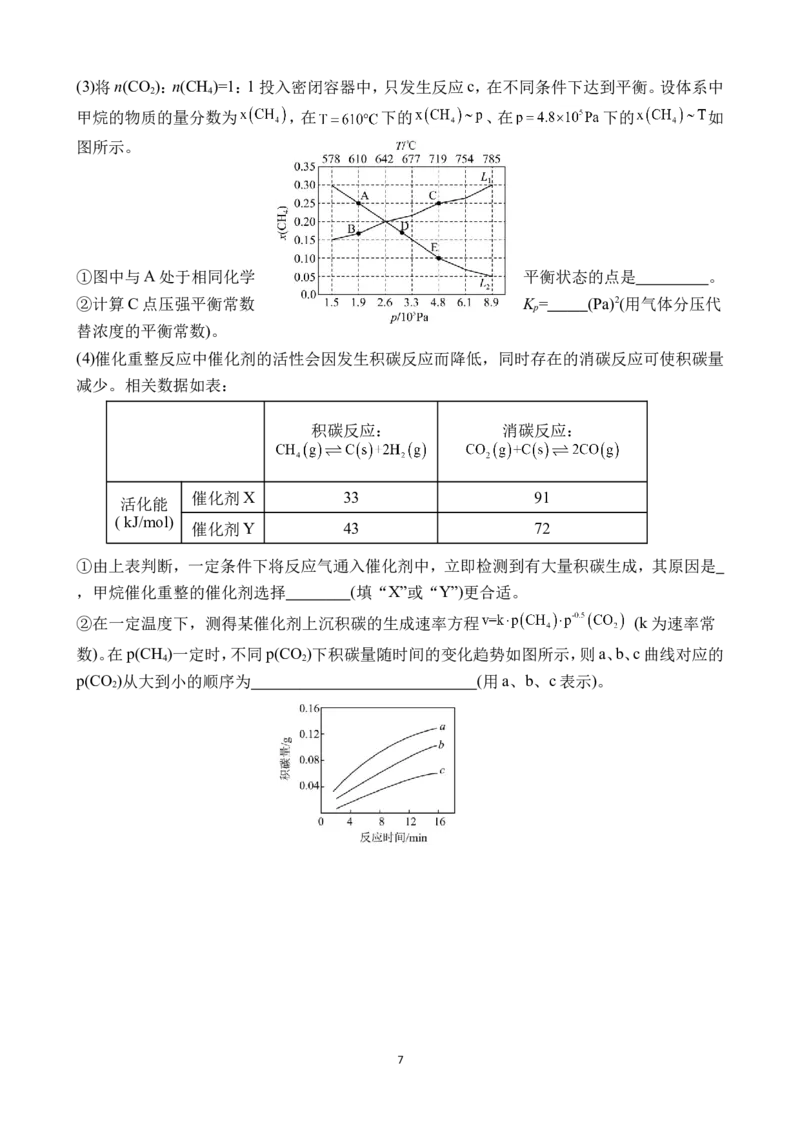
6(3)将n(CO ):n(CH )=1:1投入密闭容器中,只发生反应c,在不同条件下达到平衡。设体系中
2 4
甲烷的物质的量分数为 ,在 下的 、在 下的 如
图所示。
①图中与A处于相同化学 平衡状态的点是 。
②计算C点压强平衡常数 K = (Pa)2(用气体分压代
p
替浓度的平衡常数)。
(4)催化重整反应中催化剂的活性会因发生积碳反应而降低,同时存在的消碳反应可使积碳量
减少。相关数据如表:
积碳反应: 消碳反应:
催化剂X 33 91
活化能
( kJ/mol)
催化剂Y 43 72
①由上表判断,一定条件下将反应气通入催化剂中,立即检测到有大量积碳生成,其原因是
,甲烷催化重整的催化剂选择 (填“X”或“Y”)更合适。
②在一定温度下,测得某催化剂上沉积碳的生成速率方程 (k为速率常
数)。在p(CH )一定时,不同p(CO )下积碳量随时间的变化趋势如图所示,则a、b、c曲线对应的
4 2
p(CO )从大到小的顺序为 (用a、b、c表示)。
2
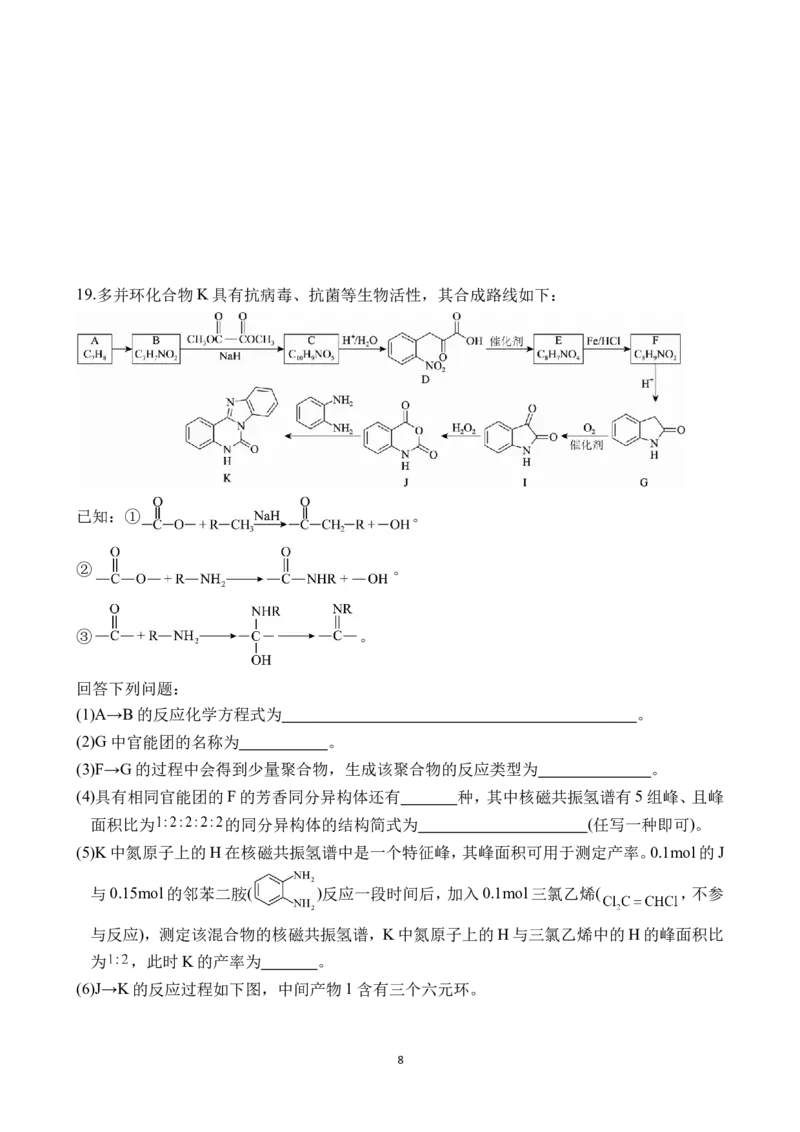
719.多并环化合物K具有抗病毒、抗菌等生物活性,其合成路线如下:
已知:① 。
② 。
③ 。
回答下列问题:
(1)A→B的反应化学方程式为 。
(2)G中官能团的名称为 。
(3)F→G的过程中会得到少量聚合物,生成该聚合物的反应类型为 。
(4)具有相同官能团的F的芳香同分异构体还有 种,其中核磁共振氢谱有5组峰、且峰
面积比为 的同分异构体的结构简式为 (任写一种即可)。
(5)K中氮原子上的H在核磁共振氢谱中是一个特征峰,其峰面积可用于测定产率。0.1mol的J
与0.15mol的邻苯二胺( )反应一段时间后,加入0.1mol三氯乙烯( ,不参
与反应),测定该混合物的核磁共振氢谱,K中氮原子上的H与三氯乙烯中的H的峰面积比
为 ,此时K的产率为 。
(6)J→K的反应过程如下图,中间产物1含有三个六元环。
8中间产物1、3的结构简式别为 、 。
9