文档内容
衢州、丽水、湖州 2025 年 4 月三地市高三教学质量检测
化学试题卷
考生须知:
1.本卷满分100分,考试时间90分钟;
2.答题前,在答题卷指定区域填写班级、姓名、试场号、座位号及准考证号;
3.所有答案必须写在答题卷上,写在试卷上无效;
4.考试结束后,只需上交答题卷。
可能用到的相对原子质量: H-1 Li-7 C-12 O-16 Na-23 Al-27 S-32 Fe-56
一、选择题(本大题共16小题,每小题3分,共48分。每个小题列出的四个备选项中只有
一个是符合题目要求的,不选、多选、错选均不得分)
1.下列物质属于碱的是
A.KOH B.Na O C.CH OH D.H SO
2 3 2 4
2.化学与生产生活密切相关,下列说法不
.
正
.
确
.
的是
A.碳酸钠溶液呈碱性,可用作食用碱或工业用碱
B.碳化硅硬度很大,可用作砂纸和砂轮的磨料
C.淀粉能发生酯化反应,其产物可用于生产可降解塑料
D.不锈钢的主要元素是铬和镍,可用于生产餐具、医疗器材等
3.下列化学用语表示正确的是
A.2−丁烯的键线式: B.乙醚的结构简式:CH OCH
3 3
C.氨气的球棍模型: D.HBr的电子式:
4.关于实验室安全,下列说法不
.
正
.
确
.
的是
A.轻微烫伤时,可先用洁净的冷水处理,降低局部温度,然后涂上烫伤药膏
B.观察钠在空气中燃烧的现象需戴护目镜,且不能近距离俯视坩埚
C.实验结束后,有利用价值的有机废液,可蒸馏回收特定馏分
D.苯酚不慎沾到皮肤上,可用酒精或65℃以上的水冲洗
5.下列说法不
.
正
.
确
.
的是
A.处于最低能量状态的原子叫基态原子 B.K、Na、Li原子半径逐渐减小
C.粉末状固体肯定不是晶体 D.HF、HCl、HBr稳定性逐渐减弱
6.关于NaNO
2
的性质,下列说法不
.
正
.
确
.
的是
A.NaNO 有一定毒性,但可用作食品添加剂
2
B.酸性条件下NaNO 能使淀粉−KI溶液变蓝,说明该条件下氧化性:NO->I
2 2 2
C.NO-、NO 、NO+三种微粒中,氧化性最强的是NO-
2 2 2 2
D.1molNaNO 被足量酸性KMnO 氧化为NaNO ,转移电子的数目为2N
2 4 3 A
7.物质结构决定性质,下列说法不
.
正
.
确
.
的是
A.纤维素结构单元中具有多个羟基,故纯棉衣物具有良好的吸汗性
B.在较低压力和温度下制得的聚乙烯支链较少,故属于低密度聚乙烯
C.石墨中每个碳原子有一个未参与杂化的2p电子,故石墨有类似于金属晶体的导电性
D.由于施加电场可使液晶的长轴取向发生不同程度的改变,故液晶可显示文字或图像
高三化学 第1页 共8页
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}8.下列方程式正确的是
A.酸催化条件下制酚醛树脂:
B.要注入炽热铁水的模具必须干燥的原因:2Fe+6H O(g) 2Fe(OH) +3H
2 3 2
C.乙醇中加入酸性KCrO 溶液:3CHCHOH+2Cr O2-+16H+═3CH COOH+4Cr3++11HO
2 2 7 3 2 2 7 3 2
D.向FeBr 溶液中通入过量的Cl :2Fe2++2Br−+2Cl ═2Fe3++Br +4Cl−
2 2 2 2
9.关于阿司匹林有效成分乙酰水杨酸( )分子结构的测定和官能团的检验,
下列说法正确的是
A.元素分析仪可确定乙酰水杨酸的分子式,红外光谱可确定分子中含有羧基和酯基
B.X射线衍射仪可测定乙酰水杨酸分子中键长、键角、键能等数据
C.将阿司匹林研碎后加入适量水,在上层清液中滴加石蕊溶液可检验羧基
D.将阿司匹林研碎后加入适量水,在上层清液中加入几滴稀硫酸,再滴入几滴FeCl
3
溶液可检验水解产物中的酚羟基
10.某实验小组按照“研磨→灰化→溶解→过滤→检验”的步骤检验菠菜中铁元素(主要
以难溶的FeC 2 O 4 存在),下列说法不 . 正 . 确 . 的是
A.向研磨后的菠菜汁中加入H O 和KSCN溶液未观察到溶液变红,说明菠菜不含
2 2
铁元素
B.灰化步骤能除去有机质且将铁元素转化为铁的氧化物,有利于后续检验
C.溶解步骤,可选用稀硝酸
D.检验步骤,加入K [Fe(CN) ]溶液后有蓝色沉淀生成说明菠菜中含有铁元素
4 6
11.下列说法正确的是
A.可燃物的燃烧均为放热熵增的过程,故能自发进行
B.某反应的正反应活化能小于逆反应活化能,则该反应ΔH<0
C.对于反应:C(s)+H O(g) CO(g)+H (g),当混合气体的平均摩尔质量保持不变,
2 2
则一定处于化学平衡状态
⇌
D.升高温度平衡向吸热方向移动,原因是吸热方向反应物分子中活化分子的百分数
增大,放热方向减小
12.异烟肼是一种抗结核药物,可以与香草醛反应生成异烟腙,其转化过程如下:
O
C OH
O H O
(香草醛)OCH
N NHNH 2 3 N NHN CH OH
(异烟肼) (异烟腙)
OCH
3
下列说法正确的是
A.异烟腙分子式为C H N O
14 14 3 3
B.异烟肼既能与酸反应又能与碱反应
C.香草醛分子中最多16个原子共平面
D.1mol香草醛与浓溴水反应时,最多消耗1molBr
2
高三化学 第2页 共8页
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}13.Cl O ( )又称高氯酸氯酰,固态Cl O 以离子形式存在,与水发生非氧化
2 6 2 6
还原反应,下列说法不正确的是
...
A.Cl O 有较强的氧化性
2 6
B.Cl O 与水反应只生成一种含氧酸
2 6
C.1molCl O 含有7molσ键
2 6
D.固态Cl O 中存在的阴阳离子分别为ClO−、ClO+
2 6 4 2
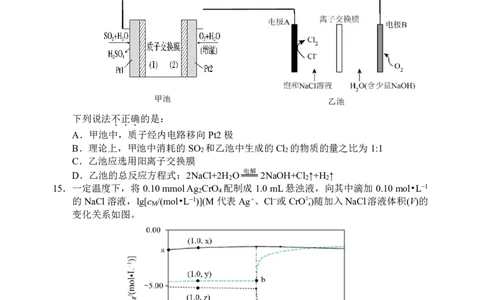
14.某小组研究设计了如下装置示意图,联合制备硫酸、氯气和氢氧化钠。该设计改变了
传统氯碱工业能耗大的缺点,可大幅度降低能耗。
甲池 乙池
下列说法不正确的是:
...
A.甲池中,质子经内电路移向Pt2极
B.理论上,甲池中消耗的SO 和乙池中生成的Cl 的物质的量之比为1:1
2 2
C.乙池应选用阳离子交换膜
电解
D.乙池的总反应方程式:2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
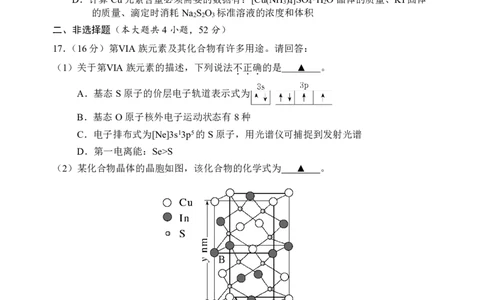
15.一定温度下,将0.10mmolAg CrO 配制成1.0mL悬浊液,向其中滴加0.10mol•L−1
2 4
的NaCl溶液,lg[c /(mol•L−1)](M代表Ag+、Cl−或CrO2−)随加入NaCl溶液体积(V)的
M 4
变化关系如图。
下列说法正确的是
A.该温度下,K (Ag CrO )=10x+2y
sp 2 4
B.a点处:2c(CrO2−)+c(OH−)=c(Ag+)+c(H+)
4
C.溶液中的c(CrO2−) 在b点时达到最大
4
D.c点处:c(CrO2−)约为0.029mol•L−1
4
高三化学 第3页 共8页
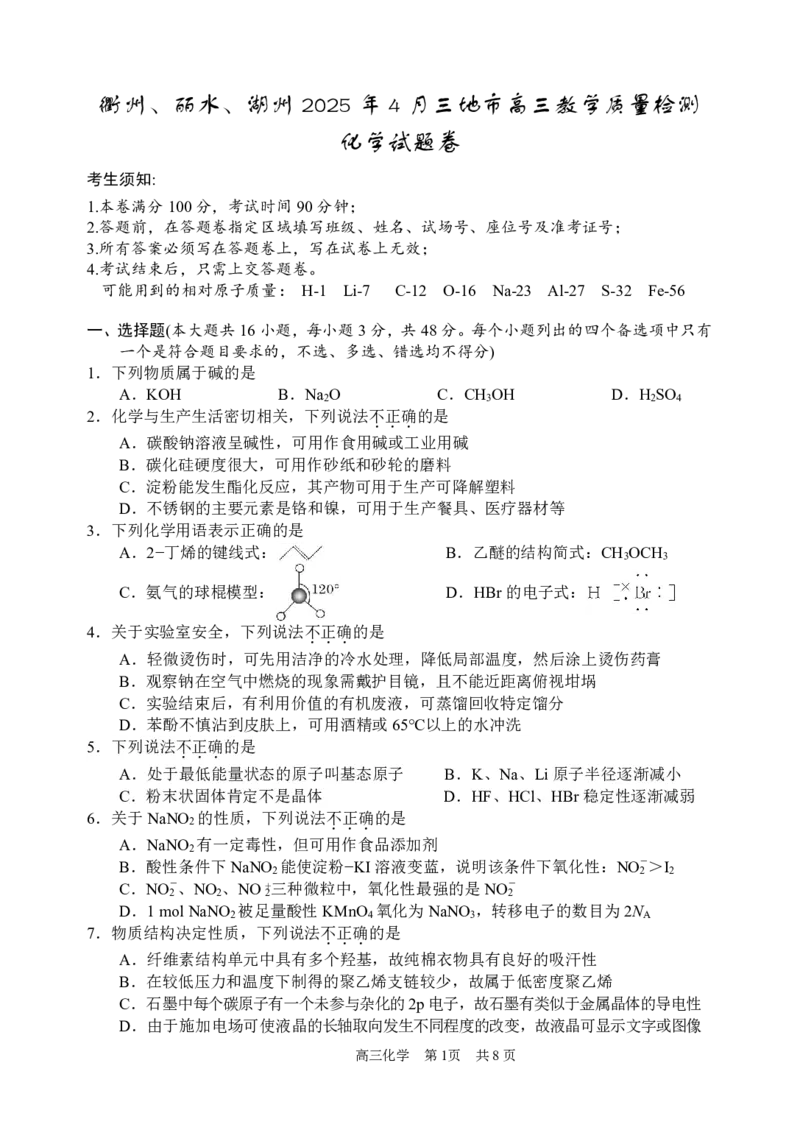
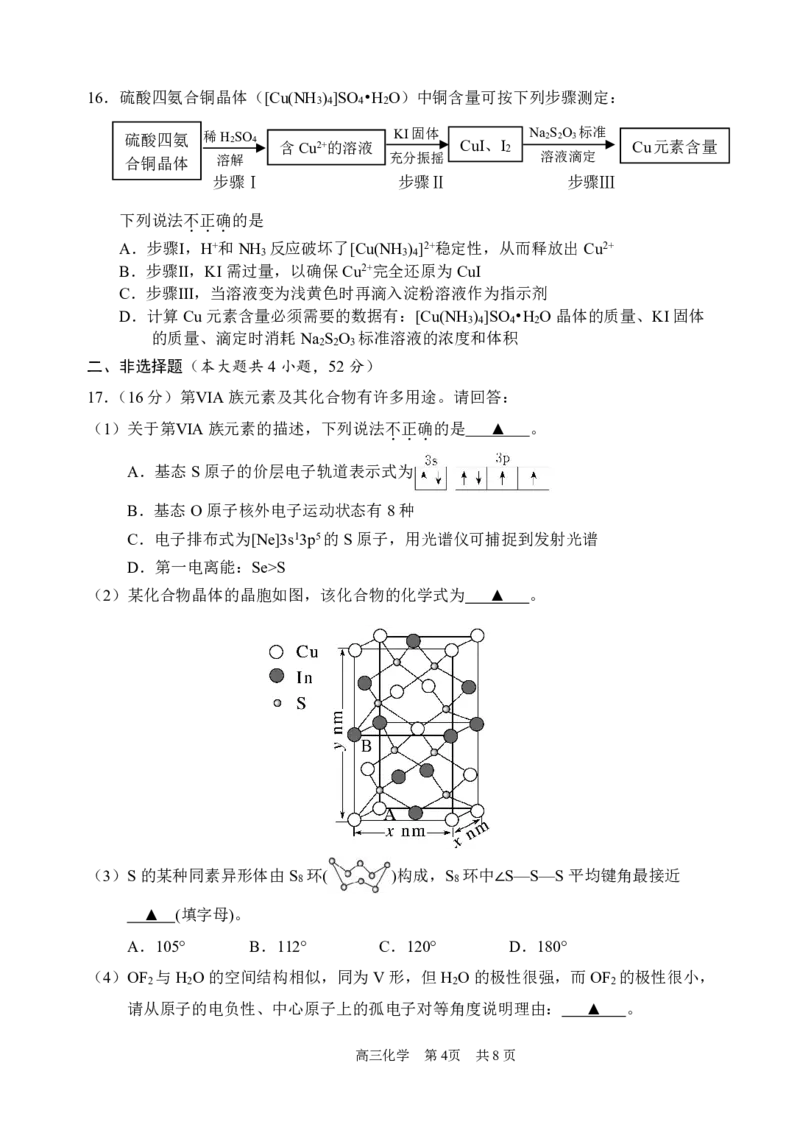
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}16.硫酸四氨合铜晶体([Cu(NH ) ]SO •H O)中铜含量可按下列步骤测定:
3 4 4 2
硫酸四氨 稀H2SO4
含Cu2+的溶液
KI固体
CuI、I 2
Na2S2O3 标准
Cu元素含量
合铜晶体 溶解 充分振摇 溶液滴定
步骤Ⅰ 步骤Ⅱ 步骤Ⅲ
下列说法不正确的是
...
A.步骤Ⅰ,H+和NH 反应破坏了[Cu(NH ) ]2+稳定性,从而释放出Cu2+
3 3 4
B.步骤Ⅱ,KI需过量,以确保Cu2+完全还原为CuI
C.步骤Ⅲ,当溶液变为浅黄色时再滴入淀粉溶液作为指示剂
D.计算Cu元素含量必须需要的数据有:[Cu(NH ) ]SO •H O晶体的质量、KI固体
3 4 4 2
的质量、滴定时消耗Na S O 标准溶液的浓度和体积
2 2 3
二、非选择题(本大题共4小题,52分)
17.(16分)第ⅥA族元素及其化合物有许多用途。请回答:
(1)关于第ⅥA族元素的描述,下列说法不 . 正 . 确 . 的是 ▲ 。
A.基态S原子的价层电子轨道表示式为
B.基态O原子核外电子运动状态有8种
C.电子排布式为[Ne]3s13p5的S原子,用光谱仪可捕捉到发射光谱
D.第一电离能:Se>S
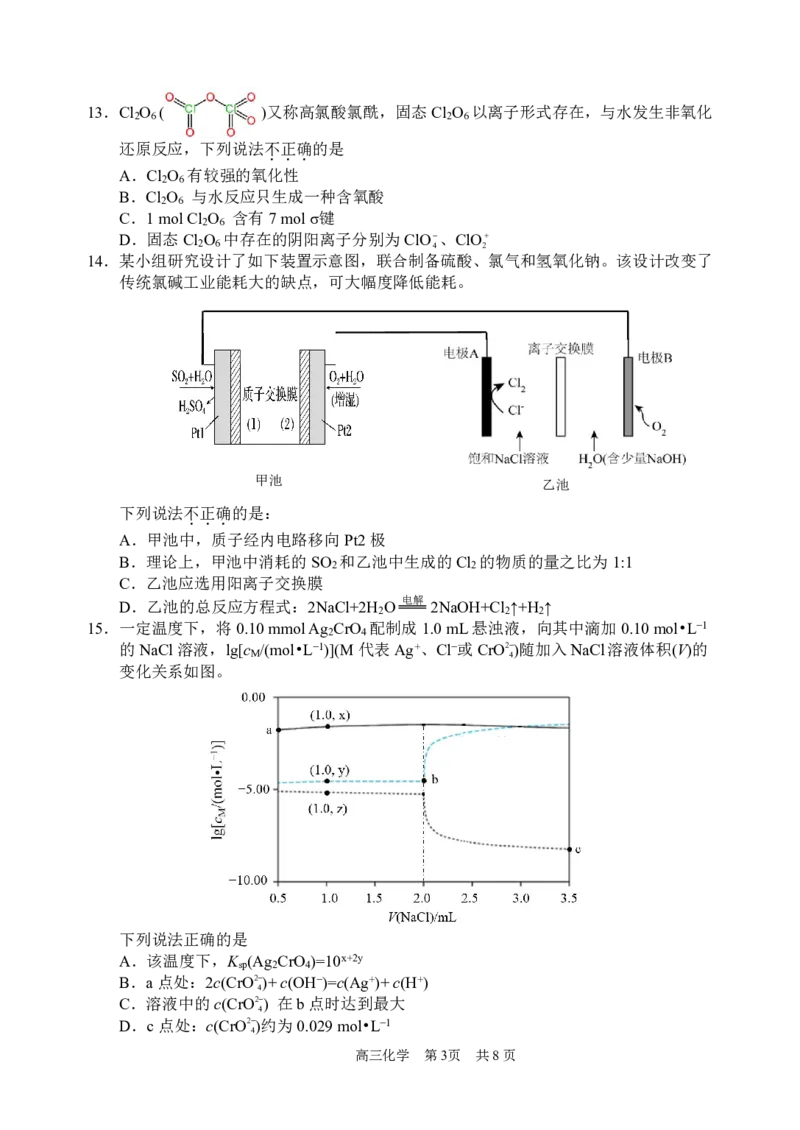
(2)某化合物晶体的晶胞如图,该化合物的化学式为 ▲ 。
(3)S的某种同素异形体由S 环( )构成,S 环中 S—S—S平均键角最接近
8 8
▲ (填字母)。 ∠
A.105° B.112° C.120° D.180°
(4)OF 与H O的空间结构相似,同为V形,但H O的极性很强,而OF 的极性很小,
2 2 2 2
请从原子的电负性、中心原子上的孤电子对等角度说明理由: ▲ 。
高三化学 第4页 共8页
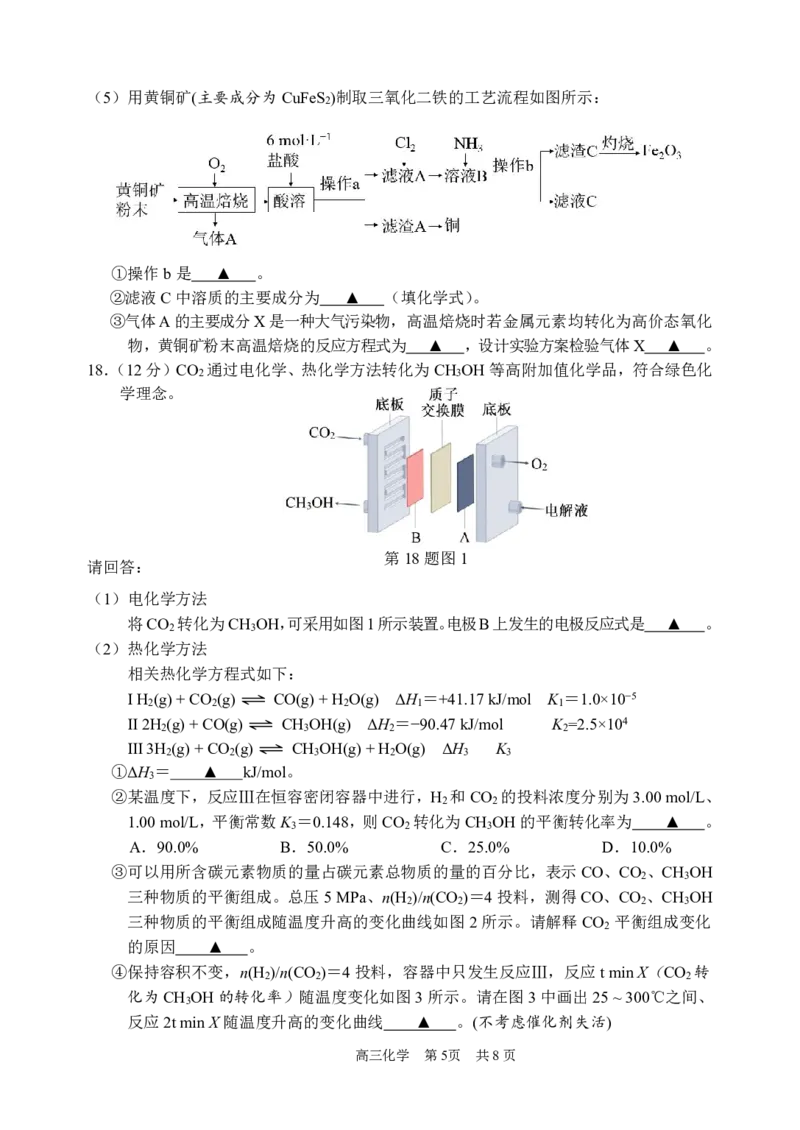
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}(5)用黄铜矿(主要成分为CuFeS )制取三氧化二铁的工艺流程如图所示:
2
①操作b是 ▲ 。
②滤液C中溶质的主要成分为 ▲ (填化学式)。
③气体A的主要成分X是一种大气污染物,高温焙烧时若金属元素均转化为高价态氧化
物,黄铜矿粉末高温焙烧的反应方程式为 ▲ ,设计实验方案检验气体X ▲ 。
18.(12分)CO 通过电化学、热化学方法转化为CH OH等高附加值化学品,符合绿色化
2 3
学理念。
第18题图1
请回答:
(1)电化学方法
将CO 转化为CH OH,可采用如图1所示装置。电极B上发生的电极反应式是 ▲ 。
2 3
(2)热化学方法
相关热化学方程式如下:
ⅠH (g)+CO (g) CO(g)+H O(g) ΔH =+41.17kJ/mol K =1.0×10−5
2 2 2 1 1
Ⅱ2H (g)+CO(g) CH OH(g) ΔH =−90.47kJ/mol K =2.5×104
2 ⇌ 3 2 2
Ⅲ3H (g)+CO (g) CH OH(g)+H O(g) ΔH K
2 2 3 2 3 3
⇌
①ΔH = ▲ kJ/mol。
3
⇌
②某温度下,反应Ⅲ在恒容密闭容器中进行,H 和CO 的投料浓度分别为3.00mol/L、
2 2
1.00mol/L,平衡常数K =0.148,则CO 转化为CH OH的平衡转化率为 ▲ 。
3 2 3
A.90.0% B.50.0% C.25.0% D.10.0%
③可以用所含碳元素物质的量占碳元素总物质的量的百分比,表示CO、CO 、CH OH
2 3
三种物质的平衡组成。总压5MPa、n(H )/n(CO )=4投料,测得CO、CO 、CH OH
2 2 2 3
三种物质的平衡组成随温度升高的变化曲线如图2所示。请解释CO 平衡组成变化
2
的原因 ▲ 。
④保持容积不变,n(H )/n(CO )=4投料,容器中只发生反应Ⅲ,反应tminX(CO 转
2 2 2
化为CH OH的转化率)随温度变化如图3所示。请在图3中画出25~300℃之间、
3
反应2tminX随温度升高的变化曲线 ▲ 。(不考虑催化剂失活)
高三化学 第5页 共8页
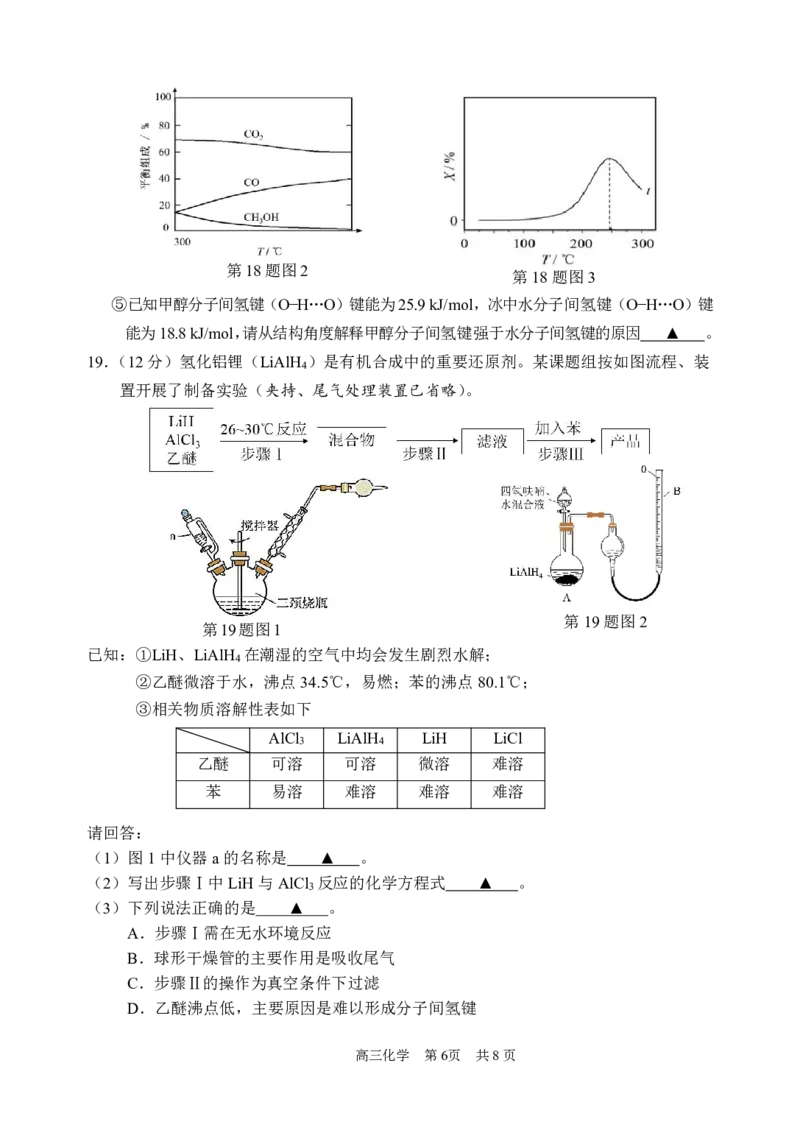
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}第18题图2
第18题图3
⑤已知甲醇分子间氢键(O−H…O)键能为25.9kJ/mol,冰中水分子间氢键(O−H…O)键
能为18.8kJ/mol,请从结构角度解释甲醇分子间氢键强于水分子间氢键的原因 ▲ 。
19.(12分)氢化铝锂(LiAlH )是有机合成中的重要还原剂。某课题组按如图流程、装
4
置开展了制备实验(夹持、尾气处理装置已省略)。
第19题图2
第19题图1
已知:①LiH、LiAlH 在潮湿的空气中均会发生剧烈水解;
4
②乙醚微溶于水,沸点34.5℃,易燃;苯的沸点80.1℃;
③相关物质溶解性表如下
AlCl LiAlH LiH LiCl
3 4
乙醚 可溶 可溶 微溶 难溶
苯 易溶 难溶 难溶 难溶
请回答:
(1)图1中仪器a的名称是 ▲ 。
(2)写出步骤Ⅰ中LiH与AlCl 反应的化学方程式 ▲ 。
3
(3)下列说法正确的是 ▲ 。
A.步骤Ⅰ需在无水环境反应
B.球形干燥管的主要作用是吸收尾气
C.步骤Ⅱ的操作为真空条件下过滤
D.乙醚沸点低,主要原因是难以形成分子间氢键
高三化学 第6页 共8页
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}(4)为提高产品的产率,应选择LiH适当过量而不是AlCl 过量,原因是 ▲ 。
3
(5)步骤Ⅲ加入苯的作用是 ▲ 。
(6)25℃,常压下,测定LiAlH(不含LiH和AlH)纯度的主要步骤如下(装置如图2所示):
4 3
①记录量气管B起始体积读数V mL
1
②调整量气管B中液面高度,读数V mL
2
③打开旋塞至滴加完所有液体,立即关闭旋塞
④称取产品LiAlH 1.90g加入圆底烧瓶A
4
⑤在分液漏斗中加入过量的四氢呋喃(可减缓LiAlH 与H O的反应速率)和水的混合液
4 2
10.0mL
上述操作正确的顺序为 ▲ →①→ ▲ → ▲ → ▲ 。计算LiAlH
4
的质量分数为 ▲ (用含V 、V 的代数式表达)。
1 2
(量气管B由碱式滴定管改装;25℃,常压下气体摩尔体积约为24.5L/mol。)
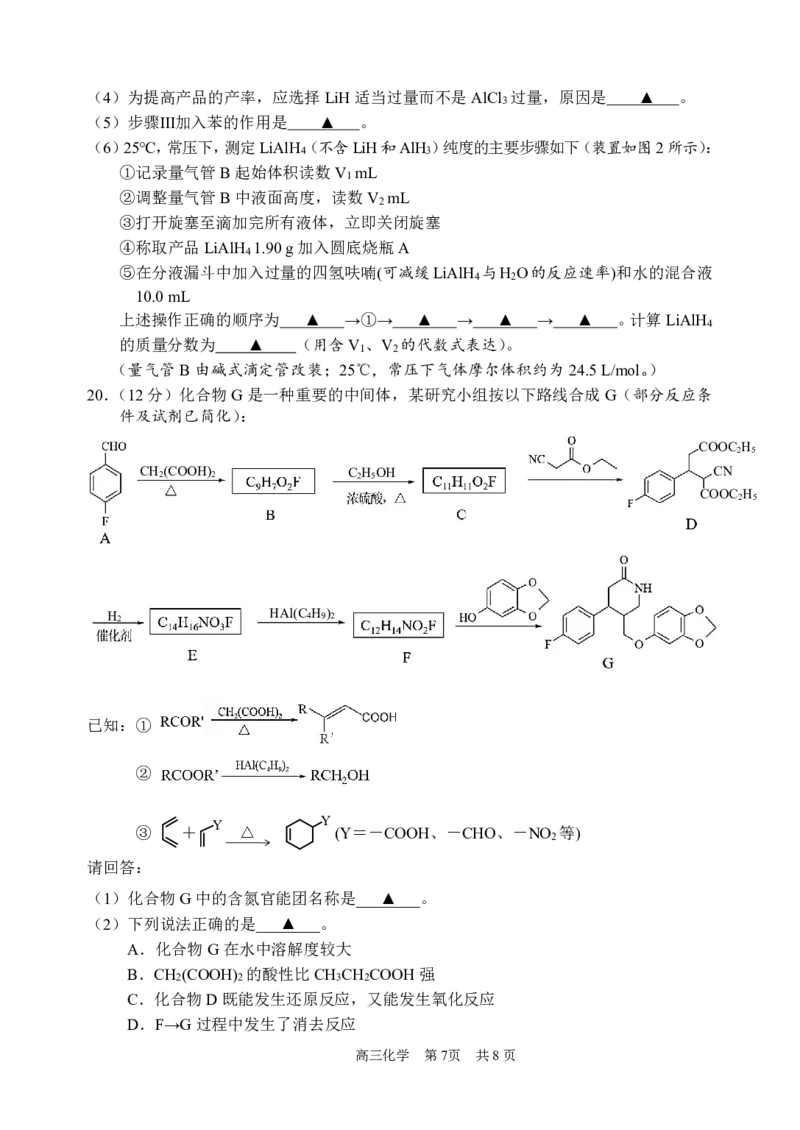
20.(12分)化合物G是一种重要的中间体,某研究小组按以下路线合成G(部分反应条
件及试剂已简化):
COOC2H5
CH2(COOH)2 C2H5OH CN
COOC2H5
H2 HAl(C4H9)2
已知:①
②
Y Y
③ + (Y=-COOH、-CHO、-NO 等)
2
请回答:
(1)化合物G中的含氮官能团名称是____▲____。
(2)下列说法正确的是___▲_____。
A.化合物G在水中溶解度较大
B.CH (COOH) 的酸性比CH CH COOH强
2 2 3 2
C.化合物D既能发生还原反应,又能发生氧化反应
D.F→G过程中发生了消去反应
高三化学 第7页 共8页
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}(3)B的结构简式是___▲_____。
(4)D→E的化学方程式是____▲____。
(5)写出3个同时符合下列条件的化合物C的同分异构体的结构简式___▲_____。
①分子中除苯环外,还有1个六元含氧杂环,且不与苯环共用碳原子;
②氟原子与苯环直接相连;
③核磁共振氢谱表明:分子中有5种不同化学环境的氢原子。
(6)以CH (COOH) 、HAl(C H ) 、1,3−丁二烯、丙酮和乙醇为有机原料,设计化合物
2 2 4 9 2
的合成路线(用流程图表示,无机试剂任选)____▲____。
高三化学 第8页 共8页
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}衢州、丽水、湖州 2025 年 4 月三地市高三教学质量检测
化学参考答案
一、选择题(本大题共16小题,每小题3分,共48分。每个小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
题号 1 2 3 4 5 6 7 8
选项 A D A D C C B C
题号 9 10 11 12 13 14 15 16
选项 C A B B B D C D
二、非选择题(本大题共4小题,52分)
17. (16分)
(1) D (2分)
(2)CuInS (2分)
2
(3)A (2分)
(4)氧和氢的电负性差大于氟与氧的电负性差;OF 中氧原子有两个孤电子对,抵消了F−O中共用
2
电子对偏向F而产生的极性 (2分)
(5) ①过滤 (2分)
②NHCl (2分)
4
高温
③4CuFeS
2
+13O 2=====4CuO+2Fe
2
O
3
+8SO
2
(2分)
④将气体通入品红溶液,溶液褪色,加热煮沸溶液,恢复红色 (2分)
18.(12分)
(1)CO +6H++6e-=CH OH+H O (2分)
2 3 2
(2)① −49.30 (2分)
② B (2分)
③ 温度升高,反应Ⅰ正向移动的程度大于反应Ⅱ逆向移动的程度 (2分)
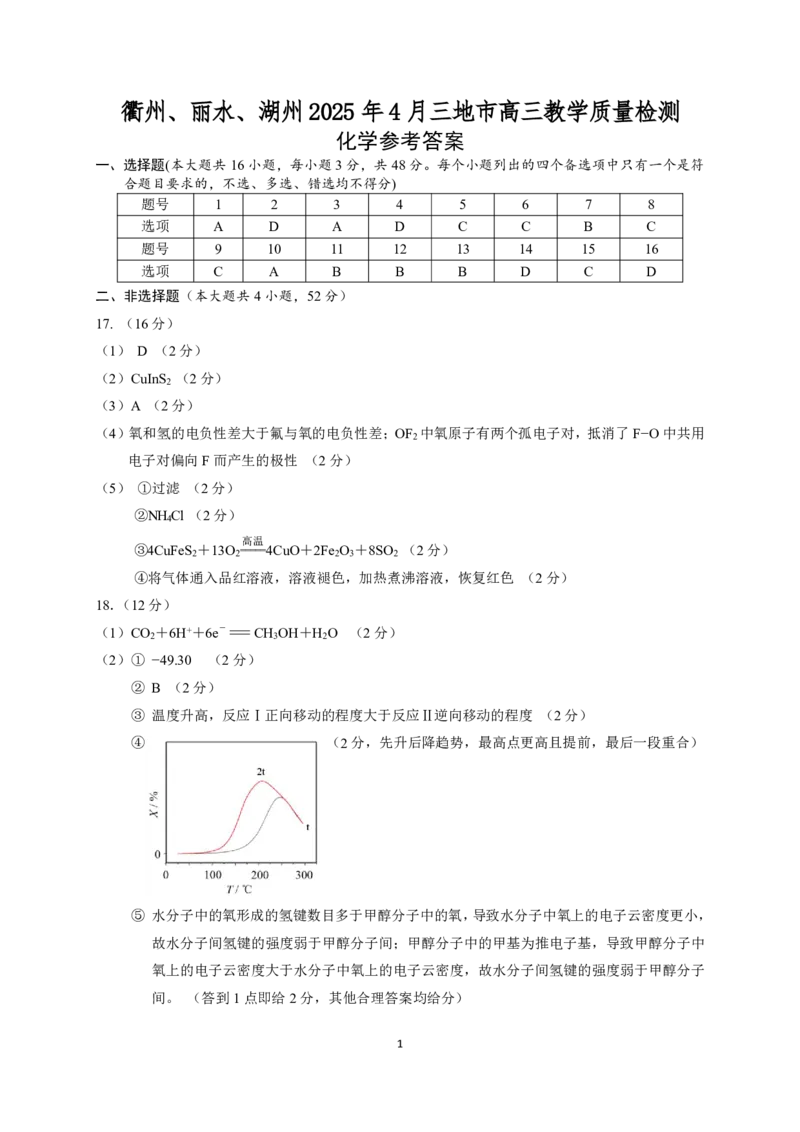
④ (2分,先升后降趋势,最高点更高且提前,最后一段重合)
⑤ 水分子中的氧形成的氢键数目多于甲醇分子中的氧,导致水分子中氧上的电子云密度更小,
故水分子间氢键的强度弱于甲醇分子间;甲醇分子中的甲基为推电子基,导致甲醇分子中
氧上的电子云密度大于水分子中氧上的电子云密度,故水分子间氢键的强度弱于甲醇分子
间。 (答到1点即给2分,其他合理答案均给分)
1
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}19.(12分)
(1)恒压滴液漏斗 (1分)
(2)4LiH+AlCl =LiAlH +3LiCl (1分)
3 4
(3)ACD (2分)
(4)生成的LiCl难溶于乙醚,会附着在LiH表面 (2分)
(5)除去LiAlH 中的AlCl ,有利于LiAlH 析出 (2分)
4 3 4
(6) ④ →①→ ⑤ → ③ → ② (2分) (2分)
20.(12分)
(1)酰胺基(1分)
(2)BC(2分)
(3) (1分)
(4) (2分)
(5) (3分,每个1分,多写看前3个)
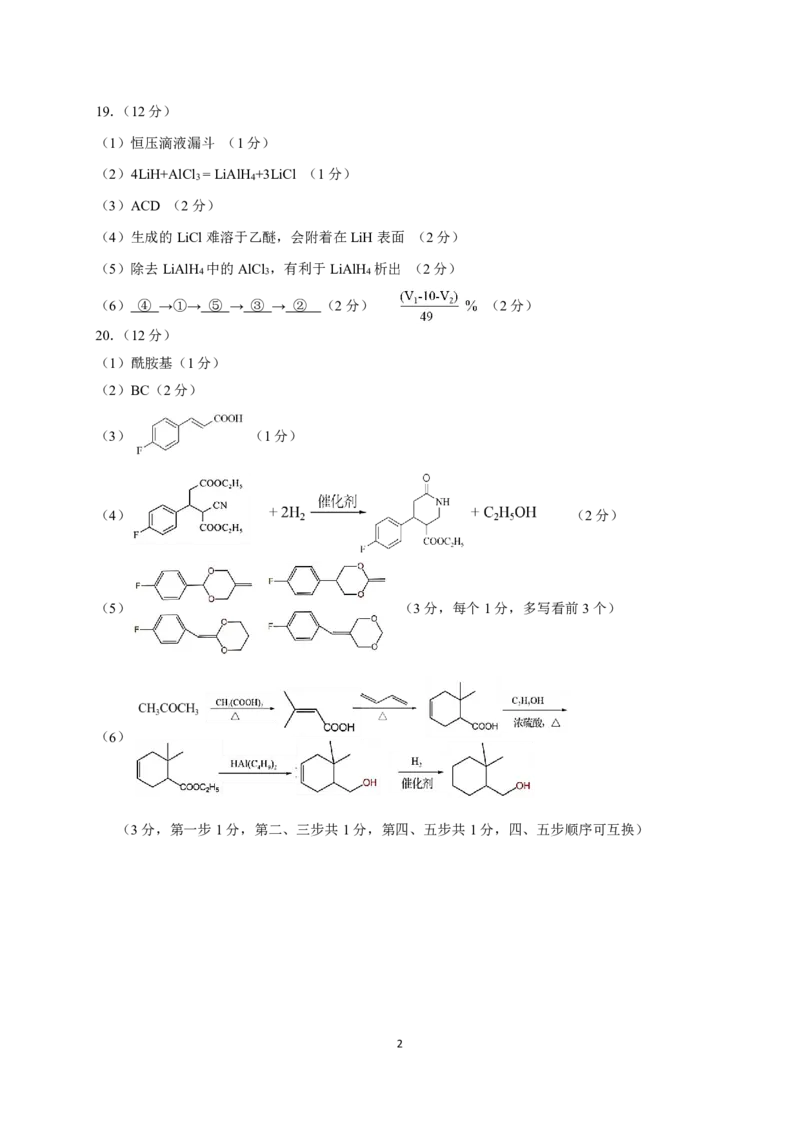
(6)
(3分,第一步1分,第二、三步共1分,第四、五步共1分,四、五步顺序可互换)
2
{#{QQABRYSEggigABIAAQgCQw1iCAGQkAGCCSoOxFAYsAABwRNABAA=}#}