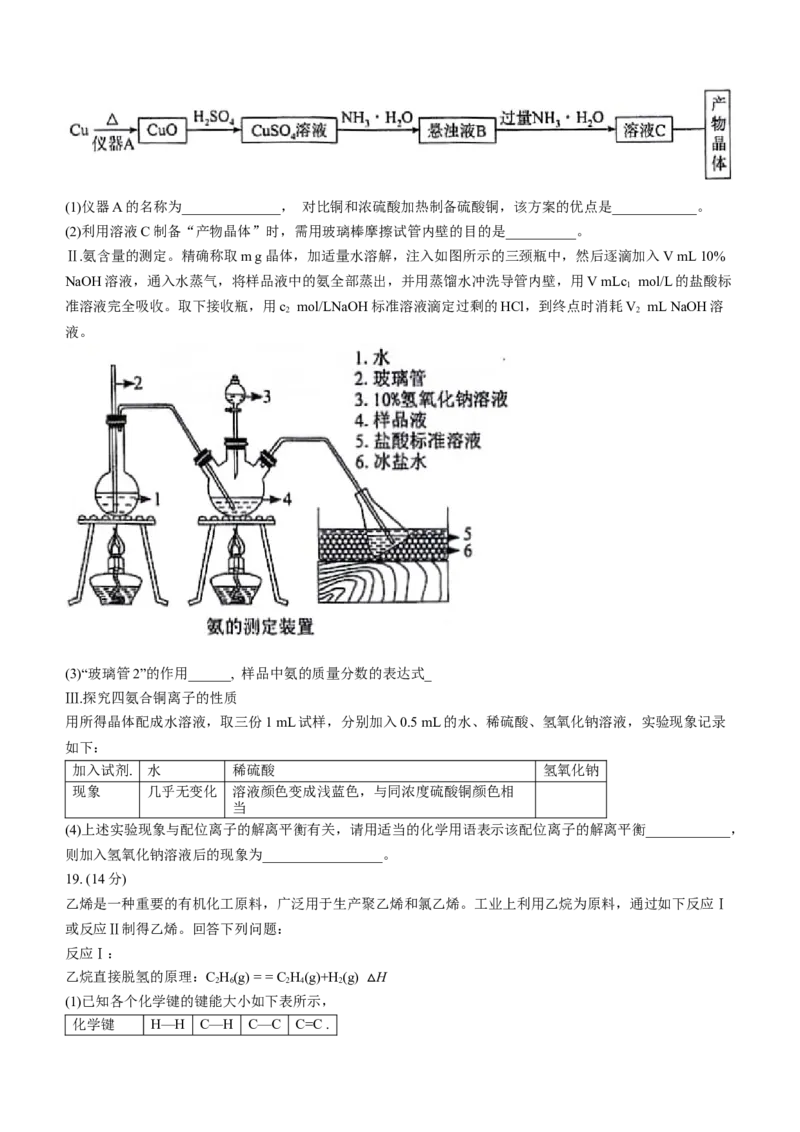
文档内容
腾·云联盟 2023——2024 学年度上学期高三年级八月联考
化学试卷
命题学校:汉阳一中 命题教师:邬帆 审题教师:何风
考试时间:2023 年8月15日 试卷满分:100分
★祝考试顺利★
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码粘贴在答
题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在试
卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡.上对应的答题区域内。写在试卷、草稿纸和
答题卡上的非答题区域均无效。
4.考试结束后,请将本试卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cu 64
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.我国为人类科技发展作出巨大贡献。下列成果研究的物质属于蛋白质的是
A.合成结晶牛胰岛素 B.黑火药 C.造纸术 D.陶瓷烧制
2.化学与生产生活密切相关。下列说法错误的是
A.长时间高温蒸煮可杀死“甲流”病毒
B.生吃新鲜蔬菜比熟吃蔬菜更有利于获取维生素C
C.碳酸钠是一种精细化学品,可用作食用碱或工业用碱
D.新能源汽车的推广与使用,有助于减少光化学烟雾的产生
3.下列化学用语表示,正确的是
A. H S分子的球棍模型: B.NH 的VSEPR模型为
2 3
C. KI的电子式: D. CH CH(CH CH) 的名称:2-甲基戊烷
3 2 3 2
4.实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A.浓盐酸:配制FeCl 溶液
3
B.稀硝酸:清洗附有银镜的试管
C.浓硫酸:蔗糖的水解
D浓硫酸和浓硝酸的混合溶液:苯的硝化
5.下列有关电极方程式或离子方程式错误的是A向AgCl 悬浊液中滴加NaS溶液,白色沉淀变成黑色2AgC1+S2- =Ag S+2Cl-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e-= PbO +4H+
2 2
C. K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D. TiCl 加入水中:TiCl +(x+2)H O =TiO·xH O↓+4H++4Cl-
4 4 2 2 2
6. 一种聚合物PHA的结构简式如下,下列说法错误的是
A. PHA的重复单元中只有一种官能团
B. PHA 可通过单体 缩聚合成
C. PHA在碱性条件下不能发生降解
D. PHA中存在手性碳原子
7.下列有关物质结构与性质的比较正确的是
A分子的极性:O>O
2 3
B.酸性:CHCOOH>CHFCOOH
3 2
C.键角:SeO<
3
D.基态原子未成对电子数:Cr>Mn
8.N 为阿伏加德罗常数的值。下列叙述中正确的是
A
A.1mol Fe(CO) 中含有的σ键的数目为5N
5 A
B.标准状况下,22.4LCH 和22.4LCl 在光照下充分反应后的分子数为2N
4 2 A
C.1 mol CaH 固体含有的离子数目为2N
2 A
D.一定条件下,5.6 g Fe 与0.1 mol Cl 充分反应,转移的电子数为0.3N
2 A
9.离子液体是室温或稍高于室温时呈液态的离子化合物,常见的阴离子如 、 等。一种离子液体的
结构如下图所示,下列与离子液体有关说法正确的是
A.第一电离能:I(C)>I(B)>I(Al)
1 1 l
B.稳定性:PH >NH
3 3
C.简单离子的半径:r(Al3+)>r(Cl- )>r(F-)
D.离子液体有体积很大的阴、阳离子,故熔点较高
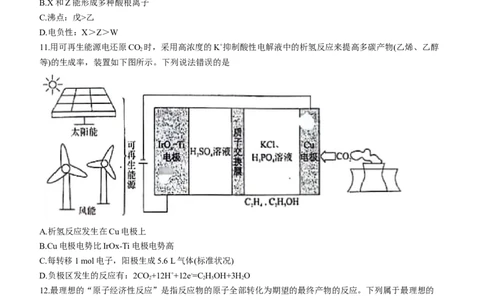
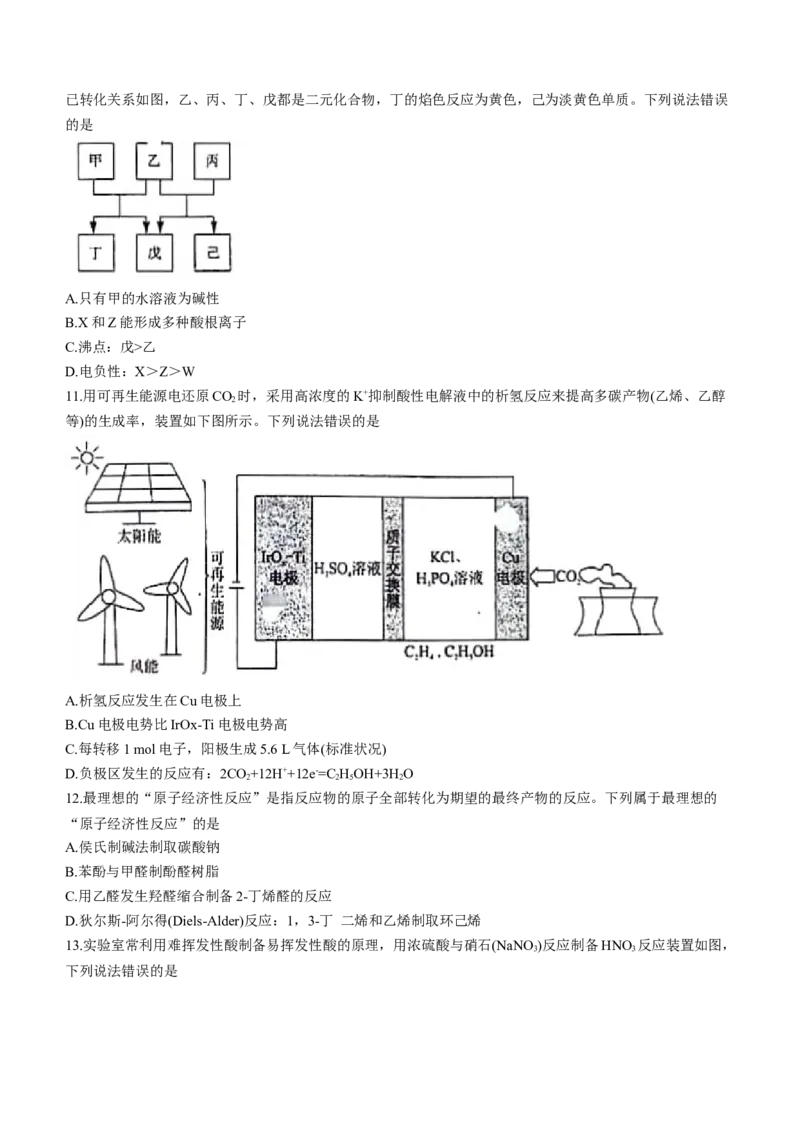
10.短周期元素W、X、Y、Z原子序数依次递增,X、Z同主族,W、Y同主族。由上述元素组成的物质甲~已转化关系如图,乙、丙、丁、戊都是二元化合物,丁的焰色反应为黄色,己为淡黄色单质。下列说法错误
的是
A.只有甲的水溶液为碱性
B.X和Z能形成多种酸根离子
C.沸点:戊>乙
D.电负性:X>Z>W
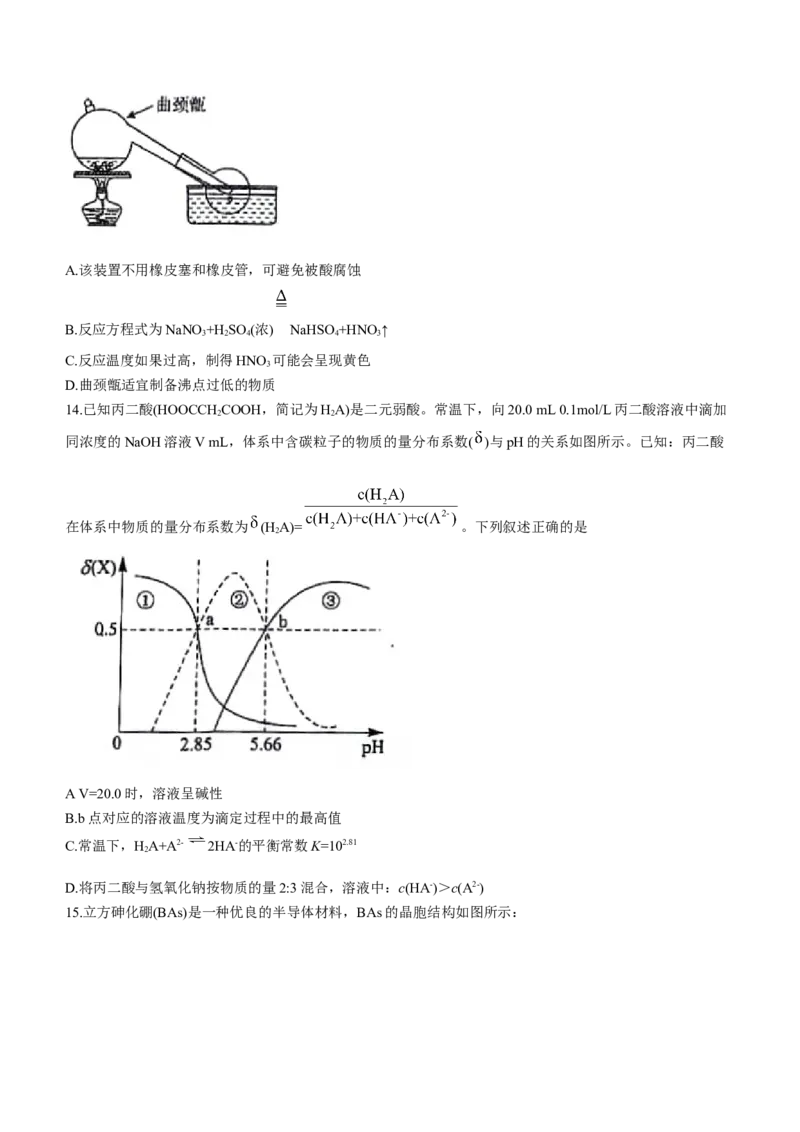
11.用可再生能源电还原CO 时,采用高浓度的K+抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇
2
等)的生成率,装置如下图所示。下列说法错误的是
A.析氢反应发生在Cu电极上
B.Cu电极电势比IrOx-Ti电极电势高
C.每转移1 mol电子,阳极生成5.6 L气体(标准状况)
D.负极区发生的反应有:2CO+12H++12e-=C HOH+3H O
2 2 5 2
12.最理想的“原子经济性反应”是指反应物的原子全部转化为期望的最终产物的反应。下列属于最理想的
“原子经济性反应”的是
A.侯氏制碱法制取碳酸钠
B.苯酚与甲醛制酚醛树脂
C.用乙醛发生羟醛缩合制备2-丁烯醛的反应
D.狄尔斯-阿尔得(Diels-Alder)反应:1,3-丁 二烯和乙烯制取环己烯
13.实验室常利用难挥发性酸制备易挥发性酸的原理,用浓硫酸与硝石(NaNO )反应制备HNO 反应装置如图,
3 3
下列说法错误的是A.该装置不用橡皮塞和橡皮管,可避免被酸腐蚀
B.反应方程式为NaNO +H SO (浓) NaHSO+HNO ↑
3 2 4 4 3
C.反应温度如果过高,制得HNO 可能会呈现黄色
3
D.曲颈甑适宜制备沸点过低的物质
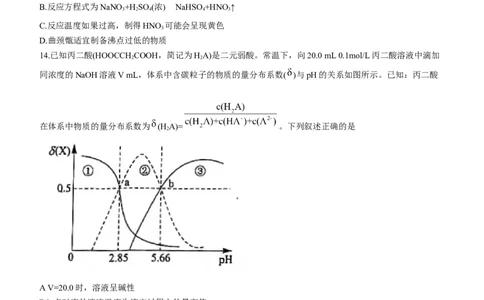
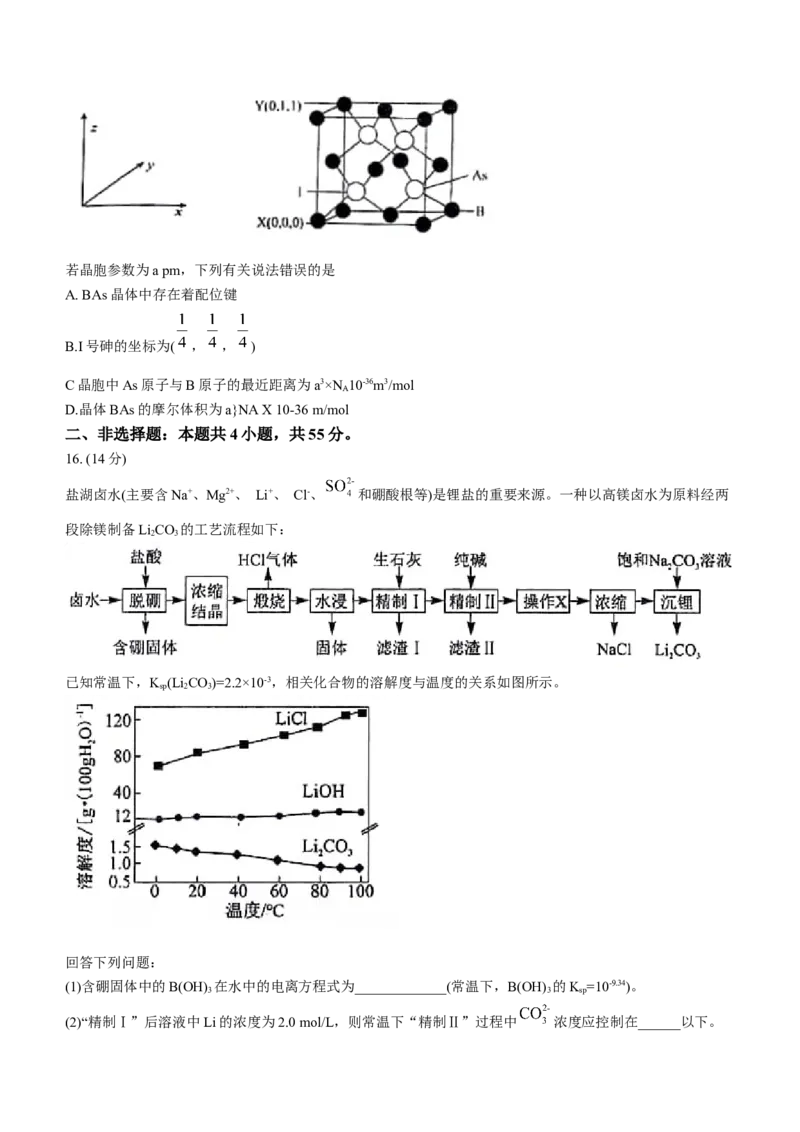
14.已知丙二酸(HOOCCH COOH,简记为HA)是二元弱酸。常温下,向20.0 mL 0.1mol/L丙二酸溶液中滴加
2 2
同浓度的NaOH溶液V mL,体系中含碳粒子的物质的量分布系数( )与pH的关系如图所示。已知:丙二酸
在体系中物质的量分布系数为 (H A)= 。下列叙述正确的是
2
A V=20.0时,溶液呈碱性
B.b点对应的溶液温度为滴定过程中的最高值
C.常温下,HA+A2- 2HA-的平衡常数K=102.81
2
D.将丙二酸与氢氧化钠按物质的量2:3混合,溶液中:c(HA-)>c(A2-)
15.立方砷化硼(BAs)是一种优良的半导体材料,BAs的晶胞结构如图所示:若晶胞参数为a pm,下列有关说法错误的是
A. BAs晶体中存在着配位键
B.I号砷的坐标为( , , )
C晶胞中As原子与B原子的最近距离为a3×N 10-36m3/mol
A
D.晶体BAs的摩尔体积为a}NA X 10-36 m/mol
二、非选择题:本题共4小题,共55分。
16. (14分)
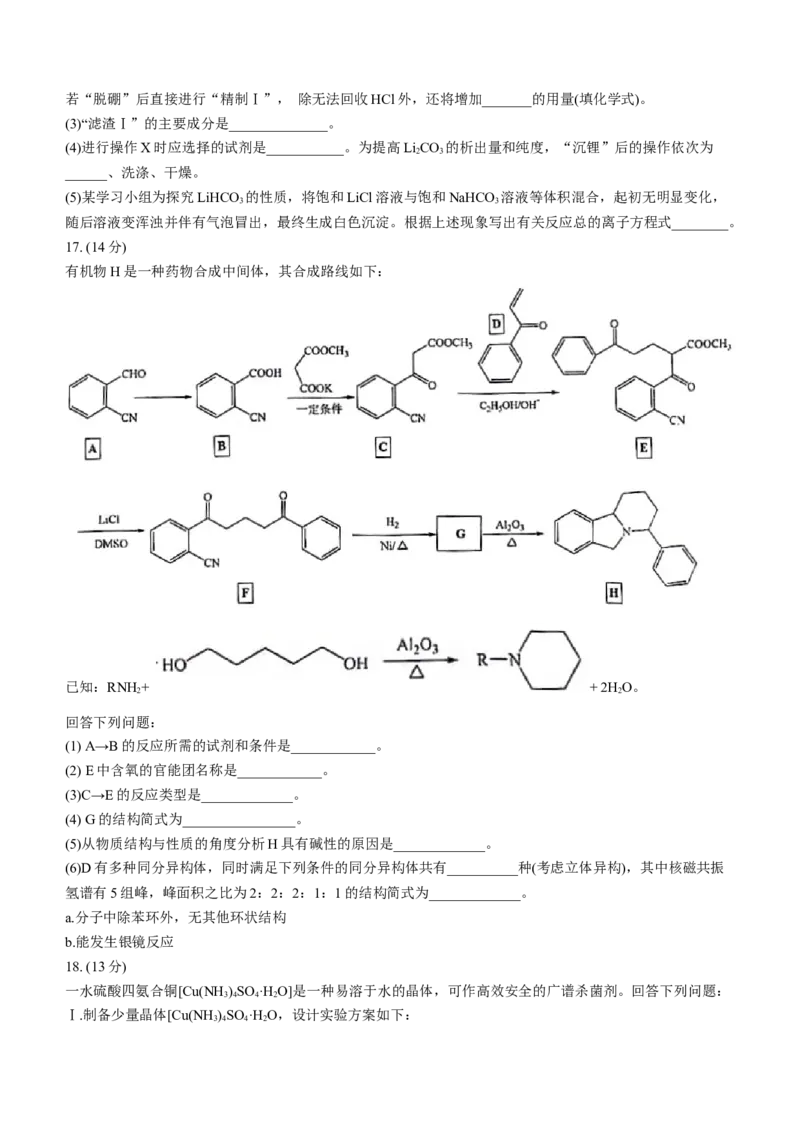
盐湖卤水(主要含Na+、Mg2+、 Li+、 Cl-、 和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两
段除镁制备LiCO 的工艺流程如下:
2 3
已知常温下,K (Li CO)=2.2×10-3,相关化合物的溶解度与温度的关系如图所示。
sp 2 3
回答下列问题:
(1)含硼固体中的B(OH) 在水中的电离方程式为_____________(常温下,B(OH) 的K =10-9.34)。
3 3 sp
(2)“精制Ⅰ”后溶液中Li的浓度为2.0 mol/L,则常温下“精制Ⅱ”过程中 浓度应控制在______以下。若“脱硼”后直接进行“精制Ⅰ”, 除无法回收HCl外,还将增加_______的用量(填化学式)。
(3)“滤渣Ⅰ”的主要成分是______________。
(4)进行操作X时应选择的试剂是___________。为提高LiCO 的析出量和纯度,“沉锂”后的操作依次为
2 3
______、洗涤、干燥。
(5)某学习小组为探究LiHCO 的性质,将饱和LiCl溶液与饱和NaHCO 溶液等体积混合,起初无明显变化,
3 3
随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。根据上述现象写出有关反应总的离子方程式________。
17. (14分)
有机物H是一种药物合成中间体,其合成路线如下:
已知:RNH + + 2H O。
2 2
回答下列问题:
(1) A→B的反应所需的试剂和条件是____________。
(2) E中含氧的官能团名称是____________。
(3)C→E的反应类型是_____________。
(4) G的结构简式为________________。
(5)从物质结构与性质的角度分析H具有碱性的原因是_____________。
(6)D有多种同分异构体,同时满足下列条件的同分异构体共有__________种(考虑立体异构),其中核磁共振
氢谱有5组峰,峰面积之比为2:2:2:1:1的结构简式为_____________。
a.分子中除苯环外,无其他环状结构
b.能发生银镜反应
18. (13分)
一水硫酸四氨合铜[Cu(NH )SO ·H O]是一种易溶于水的晶体,可作高效安全的广谱杀菌剂。回答下列问题:
3 4 4 2
Ⅰ.制备少量晶体[Cu(NH )SO ·H O,设计实验方案如下:
3 4 4 2(1)仪器A的名称为______________, 对比铜和浓硫酸加热制备硫酸铜,该方案的优点是____________。
(2)利用溶液C制备“产物晶体”时,需用玻璃棒摩擦试管内壁的目的是__________。
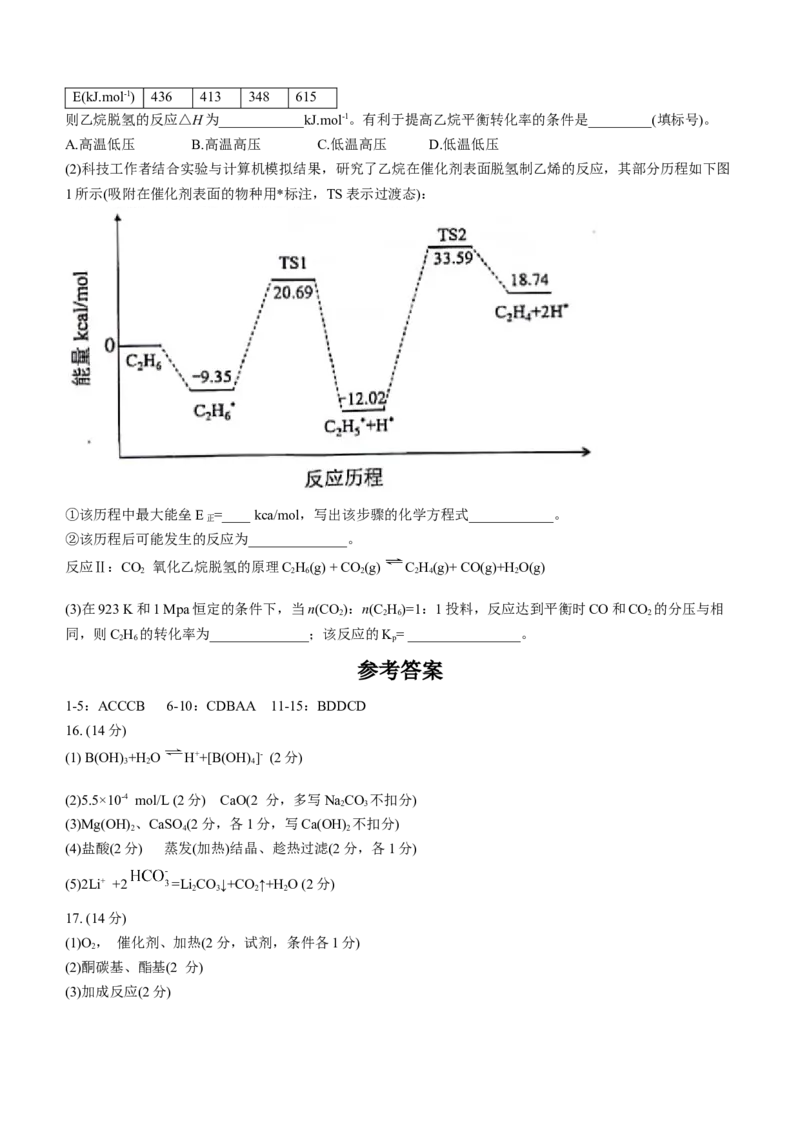
Ⅱ.氨含量的测定。精确称取m g晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入V mL 10%
NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用V mLc mol/L的盐酸标
1
准溶液完全吸收。取下接收瓶,用c mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V mL NaOH溶
2 2
液。
(3)“玻璃管2”的作用______, 样品中氨的质量分数的表达式_
Ⅲ.探究四氨合铜离子的性质
用所得晶体配成水溶液,取三份1 mL试样,分别加入0.5 mL的水、稀硫酸、氢氧化钠溶液,实验现象记录
如下:
加入试剂. 水 稀硫酸 氢氧化钠
现象 几乎无变化 溶液颜色变成浅蓝色,与同浓度硫酸铜颜色相
当
(4)上述实验现象与配位离子的解离平衡有关,请用适当的化学用语表示该配位离子的解离平衡____________,
则加入氢氧化钠溶液后的现象为_________________。
19. (14分)
乙烯是一种重要的有机化工原料,广泛用于生产聚乙烯和氯乙烯。工业上利用乙烷为原料,通过如下反应Ⅰ
或反应Ⅱ制得乙烯。回答下列问题:
反应Ⅰ:
乙烷直接脱氢的原理:C H(g) = = C H(g)+H(g) H
2 6 2 4 2
(1)已知各个化学键的键能大小如下表所示,
△
化学键 H—H C—H C—C C=C .E(kJ.mol-1) 436 413 348 615
则乙烷脱氢的反应△H为____________kJ.mol-1。有利于提高乙烷平衡转化率的条件是_________(填标号)。
A.高温低压 B.高温高压 C.低温高压 D.低温低压
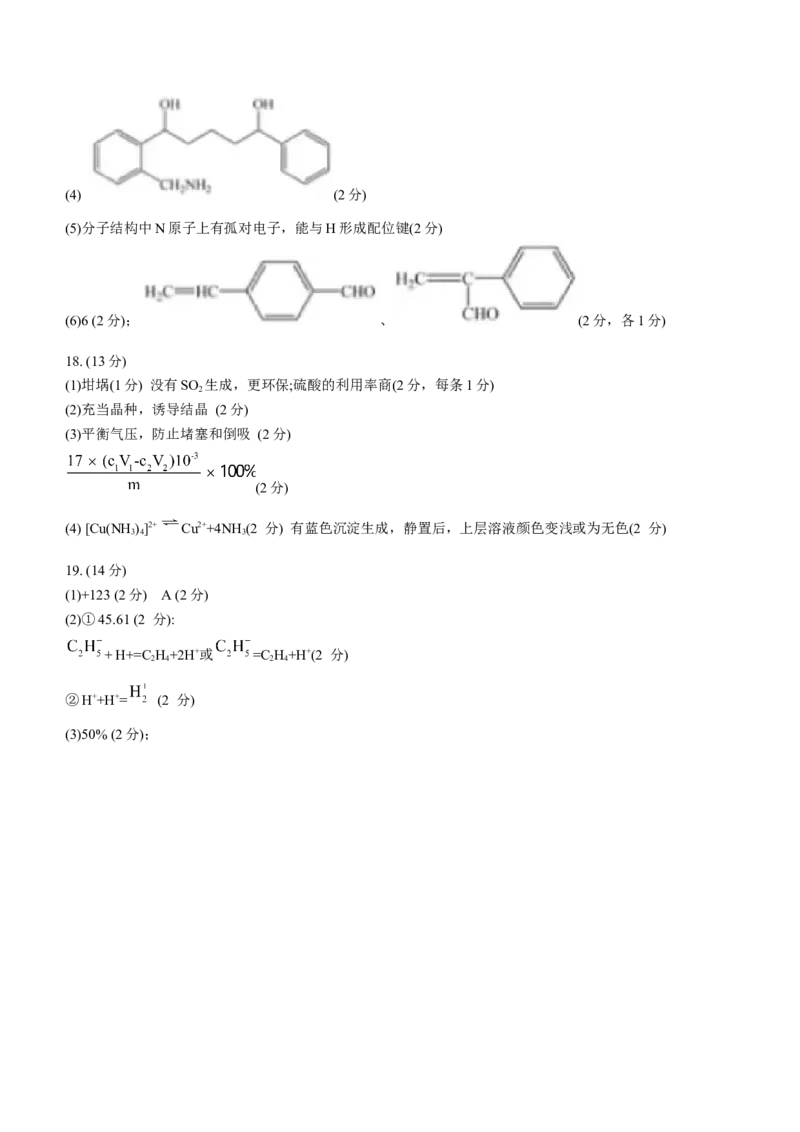
(2)科技工作者结合实验与计算机模拟结果,研究了乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如下图
1所示(吸附在催化剂表面的物种用*标注,TS表示过渡态):
①该历程中最大能垒E =____ kca/mol,写出该步骤的化学方程式____________。
正
②该历程后可能发生的反应为______________。
反应Ⅱ:CO 氧化乙烷脱氢的原理C H(g) + CO (g) C H(g)+ CO(g)+H O(g)
2 2 6 2 2 4 2
(3)在923 K和1 Mpa恒定的条件下,当n(CO):n(C H)=1:1投料,反应达到平衡时CO和CO 的分压与相
2 2 6 2
同,则C H 的转化率为______________;该反应的K= ________________。
2 6 p
参考答案
1-5:ACCCB 6-10:CDBAA 11-15:BDDCD
16. (14分)
(1) B(OH) +H O H++[B(OH) ]- (2分)
3 2 4
(2)5.5×10-4 mol/L (2分) CaO(2 分,多写NaCO 不扣分)
2 3
(3)Mg(OH) 、CaSO(2分,各1分,写Ca(OH) 不扣分)
2 4 2
(4)盐酸(2分) 蒸发(加热)结晶、趁热过滤(2分,各1分)
(5)2Li+ +2 =Li CO↓+CO ↑+H O (2分)
2 3 2 2
17. (14分)
(1)O , 催化剂、加热(2分,试剂,条件各1分)
2
(2)酮碳基、酯基(2 分)
(3)加成反应(2分)(4) (2分)
(5)分子结构中N原子上有孤对电子,能与H形成配位键(2分)
(6)6 (2分); 、 (2分,各1分)
18. (13分)
(1)坩埚(1分) 没有SO 生成,更环保;硫酸的利用率商(2分,每条1分)
2
(2)充当晶种,诱导结晶 (2分)
(3)平衡气压,防止堵塞和倒吸 (2分)
(2分)
(4) [Cu(NH )]2+ Cu2++4NH(2 分) 有蓝色沉淀生成,静置后,上层溶液颜色变浅或为无色(2 分)
3 4 3
19. (14分)
(1)+123 (2分) A (2分)
(2)①45.61 (2 分):
+ H+=C H+2H+或 =C H+H+(2 分)
2 4 2 4
②H++H+= (2 分)
(3)50% (2分);