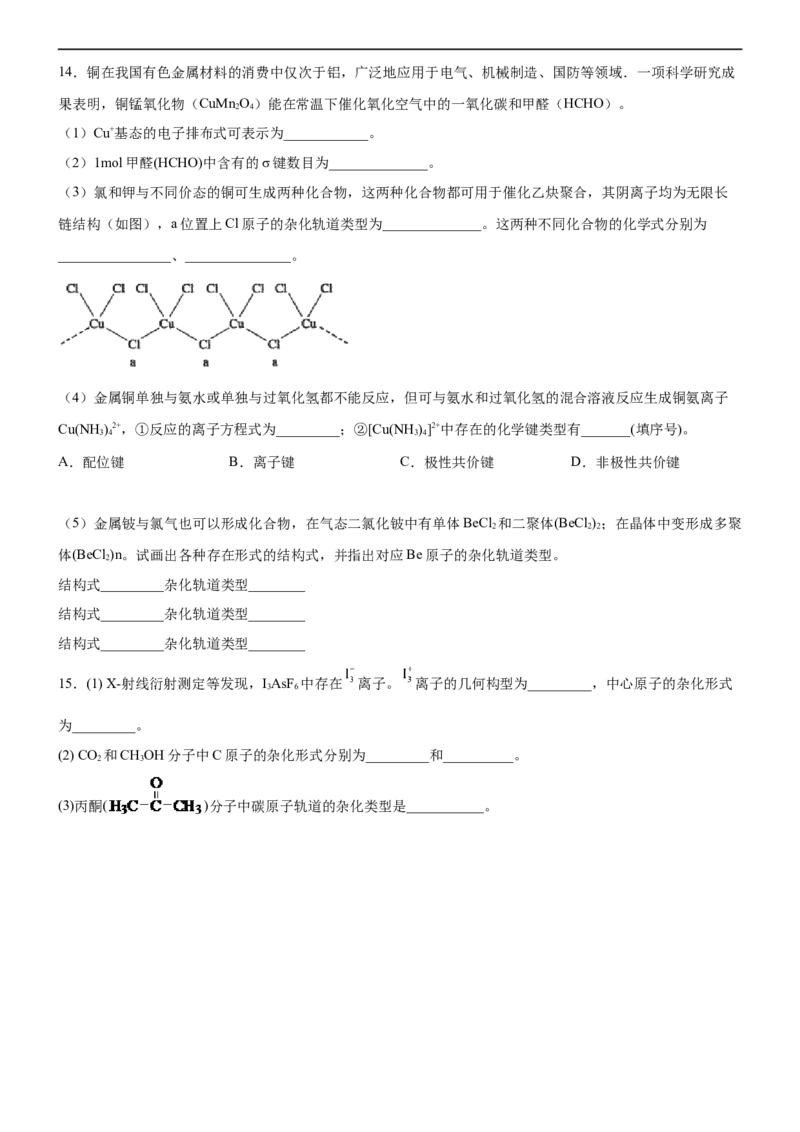文档内容
第2章 分子结构与性质
2.2.2 杂化轨道理论
一.选择题(共10小题)
1.如图所示,在乙烯分子中有5个 键、1个 键,下列表述正确的是( )
A.C、H之间是 杂化轨道形成的键,C、C之间是未参加杂化的 轨道形成的 键
B.C、C之间是 杂化轨道形成的键,C、H之间是未参加杂化的 轨道形成的 键
C. 杂化轨道形成 键,未杂化的 轨道形成 键
D. 杂化轨道形成 键,未杂化的 轨道形成 键
2.以下有关杂化轨道的说法中正确的是( )
A.sp3 杂化轨道中轨道数为 4,且 4 个杂化轨道能量相同
B.杂化轨道既可能形成σ键,也可能形成π键
C.杂化轨道不能容纳孤电子对
D.sp2杂化轨道最多可形成 2 个σ键
3.下列有关杂化轨道的说法不正确的是( )
A.原子中能量相近的某些轨道,在成键时能重新组合成能量相等的新轨道
B.轨道数目杂化前后可以相等,也可以不等
C.杂化轨道成键时,要满足原子轨道最大重叠原理、最小排斥原理
D.杂化轨道可分为等性杂化轨道和不等性杂化轨道
4.下列有关乙烯和苯分子中的化学键描述正确的是( )
A.苯分子中每个碳原子的 杂化轨道中的其中一个形成大 键
B.乙烯分子中 键是 杂化轨道形成的 键 键是未参加杂化的 轨道形成的 键
C.苯分子中碳碳键是 杂化轨道形成的 键, 键是未参加杂化的 轨道形成的 键D.乙烯和苯分子中每个碳原子都以 杂化轨道形成 键,未杂化的 轨道形成 键
5.下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是
A.sp杂化轨道的夹角最大 B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大 D.sp3、sp2、sp杂化轨道的夹角相等
6.乙烯分子中含有4个C—H键和1个C=C键,6个原子在同一平面上。下列关于乙烯分子的成键情况分析正
确的是 ( )
①每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道 ②每个C原子的2s轨道与2个2p轨道杂化,
形成3个sp2杂化轨道 ③每个C原子的2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道 ④每个C原子的3
个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
A.①③ B.②④ C.①④ D.②③
7.用Pauling的杂化轨道理论解释甲烷分子的四面体结构,下列说法不正确的是( )
A.C原子的四个杂化轨道的能量一样
B.C原子的sp3杂化轨道之间夹角一样
C.C原子的4个价电子分别占据4个sp3杂化轨道
D.C原子有1个sp3杂化轨道由孤对电子占据
8.在 分子中,羰基与甲基碳原子成键时所采取的杂化方式分别为( )
A.sp2杂化;sp2杂化 B.sp3杂化;sp3杂化
C.sp2杂化;sp3杂化 D.sp杂化;sp3杂化
9.根据价层电子对互斥理论及原子轨道的杂化理论判断 分子的 模型名称和中心原子的杂化方式
为( )
A.直线形 杂化 B.四面体形 杂化
C.三角锥形 杂化 D.三角形 杂化
10.下列分子中,各分子的立体构型和中心原子的杂化方式均正确的是( )
A.NH 平面三角形 sp3杂化 B.CCl 正四面体 sp3杂化
3 4
C.HO V形 sp2杂化 D.CO2﹣ 三角锥形 sp3杂化
2 3
二、填空题(共5题)
11.(1)BCl 中心原子的杂化方式为____。
3
(2)在S的氢化物(H S)分子中,S原子轨道的杂化类型是___。
2(3)HO的分子构型为__,中心原子的杂化轨道类型为__。COCl 中心原子的杂化轨道类型为__。
2 2
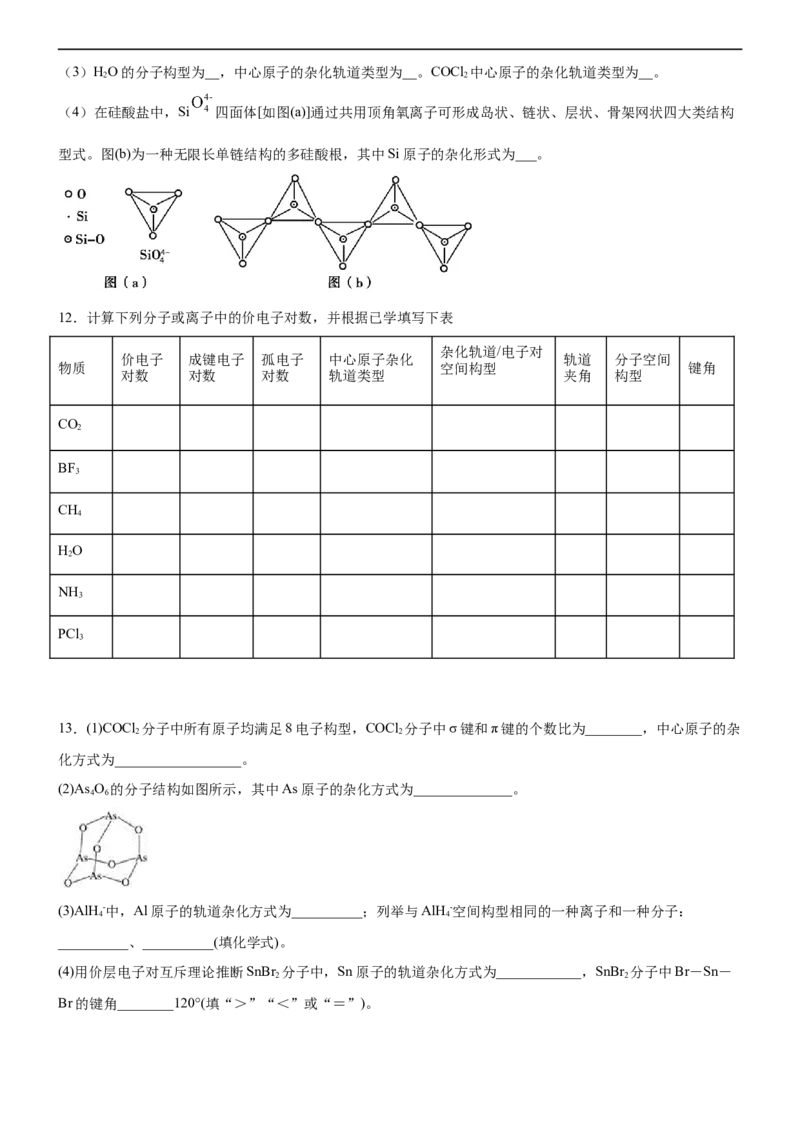
(4)在硅酸盐中,Si 四面体[如图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构
型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___。
12.计算下列分子或离子中的价电子对数,并根据已学填写下表
杂化轨道/电子对
价电子 成键电子 孤电子 中心原子杂化 轨道 分子空间
物质 空间构型 键角
对数 对数 对数 轨道类型 夹角 构型
CO
2
BF
3
CH
4
HO
2
NH
3
PCl
3
13.(1)COCl 分子中所有原子均满足8电子构型,COCl 分子中σ键和π键的个数比为________,中心原子的杂
2 2
化方式为__________________。
(2)As O 的分子结构如图所示,其中As原子的杂化方式为______________。
4 6
(3)AlH-中,Al原子的轨道杂化方式为__________;列举与AlH-空间构型相同的一种离子和一种分子:
4 4
__________、__________(填化学式)。
(4)用价层电子对互斥理论推断SnBr 分子中,Sn原子的轨道杂化方式为____________,SnBr 分子中Br-Sn-
2 2
Br的键角________120°(填“>”“<”或“=”)。14.铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成
果表明,铜锰氧化物(CuMn O)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
2 4
(1)Cu+基态的电子排布式可表示为____________。
(2)1mol甲醛(HCHO)中含有的σ键数目为______________。
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长
链结构(如图),a位置上Cl原子的杂化轨道类型为______________。这两种不同化合物的化学式分别为
________________、_______________。
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应生成铜氨离子
Cu(NH )2+,①反应的离子方程式为_________;②[Cu(NH )]2+中存在的化学键类型有_______(填序号)。
3 4 3 4
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
(5)金属铍与氯气也可以形成化合物,在气态二氯化铍中有单体BeCl 和二聚体(BeCl );在晶体中变形成多聚
2 2 2
体(BeCl )n。试画出各种存在形式的结构式,并指出对应Be原子的杂化轨道类型。
2
结构式_________杂化轨道类型________
结构式_________杂化轨道类型________
结构式_________杂化轨道类型________
15.(1) X-射线衍射测定等发现,IAsF 中存在 离子。 离子的几何构型为_________,中心原子的杂化形式
3 6
为_________。
(2) CO 和CHOH分子中C原子的杂化形式分别为_________和__________。
2 3
(3)丙酮( )分子中碳原子轨道的杂化类型是___________。