文档内容
化学反应的调控基础练习题
1.对于合成氨反应,达到平衡后,以下分析正确的是( )
A.升高温度,对正反应的反应速率影响更大 B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大 D.加入催化剂,对逆反应的反应速率影响更大
2.在合成氨反应中使用催化剂和施加高压,下列叙述中正确的是( )
A.都能提高反应速率,都对化学平衡无影响
B.都对化学平衡有影响,但都不影响达到平衡状态所用的时间
C.都能缩短达到平衡状态所用的时间,只有施加高压对化学平衡有影响
D.使用催化剂能缩短反应达到平衡状态所用的时间,而施加高压无此效果
3.下列有关合成氨工业的说法正确的是( )
A.N 的量越多,H 的转化率越大,因此,充入的N 越多越有利于NH 的合成
2 2 2 3
B.恒容条件下充入稀有气体有利于NH 的合成
3
C.工业合成氨的反应是熵增加的放热反应,在任何温度下都可自发进行
D.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行
4.可逆反应N(g)+3H(g) 2NH (g) △H<0,达到平衡后,为了使H 的转化率增大,下列选项中采用的三种方法都
2 2 3 2
正确的是( )
A.升高温度,减小压强,增加氮气 B.降低温度,增大压强,加入催化剂
C.升高温度,增大压强,增加氮气 D.降低温度,增大压强,分离出部分氨
5.在合成氨工业中,要使氨的产率增大,同时又能提高化学反应速率,可采取的措施有( )
①增大容器体积使压强减小②减小容器体积使压强增大③升高温度④降低温度⑤恒温恒容,再充入等量的 N 和H ⑥
2 2
恒温恒压,再充入等量的N 和H ⑦及时分离产生的NH ⑧使用催化剂
2 2 3
A.②④⑤⑥⑦ B.②③④⑤⑦⑧ C.只有②⑤ D.①②③⑤⑧
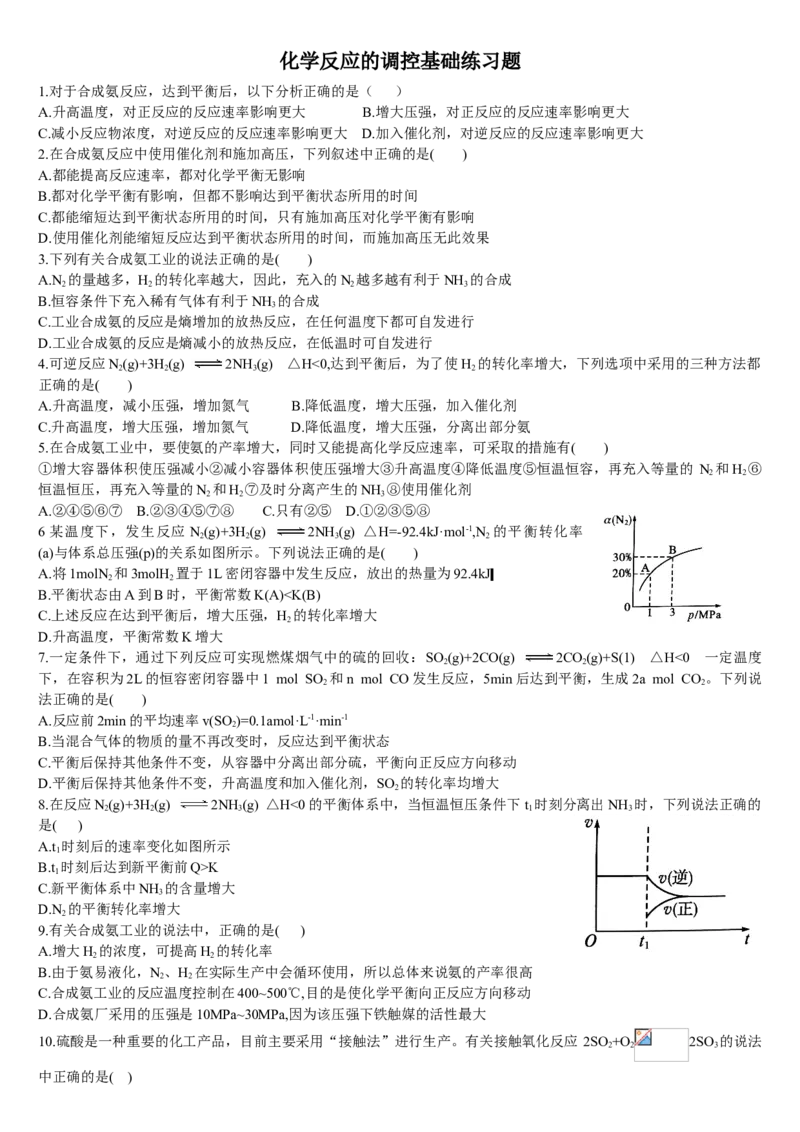
6某温度下,发生反应 N(g)+3H(g) 2NH (g) △H=-92.4kJ·mol-1,N 的平衡转化率
2 2 3 2
(a)与体系总压强(p)的关系如图所示。下列说法正确的是( )
A.将1molN
2
和3molH
2
置于1L密闭容器中发生反应,放出的热量为92.4kJ
B.平衡状态由A到B时,平衡常数K(A)K
1
C.新平衡体系中NH 的含量增大
3
D.N 的平衡转化率增大
2
9.有关合成氨工业的说法中,正确的是( )
A.增大H 的浓度,可提高H 的转化率
2 2
B.由于氨易液化,N、H 在实际生产中会循环使用,所以总体来说氨的产率很高
2 2
C.合成氨工业的反应温度控制在400~500℃,目的是使化学平衡向正反应方向移动
D.合成氨厂采用的压强是10MPa~30MPa,因为该压强下铁触媒的活性最大
10.硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关接触氧化反应 2SO +O 2SO 的说法
2 2 3
中正确的是( )A.只要选择适宜的条件,SO 和O 就能全部转化为SO
2 2 3
B.该反应达到平衡后,反应就完全停止了,即正、逆反应速率均为零
C.在达到平衡的体系中,充入由18O原子组成的O 后,SO 中18O含量减少,SO 中18O含量增多
2 2 3
D.在工业合成SO 时,要同时考虑反应速率和反应能达到的限度两方面的问题
3
11.有平衡体系:CO(g)+2H(g) CHOH(g)△H<0。为了增加甲醇(CHOH)的产量,应采取的正确措施是( )
2 3 3
A.高温,高压 B.适宜温度,高压,催化剂 C.低温,低压 D.高温,高压,催化剂
12.利用原料气在合成塔中合成NH ,为提高N 的转化率,所采取的措施是( )
3 2
A.高温 B.高压 C.使用催化剂 D.增大N 的浓度
2
13.NH 是一种重要的工业原料。下列关于合成氨的说法中,不正确的是( )
3
A.工艺涉及催化技术 B.工艺涉及高温高压技术
C.原料之一的氮气来自空气 D.从合成塔出来的气体中,氨的体积分数为100%
14.在一定条件下,可逆反应N(g)+3H(g) 2NH (g) (正反应是放热反应)达到平衡,当单独改变下列条件后,有关
2 2 3
叙述错误的是( )
A.加催化剂,v(正)、v(逆)都发生变化且变化的倍数相等
B.加压,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.降温,v(正)、v(逆)都减小,且v(正)减小的倍数小于v(逆)减小的倍数
D.等容条件下加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
15.某工业生产中发生反应:2A(g)+B(g) 2M(g)△H<0。下列有关该工业生产的说法正确的是( )
A.工业上合成M时,一定采用高压条件,因为高压有利于M的生成
B.若物质B价廉易得,工业上一般采用加入过量的B以提高A和B的转化率
C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高
D.工业生产中常采用催化剂,因为生产中使用催化剂可提高M的日产量
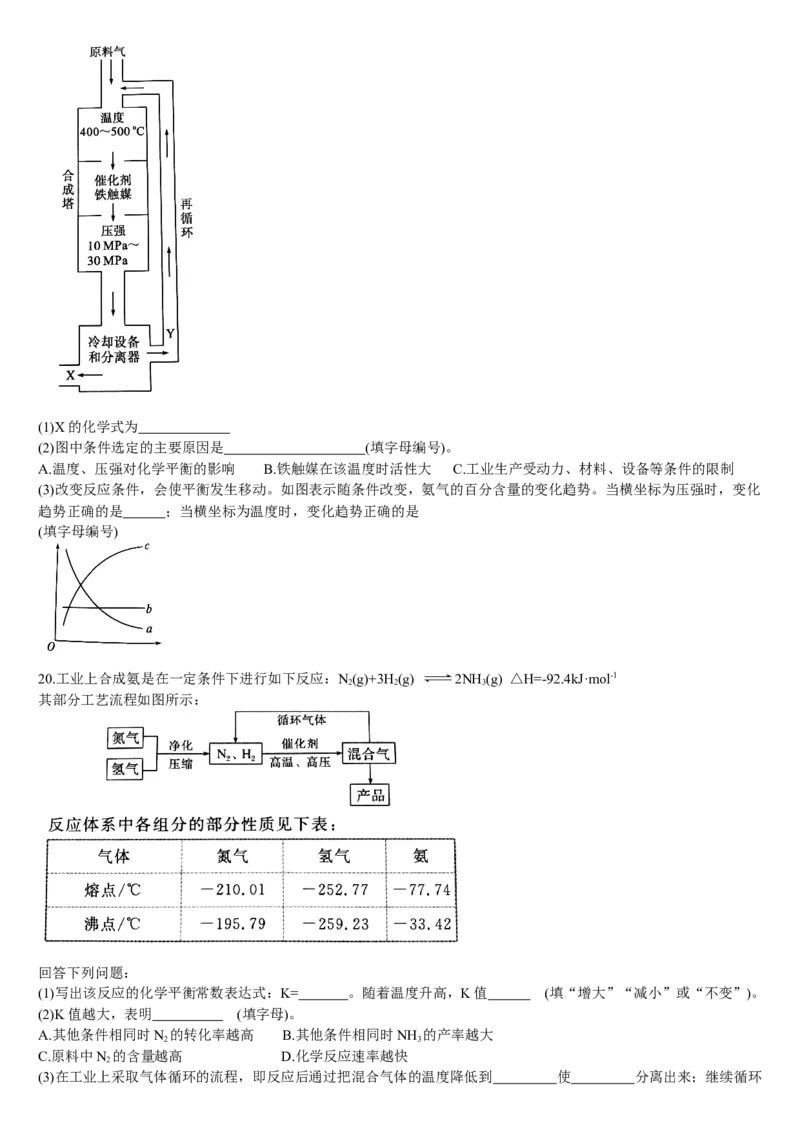
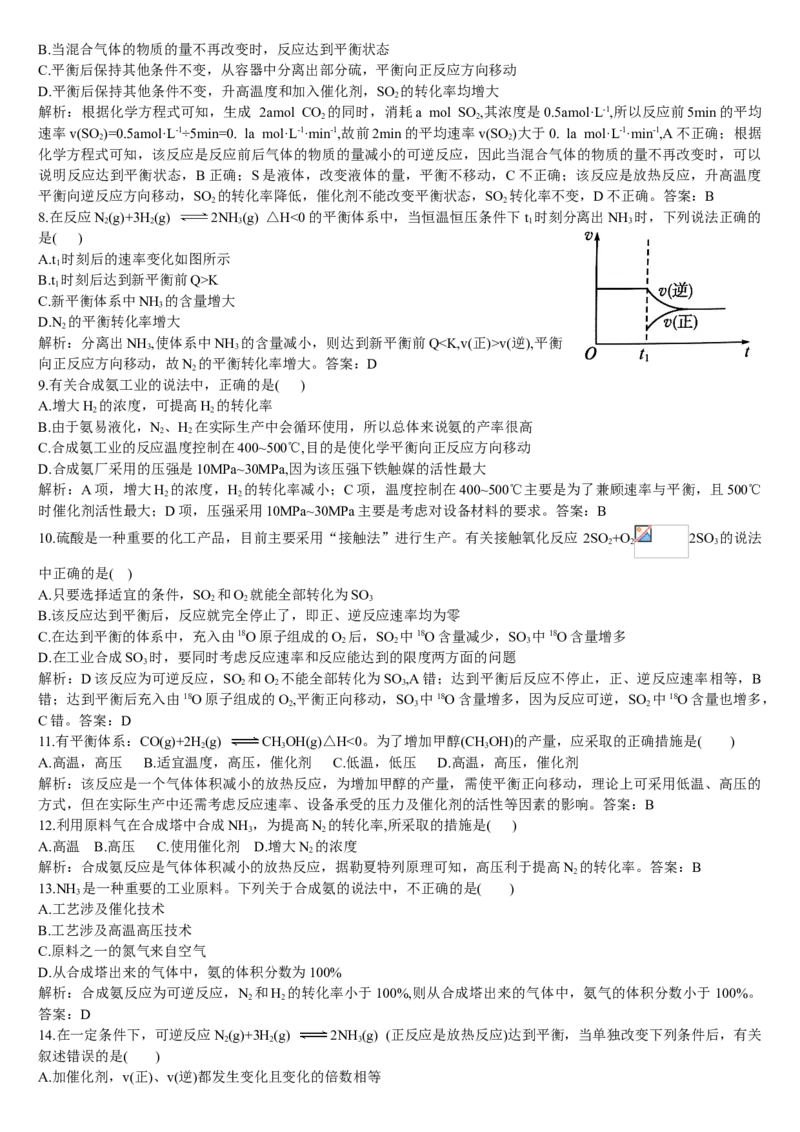
16.下面是合成氨的简易流程示意图:
沿x路线回去的物质是 ( )
A.N 和H B.催化剂 C. N D. H
2 2 2 2
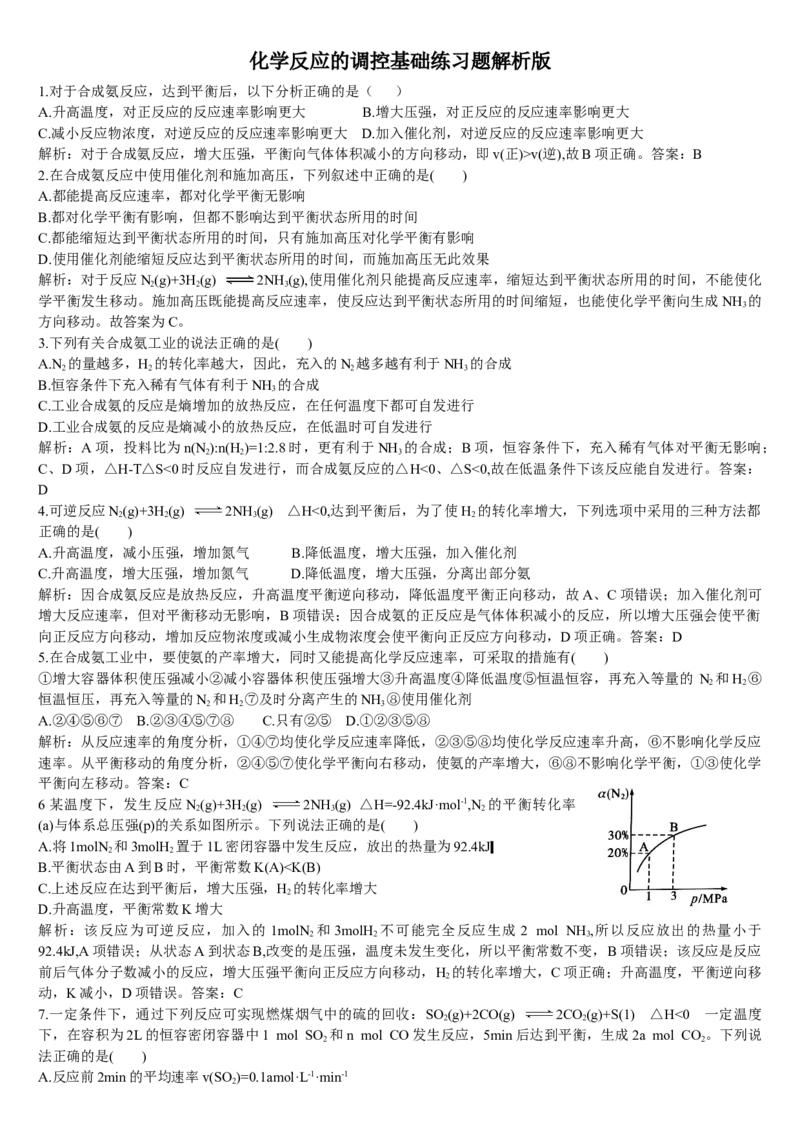
17.1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。
下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )
A.①②③ B.②④⑤ C.①③⑤ D.②③④
18.合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气
2 2 3
中的CO,其反应是[Cu(NH )]Ac+CO+NH [Cu(NH )]Ac·CO △H<0
3 2 3 3 3
(1)必须除去原料气中CO的原因是
(2)醋酸二氨合铜(I)吸收CO的适宜条件应是
(3)吸收CO后的醋酸铜氨溶液经过适当处理又可再生,恢复其吸收CO的能力以供循环使用。醋酸铜氨溶液再生的适
宜条件应是
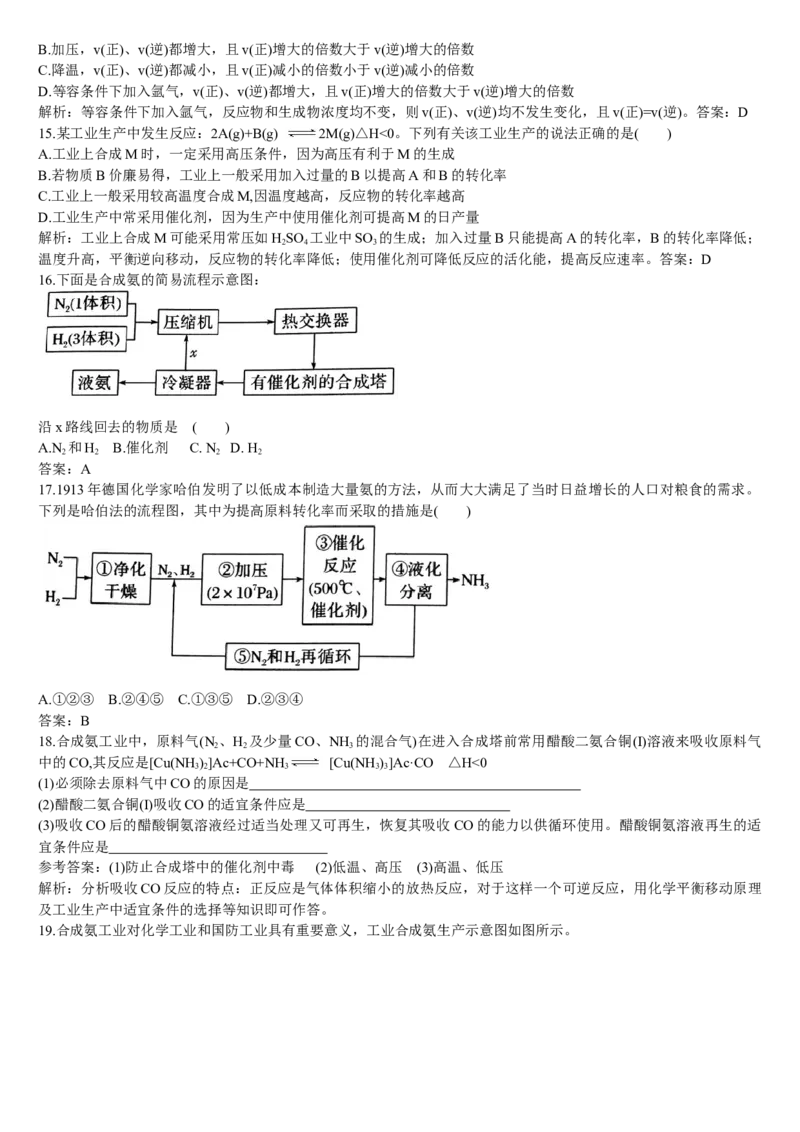
19.合成氨工业对化学工业和国防工业具有重要意义,工业合成氨生产示意图如图所示。(1)X的化学式为
(2)图中条件选定的主要原因是 (填字母编号)。
A.温度、压强对化学平衡的影响 B.铁触媒在该温度时活性大 C.工业生产受动力、材料、设备等条件的限制
(3)改变反应条件,会使平衡发生移动。如图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化
趋势正确的是 ;当横坐标为温度时,变化趋势正确的是
(填字母编号)
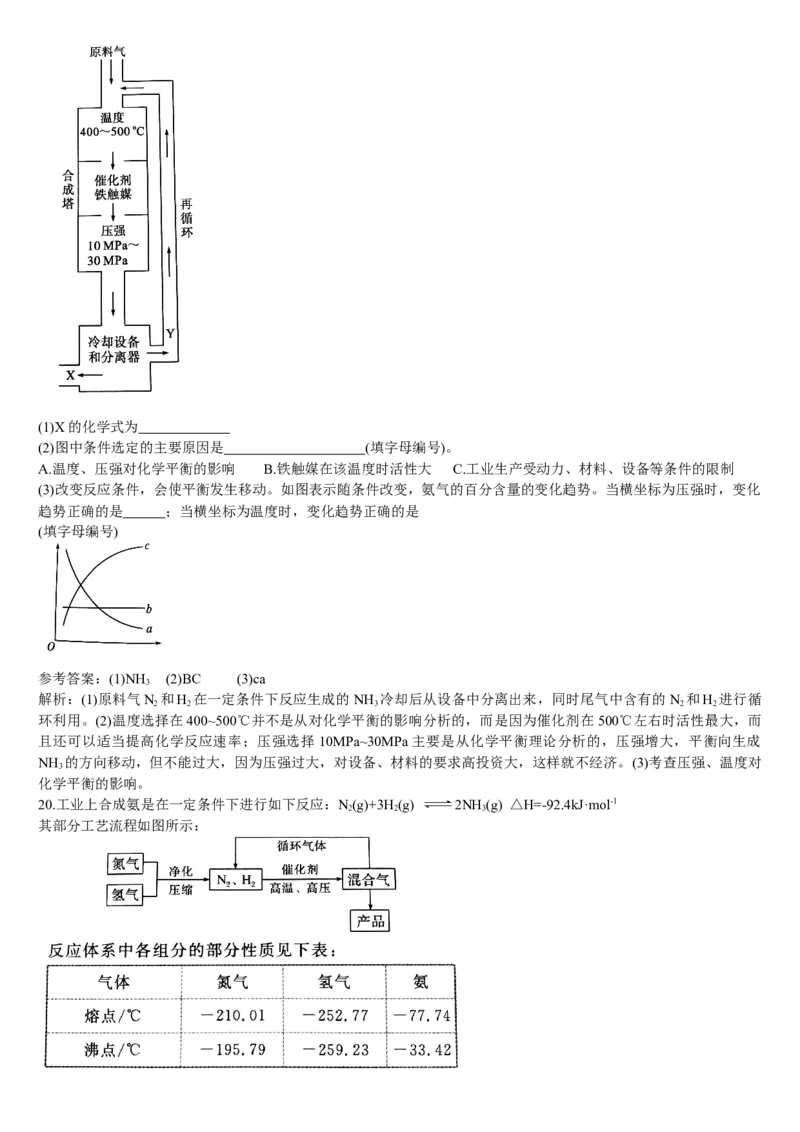
20.工业上合成氨是在一定条件下进行如下反应:N(g)+3H(g) 2NH (g) △H=-92.4kJ·mol-1
2 2 3
其部分工艺流程如图所示:
回答下列问题:
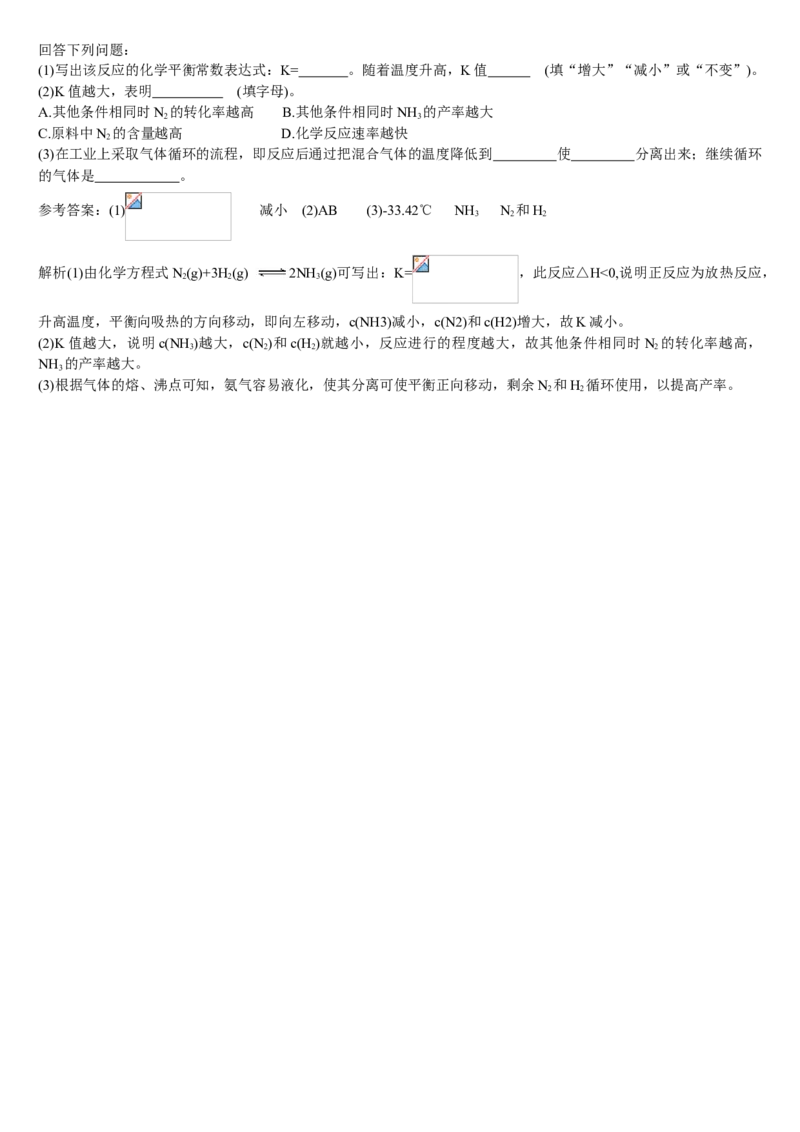
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,K值 (填“增大”“减小”或“不变”)。
(2)K值越大,表明 (填字母)。
A.其他条件相同时N 的转化率越高 B.其他条件相同时NH 的产率越大
2 3
C.原料中N 的含量越高 D.化学反应速率越快
2
(3)在工业上采取气体循环的流程,即反应后通过把混合气体的温度降低到 使 分离出来;继续循环的气体是 。化学反应的调控基础练习题解析版
1.对于合成氨反应,达到平衡后,以下分析正确的是( )
A.升高温度,对正反应的反应速率影响更大 B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大 D.加入催化剂,对逆反应的反应速率影响更大
解析:对于合成氨反应,增大压强,平衡向气体体积减小的方向移动,即v(正)>v(逆),故B项正确。答案:B
2.在合成氨反应中使用催化剂和施加高压,下列叙述中正确的是( )
A.都能提高反应速率,都对化学平衡无影响
B.都对化学平衡有影响,但都不影响达到平衡状态所用的时间
C.都能缩短达到平衡状态所用的时间,只有施加高压对化学平衡有影响
D.使用催化剂能缩短反应达到平衡状态所用的时间,而施加高压无此效果
解析:对于反应N(g)+3H(g) 2NH (g),使用催化剂只能提高反应速率,缩短达到平衡状态所用的时间,不能使化
2 2 3
学平衡发生移动。施加高压既能提高反应速率,使反应达到平衡状态所用的时间缩短,也能使化学平衡向生成NH 的
3
方向移动。故答案为C。
3.下列有关合成氨工业的说法正确的是( )
A.N 的量越多,H 的转化率越大,因此,充入的N 越多越有利于NH 的合成
2 2 2 3
B.恒容条件下充入稀有气体有利于NH 的合成
3
C.工业合成氨的反应是熵增加的放热反应,在任何温度下都可自发进行
D.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行
解析:A项,投料比为n(N ):n(H)=1:2.8时,更有利于NH 的合成;B项,恒容条件下,充入稀有气体对平衡无影响;
2 2 3
C、D项,△H-T△S<0时反应自发进行,而合成氨反应的△H<0、△S<0,故在低温条件下该反应能自发进行。答案:
D
4.可逆反应N(g)+3H(g) 2NH (g) △H<0,达到平衡后,为了使H 的转化率增大,下列选项中采用的三种方法都
2 2 3 2
正确的是( )
A.升高温度,减小压强,增加氮气 B.降低温度,增大压强,加入催化剂
C.升高温度,增大压强,增加氮气 D.降低温度,增大压强,分离出部分氨
解析:因合成氨反应是放热反应,升高温度平衡逆向移动,降低温度平衡正向移动,故A、C项错误;加入催化剂可
增大反应速率,但对平衡移动无影响,B项错误;因合成氨的正反应是气体体积减小的反应,所以增大压强会使平衡
向正反应方向移动,增加反应物浓度或减小生成物浓度会使平衡向正反应方向移动,D项正确。答案:D
5.在合成氨工业中,要使氨的产率增大,同时又能提高化学反应速率,可采取的措施有( )
①增大容器体积使压强减小②减小容器体积使压强增大③升高温度④降低温度⑤恒温恒容,再充入等量的 N 和H ⑥
2 2
恒温恒压,再充入等量的N 和H ⑦及时分离产生的NH ⑧使用催化剂
2 2 3
A.②④⑤⑥⑦ B.②③④⑤⑦⑧ C.只有②⑤ D.①②③⑤⑧
解析:从反应速率的角度分析,①④⑦均使化学反应速率降低,②③⑤⑧均使化学反应速率升高,⑥不影响化学反应
速率。从平衡移动的角度分析,②④⑤⑦使化学平衡向右移动,使氨的产率增大,⑥⑧不影响化学平衡,①③使化学
平衡向左移动。答案:C
6某温度下,发生反应N(g)+3H(g) 2NH (g) △H=-92.4kJ·mol-1,N 的平衡转化率
2 2 3 2
(a)与体系总压强(p)的关系如图所示。下列说法正确的是( )
A.将1molN
2
和3molH
2
置于1L密闭容器中发生反应,放出的热量为92.4kJ
B.平衡状态由A到B时,平衡常数K(A)K
1
C.新平衡体系中NH 的含量增大
3
D.N 的平衡转化率增大
2
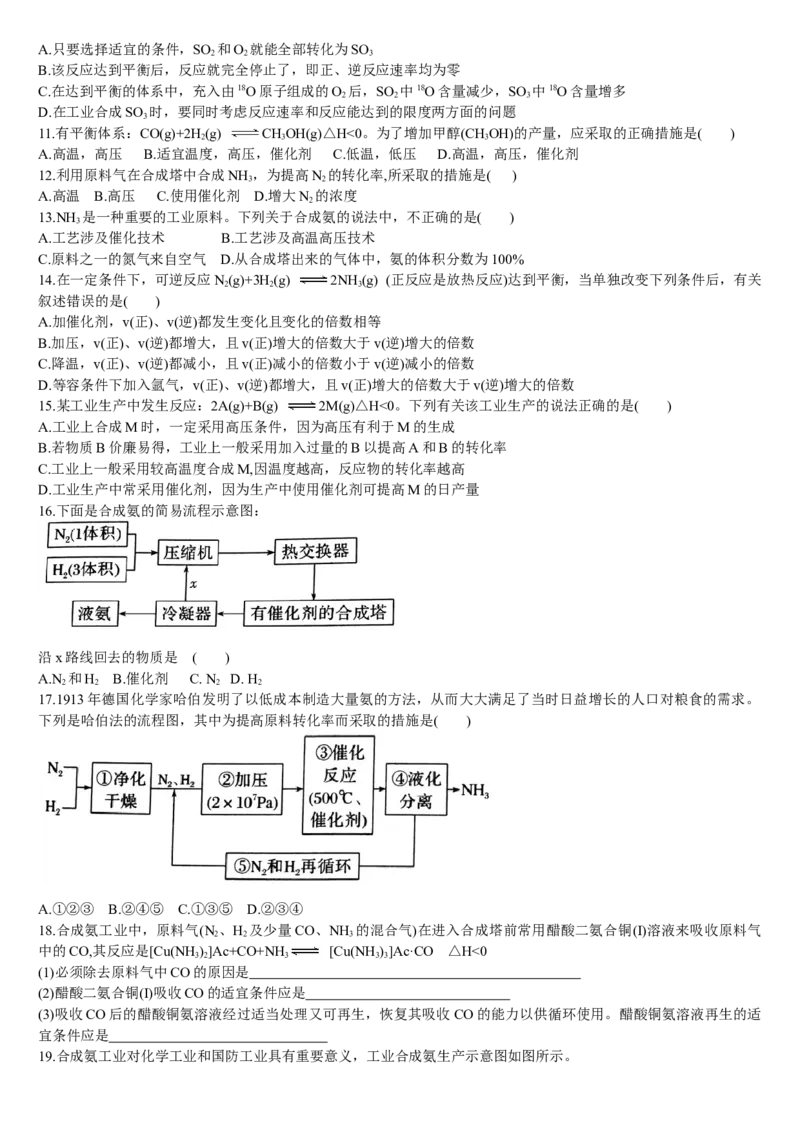
解析:分离出NH ,使体系中NH 的含量减小,则达到新平衡前Qv(逆),平衡
3 3
向正反应方向移动,故N 的平衡转化率增大。答案:D
2
9.有关合成氨工业的说法中,正确的是( )
A.增大H 的浓度,可提高H 的转化率
2 2
B.由于氨易液化,N、H 在实际生产中会循环使用,所以总体来说氨的产率很高
2 2
C.合成氨工业的反应温度控制在400~500℃,目的是使化学平衡向正反应方向移动
D.合成氨厂采用的压强是10MPa~30MPa,因为该压强下铁触媒的活性最大
解析:A项,增大H 的浓度,H 的转化率减小;C项,温度控制在400~500℃主要是为了兼顾速率与平衡,且500℃
2 2
时催化剂活性最大;D项,压强采用10MPa~30MPa主要是考虑对设备材料的要求。答案:B
10.硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。有关接触氧化反应 2SO +O 2SO 的说法
2 2 3
中正确的是( )
A.只要选择适宜的条件,SO 和O 就能全部转化为SO
2 2 3
B.该反应达到平衡后,反应就完全停止了,即正、逆反应速率均为零
C.在达到平衡的体系中,充入由18O原子组成的O 后,SO 中18O含量减少,SO 中18O含量增多
2 2 3
D.在工业合成SO 时,要同时考虑反应速率和反应能达到的限度两方面的问题
3
解析:D该反应为可逆反应,SO 和O 不能全部转化为SO ,A错;达到平衡后反应不停止,正、逆反应速率相等,B
2 2 3
错;达到平衡后充入由18O原子组成的O,平衡正向移动,SO 中18O含量增多,因为反应可逆,SO 中18O含量也增多,
2 3 2
C错。答案:D
11.有平衡体系:CO(g)+2H(g) CHOH(g)△H<0。为了增加甲醇(CHOH)的产量,应采取的正确措施是( )
2 3 3
A.高温,高压 B.适宜温度,高压,催化剂 C.低温,低压 D.高温,高压,催化剂
解析:该反应是一个气体体积减小的放热反应,为增加甲醇的产量,需使平衡正向移动,理论上可采用低温、高压的
方式,但在实际生产中还需考虑反应速率、设备承受的压力及催化剂的活性等因素的影响。答案:B
12.利用原料气在合成塔中合成NH ,为提高N 的转化率,所采取的措施是( )
3 2
A.高温 B.高压 C.使用催化剂 D.增大N 的浓度
2
解析:合成氨反应是气体体积减小的放热反应,据勒夏特列原理可知,高压利于提高N 的转化率。答案:B
2
13.NH 是一种重要的工业原料。下列关于合成氨的说法中,不正确的是( )
3
A.工艺涉及催化技术
B.工艺涉及高温高压技术
C.原料之一的氮气来自空气
D.从合成塔出来的气体中,氨的体积分数为100%
解析:合成氨反应为可逆反应,N 和H 的转化率小于100%,则从合成塔出来的气体中,氨气的体积分数小于100%。
2 2
答案:D
14.在一定条件下,可逆反应N(g)+3H(g) 2NH (g) (正反应是放热反应)达到平衡,当单独改变下列条件后,有关
2 2 3
叙述错误的是( )
A.加催化剂,v(正)、v(逆)都发生变化且变化的倍数相等B.加压,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.降温,v(正)、v(逆)都减小,且v(正)减小的倍数小于v(逆)减小的倍数
D.等容条件下加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
解析:等容条件下加入氩气,反应物和生成物浓度均不变,则v(正)、v(逆)均不发生变化,且v(正)=v(逆)。答案:D
15.某工业生产中发生反应:2A(g)+B(g) 2M(g)△H<0。下列有关该工业生产的说法正确的是( )
A.工业上合成M时,一定采用高压条件,因为高压有利于M的生成
B.若物质B价廉易得,工业上一般采用加入过量的B以提高A和B的转化率
C.工业上一般采用较高温度合成M,因温度越高,反应物的转化率越高
D.工业生产中常采用催化剂,因为生产中使用催化剂可提高M的日产量
解析:工业上合成M可能采用常压如HSO 工业中SO 的生成;加入过量B只能提高A的转化率,B的转化率降低;
2 4 3
温度升高,平衡逆向移动,反应物的转化率降低;使用催化剂可降低反应的活化能,提高反应速率。答案:D
16.下面是合成氨的简易流程示意图:
沿x路线回去的物质是 ( )
A.N 和H B.催化剂 C. N D. H
2 2 2 2
答案:A
17.1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。
下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )
A.①②③ B.②④⑤ C.①③⑤ D.②③④
答案:B
18.合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气
2 2 3
中的CO,其反应是[Cu(NH )]Ac+CO+NH [Cu(NH )]Ac·CO △H<0
3 2 3 3 3
(1)必须除去原料气中CO的原因是
(2)醋酸二氨合铜(I)吸收CO的适宜条件应是
(3)吸收CO后的醋酸铜氨溶液经过适当处理又可再生,恢复其吸收CO的能力以供循环使用。醋酸铜氨溶液再生的适
宜条件应是
参考答案:(1)防止合成塔中的催化剂中毒 (2)低温、高压 (3)高温、低压
解析:分析吸收CO反应的特点:正反应是气体体积缩小的放热反应,对于这样一个可逆反应,用化学平衡移动原理
及工业生产中适宜条件的选择等知识即可作答。
19.合成氨工业对化学工业和国防工业具有重要意义,工业合成氨生产示意图如图所示。(1)X的化学式为
(2)图中条件选定的主要原因是 (填字母编号)。
A.温度、压强对化学平衡的影响 B.铁触媒在该温度时活性大 C.工业生产受动力、材料、设备等条件的限制
(3)改变反应条件,会使平衡发生移动。如图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化
趋势正确的是 ;当横坐标为温度时,变化趋势正确的是
(填字母编号)
参考答案:(1)NH (2)BC (3)ca
3
解析:(1)原料气N 和H 在一定条件下反应生成的NH 冷却后从设备中分离出来,同时尾气中含有的N 和H 进行循
2 2 3 2 2
环利用。(2)温度选择在400~500℃并不是从对化学平衡的影响分析的,而是因为催化剂在500℃左右时活性最大,而
且还可以适当提高化学反应速率;压强选择 10MPa~30MPa主要是从化学平衡理论分析的,压强增大,平衡向生成
NH 的方向移动,但不能过大,因为压强过大,对设备、材料的要求高投资大,这样就不经济。(3)考查压强、温度对
3
化学平衡的影响。
20.工业上合成氨是在一定条件下进行如下反应:N(g)+3H(g) 2NH (g) △H=-92.4kJ·mol-1
2 2 3
其部分工艺流程如图所示:回答下列问题:
(1)写出该反应的化学平衡常数表达式:K= 。随着温度升高,K值 (填“增大”“减小”或“不变”)。
(2)K值越大,表明 (填字母)。
A.其他条件相同时N 的转化率越高 B.其他条件相同时NH 的产率越大
2 3
C.原料中N 的含量越高 D.化学反应速率越快
2
(3)在工业上采取气体循环的流程,即反应后通过把混合气体的温度降低到 使 分离出来;继续循环
的气体是 。
参考答案:(1) 减小 (2)AB (3)-33.42℃ NH N 和H
3 2 2
解析(1)由化学方程式N(g)+3H(g) 2NH (g)可写出:K= ,此反应△H<0,说明正反应为放热反应,
2 2 3
升高温度,平衡向吸热的方向移动,即向左移动,c(NH3)减小,c(N2)和c(H2)增大,故K减小。
(2)K值越大,说明c(NH )越大,c(N)和c(H)就越小,反应进行的程度越大,故其他条件相同时N 的转化率越高,
3 2 2 2
NH 的产率越大。
3
(3)根据气体的熔、沸点可知,氨气容易液化,使其分离可使平衡正向移动,剩余N 和H 循环使用,以提高产率。
2 2