文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(吉林、黑龙江卷)
高三化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 S 32 Al 27 C 59 Zn 65
O
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.中华传统文化富含化学知识,下列分析不正确的是
A.《本草纲目》“烧酒”条目写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,
味极浓烈,盖酒露也。”叙述了“蒸馏”技术在古代酿酒工艺中的应用
B.古诗《杨柳歌》中:“独忆飞絮鹅毛下,非复青丝马尾垂。”中“飞絮”的主要成分是多糖
C.宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料
[主要成分为 ],保存《千里江山图》需控制温度和湿度
D.《馀冬录》中描述的黄丹其主要成分为 ,则黄丹( )与磁性氧化铁类似,其中铅的化合价
有+2价和+3价两种化合价
【答案】D
【解析】A.用浓酒和糟入甑,蒸令气上,得到酒,为蒸馏方法的运用,A正确;
B.“飞絮”为植物纤维,主要成分是多糖,B正确;
C. 不稳定,受热易分解,故需控制温度和湿度,C正确;
D. 中铅的化合价有+2价和+4价两种化合价,D错误;
故选D。
2.“夏禹铸九鼎,天下分九州”,青铜器在古时被称为“吉金”,是红铜与锡、铅等的合金。铜锈大多更多全科试卷,请关注公众号:高中试卷君
呈青绿色,主要含有 和 。下列说法错误的是
A.基态铜原子核外电子有15种不同的空间运动状态
B.青铜的熔点低于纯铜
C.青铜器中锡、铅对铜有保护作用
D.可用 溶液浸泡青铜器来清洗水铜器的铜锈
【答案】D
【解析】A.Cu的核外电子占据1s、2s、2p、3s、3p、3d、4s轨道,核外电子有1+1+3+1+3+5+1=15种空
间运动状态,故A正确;
B.合金的熔点低于组分金属的熔点,因此青铜的熔点低于纯铜,故B正确;
C.Sn、Pb的活泼性强于Cu,青铜中的Cu和Sn、Pb形成原电池且Sn、Pb为负极,达成“牺牲阳极的阴
极保护”,故C正确;
D. 会和Cu反应而腐蚀铜器,不能用 溶液浸泡青铜器来清洗水铜器的铜锈,故D错误;
故答案为:D。
3.下列化学用语或图示表达不正确的是
A. 的电子式: B.基态Cr原子的价层电子排布式:
C.乙醇的分子式: D.乙炔的分子结构模型:
【答案】B
【解析】A.氯化钠是由钠离子和氯离子构成的 ,A正确;
B.基态Cr原子的价层电子排布式为:3d54s1,B错误;
C.乙醇结构简式为C HOH,分子式为 ,C正确;
2 5
D.乙炔为直线形分子,分子结构模型: ,D正确;
故选B。
4.工业上用 (分子结构: )与 为原料制备 ,发生反应:更多全科试卷,请关注公众号:高中试卷君
为阿伏加德罗常数的值,下列说法不正确的是
A. 既是氧化剂,又是还原剂
B.生成 ,转移电子
C.消耗 ,断裂的S-S键数目为
D. 既是氧化产物,又是还原产物
【答案】A
【解析】A.反应中C元素化合价由CH 中-4价升至CS 中+4价,CH 做还原剂,S元素化合价由0价降
4 2 4
至-2价,S 做氧化剂,A错误;
8
B.每生成4molH S,反应转移16mol电子,17gHS是0.5mol,转移电子2mol, B正确;
2 2
C.1 molS 中含有8molS-S键,消耗1 molS,断裂8molS-S键,C正确;
8 8
D.反应中C元素化合价由CH 中-4价升至CS 中+4价,S元素化合价由0价降至-2价,CS 既是氧化产物
4 2 2
又是还原产物,D正确;
答案选A。
5.为提纯下列物质(括号内的物质为杂质),所选用的除杂试剂和分离方法均正确的有几项
① ② ③ ④ ⑤
混合物 乙醇(水) 乙酸乙酯(乙酸) 苯(苯酚) 溴苯(溴)
除杂试
饱和 溶液 生石灰 饱和 溶液 溴水 苯
剂
分离方
洗气 蒸馏 分液 过滤 萃取分液
法
A.1 B.2 C.3 D.4
【答案】B
【解析】①二氧化碳和二氧化硫均会和饱和碳酸钠溶液反应,除杂方法错误;
②生石灰和水生成氢氧化钙,然后利于乙醇沸点较低的性质蒸馏出乙醇,正确;
③碳酸钠和乙酸反应生成盐溶液、和乙酸乙酯不反应且分层,能用分液的方法分离出有机层乙酸乙酯,正
确;
④溴和苯酚生成的三溴苯酚溶于苯中,不能过滤分离,错误;
⑤苯与溴苯互溶,不能分液分离,错误;更多全科试卷,请关注公众号:高中试卷君
故选B。
6.奥培米芬是一种雌激素受体调节剂,其合成中间体的结构简式如图所示:
关于该中间体,下列说法正确的是
A.含有三种官能团 B.含有2个手性碳原子
C.能发生消去反应和水解反应 D.苯环上的一氯代物有5种结构
【答案】C
【解析】A.由题干有机物的键线式可知,分子中含有碳氯键、碳碳双键、醚键和酯基四种官能团,A错
误;
B.已知同时连有四个互不相同的原子或原子团的碳原子为手性碳原子,结合题干有机物的键线式可知,
分子中不含手性碳原子,B错误;
C.由题干有机物的键线式可知,分子中含有碳氯键,且与氯原子相邻的碳原子上还有H,故能发生消去
反应和水解反应,同时含有酯基也能发生水解反应,C正确;
D.由题干有机物的键线式可知,分子中三个苯环不对称,故苯环上的一氯代物有8种结构,如图所示:
,D错误;
故答案为:C。
7.下列有关电极方程式或离子方程式错误的是
A.铅蓄电池放电时,正极反应:
B.向碘化亚铁溶液中滴加少量稀硝酸:更多全科试卷,请关注公众号:高中试卷君
C.向0.1mol·L NaHA溶液( )加入NaOH溶液:
D.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) (阴极)
【答案】B
【解析】A. 铅蓄电池正极材料为PbO ,正极发生还原反应,根据化合价变化可知得2e-,故A正确;
2
B. 碘化亚铁中,碘离子和亚铁离子都有还原性,且碘离子还原性更强,先与硝酸反应,故离子方程式为:
,故B错误;
C. 由于0.1mol·L NaHA溶液的 ,说明c(H+)= mol·L ,NaHA 中的氢离子完全电离,故C正确;
D. 铜片上电镀银阳极电极式: ,阴极电极式: ,两极电极式相加得Ag(阳极)
(阴极),故D正确;
故选B。
8.PLA是由乳酸结构单元组成的高分子聚合物,其降解产物为乳酸,而乳酸最终可被生物体进一步分解
为二氧化碳和水,工厂用PLA来生产一次性餐具,既卫生又环保。下列叙述正确的是
A.乳酸与乙酸互为同系物
B.乳酸分子和丙交酯分子中都含手性碳,且手性碳数目相同
C.乳酸合成丙交酯的反应是取代反应
D.PLA可以发生取代反应、加成反应、氧化反应
【答案】C更多全科试卷,请关注公众号:高中试卷君
【解析】A.乳酸和乙酸含有的官能团不同,不是同系物,A错误;
B.连有4个不同原子或原子团的饱和碳原子是手性碳原子,乳酸中有一个手性碳原子,丙交酯中有两个,
B错误;
C.该反应是酯化反应,也属于取代反应,C正确;
D.PLA中不含碳碳双键等能发生加成反应的结构,PLA不能发生加成反应,D错误;
故选C。
9.某储氢材料前驱体结构如下图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填
充了3个能级,其中有2个未成对电子。下列说法错误的是
A.简单氢化物沸点高低: B.Y和W位于同一主族
C.第一电离能大小: D.阴、阳离子中均有配位键
【答案】B
【分析】由题干信息可知,基态Z原子的电子填充了3个能级,其中有2个未成对电子,故Z为C或者
O,根据多孔储氢材料前驱体结构图可知Y周围形成了4个单键,再结合信息M、W、X、Y、Z五种元素
原子序数依次增大,故Y为N,故Z为O,M只形成一个单键,M为H,X为C,则W为B,据此分析解
题。
【解析】A.X为C,Y为N,由于N元素形成的简单氢化物氨气中含有氢键,则其沸点高于C的简单氢
化物甲烷,A正确;
B.Y为N,位于第VA族,W为B,位于第IIIA族,二者不属于同主族元素,B错误;
C.X为C,Y为N,Z为O,根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA,VA与
VIA反常,故第一电离能: ,C正确;
D.由于阳离子中的Y原子是N原子,形成了类似于铵根离子的阳离子,故存在配位键,阴离子中的W为
B,最外层上只有3个电子,能形成3个共价键,现在形成了4个共价键,故还有一个配位键,D正确;
故选B。
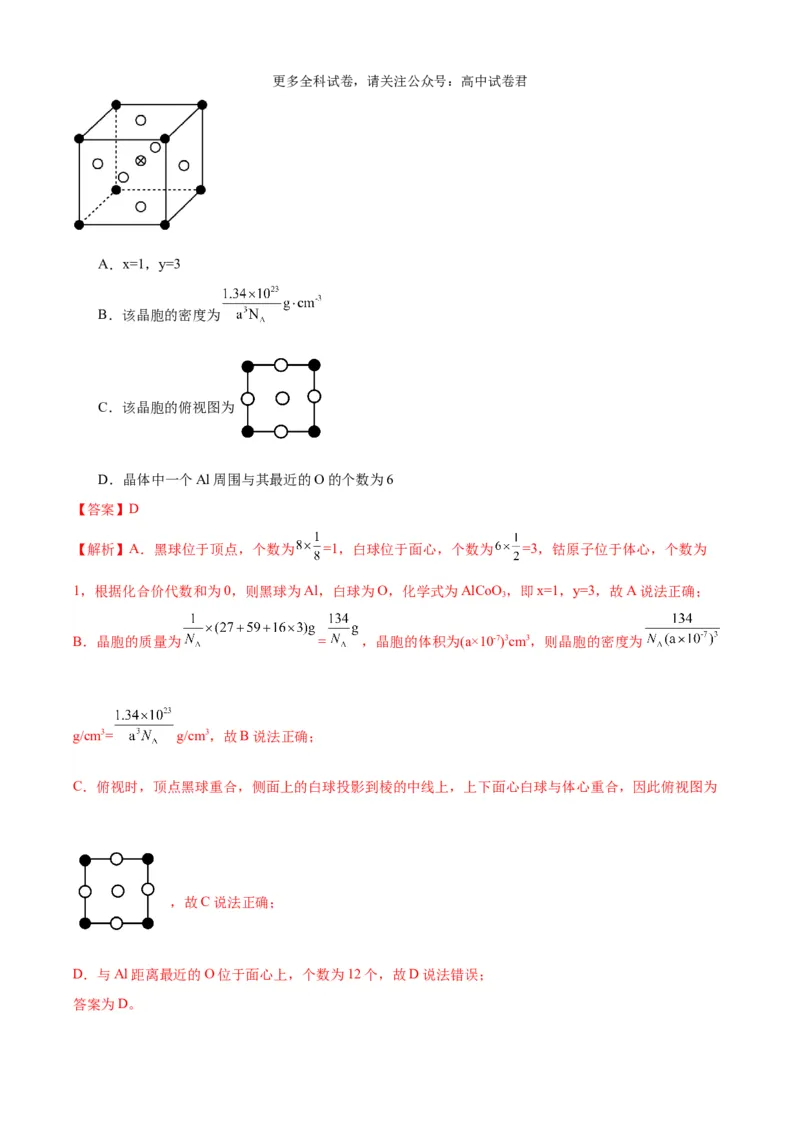
10.Al CoO 的立方晶胞如图所示,已知处在体心处的原子为Co,晶胞参数anm,下列说法错误的是
x y更多全科试卷,请关注公众号:高中试卷君
A.x=1,y=3
B.该晶胞的密度为
C.该晶胞的俯视图为
D.晶体中一个Al周围与其最近的O的个数为6
【答案】D
【解析】A.黑球位于顶点,个数为 =1,白球位于面心,个数为 =3,钴原子位于体心,个数为
1,根据化合价代数和为0,则黑球为Al,白球为O,化学式为AlCoO,即x=1,y=3,故A说法正确;
3
B.晶胞的质量为 = ,晶胞的体积为(a×10-7)3cm3,则晶胞的密度为
g/cm3= g/cm3,故B说法正确;
C.俯视时,顶点黑球重合,侧面上的白球投影到棱的中线上,上下面心白球与体心重合,因此俯视图为
,故C说法正确;
D.与Al距离最近的O位于面心上,个数为12个,故D说法错误;
答案为D。更多全科试卷,请关注公众号:高中试卷君
11.一种可用于吸收CO 的电池,其工作原理如图所示。下列说法正确的是
2
A.电极a上发生的反应为H-2e⁻=2H+
2
B.I室出口处溶液的pH大于入口处
C.该装置可以制取CaCl 和NaHCO
2 3
D.如果将阴离子交换膜改为阳离子交换膜,则电池工作时I室可能有CaCO 沉淀生成
3
【答案】C
【分析】在电极a上H 放电,为负极,由于电极a附近为碱性条件,所以电极a上发生的反应为H-2e-
2 2
+2OH-=2H O;电极b为正极,H+放电生成H,电极b上发生的反应为2H++2e-=H ,以此作答。
2 2 2
【解析】A.由分析可知,电极a上发生的反应为H-2e-+2OH-=2H O,故A错误;
2 2
B.I室中的OH-在电极a上被消耗,导致氢氧根离子减小,出口处溶液的pH小于入口处,故B错误;
C.II室的Cl-通过阴离子交换膜进入I室,可在I室获得CaCl ,II室中水电离产生的氢离子放电,使溶液
2
呈碱性,过量的CO 与OH-反应生成碳酸氢根,则可在II室获得碳酸氢钠,故C正确;
2
D.II室中有碳酸根离子生成,若将阴离子交换膜改为阳离子交换膜,则I室中的钙离子通过交换膜进入II
室,从而在II室中生成碳酸钙沉淀,故D错误;
故选C。
12.根据实验操作及现象,得出结论正确的是
选
实验操作及现象 结论
项
和稀硫酸混合产生浅黄色沉淀和刺激
A 硫酸表现氧化性, 表现还原性
性气味的气体
B 向酸性 溶液中滴加乙苯,溶液褪色 乙苯的苯环中含有碳碳双键
和 生成AgI,促进Ag和HI溶液发生反应生
C Ag与HI溶液生成黄色沉淀和无色气体
成AgI和更多全科试卷,请关注公众号:高中试卷君
氧化性: , 和Cu发生置换
D 在 溶液中加入铜粉,溶液变蓝色
反应
A.A B.B C.C D.D
【答案】C
【解析】A. 和稀硫酸混合产生浅黄色沉淀和刺激性气味的气体的化学方程式为:
,硫酸只表现酸性, 既表现氧化性,又表现还原
性,A错误;
B.苯环能使烃基活化,苯环上的乙基能被酸性 氧化,从而使酸性 溶液褪色,不能证明苯
环中含有碳碳双键,B错误;
C.体系中可生成极难溶的AgI,极大降低了Ag+浓度,促进Ag和HI溶液发生反应生成AgI和 H,C正
2
确;
D.在 溶液中加入铜粉,反应的化学方程式为: ,可说明氧
化性: ,但反应不属于置换反应,D错误;
故选C。
13.大力推广锂电池新能源汽车对实现“碳达峰”“碳中和”具有重要意义. 与 都是锂
离子电池的电极材料,可利用钛铁矿(主要成分为 ,还有少量MgO、 等杂质)来制备,工艺
流程如下:
下列叙述错误的是更多全科试卷,请关注公众号:高中试卷君
A.酸浸后,得到滤渣的主要成分是
B.在滤液②中主要的金属阳离子有 、
C.高温煅烧时发生的反应为
D.制备 过程中会生成 (Ti为+4价),则 中不含过氧键
【答案】D
【分析】利用钛铁矿(主要成分为 ,还有少量MgO、 等杂质)来制备 与 ,由
制备流程可知,加盐酸过滤后的滤渣为 ,滤液①中含Mg2+、Fe2+、TiOCl ,水解后过滤,沉淀为
,经过一系列反应得到 ;水解后的滤液②中含Mg2+、Fe2+,双氧水可氧化亚铁离子,
在磷酸条件下过滤分离出FePO ,高温煅烧LiCO、HC O、FePO 得到 ,以此解答。
4 2 3 2 2 4 4
【解析】A.由分析可知, 不和盐酸反应,酸浸后,得到滤渣的主要成分是 ,故A正确;
B.由分析可知,水解后的滤液②中含Mg2+、Fe2+,故B正确;
C.高温煅烧时草酸作还原剂将磷酸铁中三价铁还原成二价的亚铁生成磷酸亚铁锂,发生的反应为
,C正确;
D.制备 过程中会生成 (Ti为+4价,Li为+1价),根据化合物中各元素化合价代数和
为0可知 中含过氧键,15个氧中有七个氧呈现-2价,八个氧呈现-1,D错误;
故选D。
14.高电压水系锌-有机混合液流电池的装置及充、放电原理如图所示。下列说法正确的是更多全科试卷,请关注公众号:高中试卷君
A.锌元素位于元素周期表的d区
B.充电时,每转移 ,阴极增重
C.放电时,负极的电极反应式为
D.放电时,化学能全部转化为电能
【答案】B
【分析】高电压水系锌-有机混合液流电池工作原理为:放电时为原电池,金属Zn发生失电子的氧化反应
生成Zn2+,为负极,则FQ所在电极为正极,正极反应式为2FQ+2e-+2H+═FQH,负极反应式为Zn-2e-
2
+4OH-= ;充电时电解池,原电池的正负极连接电源的正负极,阴阳极的电极反应与原电池的负正
极的反应式相反,电解质中阳离子移向阴极、阴离子移向阳极,据此分析解答。
【解析】A.锌的价层电子排布式为3d104s2,该元素位于元素周期表的ds区,A错误;
B.因为放电时负极反应式为Zn-2e-+4OH-= ,每转移2mol电子,理论上负极减小1molZn,质量为
m=n∙M=1mol×65g/mol=65g,所以充电时,每转移 ,阴极增重 ,B正确;
C.放电时为原电池,金属Zn为负极,负极反应式为 ,C错误;
D.放电过程,化学能转化为电能,但同时会有热量散失,一部分能量以热能的形式转化,D错误;
故选B。
15.25℃时,用NaOH溶液分别滴定弱酸HA、CuSO 、FeSO 三种溶液,pM随pH变化关系如图所示【p
4 4
表示负对数,M表示c(HA)/c(A-)、c(Cu2+)、c(Fe2+)等】,已知K 【Cu(OH) 】