文档内容
通辽一中 2023 级高一下学期期末考试
化学试题
注意事项:
1、答卷前,考生务必将自己的姓名、考生号涂写在答题卡上。本试卷满分 100分,考试时间
75分钟。
2、做选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3、回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 Fe:56 Cu:64 I:127
.第Ⅰ卷(选择题)
一、单选题(每题3分,共45分)
1.化学与生产、生活、环保等方面密切相关,下列说法正确的是( )
A.煤的气化、液化与石油的裂化、分馏均为化学变化
B.2024年6月4日,在月球表面成功展开的五星红旗的主要材料芳纶属于合成纤维
C.马王堆一号汉墓出土的直裾素纱禅衣是西汉蚕丝制品,主要成分为纤维素
D.“歼-20”飞机上使用的碳纤维被誉为“新材料之王”,是一种新型有机高分子材料
2.下列化学用语表示不正确的是( )
A.乙烯的结构简式: B.乙醇的结构式:
C.羟基的电子式: D.乙酸分子式为CHO
2 4 2
3.下列化学反应属于加成反应的是( )
A.乙烯使酸性高锰酸钾溶液褪色 B.在铜做催化剂的条件下,乙醇与氧气反应
C.乙醇和乙酸在浓硫酸催化下的反应 D.乙烯使溴的四氯化碳溶液褪色
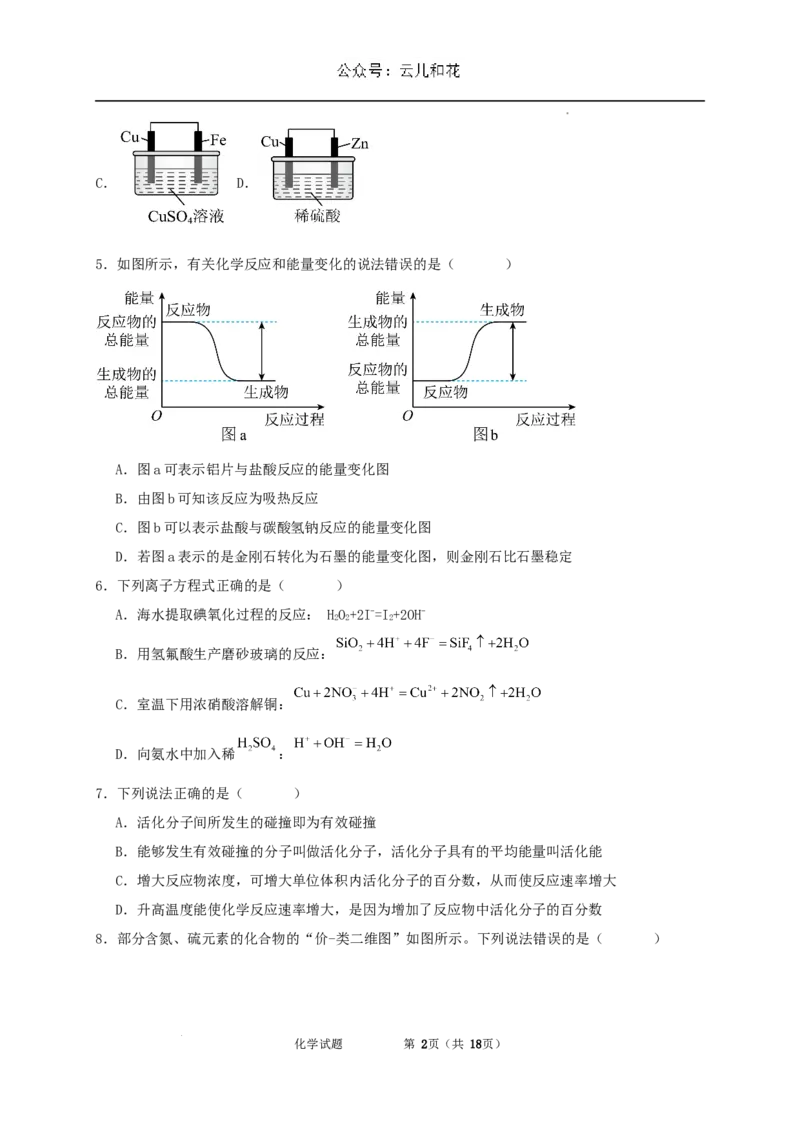
4.下列装置中不能构成原电池的是( )
A. B.
化学试题 第 1页(共 18页)
学科网(北京)股份有限公司C. D.
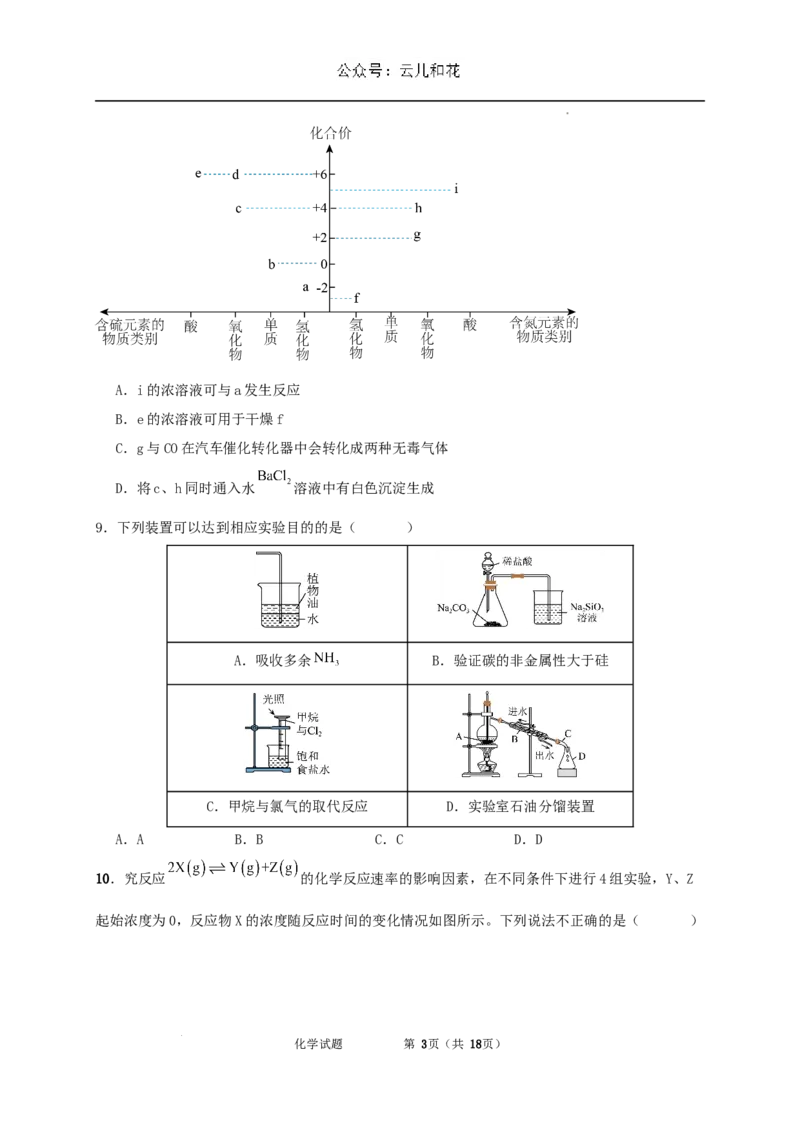
5.如图所示,有关化学反应和能量变化的说法错误的是( )
A.图a可表示铝片与盐酸反应的能量变化图
B.由图b可知该反应为吸热反应
C.图b可以表示盐酸与碳酸氢钠反应的能量变化图
D.若图a表示的是金刚石转化为石墨的能量变化图,则金刚石比石墨稳定
6.下列离子方程式正确的是( )
A.海水提取碘氧化过程的反应: HO+2I-=I+2OH-
2 2 2
B.用氢氟酸生产磨砂玻璃的反应:
C.室温下用浓硝酸溶解铜:
D.向氨水中加入稀 :
7.下列说法正确的是( )
A.活化分子间所发生的碰撞即为有效碰撞
B.能够发生有效碰撞的分子叫做活化分子,活化分子具有的平均能量叫活化能
C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大
D.升高温度能使化学反应速率增大,是因为增加了反应物中活化分子的百分数
8.部分含氮、硫元素的化合物的“价-类二维图”如图所示。下列说法错误的是( )
化学试题 第 2页(共 18页)
学科网(北京)股份有限公司A.i的浓溶液可与a发生反应
B.e的浓溶液可用于干燥f
C.g与CO在汽车催化转化器中会转化成两种无毒气体
D.将c、h同时通入水 溶液中有白色沉淀生成
9.下列装置可以达到相应实验目的的是( )
A.吸收多余 B.验证碳的非金属性大于硅
C.甲烷与氯气的取代反应 D.实验室石油分馏装置
A.A B.B C.C D.D
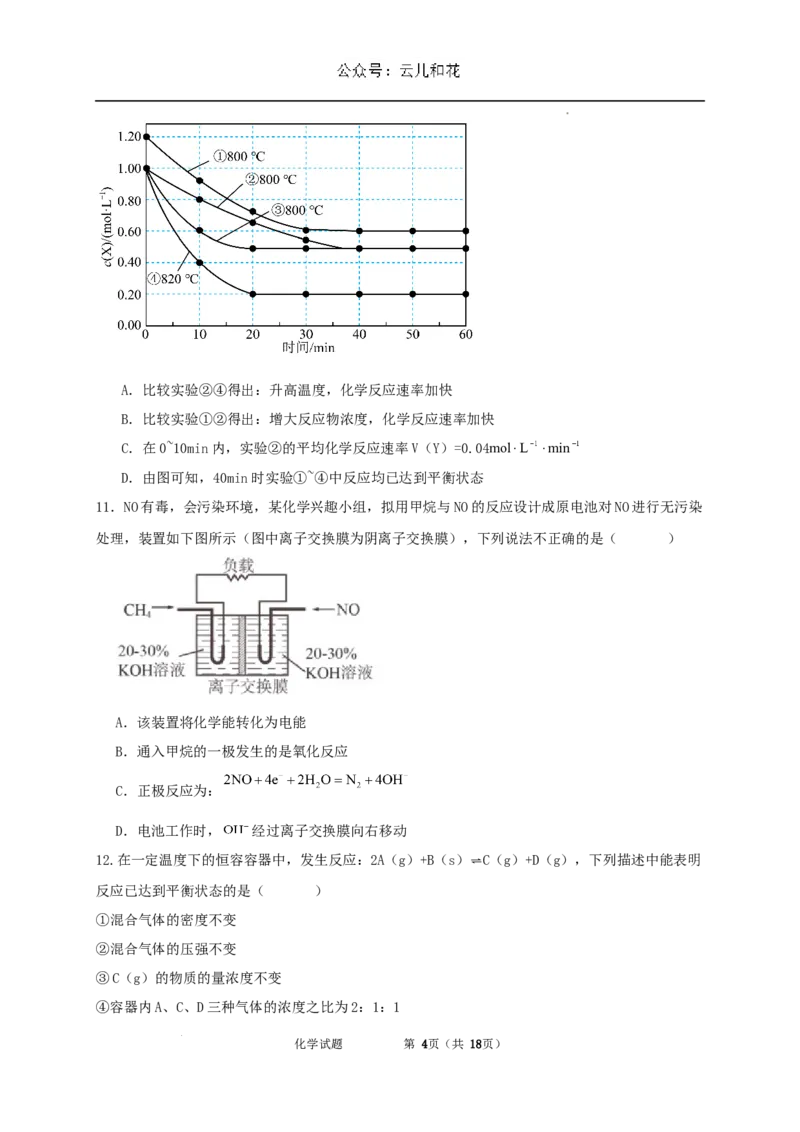
10.究反应 的化学反应速率的影响因素,在不同条件下进行4组实验,Y、Z
起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。下列说法不正确的是( )
化学试题 第 3页(共 18页)
学科网(北京)股份有限公司A.比较实验②④得出:升高温度,化学反应速率加快
B.比较实验①②得出:增大反应物浓度,化学反应速率加快
C.在0~10min内,实验②的平均化学反应速率V(Y)=0.04mol⋅L ⋅min
D.由图可知,40min时实验①~④中反应均已达到平衡状态
11.NO有毒,会污染环境,某化学兴趣小组,拟用甲烷与NO的反应设计成原电池对NO进行无污染
处理,装置如下图所示(图中离子交换膜为阴离子交换膜),下列说法不正确的是( )
A.该装置将化学能转化为电能
B.通入甲烷的一极发生的是氧化反应
C.正极反应为:
D.电池工作时, 经过离子交换膜向右移动
12.在一定温度下的恒容容器中,发生反应:2A(g)+B(s) C(g)+D(g),下列描述中能表明
⇌
反应已达到平衡状态的是( )
①混合气体的密度不变
②混合气体的压强不变
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
化学试题 第 4页(共 18页)
学科网(北京)股份有限公司⑤单位时间内生成n molC,同时生成n mol D
⑥单位时间内生成n molD,同时生成2n mol A.
A.①③⑤ B.②③④ C.②⑥ D.①③⑥
13.有机物R是金银花的一种成分,具有广谱抗病毒功效,键线式为 (已
知CH=CHCHOH的键线式为 )。下列说法错误的是( )
2 2
A.R能发生加成、氧化、取代反应
B.用酸性高锰酸钾溶液可以确认R含碳碳双键
C.R分子中所有碳原子可能共平面
D. CHO与R互为同分异构体
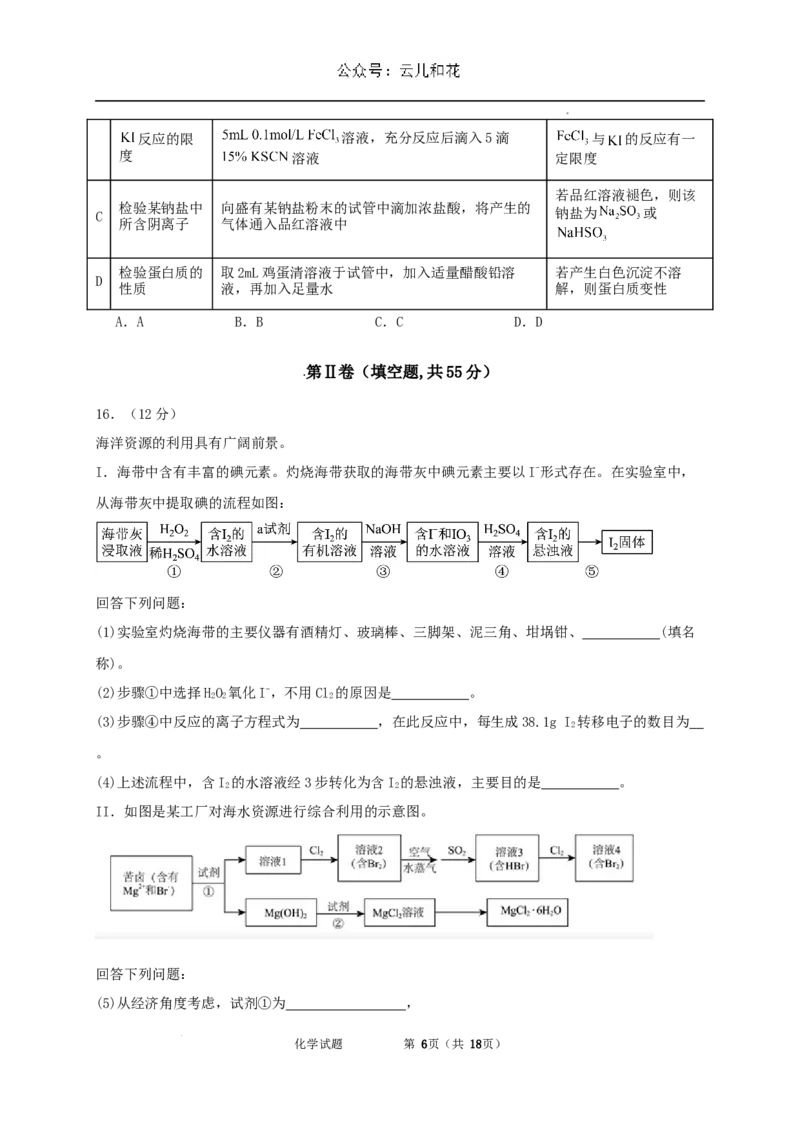
14.基于非金属原子嵌入石墨烯三嗪基 中,用于催化一氧化碳加氢生成甲醇的反应历程如
图,其中吸附在催化剂表面上的物种用“ ”标注,下列说法中错误的是( )
A.整个反应历程中有四个基元反应
B.过渡态相对能量:
C.物种吸附在催化剂表面的过程为吸热过程
D.反应决速步的活化能为0.95eV
15.下列实验方案设计、现象和结论都正确的是( )
实验目的 实验方案 现象和结论
在试管中加入0.5g淀粉和 溶
检验淀粉的水 未观察到银镜生成,则
A 液,加热,待溶液冷却后向其中加入银氨溶液,水
解程度 淀粉未发生水解
浴加热
B 探究 与 取 溶液于试管中,加入 若溶液变血红色,则
化学试题 第 5页(共 18页)
学科网(北京)股份有限公司反应的限 溶液,充分反应后滴入5滴 与 的反应有一
度 溶液 定限度
若品红溶液褪色,则该
检验某钠盐中 向盛有某钠盐粉末的试管中滴加浓盐酸,将产生的
C 钠盐为 或
所含阴离子 气体通入品红溶液中
检验蛋白质的 取2mL鸡蛋清溶液于试管中,加入适量醋酸铅溶 若产生白色沉淀不溶
D
性质 液,再加入足量水 解,则蛋白质变性
A.A B.B C.C D.D
.第Ⅱ卷(填空题,共55分)
16.(12分)
海洋资源的利用具有广阔前景。
I.海带中含有丰富的碘元素。灼烧海带获取的海带灰中碘元素主要以I-形式存在。在实验室中,
从海带灰中提取碘的流程如图:
回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、玻璃棒、三脚架、泥三角、坩埚钳、 (填名
称)。
(2)步骤①中选择HO 氧化I-,不用Cl 的原因是 。
2 2 2
(3)步骤④中反应的离子方程式为 ,在此反应中,每生成38.1g I 转移电子的数目为
2
。
(4)上述流程中,含I 的水溶液经3步转化为含I 的悬浊液,主要目的是 。
2 2
II.如图是某工厂对海水资源进行综合利用的示意图。
回答下列问题:
(5)从经济角度考虑,试剂①为 ,
化学试题 第 6页(共 18页)
学科网(北京)股份有限公司发生反应的离子方程式为 。
(6)由MgCl 溶液得到MgCl·6HO晶体的操作是 ,过滤、洗涤、干燥。
2 2 2
(7)通入SO 的作用是 (用化学方程式表示)。
2
(8)由MgCl 制备金属镁的化学方程式为 。
2
17.(13分)
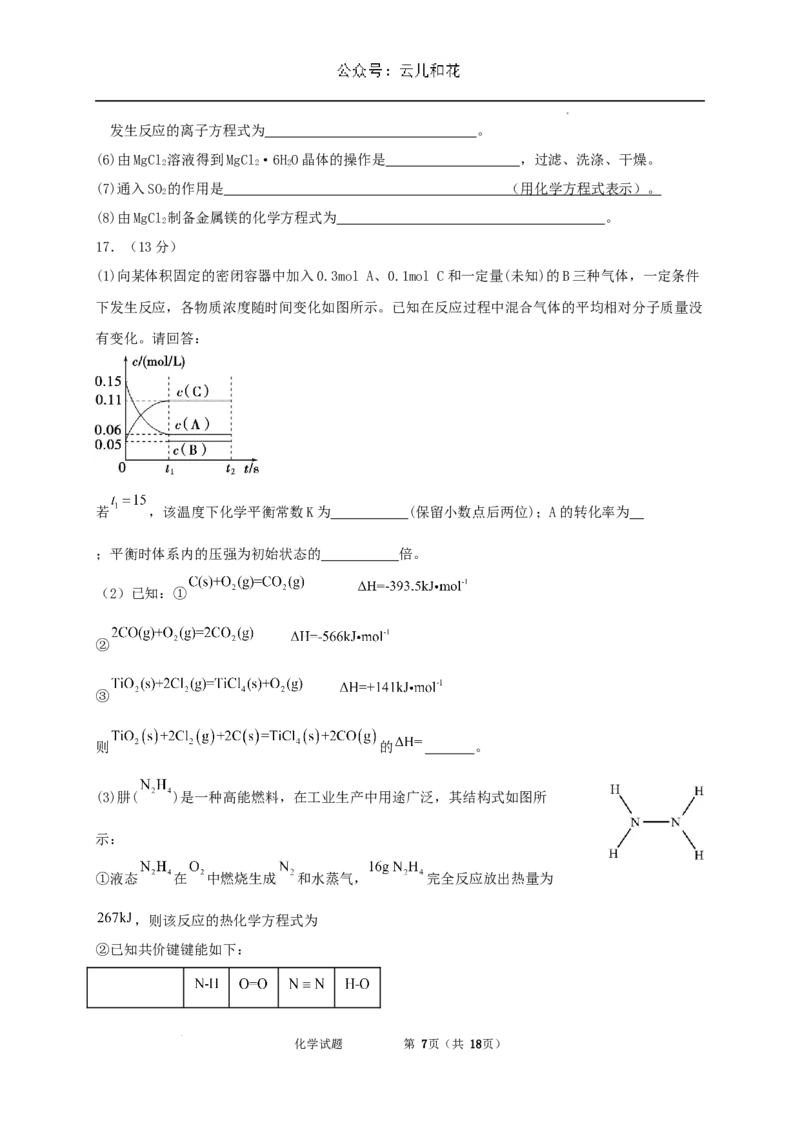
(1)向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件
下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没
有变化。请回答:
若 ,该温度下化学平衡常数K为 (保留小数点后两位);A的转化率为
;平衡时体系内的压强为初始状态的 倍。
(2)已知:①
②
③
则 的 。
(3)肼( )是一种高能燃料,在工业生产中用途广泛,其结构式如图所
示:
①液态 在 中燃烧生成 和水蒸气, 完全反应放出热量为
,则该反应的热化学方程式为
②已知共价键键能如下:
化学试题 第 7页(共 18页)
学科网(北京)股份有限公司键能
则 中N-N的键能为 。
(4)十九大报告提出要对环境问题进行全面、系统的可持续治理。回答下列问题:电化学气敏传感
器可用于监测环境中 的含量,其工作原理示意图如图。
Pt电极(b)上的电极反应式为 。当消耗0.1mol 时,理论上转移电子数为
。
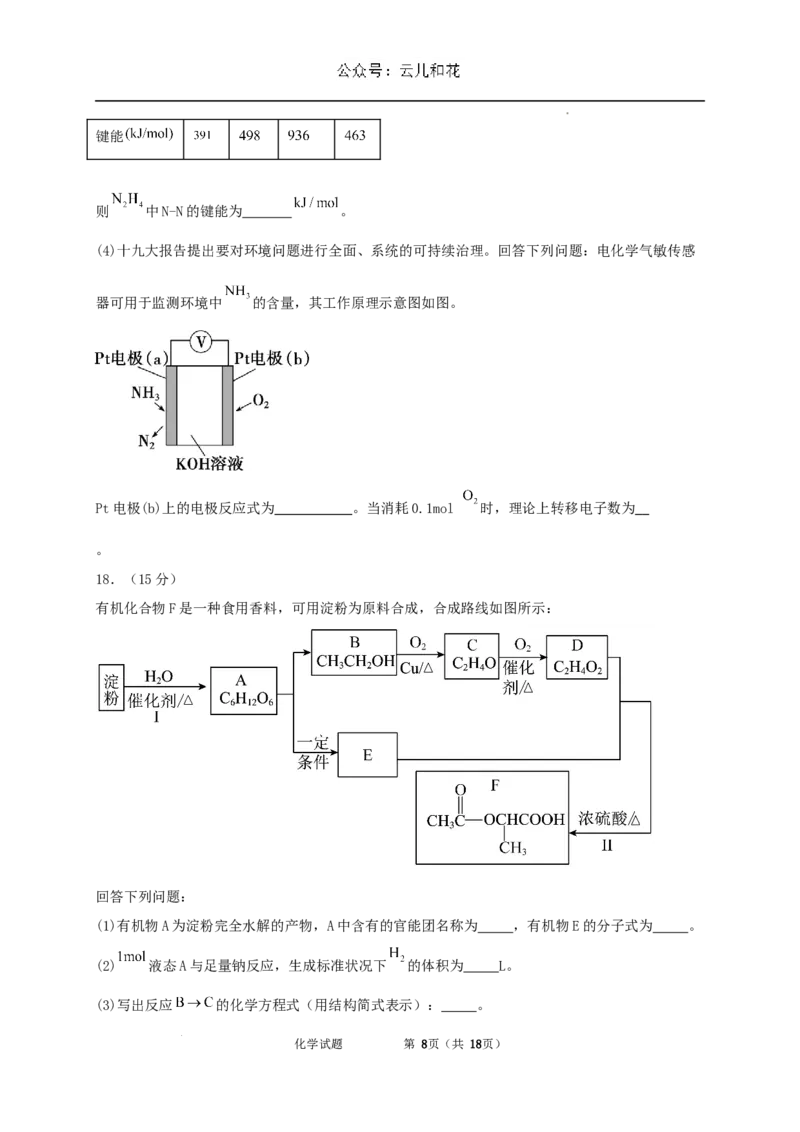
18.(15分)
有机化合物F是一种食用香料,可用淀粉为原料合成,合成路线如图所示:
回答下列问题:
(1)有机物A为淀粉完全水解的产物,A中含有的官能团名称为 ,有机物E的分子式为 。
(2) 液态A与足量钠反应,生成标准状况下 的体积为 L。
(3)写出反应 的化学方程式(用结构简式表示): 。
化学试题 第 8页(共 18页)
学科网(北京)股份有限公司(4)写出鉴别有机物B中混有D的实验方法: 。
(5)F的同分异构体中, 该物质与足量 溶液反应放出 的有 种。
(6)下列说法错误的是 (填字母)。
a.反应Ⅱ为取代反应
b.等物质的量的E分别与足量的 和 反应,消耗的 和 的物质的量相等
c.D、E互为同系物
(7)淀粉在酸性条件下可发生水解反应生成A,要证明淀粉已经水解完全。需要向水解后的溶液中
加入 (填试剂名称),完全水解的实验现象为 。
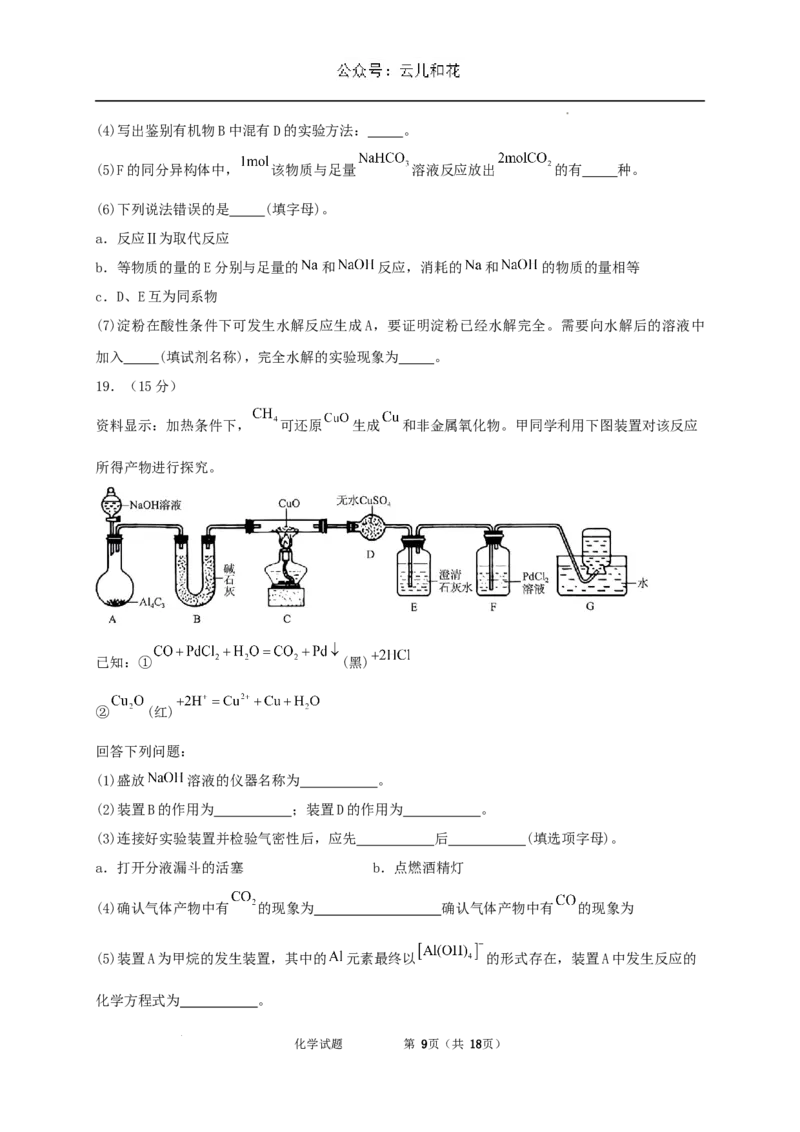
19.(15分)
资料显示:加热条件下, 可还原 生成 和非金属氧化物。甲同学利用下图装置对该反应
所得产物进行探究。
已知:① (黑)
② (红)
回答下列问题:
(1)盛放 溶液的仪器名称为 。
(2)装置B的作用为 ;装置D的作用为 。
(3)连接好实验装置并检验气密性后,应先 后 (填选项字母)。
a.打开分液漏斗的活塞 b.点燃酒精灯
(4)确认气体产物中有 的现象为 确认气体产物中有 的现象为
(5)装置A为甲烷的发生装置,其中的 元素最终以 的形式存在,装置A中发生反应的
化学方程式为 。
化学试题 第 9页(共 18页)
学科网(北京)股份有限公司(6)乙同学认为经甲烷充分反应的红色固体产物中还可能含有 。取少许固体产物,加入适量
,观察到 ,证明固体产物中没有 。
化学试题 第 10页(共 18页)
学科网(北京)股份有限公司通辽一中 2023 级高一下学期期末考试
化学试题参考答案
一、选择题
1.B
【详解】A.煤的气化、液化与石油的裂化属于化学变化,石油的分馏为物理变化,A错误;
B.芳纶属于合成纤维,B正确;
C.蚕丝主要成分是蛋白质,C错误;
D.碳纤维为碳的单质,不属于高分子材料,D错误;
2.A
【详解】A.结构简式中碳碳双键不能省略。
B.乙醇的结构式为
C.羟基的电子式为
D.乙酸分子式为C HO
2 4 2
3.D
【详解】乙烯与溴发生加成反应而使溴的四氯化碳溶液褪色。故选D。
4.A
【详解】A.乙醇为非电解质,不能构成原电池,故A错误;
5.D
【详解】图a反应物的总能量高于生成物,表示的是放热反应,铝片与盐酸的反应为放热反应,符
合图a的能量变化,A正确;图b表示的是吸热反应,故反应物从环境中吸收的能量大于生成物向
环境释放的能量,B正确;图b表示的是吸热反应,盐酸与碳酸氢钠的反应为吸热反应,C正确;
若图a表示的是金刚石转化为石墨的能量变化图,则金刚石转化为石墨要放出能量,由能量越低越
稳定可知石墨比金刚石稳定,D错误。
6.C
【详解】A.海水提取碘氧化过程的反应,为酸性条件,不能出现氢氧根。故A错误;
B.氢氟酸生产磨砂玻璃中二氧化硅反应生成四氟化硅和水,离子方程式为:
SiO+4HF=SiF ↑+2H O,故B错误;
2 4 2
C.室温下用浓HNO 溶解铜生成硝酸铜、二氧化氮和水,反应的离子方程式:
3
化学试题 第 11页(共 18页)
学科网(北京)股份有限公司,故C正确;
D.氨水是弱碱,需保留化学式,向氨水中加入稀 反应生成硫酸氨和水,离子方程式为:
NH •H O+H+═H O+ ,故D错误;
3 2 2
7.D
【详解】A. 活化分子间发生了化学反应的碰撞为有效碰撞,故错误;
B. 能够发生有效碰撞的分子叫做活化分子,活化分子多出其他反应物分子的那部分能量称为活化
能,故错误;
C. 增大反应物浓度,可增大单位体积内活化分子的数目,活化分子的百分数不变,故错误;
D. 升高温度能使化学反应速率增大,是因为增大了单位体积内活化分子的百分数,故正确。
8.B
【分析】由图可知,a为HS,b为S,c为SO ,d为SO ,e为HSO ,f为NH ,g为NO,h为
2 2 3 2 4 3
NO ,i为HNO,以此解题。
2 3
【详解】A.硝酸有氧化性,可以和硫化氢发生氧化还原反应,A正确;
B.浓硫酸可以和氨气反应,不能干燥氨气,B错误;
C.NO、CO在催化转化器中发生反应生成N 和CO 两种无毒气体,C正确;
2 2
D.二氧化硫和二氧化氮同时通入水中,会生成硫酸,与氯化钡会生成硫酸钡白色沉淀,D正确;
9.C
【详解】A.未做到防倒吸,错误;
B.稀盐酸具有挥发性,也可与硅酸钠溶液反应生成沉淀,错误;
C.甲烷光照条件下与氯气发生取代反应,正确;
D.进水口错误,应该是下进上出,温度计应放在支管口处,错误。
10.C
②、④
【详解】A.实验 中X的起始浓度相同,温度不同,由图可知,升高温度,化学反应速
率加快,A正确;
①、②
B.实验 中X的起始浓度不同、温度相同,由图可知,增大反应物浓度,化学反应速率
加快,B正确;
化学试题 第 12页(共 18页)
学科网(北京)股份有限公司C.在0 10min之间,实验 ② 的平均速率 (Y)= =0.01mol•L-1•min-1,C错误;
∼
D.由图可知,40min时实验
①~④
中X的浓度均不再改变了,即反应均已达到平衡状态,D正
确;
11.D
【详解】A. 该装置为原电池,将化学能转化为电能,故A正确;
B. 甲烷作负极,通入甲烷的一极发生的是氧化反应,故B正确;
C. NO在正极 生还原反应,生成无污染的氮气,正极反应为: ,
故C正确;
D. 电池工作时,阴离子向负极移动,应该由经过离子交换膜向左移动,故D错误;
12.D
①
【详解】 气体体积不变,反应过程中气体质量发生变化,使得混合气体的密度随着变化,当混
②
合气体的密度不变时,表明反应已达到平衡状态; 混合气体的物质的量不变,所以混合气体的
③
压强始终保持不变,与反应是否达到平衡状态无关; 反应过程中C(g)的物质的量在变化,使
得C(g)的物质的量浓度随着变化,当C(g)的物质的量浓度不变时表明反应已达到平衡状态;
④ ⑤
容器内A、C、D三种气体的浓度之比为2:1:1与反应是否已达到平衡状态无关; 都是正
⑥
反应速率,不能表明反应已达到平衡状态; 正反应速率等于逆反应速率,表明反应已达到平衡
状态。故选D。
点睛:反应达到平衡状态的实质是正反应速率等于逆反应速率,特征是各物质的物质的量保持不变。
13.B
【详解】A.R中含有双键,可以发生加成反应、氧化反应,含有羟基、烃基可以发生取代反应,
故A正确;
B.R分子的羟基也可以使酸性高锰酸钾褪色,故B错误;
化学试题 第 13页(共 18页)
学科网(北京)股份有限公司C.R中碳原子均位于碳碳双键形成的平面上,平面通过单键相连,单键可以旋转,所以所有碳原
子可能共面,故C正确;
D. 和 的分子式均为C H O,二者分子式相同,结构不同,
10 16
互为同分异构体,故D正确;
14.C
【详解】A.从微观上看,反应物分子一般总是经过若干的简单反应步骤,才最后转化为产物分子
的。每一个简单的反应步骤,就是一个基元反应。基元反应步骤要求反应物一步变成生成物,没有
任何中间产物,由图可知,整个反应历程中有四个基元反应,故A正确;
B.由图可知,过渡态相对能量的大小顺序为 ,故B正确;
C.由图可知,吸附在催化剂表面的生成物总能量低于反应物的总能量,为放热过程,故C错误;
D.反应的活化能越大,反应速率越慢,反应决速步为慢反应,由图可知,反应HCO*+H=HCO-H
2 3
的活化能最大,反应速率最慢,则反应决速步的活化能为0.35eV—(—0.60eV)=0.95eV,故D正确;
15.D
【详解】A.检验淀粉水解产生的葡萄糖需要在碱性环境中,需要先将酸性水解液调成 后再进行
检验,A错误;
B.铁离子和碘离子反应的离子方程式为: ,表格中数据显示铁离子过量,加入
KSCN溶液后溶液一定变红,不能证明该反应有限度,B错误;
C.该钠盐还可能是硫代硫酸钠,C错误;
D.醋酸铅为重金属盐,能使蛋白质变性,蛋白质变性为化学变化,不可逆,D正确;
故选D。
16.解析:【分析】Ⅰ.海带灰中含有碘化钾等物质,溶于水,加入稀硫酸酸化的双氧水氧化碘离
子,得到碘的水溶液,用苯或四氯化碳萃取,然后用氢氧化钠吸收得到含碘离子和碘酸根离子的溶
液,稀硫酸酸化得到含单质碘的悬浊液,最终得到碘;
Ⅱ.由流程可知,海水结晶、过滤分离出粗盐、母液,母液加入石灰乳沉淀镁离子生成氢氧化镁沉
淀,过滤后加入盐酸生成氯化镁溶液,浓缩结晶得到氯化镁晶体,氯化氢气流中失水得到氯化镁,
电解熔融氯化镁得到镁和氯气。贝壳煅烧得到氧化钙,氧化钙和水分与生成氢氧化钙,氢氧化钙加
入母液沉淀镁离子,以此解答该题。
【详解】(1)固体灼烧需要坩埚,实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃
棒、坩埚、坩埚钳等,故答案为:坩埚;
化学试题 第 14页(共 18页)
学科网(北京)股份有限公司(2)步骤①中选择HO 氧化I-,不用Cl 的原因是:氯气有毒,易污染环境,过氧化氢做氧化剂被
2 2 2
还原为水,无污染,故答案为:HO 无毒无污染,还原产物为HO,不会引入新的杂质;
2 2 2
(3)步骤④中碘酸根氧化碘离子,发生反应的离子方程式为6H++IO +5I-=3I+3H O,在此反应中,
2 2
每生成3mol碘,转移5mol电子,38.1gI 的物质的量是38.1g÷254g/mol=0.15mol,则转移电子的物
2
质的量是0.15mol×5/3=0.25mol,数目为0.25N ,故答案为:6H++IO +5I-=3I+3H O;0.25N ;
A 2 2 A
(4)由于海水中碘的含量较低,则含I 的水溶液经3步转化为含I 的悬浊液,主要目的是富集碘
2 2
元素,故答案为:富集碘元素;
(5)往母液中加成本较低的石灰乳Ca(OH) ,发生反应的离子方程式为:
2
Mg2++Ca(OH) =Mg(OH) +Ca2+,故答案为:Mg2++Ca(OH) =Mg(OH) +Ca2+;
2 2 2 2
(6)由MgCl 溶液得到MgCl •6H O晶体的操作是:蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到
2 2 2
晶体,故答案为:蒸发浓缩、冷却结晶;
(7)Br + SO + 2H O ==2HBr + H SO
2 2 2 2 4
(8)无水MgCl 在熔融状态下,通电后会产生Mg和Cl,故答案为: 。
2 2
17.(1) 2.8 60% 1
(2) -80KJ/mol
(3) 192
(4) (0.4N )
A
18.(1) 羟基、醛基 (2分) (1分)
(2)56(2分)
(3) (2分)
(4)取少量样品于试管中,加入少量碳酸氢钠溶液,产生气泡,证明 中混有 ;
(2分)
(5)4(2分)
化学试题 第 15页(共 18页)
学科网(北京)股份有限公司(6)bc(2分)
(7) 碘水(1分) 加入碘水,溶液不变蓝色(1分)
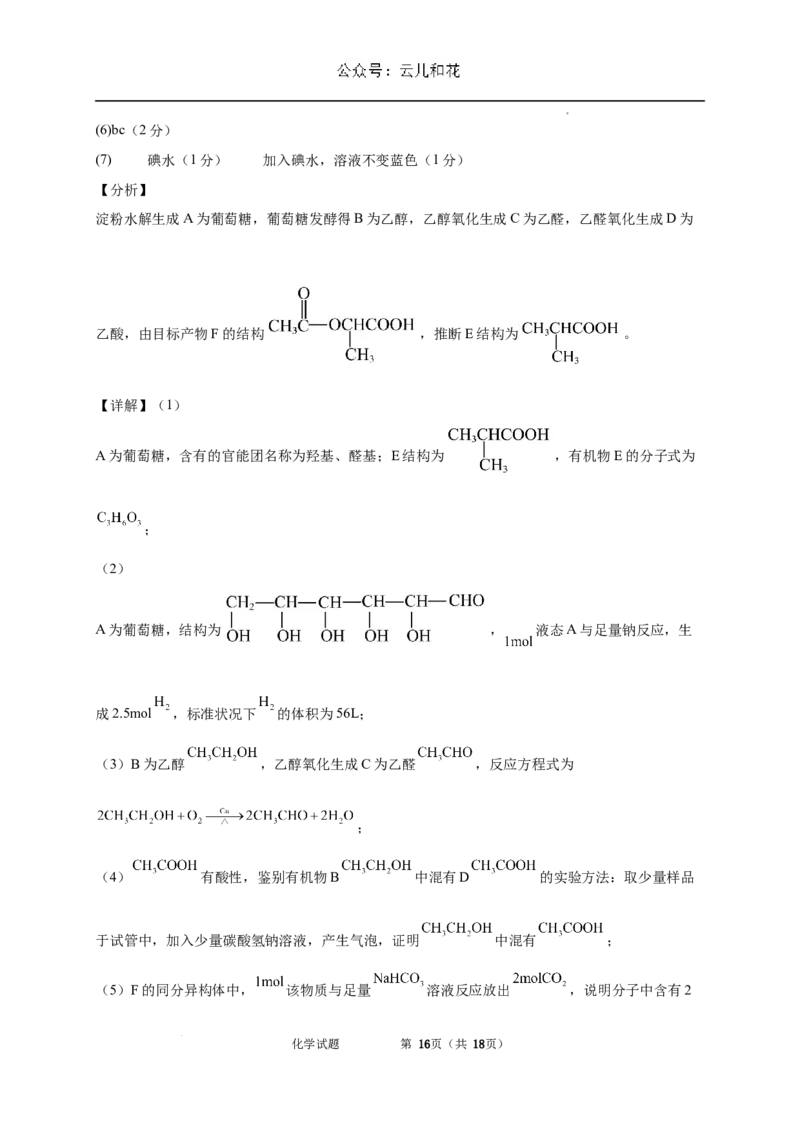
【分析】
淀粉水解生成A为葡萄糖,葡萄糖发酵得B为乙醇,乙醇氧化生成C为乙醛,乙醛氧化生成D为
乙酸,由目标产物F的结构 ,推断E结构为 。
【详解】(1)
A为葡萄糖,含有的官能团名称为羟基、醛基;E结构为 ,有机物E的分子式为
;
(2)
A为葡萄糖,结构为 , 液态A与足量钠反应,生
成2.5mol ,标准状况下 的体积为56L;
(3)B为乙醇 ,乙醇氧化生成C为乙醛 ,反应方程式为
;
(4) 有酸性,鉴别有机物B 中混有D 的实验方法:取少量样品
于试管中,加入少量碳酸氢钠溶液,产生气泡,证明 中混有 ;
(5)F的同分异构体中, 该物质与足量 溶液反应放出 ,说明分子中含有2
化学试题 第 16页(共 18页)
学科网(北京)股份有限公司个羧基,是丙烷上有2个氢原子被羧基取代,两个羧基连在同一个碳原子上,有两种结构,两个羧
基连在不同碳原子上,有两种结构,故符合要求的同分异构体共有4种;
(6)a.反应Ⅱ是酯化反应,属于取代反应,a正确;
b.E中含有羟基和羧基,等物质的量的E分别与足量的 和 反应,消耗的 和 的
物质的量之比为2:1,b错误
c.D、E中的官能团种类不完全相同,不是同系物,c错误;
故选a;
(7)淀粉已经水解完全,说明水解液中不存在淀粉,用碘水检验水解液,溶液不变蓝色,说明淀
粉不存在,判断淀粉已经水解完全;完全水解的实验现象为加入碘水,溶液不变蓝色。
19、【答案】(1)分液漏斗
(2) 除去甲烷中的水蒸气 验证甲烷还原 的产物中含有水
(3) a b
(4)E装置中澄清石灰水变浑浊、F装置中产生黑色沉淀
(5)
(6) 稀硫酸(或稀盐酸) 溶液未变蓝
【分析】A装置发生反应生成CH,B中碱石灰用于干燥CH,C中CH 与 生成 和非金属氧
4 4 4
化物,D用于检验水分,E用于检验CO,F用于检验CO,G进行尾气收集;
2
【详解】(1)盛放 溶液的仪器名称为分液漏斗;
(2)装置 的作用为除去甲烷中的水蒸气;装置 的作用为验证甲烷还原 的产物中含有水;
(3)为避免 在不纯时点燃引发危险,连接好装置后,应先打开分液漏斗的活塞,后点燃酒精
灯;
(4)确认气体产物中有 和 的现象分别为 装置中澄清石灰水变浑浊、 装置中产生黑色沉
淀;
(5)装置A中Al C 与NaOH溶液反应生成CH 和Na ,发生反应的化学方程式为
4 3 4
;
化学试题 第 17页(共 18页)
学科网(北京)股份有限公司(6)根据题意, (红) ,要证明固体产物中没有 的方法是:取少
许固体产物,加入适量稀硫酸(或稀盐酸),观察到溶液未变蓝,证明固体产物中没有 。
化学试题 第 18页(共 18页)
学科网(北京)股份有限公司