文档内容
2.3.1 物质的量 练习(原卷版)
1.对1 mol/L的NaSO 溶液的叙述中正确的是( )
2 4
A.溶液中含有1 mol NaSO
2 4
B.1 L溶液中含有142 g NaSO
2 4
C.1 mol NaSO 溶于1 L水
2 4
D.从1 L该溶液中取出500 mL以后,剩余溶液的浓度为0.5 mol/L
2.下列溶液中氯离子浓度与50 mL 1 mol/L AlCl 溶液中Cl-浓度相等的是( )
3
A.150 mL 1 mol/L的NaCl溶液
B.75 mL 2 mol/L的NHCl溶液
4
C.150 mL 3 mol/L的KCl溶液
D.75 mL 2 mol/L的FeCl 溶液
3
3.实验室中需要配制2 mol/L的NaOH溶液950 mL,配制时应选用的容量瓶的规格和称取的
NaOH的质量分别是( )
A.950 mL,76.0 g B.500 mL,80.0 g
C.1 000 mL,80.0 g D.1 000 mL,76.0 g
4.在100 mL的溶液中溶有0.1 mol NaCl和0.1 mol MgCl ,此溶液中Cl-的物质的量浓度为(
2
)
A.3 mol/L B.2 mol/L
C.0.3 mol/L D.0.2 mol/L
5.50 mL物质的量浓度为4.4 mol/L,密度为1.24 g/mL的稀硫酸的质量分数为( )
A.35% B.70%
C.17.5% D.0.035%
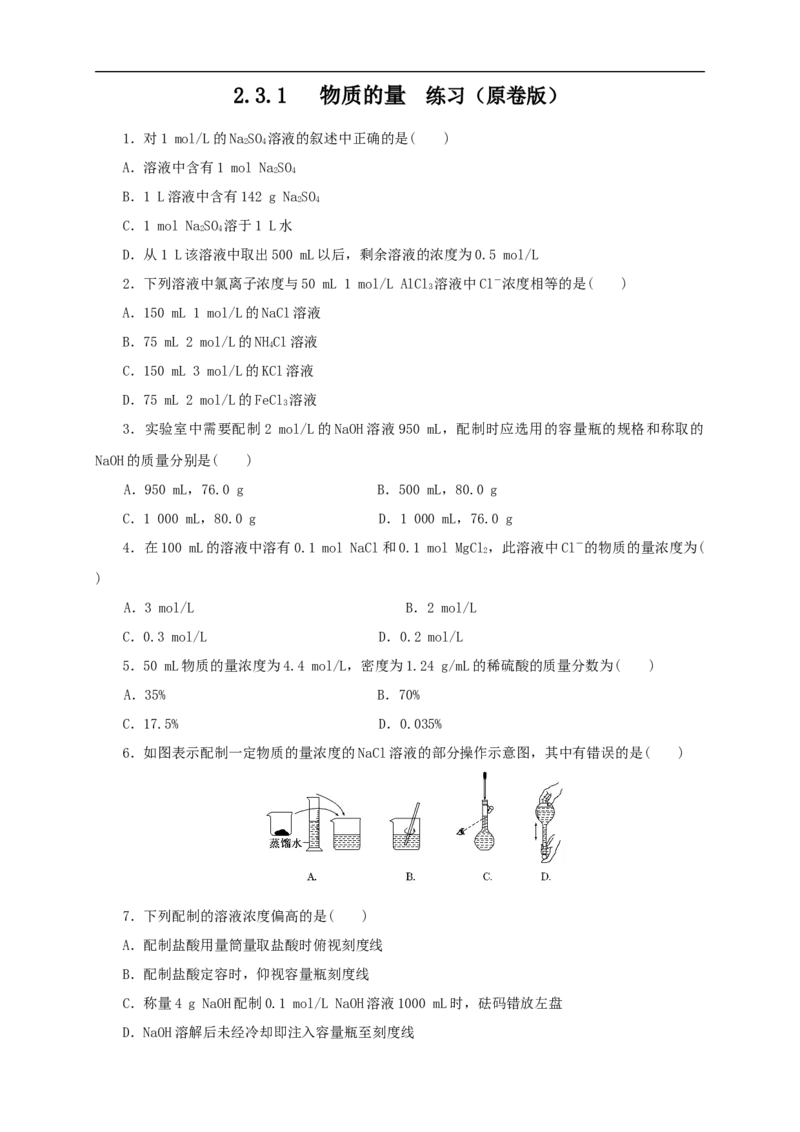
6.如图表示配制一定物质的量浓度的NaCl溶液的部分操作示意图,其中有错误的是( )
7.下列配制的溶液浓度偏高的是( )
A.配制盐酸用量筒量取盐酸时俯视刻度线
B.配制盐酸定容时,仰视容量瓶刻度线
C.称量4 g NaOH配制0.1 mol/L NaOH溶液1000 mL时,砝码错放左盘
D.NaOH溶解后未经冷却即注入容量瓶至刻度线8.下列叙述正确的是( )
A.1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol·L-1
B.从1 L 2 mol·L-1的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol·L-1
C.将2.24 L(标准状况)HCl气体溶于水制成100 mL溶液,其物质的量浓度为1 mol·L-1
D.配制1 L 0.2 mol·L-1的CuSO 溶液,需用25 g胆矾
4
9.有体积相同的两份营养液,其配方如下:
KCl KSO ZnSO ZnCl
2 4 4 2
第一份 0.3mol 0.2mol 0.1mol ﹣﹣
第二份 0.1mol 0.3mol ﹣﹣ 0.1mol
两份营养液中各离子浓度( )
A.完全不同 B.完全相同
C.仅c(K+)相同 D.仅c(Cl﹣)相同
10.某植物营养液含有0.2molK+、0.25molZn2+、0.4molCl﹣、SO2﹣,则SO2﹣的物质的量为(
4 4
)
A.0.1mol B.0.15mol C.0.3mol D.0.5mol
11.实验室配制500 mL 0.2 mol/L的NaSO 溶液,实验操作步骤有:
2 4
A.在天平上称出14.2 g硫酸钠固体,把它放在烧杯中,用适量蒸馏水使它完全溶解并冷却至
室温;
B.把制得的溶液小心转移至容量瓶中;
C.继续向容量瓶中加蒸馏水至液面距刻度线 1~2 cm处,改用胶头滴管小心滴加蒸馏水至凹
液面与刻度线相切;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶,并轻轻振荡;
E.将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为________(填序号)。
(2)本实验用到的基本仪器已有烧杯、天平(带砝码)、镊子、玻璃棒,还缺少的仪器是_______、
_______、________。
(3)下列情况会使所配溶液浓度偏高的是__________(填序号)。
a.某同学观察液面的情况如图所示
b.没有进行上述操作步骤D
c.加蒸馏水时,不慎超过了刻度线
d.砝码上沾有杂质
e.容量瓶使用前内壁沾有水珠12.某化学课外活动小组从实验室取出硫酸试剂,试剂瓶上标签的部分内容如图所示。该小组
欲使用450 mL 0.2 mol·L-1的稀硫酸溶液。配制该浓度的硫酸溶液时:
(1)所需试剂瓶内硫酸溶液的体积为________mL。
(2)所用量筒和容量瓶的规格为________和________。
(3)浓硫酸稀释时的操作是__________________________________________________
(4)下列为该小组的操作,可能导致配制溶液浓度偏高的是________。
A.移液前未冷却至室温
B.定容时加水多了,用滴管吸出
C.定容时俯视刻度线
(5)下图是该小组转移溶液的示意图,图中的错误是
__________________________________________________________________
13.(1)相同物质的量的O 和CO分子个数比为________,所含氧原子的个数比为________,常
2
温常压下的体积比:________。
(2)实验室要用NaCO 配制500 mL 0.1 mol·L-1 NaCO 溶液,回答下列问题:
2 3 2 3
①应该用托盘天平称取NaCO________g。
2 3
②需要的仪器:________,________,________,________,________。
③若实验中有下列情况,对配制溶液的浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.转移液体时部分溅出________;
B.定容时加水超过刻度线________;
C.最终定容时俯视观察液面________。