文档内容
名校联考联合体 2024 年秋季高一第一次联考
化学
时量:60分钟 满分:100分
第Ⅰ卷(选择题)
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.化学与社会、生活和生产息息相关。以下叙述错误的是( )
A.“用浓酒和糟入甑(蒸锅),蒸气令上……”。其中涉及的操作是蒸馏
B.“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及氧化还原反应
C.“以曾青涂铁,铁赤色如铜”,“曾青”是可溶性铁盐
D.“青蒿一握,以水二升渍,绞取之”,其中对青蒿素的提取属于物理变化
2.实现下列物质间的转化,一定需要加入氧化剂的是( )
A. B. C. D.
3.在无色透明的酸性溶液中,能大量共存的是( )
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
4.图a~c分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源正极相连,Y与电源
负极相连)微观示意图。下列说法正确的是( )
A.图a表示熔融氯化钠的导电实验图
B.通过图b可知,氯化钠在通电条件下才能发生电离
C.图b中向右定向移动的是钠离子
D.图b和图c说明NaCl固体受热熔化和溶于水时,均发生了电离,产生了完全相同的离子
5.下列属于氧化还原反应的是( )
A. B.
C. D.
6.某同学在实验室中进行如下实验:
编号 Ⅰ Ⅱ Ⅲ实验
现象 没有明显变化,溶液仍为无色 有白色沉淀生成,溶液为蓝色 有无色气体放出
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应
B.Ⅱ中的白色沉淀为
C.Ⅲ中的离子方程式为
D.Ⅲ中发生的反应不是离子反应
7.胶体是一种重要的分散系,下列有关叙述正确的是( )
A.明矾可用作净水剂与胶体的性质有关
B.丁达尔效应是胶体粒子对光线折射形成的,是一种物理现象
C.静电除尘,利用了胶体带电的性质
D.可用滤纸除去淀粉溶液中混有的氯化钠
8.下列物质间的转化不能通过化学反应一步实现的是( )
A. B.
C. D.
9.下列说法正确的有( )
①酸性氧化物在一定条件下均能与碱发生反应
②离子方程式 可以表示所有强酸和强碱之间的中和反应
③溶于水后能电离出氢离子的化合物一定是酸
④某物质经分析只含有一种元素,则该物质一定是纯净物
⑤两种化合物生成另外两种化合物的反应一定是复分解反应
⑥某元素由化合态变为游离态,则它可能被还原也可能被氧化
⑦酸性氧化物不一定都是非金属氧化物,但碱性氧化物一定都是金属氧化物
A.3个 B.4个 C.5个 D.6个
10.下列离子方程式正确的是( )
A.硝酸银溶液与铜反应:
B.碳酸钙溶于醋酸:C.将 溶液和NaOH溶液混合:
D.硫酸铜溶液与氢氧化钡溶液反应:
11.航天科学技术测得三氧化二碳( )是金星大气层的成分之一,下列有关 的说法不正确的是
( )
A. 和 都属于非金属氧化物 B. 和CO的完全燃烧产物都是
C. 和CO都是酸性氧化物 D. 中C的化合价为+3
12.下列各组中两个溶液间的反应,均可用同一离子方程式表示的是( )
A.NaOH和 与 和
B.HCl和 与HCl和
C. 和 与 和
D. 和 与 和
13.科学家利用太阳光在新型催化剂Ⅰ表面高效分解水后,再利用高效催化剂Ⅱ将二氧化碳转化为乙烯,
其反应的微观示意图如下。下列说法正确的是( )
A.反应Ⅰ中,反应前后分子总数保持不变
B.反应Ⅱ为置换反应
C.整个反应过程中涉及到3种氧化物
D.反应Ⅱ的化学方程式为
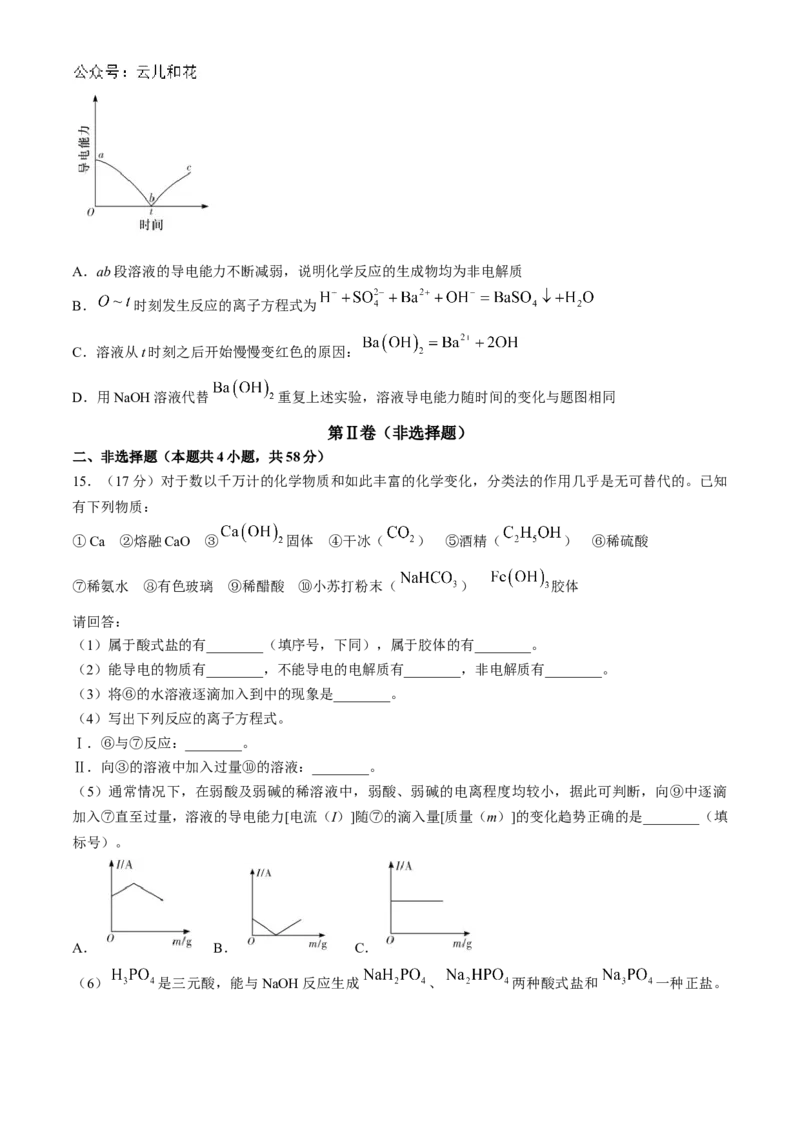
14.向稀硫酸中滴入几滴酚酞溶液,然后匀速逐滴加入 溶液,测得混合溶液的导电能力随时间
变化的曲线如图。下列说法正确的是( )A.ab段溶液的导电能力不断减弱,说明化学反应的生成物均为非电解质
B. 时刻发生反应的离子方程式为
C.溶液从t时刻之后开始慢慢变红色的原因:
D.用NaOH溶液代替 重复上述实验,溶液导电能力随时间的变化与题图相同
第Ⅱ卷(非选择题)
二、非选择题(本题共4小题,共58分)
15.(17分)对于数以千万计的化学物质和如此丰富的化学变化,分类法的作用几乎是无可替代的。已知
有下列物质:
①Ca ②熔融CaO ③ 固体 ④干冰( ) ⑤酒精( ) ⑥稀硫酸
⑦稀氨水 ⑧有色玻璃 ⑨稀醋酸 ⑩小苏打粉末( ) 胶体
请回答:
(1)属于酸式盐的有________(填序号,下同),属于胶体的有________。
(2)能导电的物质有________,不能导电的电解质有________,非电解质有________。
(3)将⑥的水溶液逐滴加入到中的现象是________。
(4)写出下列反应的离子方程式。
Ⅰ.⑥与⑦反应:________。
Ⅱ.向③的溶液中加入过量⑩的溶液:________。
(5)通常情况下,在弱酸及弱碱的稀溶液中,弱酸、弱碱的电离程度均较小,据此可判断,向⑨中逐滴
加入⑦直至过量,溶液的导电能力[电流(I)]随⑦的滴入量[质量(m)]的变化趋势正确的是________(填
标号)。
A. B. C.
(6) 是三元酸,能与NaOH反应生成 、 两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸( ),是二元弱酸,那么 为________(填“正盐”或“酸式
盐”)。
16.(15分)宏观辨识与微观探析是化学学科重要的学科素养。回答下列问题:
Ⅰ.已知某无色水样中只含有 、 、 、 、 、 、 、 、 中的若干
种。某化学研究性学习小组对该水样的成分进行检验:
①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
该水样中一定存在的离子是________(填离子符号,下同),可能存在的离子是________,一定不存在的
离子是________。
Ⅱ.现有三种可溶性物质A、B、C,其中有一种是碱,两种是盐,溶于水后电离产生的离子如下表所示:
阳离子
阴离子
为鉴别它们,分别完成一些实验。请根据实验的结果回答下列问题:
(1)A溶液与B溶液反应可生成气体X。根据上述六种离子之间的可能反应判断X的化学式为________,
A溶液与B溶液反应的离子方程式为________,。
(2)气体X可以和C溶液反应生成沉淀D,沉淀D可与B溶液反应。则C的化学式为________,B溶于
水后的电离方程式为________。D与足量B反应的离子方程式为________。
17.(14分)近年来,人类生产、生活所产生的污染,如机动车、燃煤、工业等排放的废气,使灰霾天气
逐渐增多。灰霾粒子比较小,平均直径大约在1000~2000nm左右。
(1)下列有关说法正确的是________(填标号)。
A.灰霾是一种分散系B.灰霾能产生丁达尔效应
C.灰霾形成的是稳定的体系 D.戴口罩不能阻止吸入灰霾粒子
(2)雾是由大量悬浮在近地面空气中的微小水滴或冰晶组成的气溶胶系统,是近地面层空气中水汽凝结
(或凝华)的产物。霾也称灰霾,空气中的灰尘(如煤炭及三氧化二铁粉尘)、一氧化氮、二氧化碳、二
氧化氮、二氧化硫、硫酸、有机碳氢化合物等粒子使大气浑浊,造成视野模糊并导致能见度较低,形成灰
霾的主要物质中能发生若干反应,其中金属氧化物与硫酸反应的化学方程式为________,足量碳氧化物与
少量氢氧化钠溶液反应的离子方程式为________。
(3)雾是气溶胶,氢氧化铁胶体是液溶胶,写出实验室制备氢氧化铁胶体的化学方程式:________,提
纯胶体的方法是________。
(4)现有甲、乙、丙三名同学分别进行硅酸胶体的制备实验:
分组 实验操作 实验现象
甲 将1%硅酸钠溶液滴入沸水中,冷却后用激光笔 无明显现象,未出现“光亮的通路”
进行照射
乙 向1%硅酸钠溶液中加入几滴酚酞溶液,缓慢滴 出现“光亮的通路”
入稀盐酸,溶液红色褪去后停止滴加,用激光笔进行照射
丙 向1%硅酸钠溶液中加入等体积的稀盐酸,用激 未出现“光亮的通路”,溶液中出现浑
光笔进行照射 浊
已知:硅酸钠( )溶液呈碱性,遇酚酞变红;常温下硅酸( )难溶于水。试回答:成功
制备硅酸胶体的是________同学,根据三位同学的实验操作可知,成功制备硅酸胶体的关键在于________,
丙同学实验中出现浑浊的原因是________。
18.(12分) 、 、 、NaClO等都是重要的氧化剂,其中 、 、NaClO还是
常见的水处理剂,这些物质之间存在如图所示的转化关系。
回答下列问题:
(1)已知电解质在水溶液里或熔融状态时通电会发生氧化还原反应,其中阳极发生失电子的反应,阴极
发生得电子的反应,则反应②中单质Na在________(填“阴”或“阳”)极产生。
(2)反应④体现了金属Na的________性(填“氧化”或“还原”)。
(3)反应⑤在碱性条件下进行,生成物 中Fe元素的化合价为________。
(4)反应⑥的化学方程式为 ,该反应
的氧化剂为________(填化学式,下同),氧化产物为________。
(5)反应⑦是在饱和 溶液中加入KOH,可得 沉淀,该反应的反应类型是________(填
四大基本反应类型)。
名校联考联合体 2024 年秋季高一第一次联考
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意)
题 1 2 3 4 5 6 7 8 9 10 11 12 13 14
号
答 C A D C D C A C A C C C D C
案
2.A 【解析】 中铁元素化合价升高,Fe作还原剂,一定需要加入氧化剂才能实现转化,A项符合题意; 加入催化剂 即可,不一定需要加入氧化剂,B 项不符合题意:
中碳元素化合价降低,应加入还原剂,C项不符合题意; 中铜元素化合价降低,
应加入还原剂,D项不符合题意。
4.C 【解析】根据离子移动方向知,是钠离子和氯离子发生定向移动而导电,故图 b可以表示熔融状态
下氯化钠的导电过程,图a中阴阳离子不可自由移动,为固态NaCl,A错误;氯化钠在水溶液里或熔融状
态下都可以电离出自由移动的离子,电离不需要通电,B错误;根据X与电源正极相连,Y与电源负极相
连,所以图b中向右定向移动的是钠离子,C正确;图b表示在熔融状态下,存在自由移动的 、 ,
图c中离子以水合离子的形式存在,即水合钠离子和水合氯离子,产生了不同的离子,D错误。
5.D 【解析】 反应前后无元素化合价变化,不是氧化还原反应,A不
符合; 反应前后无元素化合价变化,不是氧化还原反应,B不符
合; 反应前后无元素化合价变化,不是氧化还原反应,C 不符合;
中O的化合价在反应前后发生了变化,该反应属于氧化还原反应,D
符合。
6.C 【解析】氢氧化钠和硫酸反应生成硫酸钠和水,但是没有明显现象,A错误;氯化钡和硫酸铜反应
生成白色的硫酸钡沉淀和氯化铜,B 错误;稀盐酸和锌反应生成氯化锌和氢气,其离子方程式为
,C正确;Ⅲ中锌和稀盐酸的反应有离子参与,属于离子反应,D错误。
11.C 【解析】 和 都是碳的氧化物,属于非金属氧化物,故A正确;根据元素守恒, 和
CO在氧气中完全燃烧,生成的产物都是 ,故B正确;CO不能与酸反应,也不能与碱反应,是不成
盐氧化物,故C错误: 中O元素化合价为-2价,则碳元素化合价为+3价,故D正确。
12.C 【解析】氢氧化钠与稀硫酸反应的离子方程式为 ;而氢氧化钡与硫酸反应的离
子方程式为 ,不能用同一离子方程式表示,故A错误;
碳酸钠与盐酸反应的离子方程式为 ;碳酸钙与盐酸反应的离子方程式为
, 故 B 错 误 ; 氯 化 钡 与 硫 酸 钠 反 应 的 离 子 方 程 式 为;氢氧化钡与硫酸钠反应的离子方程式也为 ,能用同一
离 子 方 程 式 表 示 , 故 C 正 确 ; 醋 酸 与 碳 酸 钠 反 应 的 离 子 方 程 式 为
; 碳 酸 钠 与 稀 硫 酸 反 应 的 离 子 方 程 式 为
,故D错误。
13.D 【解析】反应Ⅰ是水在太阳光和催化剂的作用下分解生成氢气和氧气,反应的化学方程式为
,反应前后分子总数改变,故A错误;反应Ⅱ是二氧化碳和氢气在催化剂
的作用下生成 和水,反应的化学方程式为 ,生成物有两种化合
物,不属于置换反应,故B错误;整个反应过程中涉及到二氧化碳和水 2种氧化物,故C错误;反应Ⅱ是
二 氧 化 碳 和 氢 气 在 催 化 剂 的 作 用 下 生 成 和 水 , 反 应 的 化 学 方 程 式 为
,故D正确。
14 . C 【 解 析 】 ab 段 溶 液 的 导 电 能 力 不 断 减 弱 , 是 由 于 发 生 反 应 :
,反应产生的 是难溶性强电解质,主要以固体存在,
是弱电解质,导致溶液中自由移动的离子浓度减小,溶液导电能力减弱,A错误; 时刻,反应
的离子方程式为 ,B错误;溶液从t时刻之后开始慢慢变
红色的原因:由于 是二元强碱,在水中电离产生 ,使溶液显碱性,电离方程式为
,C正确;若用NaOH溶液代替 重复上述实验,NaOH与 发
生中和反应产生可溶性盐 和 ,溶液中始终存在大量自由移动的离子,因此溶液导电能力几
乎不变,因此不会发生上述变化,D错误。
二、非选择题(本题共4小题,除标注外,每空2分,共58分)
15.(17分)(1)⑩(1分) ⑧(1分,漏选且无错选给0。5分,错选不给分)
(2)①②⑥⑦⑨(2分,漏选但选对3个及以上且无错选给1分,错选或虽无错选但所选少于3个的不给
分)③⑩(2分,漏选且无错选给1分,错选不给分)④⑤(1分,漏选且无错选给0.5分,错选不给分)(3)先生成红褐色沉淀,随着硫酸的不断加入,沉淀溶解,溶液变黄色
(4)Ⅰ. Ⅱ.
(5)A (6)正盐
16.(15分)Ⅰ. 、 、 、 、 、 、
Ⅱ.(1) (1分)
(2)
17.(14分)(1)A(1分)
(2)
(3) 渗析
(4)乙(1分) 稀盐酸的加入量过量的盐酸导致胶体发生聚沉
18.(12分)(1)阴 (2)还原 (3)+6
(4) 、 (5)复分解反应