文档内容
2024 届高三模拟考试
化学试题
2024.03
注意事项:
1.答题前,考生务必将自己的姓名、考生号、座号填写在相应位置,认真核对条形码上的姓
名、考生号和座号,并将条形码粘贴在指定位置上。
2.选择题答案必须使用 2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用 0.5毫米
黑色签字笔书写,字体工整、笔迹清楚。
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效:在草稿纸、试题
卷上答题无效,保持卡面清洁,不折叠、不破损。
可能用到的相对原子质量:H1 Li7 N14 O16 Na23 S32 Cr52 Mn55 Fe56 Cu65 Ba137
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.齐鲁文化源远流长,馆藏文物见证历史。下列文物制作过程涉及化学变化的是( )
A.北辛石器 B.红陶兽形壶 C.鲁国大玉壁 D.银雀山竹木简牍
2.下列物质的构成微粒间相互作用与其它三者不同的是( )
A.干冰 B.水晶 C.汽油 D.液氯
3.下列应用与氧化还原反应无关的是( )
A.稀硝酸用于溶解铜锈 B.铁粉暖贴用于冬天取暖
C.青蒿素氢化制备双氢青蒿素 D.三元催化器处理机动车尾气
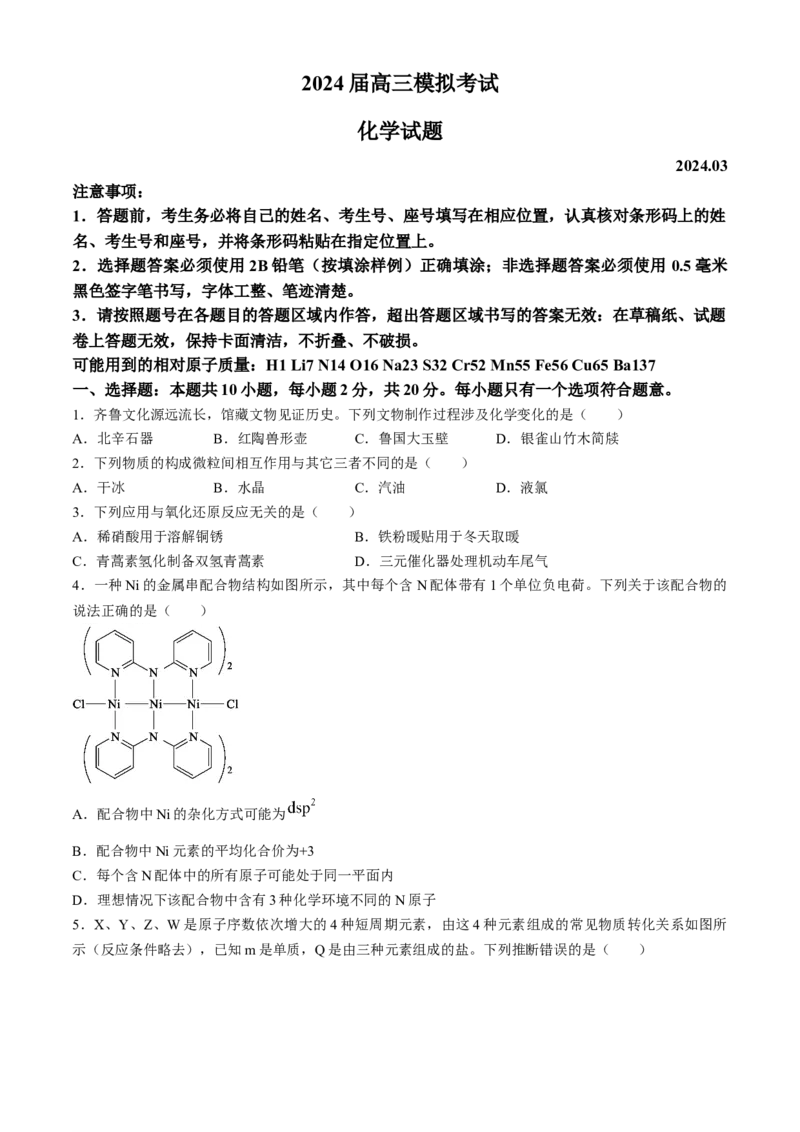
4.一种Ni的金属串配合物结构如图所示,其中每个含N配体带有1个单位负电荷。下列关于该配合物的
说法正确的是( )
A.配合物中Ni的杂化方式可能为
B.配合物中Ni元素的平均化合价为+3
C.每个含N配体中的所有原子可能处于同一平面内
D.理想情况下该配合物中含有3种化学环境不同的N原子
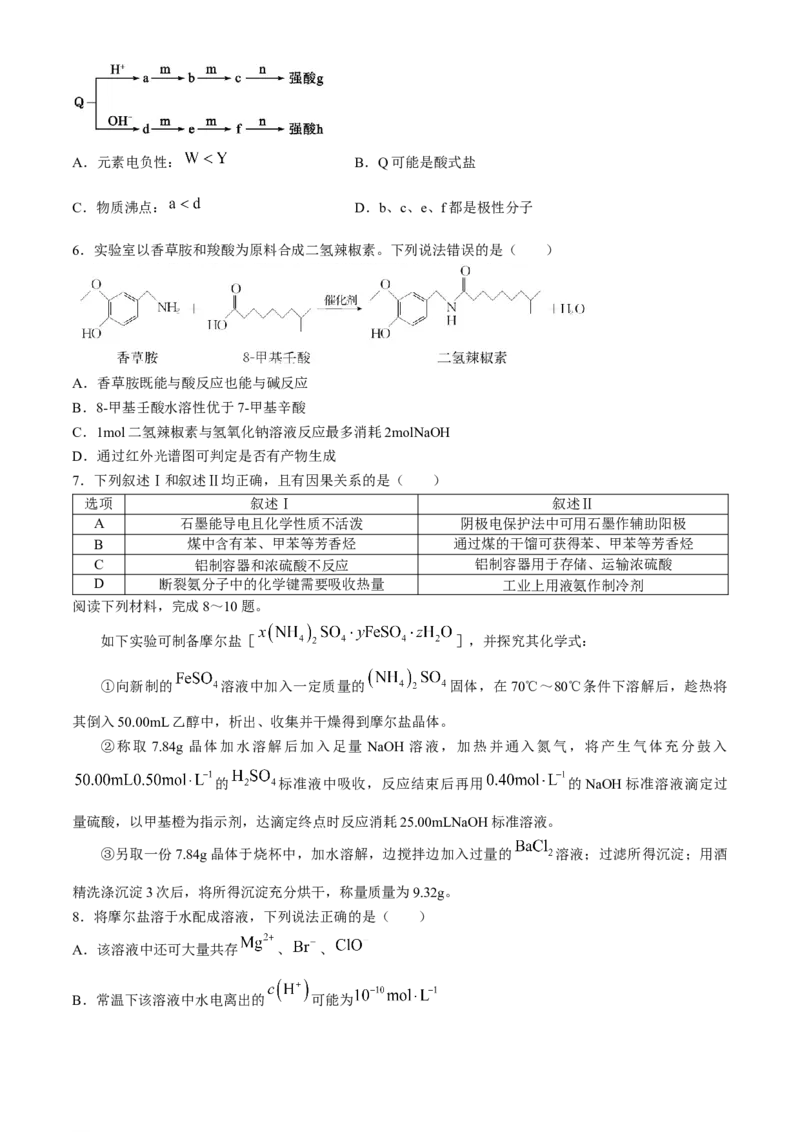
5.X、Y、Z、W是原子序数依次增大的4种短周期元素,由这4种元素组成的常见物质转化关系如图所
示(反应条件略去),已知m是单质,Q是由三种元素组成的盐。下列推断错误的是( )
学科网(北京)股份有限公司A.元素电负性: B.Q可能是酸式盐
C.物质沸点: D.b、c、e、f都是极性分子
6.实验室以香草胺和羧酸为原料合成二氢辣椒素。下列说法错误的是( )
A.香草胺既能与酸反应也能与碱反应
B.8-甲基壬酸水溶性优于7-甲基辛酸
C.1mol二氢辣椒素与氢氧化钠溶液反应最多消耗2molNaOH
D.通过红外光谱图可判定是否有产物生成
7.下列叙述Ⅰ和叙述Ⅱ均正确,且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A 石墨能导电且化学性质不活泼 阴极电保护法中可用石墨作辅助阳极
B 煤中含有苯、甲苯等芳香烃 通过煤的干馏可获得苯、甲苯等芳香烃
C 铝制容器和浓硫酸不反应 铝制容器用于存储、运输浓硫酸
D 断裂氨分子中的化学键需要吸收热量 工业上用液氨作制冷剂
阅读下列材料,完成8~10题。
如下实验可制备摩尔盐[ ],并探究其化学式:
①向新制的 溶液中加入一定质量的 固体,在70℃~80℃条件下溶解后,趁热将
其倒入50.00mL乙醇中,析出、收集并干燥得到摩尔盐晶体。
②称取 7.84g 晶体加水溶解后加入足量 NaOH 溶液,加热并通入氮气,将产生气体充分鼓入
的 标准液中吸收,反应结束后再用 的NaOH标准溶液滴定过
量硫酸,以甲基橙为指示剂,达滴定终点时反应消耗25.00mLNaOH标准溶液。
③另取一份7.84g晶体于烧杯中,加水溶解,边搅拌边加入过量的 溶液;过滤所得沉淀;用酒
精洗涤沉淀3次后,将所得沉淀充分烘干,称量质量为9.32g。
8.将摩尔盐溶于水配成溶液,下列说法正确的是( )
A.该溶液中还可大量共存 、 、
B.常温下该溶液中水电离出的 可能为
学科网(北京)股份有限公司C.加入少量 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含
D.向溶液中滴入 溶液使 恰好沉淀时, 和 都会参与反应
9.关于上述实验,下列说法正确的是( )
A.抑制溶液中 水解,可加入少量硝酸 B.吸收逸出的氨气,可改用浓盐酸标准液
C.用稀硫酸洗涤沉淀,可以使结果更准确 D.为确定所得沉淀质量,至少要称量两次
10.根据实验数据,下列分析错误的是( )
A. B.改用酚酞做指示剂会使 值偏低
C.如沉淀未充分干燥会使 值偏低 D.制备时因氧化混入硫酸铁会使 值偏低
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
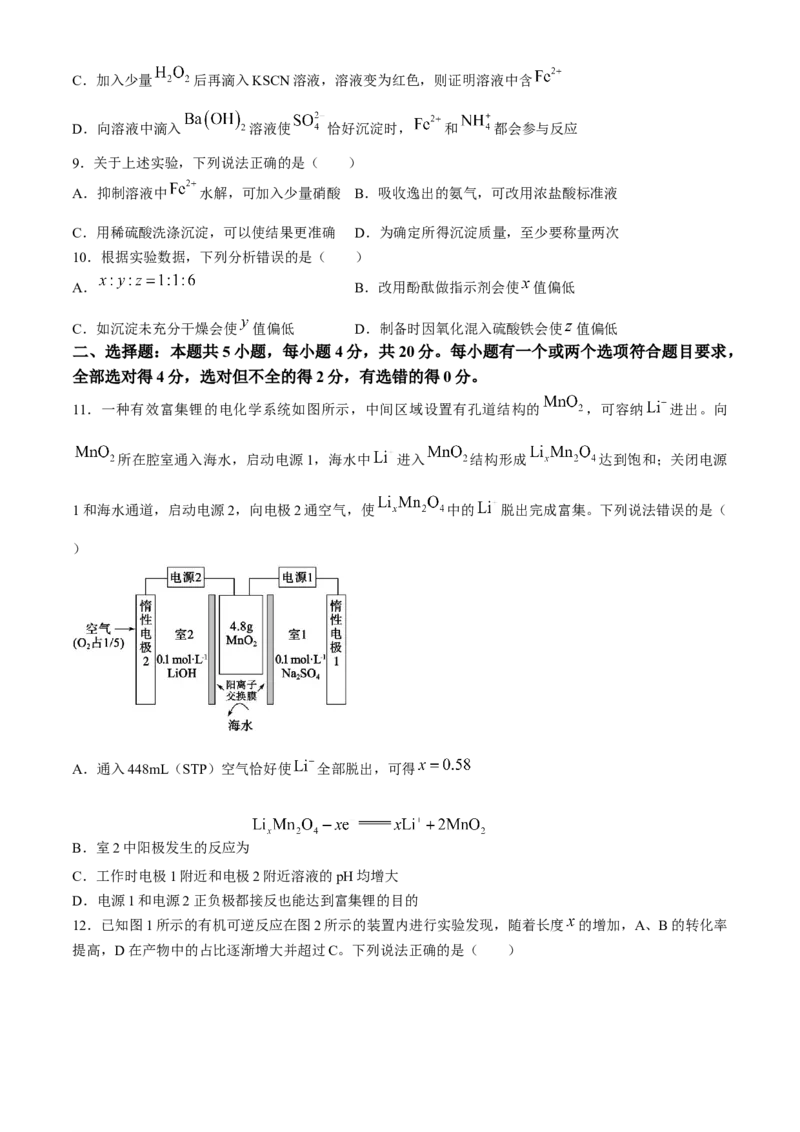
11.一种有效富集锂的电化学系统如图所示,中间区域设置有孔道结构的 ,可容纳 进出。向
所在腔室通入海水,启动电源1,海水中 进入 结构形成 达到饱和;关闭电源
1和海水通道,启动电源2,向电极2通空气,使 中的 脱出完成富集。下列说法错误的是(
)
A.通入448mL(STP)空气恰好使 全部脱出,可得
B.室2中阳极发生的反应为
C.工作时电极1附近和电极2附近溶液的pH均增大
D.电源1和电源2正负极都接反也能达到富集锂的目的
12.已知图1所示的有机可逆反应在图2所示的装置内进行实验发现,随着长度 的增加,A、B的转化率
提高,D在产物中的占比逐渐增大并超过C。下列说法正确的是( )
学科网(北京)股份有限公司图1 图2
A.升高温度两个反应的平衡常数均减小 B.反应1的活化能小于反应2的活化能
C.装置中长度 越小C的产率越高 D.物质C和D等比加聚可得到三种产物
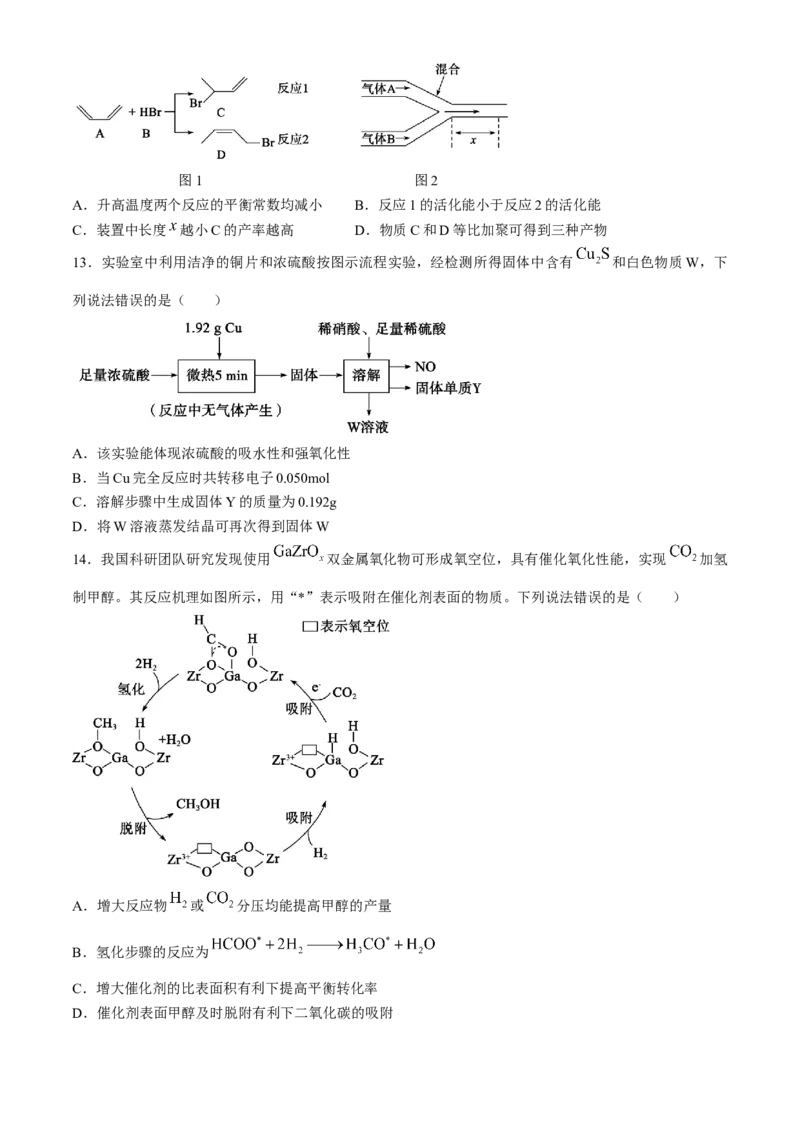
13.实验室中利用洁净的铜片和浓硫酸按图示流程实验,经检测所得固体中含有 和白色物质W,下
列说法错误的是( )
A.该实验能体现浓硫酸的吸水性和强氧化性
B.当Cu完全反应时共转移电子0.050mol
C.溶解步骤中生成固体Y的质量为0.192g
D.将W溶液蒸发结晶可再次得到固体W
14.我国科研团队研究发现使用 双金属氧化物可形成氧空位,具有催化氧化性能,实现 加氢
制甲醇。其反应机理如图所示,用“*”表示吸附在催化剂表面的物质。下列说法错误的是( )
A.增大反应物 或 分压均能提高甲醇的产量
B.氢化步骤的反应为
C.增大催化剂的比表面积有利下提高平衡转化率
D.催化剂表面甲醇及时脱附有利下二氧化碳的吸附
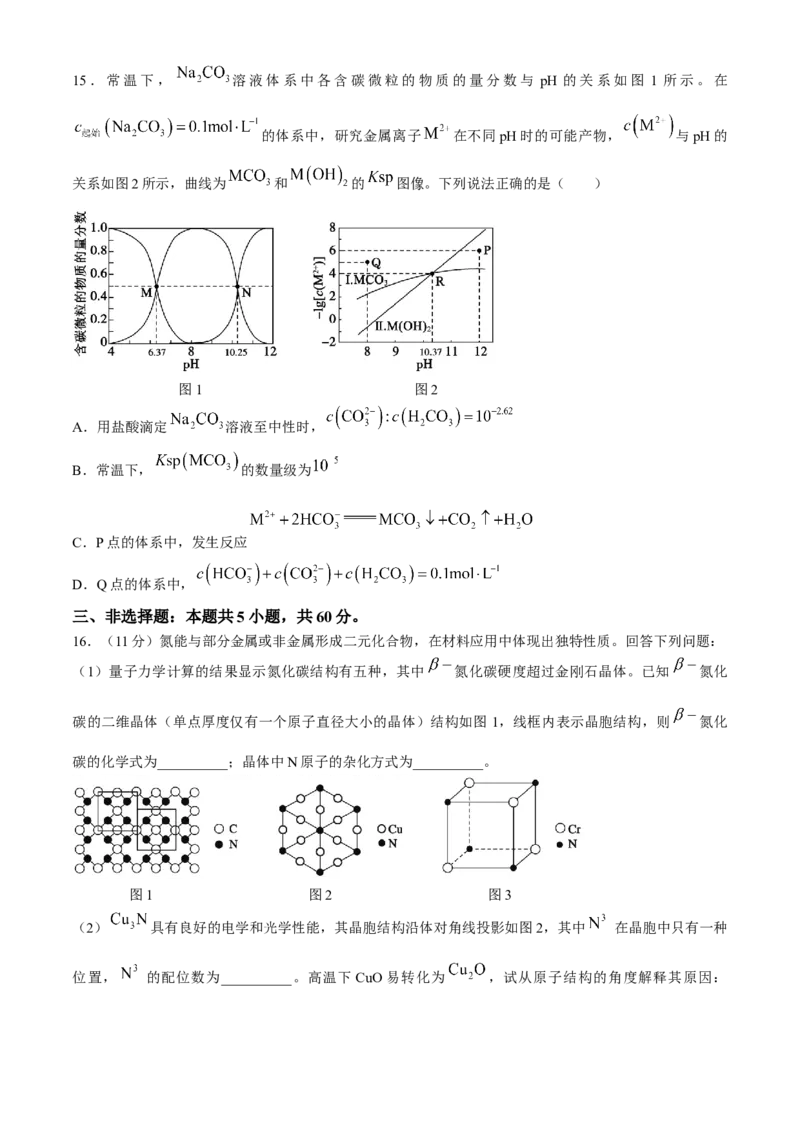
学科网(北京)股份有限公司15.常温下, 溶液体系中各含碳微粒的物质的量分数与 pH 的关系如图 1 所示。在
的体系中,研究金属离子 在不同pH时的可能产物, 与pH的
关系如图2所示,曲线为 和 的 图像。下列说法正确的是( )
图1 图2
A.用盐酸滴定 溶液至中性时,
B.常温下, 的数量级为
C.P点的体系中,发生反应
D.Q点的体系中,
三、非选择题:本题共5小题,共60分。
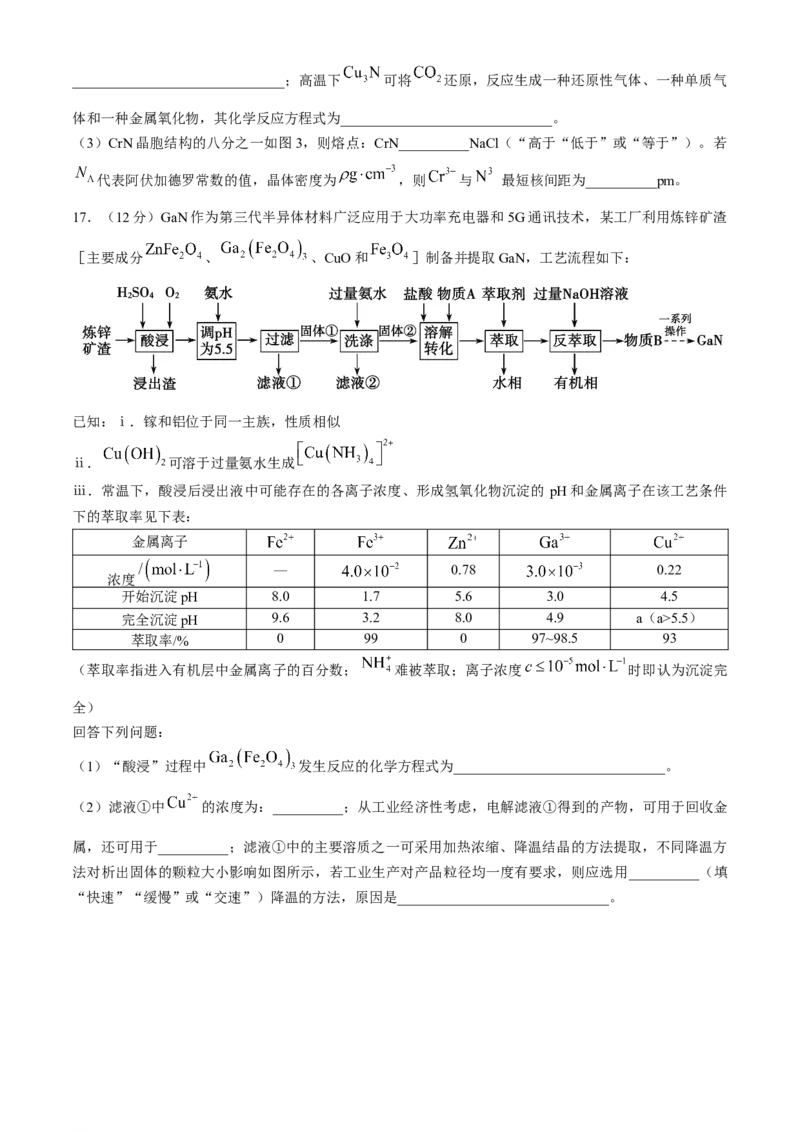
16.(11分)氮能与部分金属或非金属形成二元化合物,在材料应用中体现出独特性质。回答下列问题:
(1)量子力学计算的结果显示氮化碳结构有五种,其中 氮化碳硬度超过金刚石晶体。已知 氮化
碳的二维晶体(单点厚度仅有一个原子直径大小的晶体)结构如图 1,线框内表示晶胞结构,则 氮化
碳的化学式为__________;晶体中N原子的杂化方式为__________。
图1 图2 图3
(2) 具有良好的电学和光学性能,其晶胞结构沿体对角线投影如图2,其中 在晶胞中只有一种
位置, 的配位数为__________。高温下CuO易转化为 ,试从原子结构的角度解释其原因:
学科网(北京)股份有限公司______________________________;高温下 可将 还原,反应生成一种还原性气体、一种单质气
体和一种金属氧化物,其化学反应方程式为______________________________。
(3)CrN晶胞结构的八分之一如图3,则熔点:CrN__________NaCl(“高于“低于”或“等于”)。若
代表阿伏加德罗常数的值,晶体密度为 ,则 与 最短核间距为__________pm。
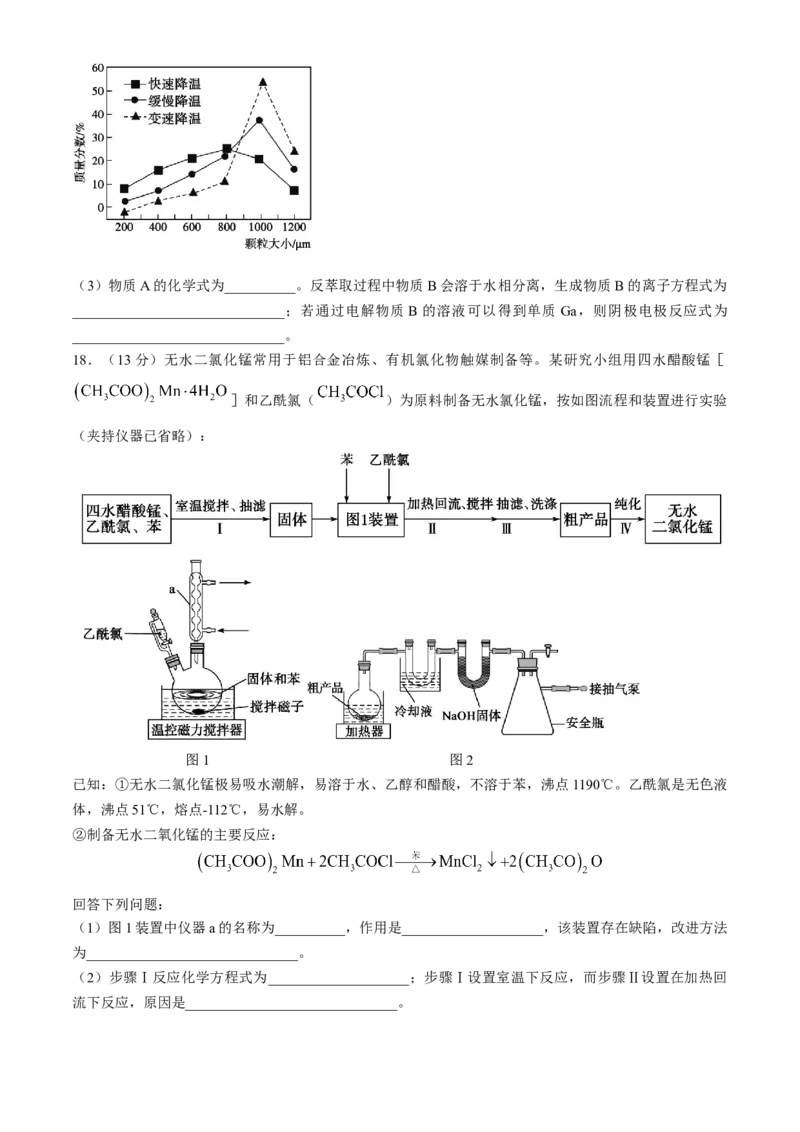
17.(12分)GaN作为第三代半异体材料广泛应用于大功率充电器和5G通讯技术,某工厂利用炼锌矿渣
[主要成分 、 、CuO和 ]制备并提取GaN,工艺流程如下:
已知:ⅰ.镓和铝位于同一主族,性质相似
ⅱ. 可溶于过量氨水生成
ⅲ.常温下,酸浸后浸出液中可能存在的各离子浓度、形成氢氧化物沉淀的 pH和金属离子在该工艺条件
下的萃取率见下表:
金属离子
— 0.78 0.22
浓度
开始沉淀pH 8.0 1.7 5.6 3.0 4.5
完全沉淀pH 9.6 3.2 8.0 4.9 a(a>5.5)
萃取率/% 0 99 0 97~98.5 93
(萃取率指进入有机层中金属离子的百分数; 难被萃取;离子浓度 时即认为沉淀完
全)
回答下列问题:
(1)“酸浸”过程中 发生反应的化学方程式为______________________________。
(2)滤液①中 的浓度为:__________;从工业经济性考虑,电解滤液①得到的产物,可用于回收金
属,还可用于__________;滤液①中的主要溶质之一可采用加热浓缩、降温结晶的方法提取,不同降温方
法对析出固体的颗粒大小影响如图所示,若工业生产对产品粒径均一度有要求,则应选用__________(填
“快速”“缓慢”或“交速”)降温的方法,原因是______________________________。
学科网(北京)股份有限公司(3)物质A的化学式为__________。反萃取过程中物质B会溶于水相分离,生成物质B的离子方程式为
______________________________;若通过电解物质 B的溶液可以得到单质 Ga,则阴极电极反应式为
______________________________。
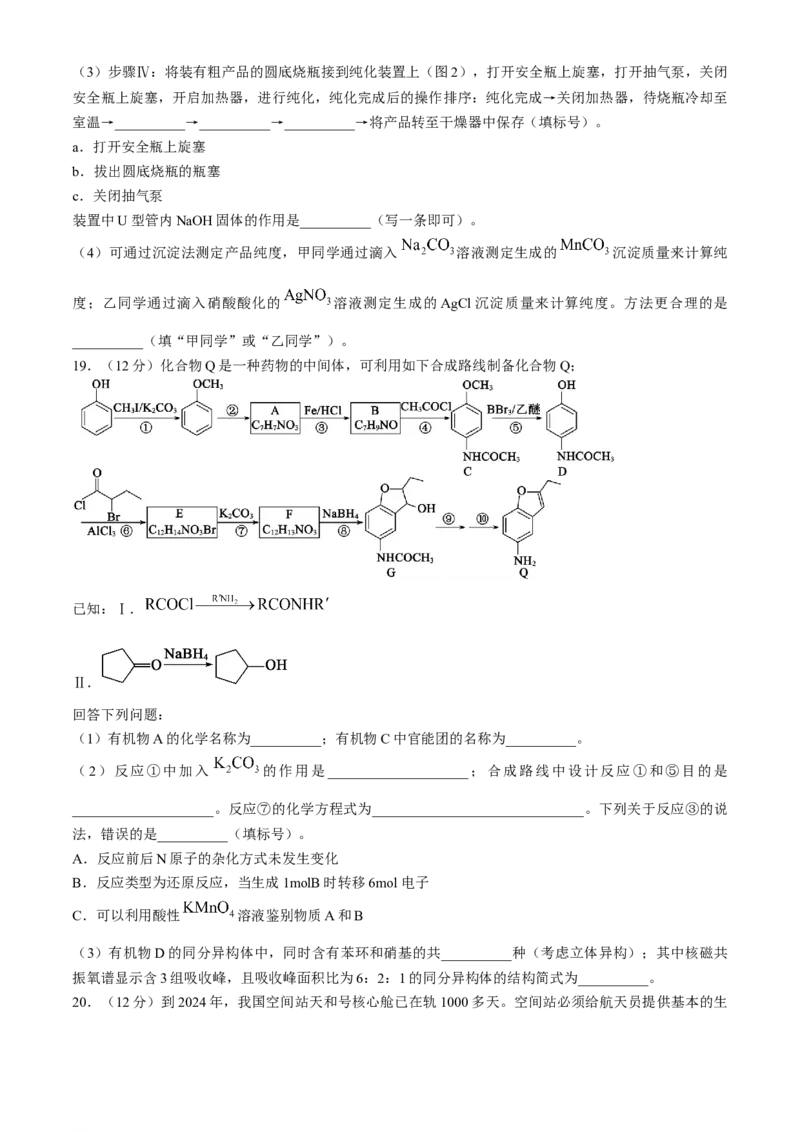
18.(13分)无水二氯化锰常用于铝合金冶炼、有机氯化物触媒制备等。某研究小组用四水醋酸锰[
]和乙酰氯( )为原料制备无水氯化锰,按如图流程和装置进行实验
(夹持仪器已省略):
图1 图2
已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯,沸点1190℃。乙酰氯是无色液
体,沸点51℃,熔点-112℃,易水解。
②制备无水二氧化锰的主要反应:
回答下列问题:
(1)图1装置中仪器a的名称为__________,作用是____________________,该装置存在缺陷,改进方法
为______________________________。
(2)步骤Ⅰ反应化学方程式为____________________;步骤Ⅰ设置室温下反应,而步骤Ⅱ设置在加热回
流下反应,原因是______________________________。
学科网(北京)股份有限公司(3)步骤Ⅳ:将装有粗产品的圆底烧瓶接到纯化装置上(图2),打开安全瓶上旋塞,打开抽气泵,关闭
安全瓶上旋塞,开启加热器,进行纯化,纯化完成后的操作排序:纯化完成→关闭加热器,待烧瓶冷却至
室温→__________→__________→__________→将产品转至干燥器中保存(填标号)。
a.打开安全瓶上旋塞
b.拔出圆底烧瓶的瓶塞
c.关闭抽气泵
装置中U型管内NaOH固体的作用是__________(写一条即可)。
(4)可通过沉淀法测定产品纯度,甲同学通过滴入 溶液测定生成的 沉淀质量来计算纯
度;乙同学通过滴入硝酸酸化的 溶液测定生成的AgCl沉淀质量来计算纯度。方法更合理的是
__________(填“甲同学”或“乙同学”)。
19.(12分)化合物Q是一种药物的中间体,可利用如下合成路线制备化合物Q;
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)有机物A的化学名称为__________;有机物C中官能团的名称为__________。
(2)反应①中加入 的作用是____________________;合成路线中设计反应①和⑤目的是
____________________。反应⑦的化学方程式为______________________________。下列关于反应③的说
法,错误的是__________(填标号)。
A.反应前后N原子的杂化方式未发生变化
B.反应类型为还原反应,当生成1molB时转移6mol电子
C.可以利用酸性 溶液鉴别物质A和B
(3)有机物D的同分异构体中,同时含有苯环和硝基的共__________种(考虑立体异构);其中核磁共
振氧谱显示含3组吸收峰,且吸收峰面积比为6:2:1的同分异构体的结构简式为__________。
20.(12分)到2024年,我国空间站天和号核心舱已在轨1000多天。空间站必须给航天员提供基本的生
学科网(北京)股份有限公司存条件,涉及氧气供给、一氧化碳清除、水处理等。电解水技术除用于供氧外,生成的氢气通过萨巴蒂尔
反 应 , 实 现 了 二 氧 化 碳 的 清 除 , 同 时 将 氢 气 转 化 为 更 安 全 的 甲 烷 , 原 理 :
。
回答下列问题:
(1)已知同条件下甲烷摩尔燃烧焓约是氢气的 3.1倍, ,
的摩尔燃烧焓约为__________kJ/mol。
(2)在恒容密闭容器中加人等量 和 ,分压均为20kPa,一定条件下发生萨巴蒂尔反应,随着反应
的进行, 的体积分数会__________(填“变大”变小”或“不变”)。某时刻测得 的分压
5kPa,若 的反应速率 ,计算该时期
__________ ;当测得 的分压为4kPa时,求得浓度商 __________。
(3)某条件下,萨巴蒂尔反应发生的同时也会发生副反应:
反应Ⅰ:
反应Ⅱ:
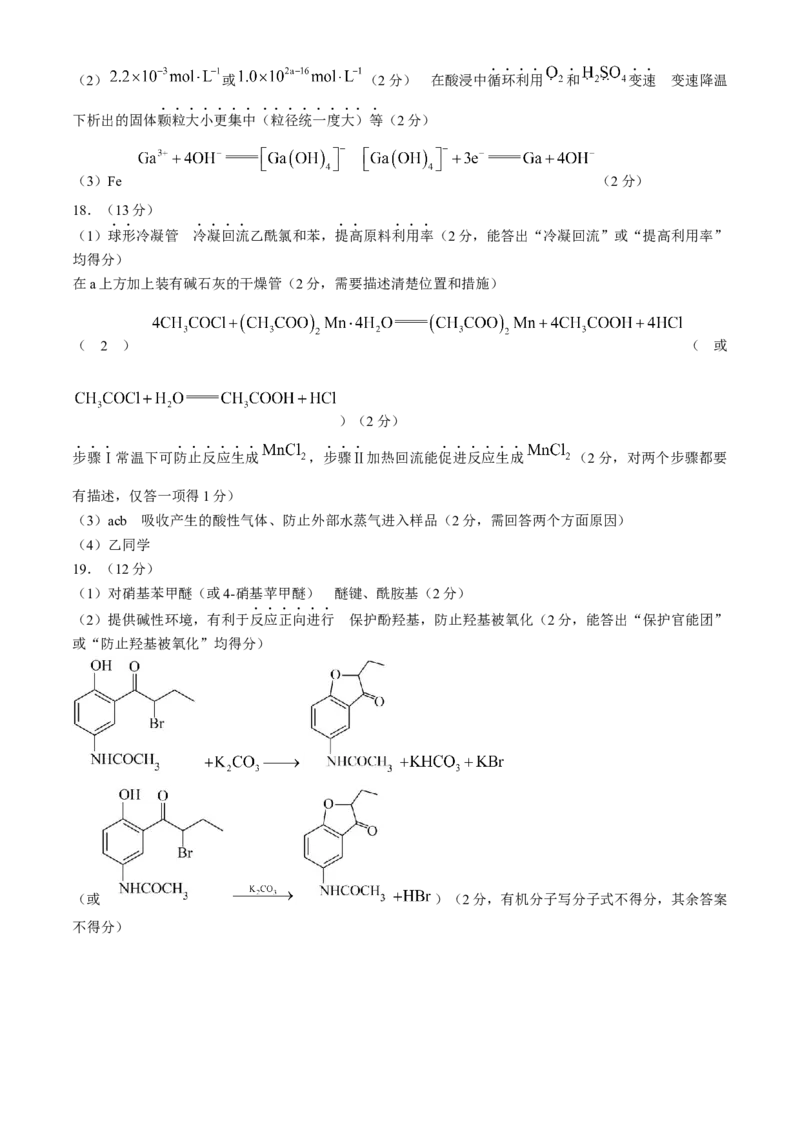
将 和 按体积比1:4混合( ),匀速通入装有催化剂的反应容器中发生以上反应相同时
间, 转化率, 选择性(选择性;转化的 中生成 的百分比)随温度变化曲线分别如图所
示。
已知反应Ⅰ为吸热反应,能较快建立平衡。图中 A、B、C三点,能表示萨巴蒂尔反应达到平衡的点是
__________。由图分析320℃时反应Ⅱ是否已经平衡:__________(填“是”“否”或“不能确定”),
学科网(北京)股份有限公司原因是______________________________。
学科网(北京)股份有限公司2024 届高三模拟考试
化学试题参考答案及评分标准
一、选择题
1.B 2.B 3.A 4.C
5.D 6.B 7.A 8.D
9.D 10.C
二、选择题
11.CD 12.AB 13.B 14.C
15.AD
三、非选择题(除标注外,每空1分)
阅卷总体原则(不是高考阅卷原则):
1.规范要求,严格要求,统一标准,公平公正,题组阅卷组长负责制。
2.答案为数值的,只看效值是否正确,不考虑单位。
3.学生写出的答案个数超过标准答案个数的(设为N个),以前N个为准。
4.选择型填空题不区分大对小写字母,多选的选对1个得1分,错选不得分。
5.方程式给分原则:
a.用“ ”“ ”“ ”不扣分,用“—”或无连接符号不得分;不写“↓”“↑”不扣分,
不写反应条件不扣分。
b.反应物或产物不全或错误不得分,方程式不配平或配平错误不得分,使用非最小公约数配平不得分。
c.要求写高子方程式的,写成化学方程式不得分。
6.名词术语或仪器名称等关键字或关键词写错,均不得分。
16.(11分)
(1) (2分,不区分大小写,上下标)
(2)6 亚铜离子( )价层电子排布处于全充满状态,比价层电子排布为 的铜离子( )更稳
定(2分) (2分)
(3)高于 (2分,算式等值即得分)
17.(12分)
(1) (2分)
学科网(北京)股份有限公司(2) 或 (2分) 在酸浸中循环利用 和 变速 变速降温
下析出的固体颗粒大小更集中(粒径统一度大)等(2分)
(3)Fe (2分)
18.(13分)
(1)球形冷凝管 冷凝回流乙酰氯和苯,提高原料利用率(2分,能答出“冷凝回流”或“提高利用率”
均得分)
在a上方加上装有碱石灰的干燥管(2分,需要描述清楚位置和措施)
( 2 ) ( 或
)(2分)
步骤Ⅰ常温下可防止反应生成 ,步骤Ⅱ加热回流能促进反应生成 (2分,对两个步骤都要
有描述,仅答一项得1分)
(3)acb 吸收产生的酸性气体、防止外部水蒸气进入样品(2分,需回答两个方面原因)
(4)乙同学
19.(12分)
(1)对硝基苯甲醚(或4-硝基苹甲醚) 醚键、酰胺基(2分)
(2)提供碱性环境,有利于反应正向进行 保护酚羟基,防止羟基被氧化(2分,能答出“保护官能团”
或“防止羟基被氧化”均得分)
(或 )(2分,有机分子写分子式不得分,其余答案
不得分)
学科网(北京)股份有限公司(3)15
20.(12分)
(1)-883.5(2分)
(2)不变 0.84(2分) (或0.0625)(2分)
(3)①BC(2分)
②否 320℃后升高温度 转化率下降但 选择性基本不变,说明 和CO同比减少,反应Ⅰ吸热
升温后平衡右移CO增加,因此升温反应Ⅱ右移,反应Ⅱ为放热反应,因此未平衡(2分,分析合理即得
分)
学科网(北京)股份有限公司