文档内容
班级 姓名 学号 分数
第三章 水溶液中的离子反应与平衡(A卷·知识通关练)
核心知识1 弱电解质的电离平衡
1.(2021·前郭尔罗斯蒙古族自治县蒙古族中学高二期末)下列有关强、弱电解质的叙述正确的是
A.强电解质溶液的导电性不一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在分子
C.强电解质都是离子化合物,而弱电解质都是共价化合物
D.不同的弱电解质只要物质的量浓度相同,电离程度也相同
2.食用白醋是生活中重要的调味品,其中含3% ~5%的醋酸。以下实验能证明醋酸为弱电解质的是( )
A.用食用白醋做导电实验,灯泡很暗
B.将水垢浸泡在白醋中,有CO 气体放出
2
C.向白醋中滴入紫色石蕊试液,溶液呈红色
D.中和等pH、等体积的盐酸和白醋,白醋消耗NaOH多
3.与0.1mol/L的氨水溶液中c(OH-)最接近的数值是
A.0.1mol/L B.1.0×10-3mol/L C.1.0×10-7mol/L D.1.0×10-13mol/L
4.下列属于电离方程式且书写正确的一项是
A.HCO3
-
+H
OHCO+OH-
2 2 3
B.HCO
2H++CO3 2-
2 3
C.CHCOOH+OH-CHCOO-+H
O
3 3 2
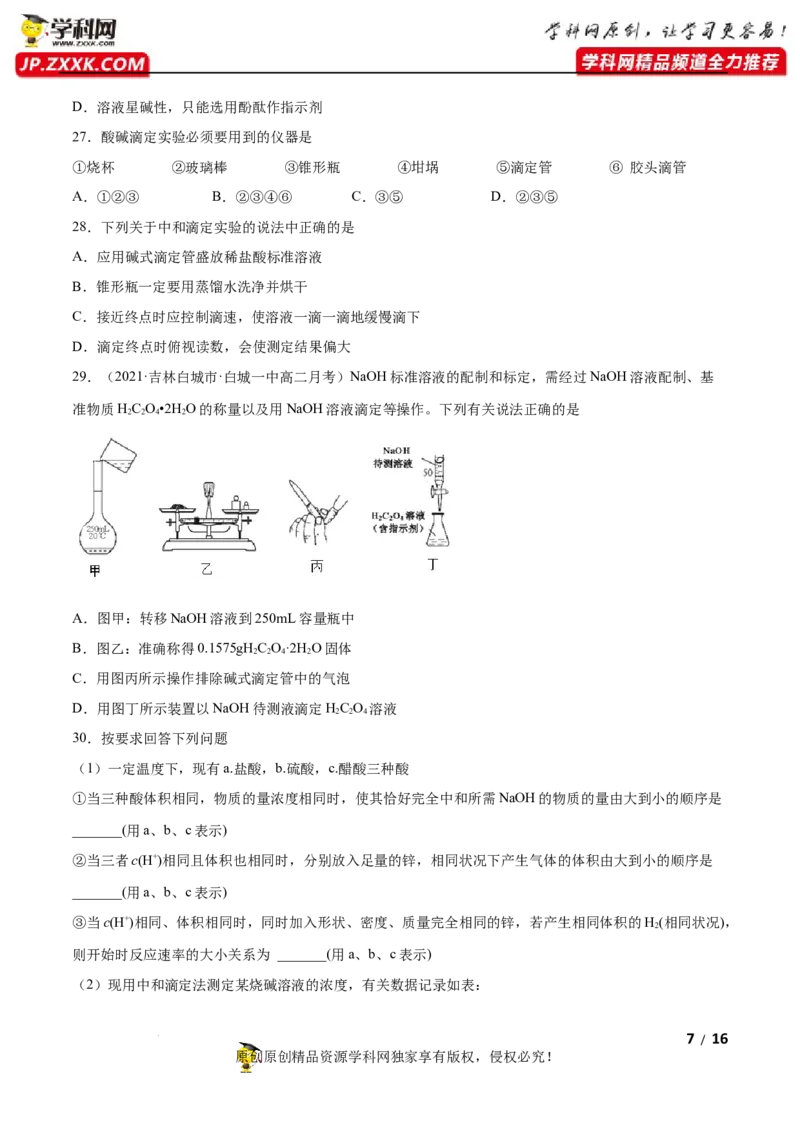
D.CHCOOHCHCOO-+H+
3 3
5.已知醋酸溶液达到电离平衡后,改变某一条件使电离平衡向正反应方向移动,则下列说法正确的是
A.醋酸的电离程度一定变大 B.溶液的导电能力一定变强
C.溶液的pH一定减小 D.发生电离的分子总数增多
6.用水稀释 0.1mol/L 氨水时,溶液中随着水量的增加而减小的是( )
A.c(OH﹣)/ c(NH .H O) B.c(NH .H O)/ c(OH﹣)
3 2 3 2
C.c(H+)和 c(OH﹣)的乘积 D.OH﹣的物质的量
1 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
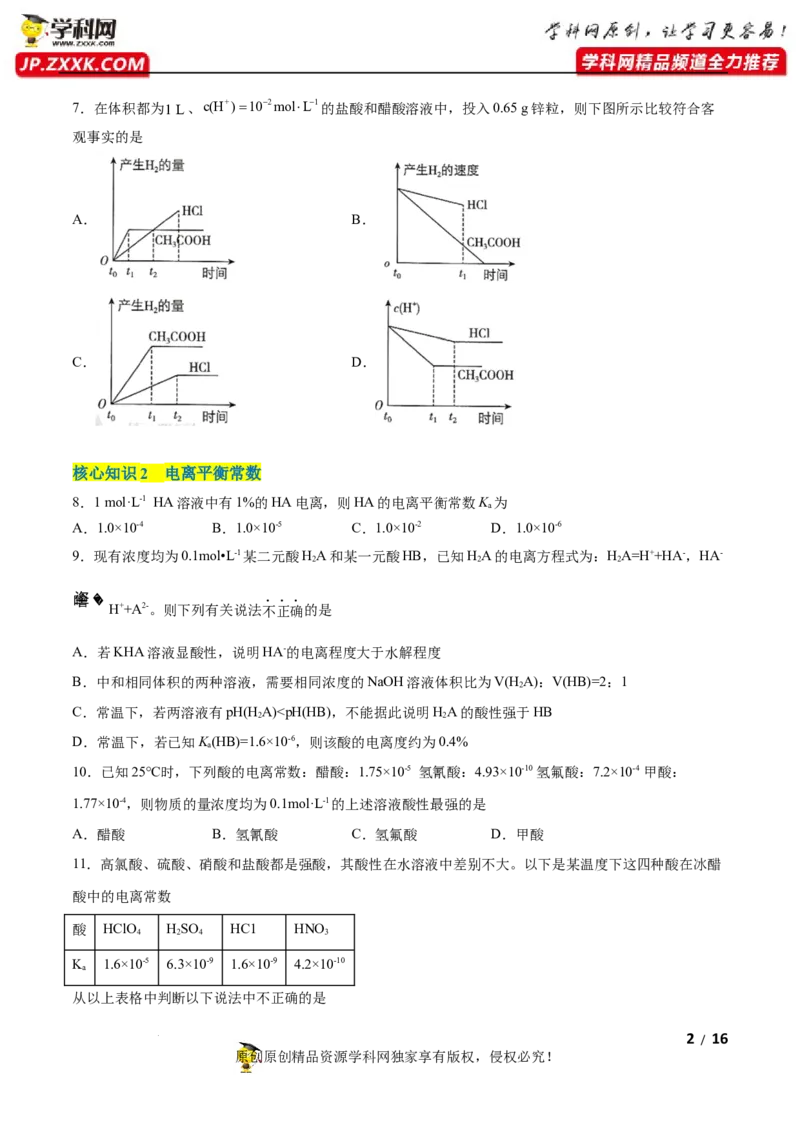
学科网(北京)股份有限公司7.在体积都为1 L、c(H+)102molL1的盐酸和醋酸溶液中,投入0.65 g锌粒,则下图所示比较符合客
观事实的是
A. B.
C. D.
核心知识2 电离平衡常数
8.1 mol·L-1 HA溶液中有1%的HA电离,则HA的电离平衡常数K 为
a
A.1.0×10-4 B.1.0×10-5 C.1.0×10-2 D.1.0×10-6
9.现有浓度均为0.1mol•L-1某二元酸HA和某一元酸HB,已知HA的电离方程式为:HA=H++HA-,HA-
2 2 2
噲垐��
H++A2-。则下列有关说法不正确的是
A.若KHA溶液显酸性,说明HA-的电离程度大于水解程度
B.中和相同体积的两种溶液,需要相同浓度的NaOH溶液体积比为V(H A):V(HB)=2:1
2
C.常温下,若两溶液有pH(H A)”或“=”)25。
w
(2)该NaOH溶液中NaOH的物质的量浓度为_______,该NaOH溶液中由水电离出的c(OH-)为_______。
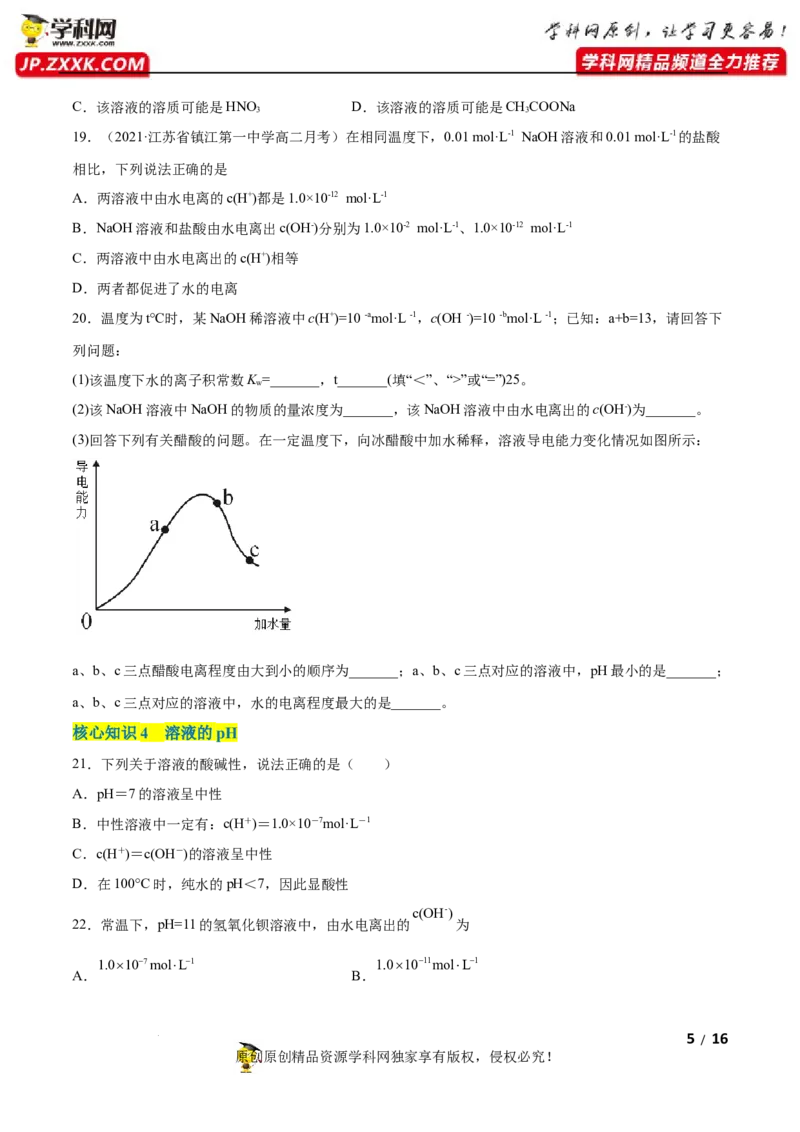
(3)回答下列有关醋酸的问题。在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示:
a、b、c三点醋酸电离程度由大到小的顺序为_______;a、b、c三点对应的溶液中,pH最小的是_______;
a、b、c三点对应的溶液中,水的电离程度最大的是_______。
核心知识4 溶液的pH
21.下列关于溶液的酸碱性,说法正确的是( )
A.pH=7的溶液呈中性
B.中性溶液中一定有:c(H+)=1.0×10-7mol·L-1
C.c(H+)=c(OH-)的溶液呈中性
D.在100°C时,纯水的pH<7,因此显酸性
c(OH-)
22.常温下,pH=11的氢氧化钡溶液中,由水电离出的 为
1.0107molL1 1.01011molL1
A. B.
5 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司2.0103molL1 5.01012molL1
C. D.
pH
23.室温下,对于等体积、 均为2的醋酸和盐酸两种溶液,下列叙述不正确的是
A.分别加足量的锌充分反应后,醋酸溶液产生的氢气多
pH
B.分别加水稀释10倍数后,两溶液的 均为3
C.若HA表示 HCl 或 CH 3 COOH ,两溶液中都有
c2 H
c
H
c
A
K w
pH
D.温度都升高20℃后,两溶液的 不再相等
24.下列关于常温下,体积均为10mL,pH均为4的HCl溶液a和CHCOOH溶液b的有关说法不正确的
3
是
A.对水的电离的抑制程度相同
B.稀释至相同pH后,Vc(CH COOH)>c(CH COO-)>c(H+)
3 3
C.该溶液中存在:c(H+)+c(CH COOH)>c(OH-)
3
cCH COOH
3
D.向溶液中加入少量水, c
CH
COO-
增大
3
32.某温度下,0.1 mol·L-1NaHCO 溶液pH=10,下列判断正确的是
3
A.c(OH-)=10-4 mol·L-1
B.加入少量NaOH固体,c(Na+)和c(HCO3)均增大
C.c(Na+)+c(H+)=c(HCO3)+c(OH-)
8 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司 2
D.c(Na+)=c(HCO3)+c(CO3 )+c(H CO)
2 3
33.下列离子方程式的书写正确的是
A.硫化钠水解:S2-+2H O HS↑+2OH-
2 2
HSO⇌- SO2-
B.亚硫酸氢钠水解: 3+H O HO++ 3
2 3
⇌
C.硫化钾水解:S2-+H O=HS-+OH-
2
AlO-
D.硫酸铝溶液跟偏铝酸钠溶液反应:Al3++3 2+6H O=4Al(OH) ↓
2 3
核心知识7 影响盐类水解的主要因素
34.下列关于盐类水解的说法错误的是
A.在纯水中加入能水解的盐一定促进水的电离
pH7
B.常温下,醋酸分子不可能存在于 的碱性溶液中
NH Cl NH
C.在 4 溶液中加入稀盐酸能抑制 4水解
c
CH
COO
3
D.加热 CH COONa 溶液,溶液中 c Na 的值将减小
3
Al3 3H O Al(OH) 3H
35.在反应 2 3 的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,
应采取的措施是
HCl NaOH AlCl
A.加热 B.通入 气体 C.加入适量的 溶液 D.加入固体 3
c
Na
36.为使
Na S
溶液中
c
S2 的值减小,可加入的物质是( )
2
①HCl ②适量的NaOH固体 ③适量的KOH固体 ④适量的KHS固体
A.①② B.②③ C.③④ D.①④
37.某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响:用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度(mol/L) 0.0010 0.0100 0.0200 0.1000 0.2000
pH 3.88 3.38 3.23 2.88 2.73
9 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司回答下列问题:
(1)若用pH试纸测醋酸的pH,实验操作为:_______。
(2)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:_______。
(3)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度_______(填增大、减小
或不变)
Na CO CO2 K =210-4
(4) 2 3俗称纯碱,因 3 水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时, h ,
c
HCO
:c
CO2
2:1
则当溶液中 3 3 时,溶液的pH=_______。
核心知识8 盐类水解的应用
38.下列说法不正确的是
Mg(OH) FeCl
A.向 2悬浊液中滴加 3溶液,生成红褐色沉淀
B.碳酸氢钠药片,该药是抗酸药,服用时喝些醋能提高药效
C.配制氯化铁溶液时需加入适量盐酸抑制水解
CaSO Na CO
D.水垢中的 4,可先用 2 3溶液处理,而后用酸除去
39.实验室在配制氯化铁溶液时,先把氯化铁晶体溶解在稀盐酸中,再加水稀释所需浓度,如此操作的目
的是
A.防止氯化铁电离 B.抑制氯化铁水解
C.提高溶液的pH D.提高氯化铁的溶解度
40.根据下列实验操作所得的现象及结论不正确的是
选项 实验操作 现象及结论
A 将MgCl 溶液加热蒸干并灼烧 得到的白色固体为MgO
2
向体积均为20mL的冷水和沸水中分别滴入3滴
前者为黄色,后者为红褐色,说明温度升高,
B
FeCl 饱和溶液 Fe3+的水解程度增大
3
取CH COONa溶液于试管中并加入几滴酚酞试 溶液颜色变深,说明CH COONa溶液中存在水
3. 3.
C
剂,再给试管加热 解平衡
室温下,用pH试纸测0.1molL1的NaHSO 溶
3
D 说明HSO的水解大于电离
3
液的pH约为5
10 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司核心知识9 溶液中粒子浓度的关系
0.1molL1 NH HSO
4 4
41.在 的 溶液中,下列关于微粒物质的量浓度的关系式不正确的是( )
c
H
c
SO2
c
NH
A. 4 4
c
NH
c
H
2c
SO2
c
OH
B. 4 4
c H c NH cNH H Oc OH
C. 4 3 2
c
Na
c
SO2
c
NH
c
OH
c
H
D.常温下向该溶液中滴加 NaOH 溶液至中性后: 4 4
42.下列说法正确的是
2- -
A.常温下pH= 10的NaC O 溶液中:2c(Na+) = c(C O4 ) + c(HC O4) + c(H C O)
2 2 4 2 2 2 2 4
B.向醋酸溶液中加入醋酸钠晶体使溶液呈中性,此时混合液中c(Na+) < c(CHCOO-)
3
+
C.0.2 mol/L NH Cl溶液和0.1 mol/L (NH )SO 溶液中,c(NH4)前者较大
4 4 2 3
D.浓度均为0.1 mol/L的NaCl溶液和NaF溶液中,离子总浓度后者较大
43.常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
实验编号 c(HA)/mol·L-1 c(NaOH)/mol·L-1 反应后溶液pH
甲 0.1 0.1 pH=9
乙 c 0.2 pH=7
1
下列判断不正确的是
A.c 一定大于0.2
1
噲垐��
B.HA的电离方程式是HA H++A-
C.乙反应后溶液中:c(Na+)=c(HA)+c(A-)
D.甲反应后溶液中:c(Na+)>c(A-)>c(OH-)>c(H+)
44.在水质检验中,测定水的硬度时,用到氨和氯化铵(NH ·HO~ NH Cl)缓冲溶液,控制溶液在pH=9.1左
3 2 4
右。则关于该缓冲溶液的说法正确的是
+
A.在缓冲溶液中,不可能有c(Cl- )>c(NH4 )>c(H+) >c(OH-)
11 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司+
B.在缓冲溶液中,一定有c(NH4) +c(NH ) =2c(Cl-)
3
C.在有效缓冲范围内,将缓冲溶液加水稀释时,pH基本不变
D.在缓冲溶液中,水的电离可能受到促进也可能受到抑制
45.某二元酸(化学式用HA表示)在水中的电离方程式是:HA==H++HA-、HA-
H++A2-
2 2
回答下列问题:
(1)Na A溶液显____________(填“酸性”“中性”或“碱性”)。理由是____________(用离子方程式表示)。
2
(2)在0.1mol·L-1的NaA溶液中,下列粒子浓度关系式正确的是____________。
2
A.c(A2-)+c(HA-)+c(H A)=0.1mol·L-1 B.c(Na+)+c(OH-)=c(H+)+c(HA-)
2
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-) D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1HA溶液中氢离子的物质的量浓度可能是
2
____________0.11mol·L-1(填“<”“>”或“=”),理由是____________。
(4)0.1mol·L-1NaHA溶液中各种离子浓度由大到小的顺序是____________。
核心知识10 沉淀溶解平衡
46.常温下,将足量的AgCl固体分别放入下列液体中,AgCl溶解的量最小的是
A.20 ml蒸馏水 B.30mL 0.03mol/L HCl溶液
C.40mL 0.05mol/L AgNO 溶液 D.50mL 0.02mol/L CaCl 溶液
3 2
噲垐��
47.常温下,某PbI 悬浊液中存在平衡PbI (s) Pb2+(aq)+2I-(aq),加入少量KI固体并完全溶解。下列
2 2
说法错误的是
A.溶度积常数K (PbI )减小 B.溶液中c(I-)增大
sp 2
C.沉淀溶解平衡向左移动 D.悬浊液中固体质量增大
48.下列说法不正确的是
Mg(OH) FeCl
A.向 2悬浊液中滴加 3溶液,生成红褐色沉淀
B.碳酸氢钠药片,该药是抗酸药,服用时喝些醋能提高药效
C.配制氯化铁溶液时需加入适量盐酸抑制水解
CaSO Na CO
D.水垢中的 4,可先用 2 3溶液处理,而后用酸除去
49.已知25℃时,RSO (s)+CO2-(aq) RCO(s)+SO 2-(aq)的平衡常数K=1.75×104,K (RCO)=2.80×10-9,下
4 3 3 4 sp 3
列叙述中正确的是 ⇌
12 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司A.25℃ 时,RSO 的K 约为4.9×10-5
4 sp
B.将浓度均为6×10-5mol/L的RCl 、NaCO 溶液等体积混合后可得到RCO 沉淀
2 2 3 3
C.向c(CO2-)=c(SO 2-)的混合液中滴加RCl 溶液,首先析出RSO 沉淀
3 4 2 4
D.相同温度下,RCO 在水中的K 大于在NaCO 溶液中的K
3 sp 2 3 sp
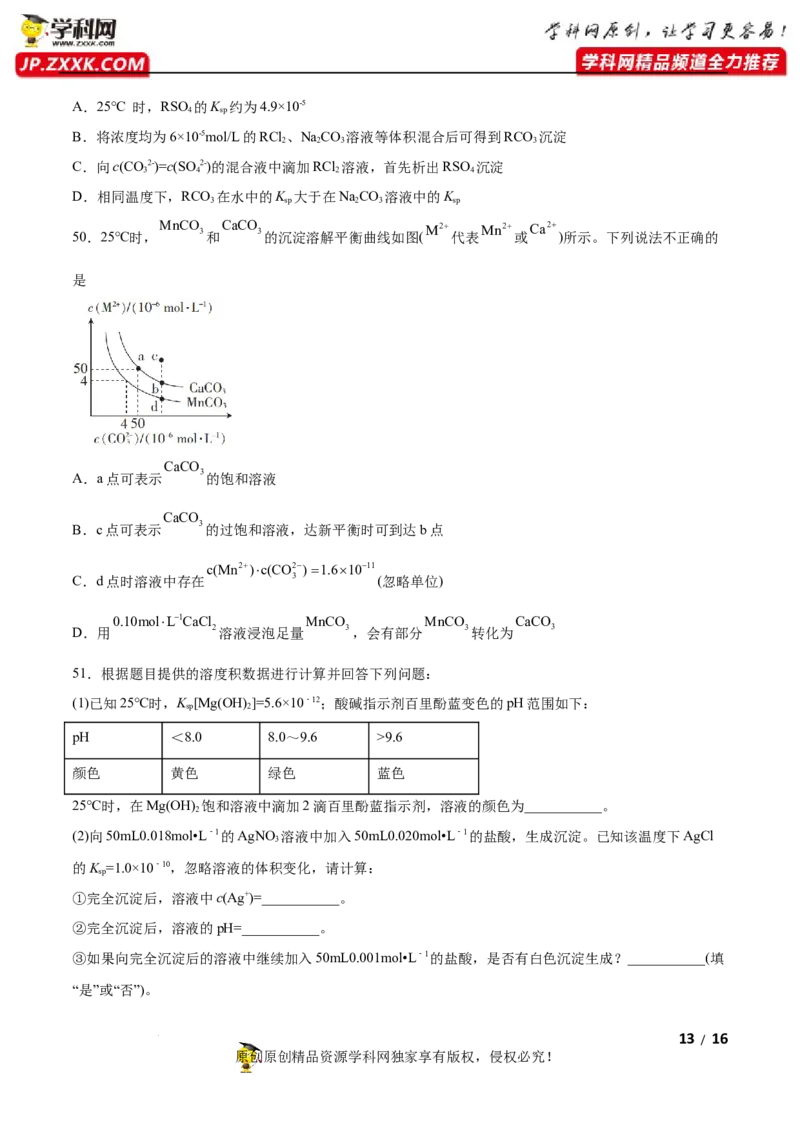
50.25℃时,
MnCO
3和
CaCO
3的沉淀溶解平衡曲线如图(
M2
代表
Mn2
或
Ca2
)所示。下列说法不正确的
是
CaCO
A.a点可表示 3的饱和溶液
CaCO
B.c点可表示 3的过饱和溶液,达新平衡时可到达b点
c(Mn2)c(CO2)1.61011
C.d点时溶液中存在 3 (忽略单位)
0.10molL1CaCl MnCO MnCO CaCO
D.用 2溶液浸泡足量 3,会有部分 3转化为 3
51.根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25℃时,K [Mg(OH) ]=5.6×10﹣12;酸碱指示剂百里酚蓝变色的pH范围如下:
sp 2
pH <8.0 8.0~9.6 >9.6
颜色 黄色 绿色 蓝色
25℃时,在Mg(OH) 饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为___________。
2
(2)向50mL0.018mol•L﹣1的AgNO 溶液中加入50mL0.020mol•L﹣1的盐酸,生成沉淀。已知该温度下AgCl
3
的K =1.0×10﹣10,忽略溶液的体积变化,请计算:
sp
①完全沉淀后,溶液中c(Ag+)=___________。
②完全沉淀后,溶液的pH=___________。
③如果向完全沉淀后的溶液中继续加入50mL0.001mol•L﹣1的盐酸,是否有白色沉淀生成?___________(填
“是”或“否”)。
13 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司(3)在某温度下,K (FeS)=6.25×10﹣18,FeS饱和溶液中c(H+)与c(S2﹣)之间存在关系:c2(H+)•c(S2﹣)=1.0×10﹣
sp
22,为了使溶液里c(Fe2+)达到1mol•L﹣1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
___________。
52.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理
含砷废水,相关数据如表。
K
表1 几种砷酸盐的 sp
难溶物 K
sp
Ca AsO 6.81019
3 4 2
AlAsO 1.61016
4
FeAsO 5.71021
4
表2 工厂污染物排放浓度及允许排放标准
污染物 H SO As
2 4
浓度 28.42gL1 1.6gL1
排放标准 pH6~9 0.5mgL1
回答以下问题:
H SO molL1
2 4
(1)该工厂排放的废水中 的物质的量浓度为_______ 。
(2)若处理后的工厂废水中Al3 、 Fe3 的浓度均为1.0104molL1 ,则此时废水中 c AsO3 4 最大是_______
molL1。
H AsO MnO
3 3 2
(3)工厂排放出的酸性废水中的三价砷( ,弱酸)不易沉降,可投入 先将其氧化成五价砷(
H AsO
3 4,弱酸),写出该反应的离子方程式:_______。
(4)在处理含砷废水时采用分段式,先向废水中投入适量生石灰调节pH为2,再投入适量生石灰将pH调节
Ca AsO
为8左右,使五价砷以 3 4 2形式沉降。
①将pH调节为2时废水中有大量沉淀产生,沉淀主要成分的化学式为_______。
14 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司Ca AsO
②在pH调节为8左右才出现大量 3 4 2沉淀的原因为_______。
15 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司16 / 16
原创原创精品资源学科网独家享有版权,侵权必究!
学科网(北京)股份有限公司